文档内容
2024 年中考第二次模拟考试(深圳卷)
化 学
(考试时间:40分钟 试卷满分:50分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Zn-65 Fe-56 Cl-35.5 K-39 S-32
一、选择题(本大题共12小题,1-8题每小题1.5分,9-12题每小题2分,共20分。每小题给出的四个选
项中,只有一个选项最符合题目的要求)
1.混合物分离的方法在生产、生活和科学实验中有着广泛的应用。下列做法中应用了过滤方法的是(
)
A.除去盐酸中的硫酸 B.分离豆浆和豆渣
C.除去混在铜粉中的铁粉 D.用海水晒盐
【答案】B
【解析】A、盐酸和硫酸均是液体,不能用过滤的方法除杂,故A错误;
B、豆渣不溶于水,可采用过滤的方法分离豆浆和豆渣,故B正确;
C、铜粉和铁粉都不溶于水,不能用过滤的方法除杂,故C错误;
D、海水晒盐是利用了蒸发结晶的方法得到粗盐,所以该过程中应用了结晶的方法,故D错误;
故选:B。
2.如图所示为探究硬水性质实验的部分操作,其中正确的是( )
A. 吸取肥皂水 B. 振荡
C. 点燃酒精灯 D. 加热水样
【答案】D
【解析】A、吸取过液体的胶头滴管不能倒放,该选项操作不正确;
B、振荡试管时,不能上下振荡,应左右振荡,该选项操作不正确;C、禁止用燃着的酒精灯点燃另一只酒精灯,该选项操作不正确;
D、加热液体时,用酒精灯外焰加热,液体体积不能超过试管容器的三分之一,且试管夹夹在距试管口约
三分之一处,该选项操作正确。
故选D。
3.下图是元素周期表中的一部分以及硒的原子结构示意图。下列有关说法正确的是( )
A.图中x值为33,y值为8 B. 表示两个砷元素
C.等质量金属镓和锗中镓原子个数多 D.硒离子的符号是
【答案】C
【解析】A、元素周期表是按原子序数递增的顺序排列的,故图中x值为33,在原子中质子数=核外电子
数,y=34-2-8-6=18,故A说法错误;
B、原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数
字。2As 表示两个砷原子,元素只讲种类不讲个数,故B说法错误;
C、由元素周期表中的一格可知,汉字下方的数字表示相对原子质量,则镓元素的相对原子质量为69.72,
锗元素的相对原子质量为72.64,原子的相对原子质量与其实际质量是成正比,由于相对原子质量的大小
关系是镓<锗,真实质量也是这一关系,则等质量的金属镓和锗中,含原子多少关系是镓>锗,故C说法
正确;
D、硒原子最外层有6个电子,易得到2个电子,形成的硒离子带两个单位的负电荷,其符号是Se2-,故D
说法错误;
故选A。
4.艾草中含有丰富的矢车菊黄素,有平喘镇咳,缓解风寒感冒的效果,其化学式为C H O,下列关于
18 16 8
C H O 的说法正确的是( )
18 16 8
A.矢车菊黄素由碳、氢、氧原子构成
B.一个矢车菊黄素分子由18个碳原子、16个氢原子、8个氧原子构成
C.矢车菊黄素中氧元素的质量分数最大
D.一个矢车菊黄素分子中含有8个氢分子
【答案】B
【解析】
A、矢车菊黄素由分子构成,其分子由碳、氢、氧原子构成,故说法不正确;
B、由化学式可知,一个矢车菊黄素分子由18个碳原子、16个氢原子、8个氧原子构成,故说法正确;
C、矢车菊黄素中碳、氢、氧元素的质量比为(12×18):(1×16):(16×8)=27:2:16,碳元素质量比
最大,则碳元素的质量分数最大,故说法不正确;D、分子是由原子构成的,一个矢车菊黄素分子中含有16个氢原子,故说法不正确。
故选B。
5.2023年8月30日,华为发布了首款自主研发的5G智能手机Mate60 Pro,标志着中国终于在芯片领域
实现突破,不再长期依赖外部输入。芯片的基材主要是高纯硅,下图是制备高纯硅的微观示意图。下列说
法中正确的是( )
A.该反应属于化合反应 B.X中一定含有●、○
C.反应前后分子的种类和个数均不变 D.反应前后硅元素的化合价没有改变
【答案】B
【解析】A、由图可知,反应物和生成物均有两种,不属于化合反应,该选项说法不正确;
B、根据反应前后原子的种类不变,反应前有氢原子、氯原子和硅原子,而反应后除X外只有硅原子,则
X中一定含有氢原子和氯原子,该选项说法正确;
C、化学反应前后,分子的种类肯定改变,该选项说法不正确;
D、反应物中,硅在化合物中,化合价不为零,但生成物中硅位于单质中,化合价为零,则硅元素化合价
改变,该选项说法不正确。
故选B。
6.如图是电解水的实验装置,下列关于该实验的说法中,正确的是( )
A.管a中的气体为氧气 B.与管b相连的是电源的正极
C.管a与管b中气体质量比为2:1 D.该实验可说明水是由氢气和氧气组成的
【答案】B
【解析】A、电解水时,正极产生氧气,负极产生氢气,且生成的氧气和氢气的体积比为1:2,由图可
知,管a收集的气体较多,则收集的气体为氢气,该选项说法不正确;
B、由前面分析可知,管b收集的气体为氧气,则与管b相连的是电源的正极,该选项说法正确;
C、由前面分析可知,管a与管b中气体体积比为2:1,而不是质量比,质量比为1:8,该选项说法不正
确;
D、水中不含氢气和氧气,该实验能说明水是由氢、氧元素组成,该选项说法不正确。故选B。
7.某溶液能使紫色石蕊溶液变红,下列各组离子在该溶液中能大量共存且形成无色溶液的是( )
A.Na+、Ca2+、Cl- B.K+、 、OH-
C.Cu2+、 、Cl- D.Ba2+、Mg2+ 、
【答案】A
【分析】能使紫色石蕊溶液变红,说明溶液显酸性,存在大量H+,能形成无色溶液,说明溶液中不含有有
色离子。
【解析】A、H+、Na+、Ca2+、Cl-在溶液中不能结合生成沉淀、气体、水,能大量共存,且不存在有色离
子,故选项正确;
B、碳酸根离子和氢离子会结合生成水和二氧化碳,氢离子和氢氧根离子能结合生成水,故选项错误;
C、铜离子在溶液中显蓝色,故选项错误;
D、钡离子和硫酸根离子结合生成硫酸钡沉淀,故选项错误;
故选:A。
8.下列实验操作能达到实验目的的是( )
选 目
物质 主要实验操作
项 的
鉴
A 羊毛、棉线、涤纶 点燃,闻燃烧产生的气味
别
检
B 检验氢氧化钠固体是否变质 取样,加水溶解后,滴加酚酞溶液,观察溶液颜色是否变红
验
除
C 除去H 中混有的少量HCl 依次通过NaHCO 溶液,浓硫酸
2 3
杂
KNO 和Ba(NO ) 的混合 分 先加入适量的KSO 溶液,过滤,再向滤渣中加入一定量稀
3 3 2 2 4
D
溶液 离 HNO,充分搅拌
3
A.A B.B C.C D.D
【答案】A
【解析】A、羊毛的主要成分是蛋白质,灼烧时会产生烧焦羽毛的气味,棉线的主要成分是植物纤维,灼
烧时会产生烧纸的气味,涤纶是合成纤维,灼烧时有特殊气味,可以鉴别,故A能达到目的;
B、氢氧化钠溶液显碱性能使无色酚酞溶液变红,氢氧化钠变质后生成碳酸钠,碳酸钠溶液显碱性也能使
无色酚酞溶液变红,故B不能达到实验目的;
C、将混合气体依次通过饱和碳酸氢钠溶液和浓硫酸,碳酸氢钠和氯化氢反应生成氯化钠、二氧化碳和
水,虽然除去了杂质,但是引入了新的杂质二氧化碳,不符合除杂原则,故C不能达到实验目的;
D、向溶液中加入适量的硫酸钾溶液,硫酸钾与硝酸钡反应生成硫酸钡沉淀和硝酸钾,过滤后向滤渣中加
入稀硝酸,硝酸与硫酸钡不反应,不能达到分离的目的,故D不能达到实验目的;故选A。
9.下图各实验装置气密性均良好。对实验分析的说法正确的是( )
A.向广口瓶中滴入稀盐酸后,气球变大,说明氢氧化钠和盐酸反应放热
B.氢氧化钡溶液变浑浊,说明通入的二氧化碳与氢氧化钡发生了反应
C.红磷燃烧过程中弹簧夹未夹紧,待集气瓶冷却至室温后,将导管伸入水中,则测得空气中氧气的体积
分数偏大
D.向试管中加入氧化钙后,石灰水中溶质质量减小,玻璃弯管左侧液面会降低
【答案】D
【解析】A、向广口瓶中滴入稀盐酸后,气球变大,不能说明氢氧化钠和盐酸反应放热,也可能是氢氧化
钠固体溶于水放热造成的,故选项说法错误;
B、通入二氧化碳后,碳酸钠溶液被压入氢氧化钡溶液中,碳酸钠能与氢氧化钡溶液反应生成碳酸钡沉淀
和氢氧化钠,不说明通入的二氧化碳与氢氧化钡发生了反应,故选项说法错误;
C、红磷燃烧过程中弹簧夹未夹紧,待集气瓶冷却至室温后,导致部分空气进入装置中,将导管伸入水
中,使得进入集气瓶中的水减小,则测得空气中氧气的体积分数偏小,故选项说法错误;
D、向试管中加入氧化钙后,氧化钙与水反应生成氢氧化钙,反应放出大量的热,氢氧化钙的溶解度随着
温度的升高而减小,氢氧化钙的溶解度减小,有氢氧化钙析出,石灰水中溶质质量减小,集气瓶中温度升
高导致压强增大,玻璃弯管左侧液面降低,故选项说法正确;
故选D。
10.如图为氯化钠、碳酸钠的溶解度曲线,下列说法正确的是( )
A.10℃时, 碳酸钠放入 水中,得到溶液的质量是
B.40℃时,等质量的氯化钠和碳酸钠配成饱和溶液,氯化钠需要的水更多
C.20℃时,氯化钠溶液的浓度一定大于碳酸钠溶液的浓度
D.可通过蒸发结晶的方式提纯混有少量 的【答案】B
【解析】A、10℃时, 碳酸钠的溶解度为10g,即100g水中最多能溶解10g碳酸钠,达到饱和状态,则
10g 碳酸钠放入 50g 水中,只能溶解5g碳酸铵,则得到溶液的质量是50g+5g=55g,故A说法错误;
B、40℃时,碳酸钠的溶解度大于氯化钠,等质量的氯化钠和碳酸钠配成饱和溶液,氯化钠需要的水更
多,故B说法正确;
C、由于不确定溶液的状态,所以无法比较其浓度大小,故C说法错误;
D、碳酸钠溶解度受温度变化影响较大,氯化钠溶解度受温度变化影响较小,可通过蒸发结晶的方式提纯
混有少量NaCl的 NaCO,故D说法错误;
2 3
故选:B。
11.下列图像能正确反映其对应关系的是( )
甲 乙 丙 丁
A.甲表示常温下,向pH=3的某溶液中加水稀释
B.乙表示一定温度时,向不饱和的NaCl溶液中加入NaCl固体并搅拌
C.丙表示向质量和质量分数都相同的盐酸中分别加入锌和铁
D.丁表示向一定质量的氧化镁固体中逐渐加入稀盐酸
【答案】B
【解析】A、pH<7的溶液显酸性,且pH越大,酸性越弱,则向pH=3的某溶液中加水稀释,酸性会减
弱,pH会接近7,但不会等于7,更不会大于7,该选项图像不正确;
B、向不饱和的氯化钠溶液中加入氯化钠,开始时固体会继续溶解,溶质质量分数增大,但当溶液饱和
时,固体不再继续溶解,溶质质量分数不变,该选项图像正确;
C、由于最终金属过量,则消耗的盐酸的质量相同,根据氢元素守恒,则最终生成的氢气质量相同,又由
于 、 ,刚开始时消耗等质量的铁和
锌,铁生成的氢气较多,该选项图像不正确;
D、氧化镁和盐酸反应生成氯化镁和水,反应过程中溶液质量增大,但反应结束后,随着稀盐酸质量的增
加,溶液质量继续增大,该选项图像不正确。
故选B。
12.已知①中盛有一定量的碳酸钠溶液,根据如图所示的实验过程,下列说法不正确的是( )A.②中溶液为红色
B.③中溶液的溶质一定含有氢氧化钠
C.④中溶液中存在大量的Cl-、Na+、H+
D.加入过量稀盐酸后,③中观察到沉淀消失,溶液由红色变为无色、产生大量气泡
【答案】C
【解析】A、碳酸钠溶液呈碱性,能使无色酚酞变红,则②中溶液为红色,故A说法正确;
B、碳酸钠溶液和石灰水反应生成碳酸钙沉淀和氢氧化钠,所以③中溶液的溶质一定含有氢氧化钠,故B
说法正确;
C、加入过量的稀盐酸,稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,稀盐酸和氢氧化钠反应生成氯
化钠和水,所以④中溶液的溶质除酚酞外,有氯化钠、氯化钙和盐酸,故④ 溶液中存在大量的Cl−、
Na+、Ca2+、H+,故C说法错误;
D、碳酸钠溶液呈碱性,能使无色酚酞变红,则②中溶液为红色,当③中加入过量的稀盐酸,稀盐酸和碳
酸钙反应生成氯化钙、水和二氧化碳,稀盐酸和氢氧化钠反应生成氯化钠和水,③中观察到沉淀消失,产
生大量气泡,红色也会消失,故D说法正确;
故选:C。
二、综合题(共30分)
13.(8分)下图是实验室制取和收集气体的部分装置:
(1)仪器①的名称是 。
(2)实验室制取氧气,应选用的发生装置是 (填字母编号),反应的化学方程式是 。
(3)若G中装满水收集氧气,气体应该从 (填“a”或“b”)口进入。
(4)实验室常用装置B制取CO,选用的药品是 (填名称),其反应的化学方程式为 。若使
2
用装置D作为制取CO 的发生装置,与装置B比较,除了利用废物的优点外,请写出其他一个优点
2
,该装置使用铜丝网而不使用铁丝网盛放固体的原因是 (用化学方程式表示)。
【答案】(1)锥形瓶
(2) A(不唯一,和下个空保持一致)
(3)b
(4) 大理石和稀盐酸
控制反应的开始与停止【解析】(1)由图可知,仪器①为锥形瓶。
(2)实验室制取氧气的发生装置可选A或B或C,其中A为加热固体的反应,且试管口没有塞棉花,适
用于氯酸钾制取氧气,氯酸钾在二氧化锰催化作用下生成氯化钾和氧气,反应的化学方程式为:
;B、C为固液常温装置,适用于过氧化氢制取氧气,过氧化氢在二氧化锰催化
作用下生成水和氧气,反应的化学方程式为: 。
(3)氧气密度比水小,若G中装满水收集氧气,氧气应从b口通入。
(4)实验室用大理石和稀盐酸制取二氧化碳,大理石的主要成分为碳酸钙,碳酸钙和盐酸反应生成氯化
钙、水和二氧化碳,反应的化学方程式为: ;
装置D中,固体放在铜丝网中,关闭止水夹,产生的气体使装置中的压强增大,液体被压入去底塑料瓶
中,固液分离,反应停止,打开止水夹,液体重新进入,与固体接触,反应开始,则该装置能控制反应的
开始与停止;
由于铁和盐酸反应生成氯化亚铁和氢气,会使制取的二氧化碳不纯,反应的化学方程式为:
。
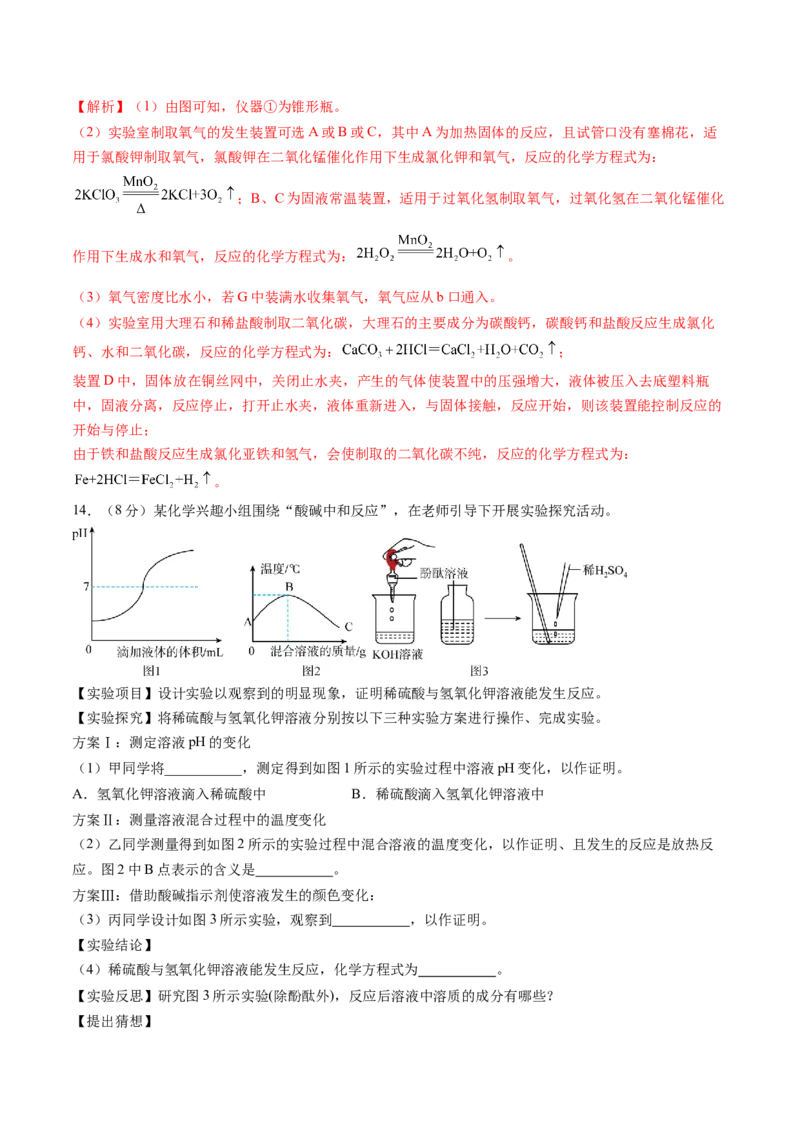
14.(8分)某化学兴趣小组围绕“酸碱中和反应”,在老师引导下开展实验探究活动。
【实验项目】设计实验以观察到的明显现象,证明稀硫酸与氢氧化钾溶液能发生反应。
【实验探究】将稀硫酸与氢氧化钾溶液分别按以下三种实验方案进行操作、完成实验。
方案Ⅰ:测定溶液pH的变化
(1)甲同学将___________,测定得到如图1所示的实验过程中溶液pH变化,以作证明。
A.氢氧化钾溶液滴入稀硫酸中 B.稀硫酸滴入氢氧化钾溶液中
方案Ⅱ:测量溶液混合过程中的温度变化
(2)乙同学测量得到如图2所示的实验过程中混合溶液的温度变化,以作证明、且发生的反应是放热反
应。图2中B点表示的含义是 。
方案Ⅲ:借助酸碱指示剂使溶液发生的颜色变化:
(3)丙同学设计如图3所示实验,观察到 ,以作证明。
【实验结论】
(4)稀硫酸与氢氧化钾溶液能发生反应,化学方程式为 。
【实验反思】研究图3所示实验(除酚酞外),反应后溶液中溶质的成分有哪些?
【提出猜想】(5)猜想Ⅰ: ;猜想Ⅱ:KSO 和HSO ;猜想Ⅲ:KSO 和KOH。
2 4 2 4 2 4
同学们经讨论后发现猜想Ⅲ不合理,其理由是 。
【实验操作】
(6)兴趣小组选用Fe O 粉末进行如下探究:取少量反应后的溶液于试管中,加入Fe O 粉末,根据观察
2 3 2 3
到的 的实验现象,同学们一致确定猜想Ⅱ是正确的。
【实验讨论】
(7)同学们认为可用物质___________(填字母序号)代替选用的Fe O 粉末,也能得到相同结果。
2 3
A.BaCl B.Zn C.KCO D.NaOH E.紫色石蕊溶液
2 2 3
【答案】(1)A
(2)KOH和稀HSO 恰好完全反应
2 4
(3)溶液红色变成无色
(4)HSO +2KOH=K SO +2H O
2 4 2 4 2
(5) 硫酸钾/K SO 溶液变成无色,说明溶液中不可能有KOH
2 4
(6)红色固体消失,溶液由无色变为黄色
(7)BCDE
【解析】(1)根据pH图像可知,pH由小到大,则是将氢氧化钾加到稀硫酸中,故选A ;
(2)酸碱中和是属于放热反应,当温度达到最高时,说明恰好完全反应,则图2中B点表示的含义是
KOH和稀HSO 恰好完全反应;
2 4
(3)氢氧化钾溶液呈碱性,能使酚酞溶液变红,滴加稀硫酸,观察到溶液由红色变为无色,证明酸碱发
生反应;
(4)稀硫酸与氢氧化钾反应生成硫酸钾和水,化学反应方程式为HSO +2KOH=K SO +2H O;
2 4 2 4 2
(5)①稀硫酸和氢氧化钾反应溶质成分有三种情况:恰好完全反应:KSO ;稀硫酸有剩余:HSO 和
2 4 2 4
KSO ;氢氧化钾有剩余:KOH和KSO ,故猜想I是KSO ;
2 4 2 4 2 4
②酚酞遇碱变红,溶液变成无色,说明溶液中不可能有KOH,故猜想Ⅲ不合理,其理由是溶液变成无色,
说明溶液中不可能有KOH;
(6)猜想Ⅱ正确,说明溶质成分是HSO 和KSO ,则取少量反应后的溶液于试管中,加入Fe O 粉末,
2 4 2 4 2 3
根据观察到的红色固体消失,溶液由无色变为黄色;
(7)A、HSO 和KSO 都能和BaCl 反应生成硫酸钡沉淀,无法证明硫酸存在;
2 4 2 4 2
B、Zn和稀硫酸反应生成硫酸锌和氢气,观察到有气泡产生,可以证明硫酸存在;
C、KCO 和稀硫酸反应生成硫酸钾,二氧化碳和水,观察到有气泡产生,可以证明硫酸存在;
2 3
D、NaOH和稀硫酸反应生成硫酸钠和水,烧杯中有酚酞,滴加氢氧化钠溶液不会立即变成红色,可以证
明硫酸存在;
E、紫色石蕊遇硫酸会变红,可以证明硫酸存在;
故选BCDE;
(8)过程见答案。
15.(7分)硝酸钙晶体[Ca(NO )·4H O,M=236]常用于电子、仪表及冶金工业[已知Ca(NO ) 溶液呈中
3 2 2 3 2
性]。一种利用CaO制备Ca(NO )·4H O的流程如下:
3 2 2(1)“制浆池”中发生反应的基本反应类型是 。
(2)“反应池”中逸出有刺激性气味的气体X,其化学式为 。
【提出问题】“反应池”混合物中溶质是什么?
【作出猜想】
(3)猜想一:
猜想二:含有Ca(NO ) 和NH NO ;
3 2 4 3
猜想三:含有Ca(NO ) 和Ca(OH)
3 2 2.
【实验探究】设计如下表所示实验方案,在两支试管中各取少量上层清液进行实验。
试管序号 实验操作 实验现象 实验结论
① 滴加NaOH溶液 Ⅰ: 猜想二不合理
② 滴加无色酚酞溶液 Ⅱ: 猜想一不合理,猜想三正确
(4)试管①的实验现象是 。
(5)试管②的实验现象是 。
【实验反思】有同学提出在试管②中“通入CO 气体”同样能得相同结论。
2
(6)写出你的观点及理由:
(7)“酸化池”中发生反应的化学方程式为 。
【答案】(1)化合
(2)NH
3
(3)只含Ca(NO )
3 2
(4)无明显现象
(5)溶液变红
(6)同意,CO 能与Ca(OH) 反应,不与硝酸钙反应
2 2
(7)Ca(OH) +2HNO =Ca(NO)+2H O
2 3 3 2 2
【解析】(1)“制浆池”中发生反应的为氧化钙与水反应生成氢氧化钙,反应符合多变一,属于化合反
应;
(2)硝酸铵与氢氧化钙发应产生硝酸钙、水和氨气,氨气有刺激性气味,化学式为:NH ;
3
(3)硝酸铵与氢氧化钙反应可能恰好完全反应,也可能某一种物质有剩余,结合猜想二、三,猜想一
为:只含有Ca(NO );
3 2
(4)氢氧化钠与硝酸铵反应产生硝酸钠、水和氨气,根据结论:猜想二不合理,可知溶液中不含硝酸
铵,故实验现象为:无明显现象;
(5)根据结论:猜想一不合理,猜想三正确,说明溶液中含有氢氧化钙,氢氧化钙溶液显碱性,能使酚酞溶液变红,所以实验现象为:溶液变红;
(6)二氧化碳与氢氧化钙反应产生白色沉淀碳酸钙,不与硝酸钙反应,故有同学提出在试管②中“通入
CO 气体”同样能得相同结论,是合理的;
2
(7)酸化池中加入的硝酸与过量的氢氧化钙反应生成硝酸钙和水,方程式为:
Ca(OH) +2HNO =Ca(NO)+2H O;
2 3 3 2 2
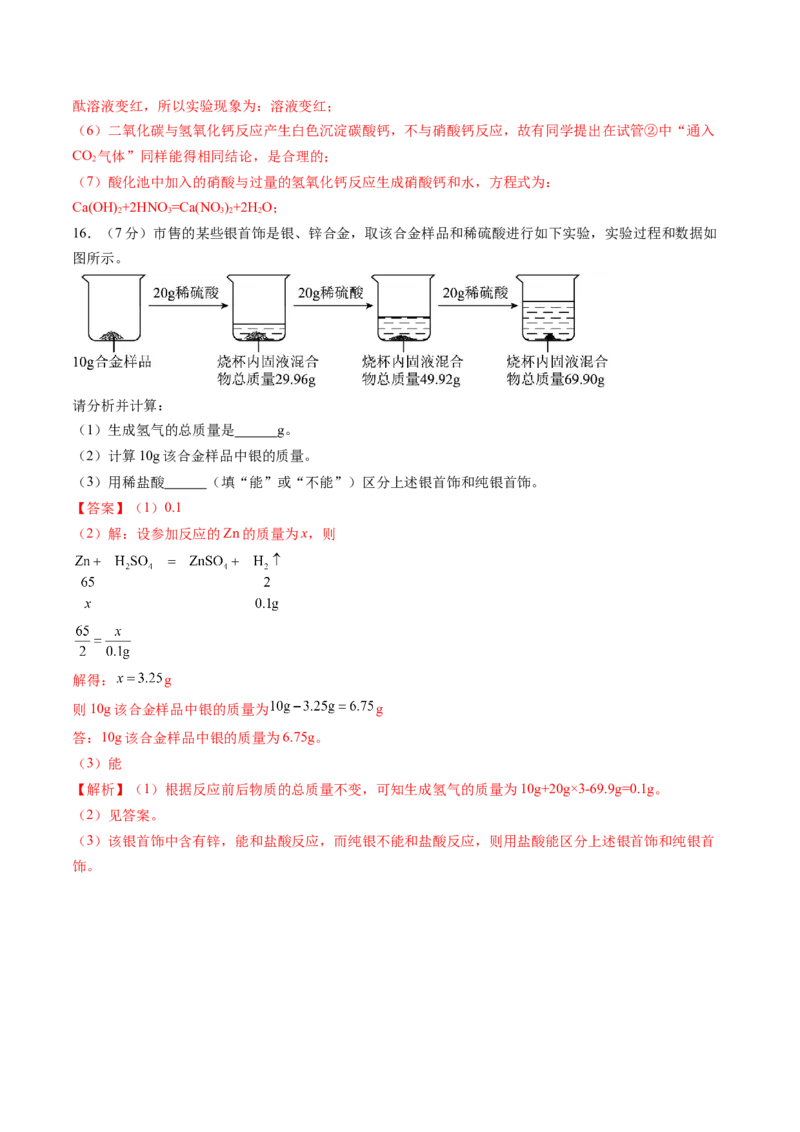
16.(7分)市售的某些银首饰是银、锌合金,取该合金样品和稀硫酸进行如下实验,实验过程和数据如
图所示。
请分析并计算:
(1)生成氢气的总质量是 g。
(2)计算10g该合金样品中银的质量。
(3)用稀盐酸 (填“能”或“不能”)区分上述银首饰和纯银首饰。
【答案】(1)0.1
(2)解:设参加反应的Zn的质量为x,则
解得: g
则10g该合金样品中银的质量为 g
答:10g该合金样品中银的质量为6.75g。
(3)能
【解析】(1)根据反应前后物质的总质量不变,可知生成氢气的质量为10g+20g×3-69.9g=0.1g。
(2)见答案。
(3)该银首饰中含有锌,能和盐酸反应,而纯银不能和盐酸反应,则用盐酸能区分上述银首饰和纯银首
饰。