文档内容
第九讲 常见的盐
模块一 常见的盐的用途
知识精讲
1.简单回顾盐的含义
盐:指一类组成里含有金属离子(或NH +)和酸根离子的化合物。
4
盐的命名:
①‘某化某’:如NaCl — 氯化钠,写出名字KCl: ;AgCl: ;
②‘某酸某’:如NaCO — 碳酸钠,写出名字CaCO: ;BaSO: ;
2 3 3 4
思考与交流
1.下列物质中哪些是酸?哪些是碱?哪些是盐?在下列横线上写上化学式。
CaCO HCl NaCl Na CO NaOH NaHCO
3 2 3 3
HSO Ca(OH) Cu(OH) NH •HO H CO
2 4 2 2 3 2 2 3
(1)酸:
(2)碱:
(3)盐:
2.生活中常见的盐
氯化钠 碳酸钠 碳酸氢钠 碳酸钙
化学式 NaCl NaCO NaHCO CaCO
2 3 3 3
俗称 苏打、纯碱 小苏打 石灰石、大理石
溶解性 36g 21.2g 9.6g 0.0013g
(20℃) 易溶 易溶 可溶 难溶
中性 碱性 碱性 中性
水溶液的酸碱性
发酵粉、治疗胃酸过
用途 调味剂、防腐剂 洗涤剂、生产玻璃 建筑材料、补钙剂
多
思考与交流
(1)NaCO 俗称纯碱,水溶液呈碱性,它属于碱,对吗?
2 3
(2)碱性溶液能使无色酚酞溶液变红,则能使酚酞变红的都是碱,对吗?
(3)食盐的主要成分是NaCl,则NaCl就是食盐,对吗?
(4)有人误食用工业盐而中毒,工业盐和食用盐是同种物质吗?
资料卡片——NaCl的用途·
(1)生活上:调味剂,防腐剂(腌制蔬菜、肉蛋等);
(2)农业上:用10%~20%的NaCl溶液选种;
(3)医疗上:生理盐水(100 mL生理盐水含0.9g NaCl)
(4)工业上:制烧碱。反应原理:2NaCl+2HO 2NaOH+H ↑+Cl↑
2 2 2归纳总结——常见物质的俗名
化学式
俗名 生石灰 熟石灰 石灰石、大理石 铁红、赤铁矿 磁铁矿
化学式
俗名 火碱、苟性钠、烧碱 胃酸 生理盐水 纯碱、苏打 小苏打
根据俗名,书写化学式。
经典例题
常见盐的俗名
【例1】下列有关物质的化学式、俗名、类别不完全对应的是( )
A.NaOH 烧碱 碱
B.CaO 生石灰 氧化物
C.NaCO 纯碱 碱
2 3
D.NaCl 食盐 盐
【例2】下列物质的名称、俗称、物质分类完全对应正确的是( )
A.碳酸氢钠、苏打、盐
B.氧化钙、熟石灰、氧化物
C.乙醇、酒精、碱
D.二氧化碳、干冰、化合物
【例3】我国海水晒盐具有悠久的历史,所得“盐”的主要成分是( )
A.NaSO B.NaCl C.CaCl D.NaCO
2 4 2 2 3
【例4】下列各组物质名称不代表同一物质的一组是( )
A.氯化钠、盐 B.氢氧化钠、苛性钠
C.碳酸钠、纯碱 D.碳酸氢钠、小苏打
常见盐的用途
【例1】下列关于物质用途的说法中,正确的是( )
A.碳酸钙用作发酵粉 B.苏打用作建筑材料
C.亚硝酸钠用于食品调味 D.小苏打用于治疗胃酸过多
【例2】中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是( )
A.食醋 B.烧碱 C.纯碱 D.生石灰
【例3】关于钙等氧化物、氢氧化物和碳酸盐的说法不正确的是( )
A.氢氧化钙俗称熟石灰,可以由生石灰与水反应得到
B.熟石灰和生石灰都可以与二氧化碳发生化合反应生成碳酸钙
C.氢氧化钙可用于改良酸性土壤也可用于配制农药波尔多液
D.碳酸钙难溶于水,能溶于胃酸,可以用作补钙剂
【例4】下表物质的名称、化学式、物质类别及用途都正确的一组是:( )
名称 化学式 物质类别 主要用途
A 干冰 CO 金属氧化物 人工降雨
2
B 纯碱 NaHCO 盐 做面点发酵剂
3
C 生石灰 Ca(OH) 碱 改良酸性土壤
2
D 盐酸 HCl 酸 清洗铁锈
模块二 常见盐的化学性质
知识精讲
知识点二 盐的化学性质
1.盐与酸的反应
思考与交流制取CO 时,是选用碳酸钙与稀盐酸反应制取的。反应过程产生大量气泡:
2
该反应方程式:CaCO +2HCl==2CaCl+H O +CO ↑
3 2 2
实质上,这个反应的方程式是分两步进行的:
① CaCO +2HCl==2CaCl+H CO
3 2 3
② HCO == H O+CO↑(碳酸不稳定,会分解)
2 3 2 2
将反应① + ②可得出总反应式:CaCO +2HCl==2CaCl+H O +CO ↑
3 2 2
思考下列问题:
(1)CaCO 属于 类(填‘酸’、‘碱’、‘盐’),稀HCl属于 类;它们能反应,说明盐
3
类能与酸反应。
(2)那NaCO、NaHCO 也属于盐类,它也能与稀盐酸反应吗?
2 3 3
实验一
向盛有0.5g Na CO 的试管中加入2 mL稀盐酸,迅速用带导管的橡胶塞塞紧试管口,并将导管的另一端通
2 3
入盛有澄清石灰水的烧杯中,如下图,观察现象。再用0.5g NaHCO 替代碳酸钠,重复实验:
3
碳酸钠+盐酸 碳酸氢钠+盐酸
试管 烧杯 试管 烧杯
现象
迅速反应,产生大量气泡, 反应更迅速,产生的气泡更多,试管中的澄清石灰水变浑浊 试管中的澄清石灰水变浑浊
结论 在相同条件下,NaHCO 与稀盐酸的反应比NaCO 的更剧烈,且生成的气体更多。
3 2 3
分析 NaCO、NaHCO 与盐酸反应,产生了二氧化碳、NaCl、HO
2 3 3 2
化学方程式
拓展延伸——CO 2-离子的检验方法
3
CO2- 无色气体 石灰水变浑浊
3
(1)检验原理:组成中含有CO2-(或HCO -)的盐能与酸反应生成气体CO:
3 3 2
(2)检验试剂:稀HCl、澄清石灰水
(3)检验方法:向待测液中加入稀HCl,有气泡产生,将产生的气体通入澄清石灰水中,若石灰水变
浑浊,则该物质中含有CO2-(或HCO -)。
3 3
如:可以鉴别NaCO 和NaCl粉末。
2 3
及时小练
【练1】欲证明生石灰中含有未烧透的石灰石,最简单的方法是( )
A.加热 B. 滴加稀盐酸 C. 加水溶解 D.滴加酚酞试液
2.盐与碱的反应
思考与交流
某天小明想拿发酵粉NaHCO 来做馒头,但是厨房还有除污剂NaCO,而碳酸钠和碳酸氢钠外观都是
3 2 3
白色粉末,那如何鉴别它们呢?
NaCO NaHCO
2 3 3
(1)若向两种粉末中,加入食醋,会有什么现象?
(2)若加入澄清石灰水,现象是怎样的呢?
实验二实验内容 实验现象 化学方程式
向盛有碳酸钠溶液
的试管里滴入澄清 溶液变浑浊 NaCO+Ca(OH) == CaCO ↓+2NaOH
2 3 2 3
石灰水
NaCO + Ca(OH) == CaCO ↓ + 2NaOH
2 3 2 3
化合物 + 化合物 = 化合物 + 化合物
AB + CD = AD + BC
由两种化合物相互交换成分,生成另外两种化合物的反应,叫复分解反应。
农业上用CuSO 溶液和澄清石灰水Ca(OH) 制取农药‘波尔多液’,试着书写反应的化学方程式:
4 2
。
3.盐与盐的反应
思考与交流依然思考如何鉴别发酵粉NaHCO 、除污剂NaCO?
3 2 3
NaCO NaHCO
2 3 3
(1)若向两种粉末中,加入稀HCl,会有什么现象?
Na CO+2HCl=2NaCl+H O+CO↑
2 3 2 2
NaHCO +HCl=NaCl+H O+CO↑
3 2 2
都产生气泡,鉴别不出。
(2)若加入CaCl 溶液,现象是怎样的呢?(已知Ca(HCO ) 能溶于水,CaCO 难溶)
2 3 2 3
发酵粉无现象,除污剂有沉淀。
NaCO + CaCl == CaCO ↓ + 2NaCl
2 3 2 3
2NaHCO + CaCl → Ca(HCO ) + 2NaCl(此反应溶液中离子没有变化,反应不能发生)
3 2 3 2
用BaCl 溶液也能鉴别它们,(已知Ba(HCO ) 能溶于水,BaCO 难溶)
2 3 2 3
模仿CaCl 与碳酸钠的反应,试着书写BaCl 和NaCO 的反应方程式: 。
2 2 2 3
【答案】NaCO + BaCl == BaCO ↓ + 2NaCl
2 3 2 3
经典例题
盐与酸的反应
【例1】(2020·广东省考)除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )
物 质 杂质(少量) 加入试剂、方法
A KCl MnO 加水溶解、过滤、烘干
2
B NaCl NaCO 加过量的盐酸,加热蒸发
2 3
C Cu(NO ) AgNO 加水溶解后加足量铜粉,过滤、将滤渣烘干
3 2 3
D N O 通过足量的灼热碳粉
2 2
【例2】小明想探究家中厨房用某种洗涤剂的成分,他将洗涤剂的粉末带到学校寻求老师的帮助。在老师
指导下,小明进行了大胆的猜想与实验:
(提出问题)洗涤剂中主要含有哪些物质?(做出猜想)小明根据所学酸碱盐知识做出以下猜想:
猜想一:可能含有CO ,
猜想二:可能含有_________,
猜想三:可能含有CO 和OH-。
(进行实验)实验一:取少量粉末,加水溶解得到无色溶液,滴加紫色石蕊溶液后,溶液变为_________
色,说明洗涤剂的溶液显碱性。
实验二:取少量粉末,滴加足量的稀盐酸,有无色无味气体产生。将生成气体通入澄清石灰水,观察到
,证实洗涤剂中含有CO 。
(查阅资料)小明查阅资料得知(1)该洗涤剂中含有NaCO、NaOH等;
2 3
(2)NaCO 溶液显碱性。
2 3
(小结反思)实验二中产生气体的化学方程式为____________________。
(实验验证)该洗涤剂中还含有NaOH。
【例3】有一包白色固体样品,可能含有CaCO 、NaCO、CaCl 中的两种,为确定其组成,进行如下实验:
3 2 3 2
步骤I:取少量样品于烧杯中,加足量水,充分搅拌,静置,有白色固体剩余。
步骤II:过滤步骤I的混合物,得到滤液和滤渣。
步骤III:取少量滤液于试管中,再加入稀盐酸,有无色气泡产生。
根据上述实验,回答下列问题:
(1)步骤I中的白色固体是_____;步骤III的无色气泡是_____。
(2)分析上述实验过程,关于样品的组成,可以得到的结论是_____。
盐与碱的反应
【例1】(2020·广东深圳)小深同学用思维导图梳理了NaCO 的相关知识,其中描述错误的是( )
2 3
A.A B.B C.C D.D
【例2】除去下列物质中所含的少量杂质,方法正确的是( )
物 质 所含杂质 除杂质的方法A NaCO NaHCO 加水溶解,过滤
2 3 3
B NaCl溶液 NaCO 加入过量稀盐酸,加热蒸发
2 3
C CaCl 溶液 稀盐酸 加入过量氢氧化钙,过滤
2
D NaOH溶液 NaCO 加入适量的澄清Ca(OH)
2 3 2
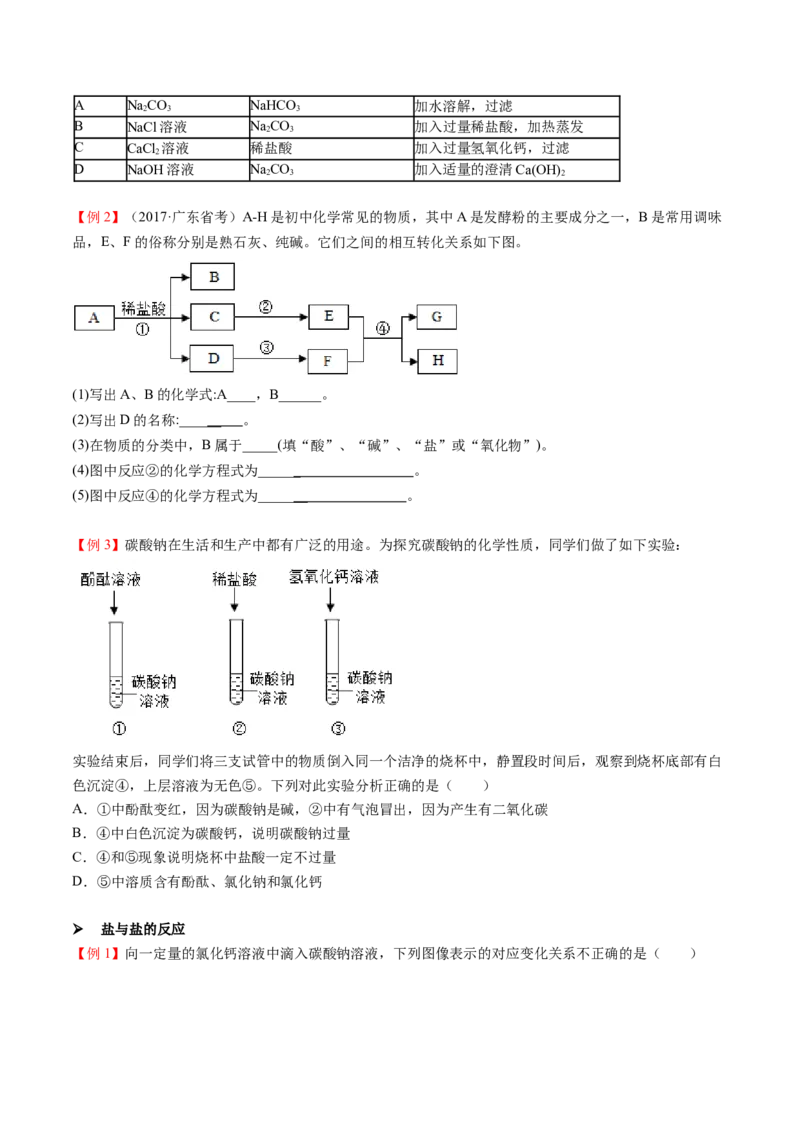
【例2】(2017·广东省考)A-H是初中化学常见的物质,其中A是发酵粉的主要成分之一,B是常用调味
品,E、F的俗称分别是熟石灰、纯碱。它们之间的相互转化关系如下图。
(1)写出A、B的化学式:A____,B______。
(2)写出D的名称:______ 。
(3)在物质的分类中,B属于_____(填“酸”、“碱”、“盐”或“氧化物”)。
(4)图中反应②的化学方程式为______ 。
(5)图中反应④的化学方程式为_______ 。
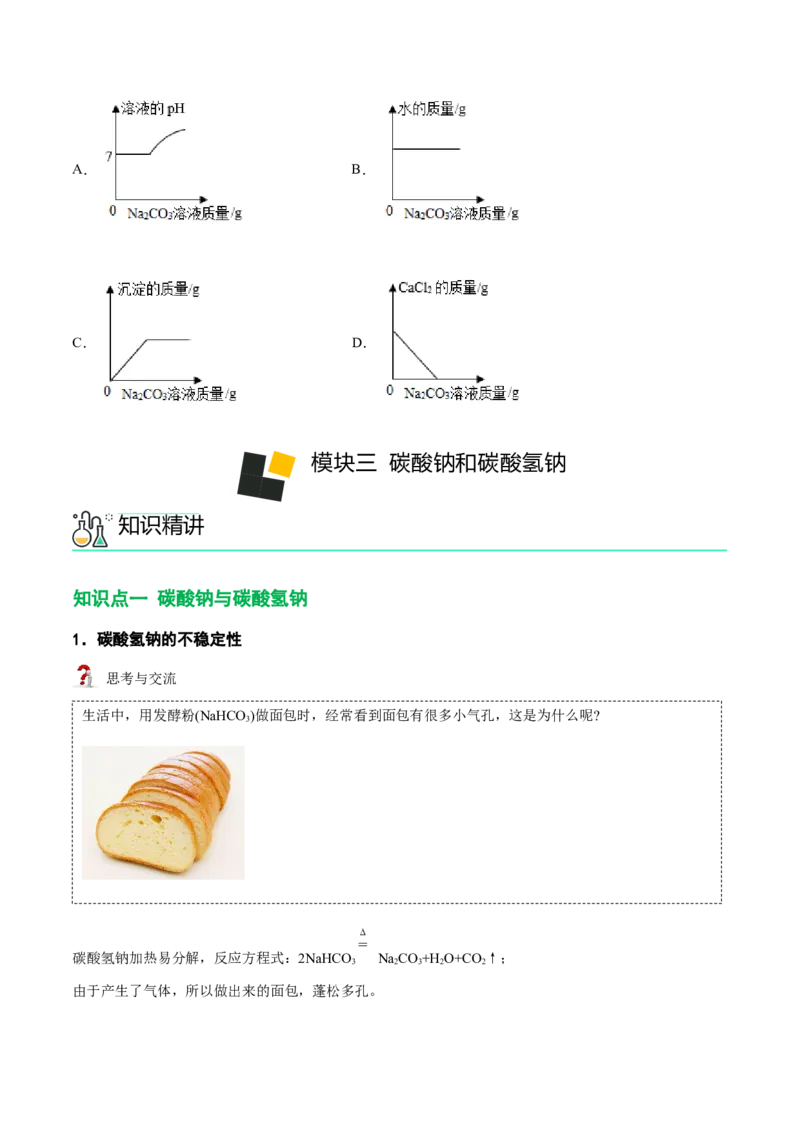
【例3】碳酸钠在生活和生产中都有广泛的用途。为探究碳酸钠的化学性质,同学们做了如下实验:
实验结束后,同学们将三支试管中的物质倒入同一个洁净的烧杯中,静置段时间后,观察到烧杯底部有白
色沉淀④,上层溶液为无色⑤。下列对此实验分析正确的是( )
A.①中酚酞变红,因为碳酸钠是碱,②中有气泡冒出,因为产生有二氧化碳
B.④中白色沉淀为碳酸钙,说明碳酸钠过量
C.④和⑤现象说明烧杯中盐酸一定不过量
D.⑤中溶质含有酚酞、氯化钠和氯化钙
盐与盐的反应
【例1】向一定量的氯化钙溶液中滴入碳酸钠溶液,下列图像表示的对应变化关系不正确的是( )A. B.
C. D.
模块三 碳酸钠和碳酸氢钠
知识精讲
知识点一 碳酸钠与碳酸氢钠
1.碳酸氢钠的不稳定性
思考与交流
生活中,用发酵粉(NaHCO )做面包时,经常看到面包有很多小气孔,这是为什么呢?
3
碳酸氢钠加热易分解,反应方程式:2NaHCO NaCO+H O+CO↑;
3 2 3 2 2
由于产生了气体,所以做出来的面包,蓬松多孔。2.候式制碱法
(1)发明人:侯德榜。
(2)制碱原理:向饱和的食盐水中,先通入足量的氨气,再加入二氧化碳,生成碳酸氢钠。由于氯化钠
是饱和溶液,生成的碳酸氢钠溶解度小于氯化钠,所以碳酸氢钠以沉淀析出。
反应方程式:NaCl + CO +NH+H O=NaHCO ↓+NHCl;
2 3 2 3 4
2NaHCO =Na CO+H O+CO↑
3 2 3 2 2
知识点二 碳酸钙与碳酸氢钙的转化
奇妙的钟乳石
石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,反应生成溶解性更大的碳酸氢钙。模仿碳酸钠
与二氧化碳的反应方程式,书写碳酸氢钙形成的化学方程式: 。
遇热后,溶解在水中的碳酸氢钙就会分解,重新生成碳酸钙,同时放出二氧化碳,书写化学方程式:
。
经典例题
碳酸氢钠和碳酸氢钠
【例1】已知:CO+ CaCO+ H O = Ca(HCO ),Ca(HCO ) 能溶于水。向澄清石灰水中通入过量的CO,
2 3 2 3 2 3 2 2
下列图示能正确表示该过程中各个量之间关系的是( )A. B.
C. D.
【例2】(2020·广东广州)将足量NH 和CO 依次通入饱和食盐水,发生反应:
3 2
① ;② 。
下列说法正确的是( )
A.总的化学方程式为
B.上述反应过程中观察不到明显现象
C.反应②是有沉淀生成的复分解反应
D.上述反应中有元素化合价发生变化
【例3】NaCO 和 NaHCO 有相似的化学性质,都能与酸、某些碱反应。
2 3 3
(查阅资料)获得如下信息:
①氯化钙溶液呈中性,与碳酸氢钠溶液混合不发生反应。
②碳酸钠稳定,而NaHCO 受热分解: 。
3
(1)NaHCO 遇到盐酸的化学反应方程式为_____。
3
(2)工业上用碳酸钠制烧碱的化学反应方程式为_____。
(3)同学们在探究其化学性质实验后,将剩余固体药品集中放在烧杯中。小明为了弄清剩余固体的成分,
进行了如下的探究:
(提出猜想)剩余固体是:I、NaCO;Ⅱ、NaHCO ;Ⅲ、_____。
2 3 3
(进行实验)
操作 现象 结论
①取少量剩余固体于试管中,加入足量 溶液由无色变_____。 剩余固体一定有:水,充分溶解后,滴加几滴酚酞溶液。
_____。
②取适量剩余固体于试管中,固定在铁架 白色固体质量减少,试管内壁
台上,充分加热。 有较多水珠出现。
模块四 酸、碱、盐的化学性质
知识精讲
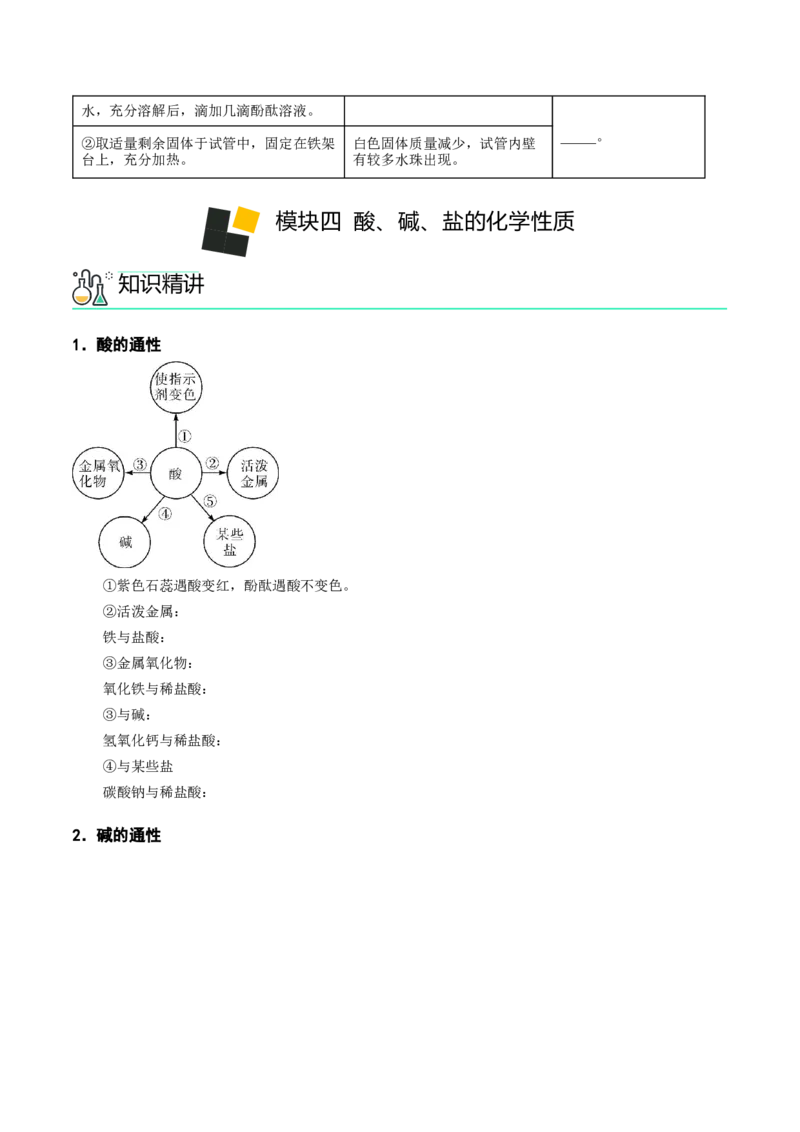
1.酸的通性
①紫色石蕊遇酸变红,酚酞遇酸不变色。
②活泼金属:
铁与盐酸:
③金属氧化物:
氧化铁与稀盐酸:
③与碱:
氢氧化钙与稀盐酸:
④与某些盐
碳酸钠与稀盐酸:
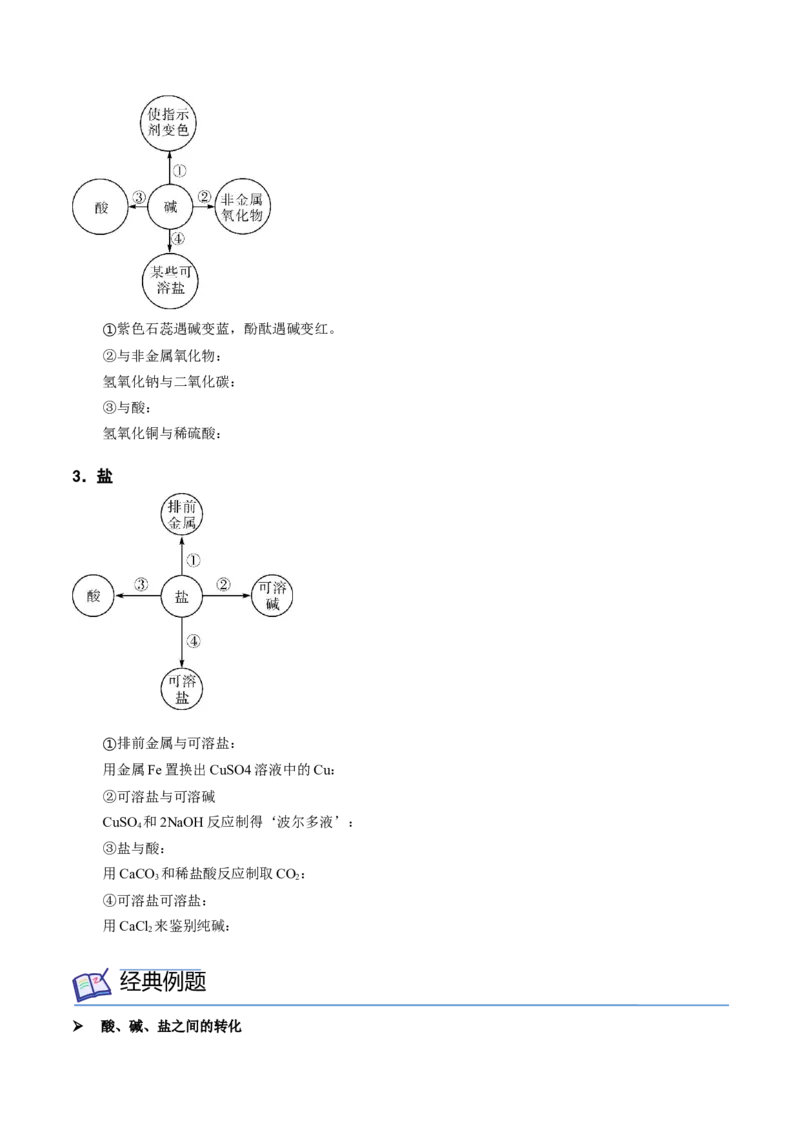
2.碱的通性①紫色石蕊遇碱变蓝,酚酞遇碱变红。
②与非金属氧化物:
氢氧化钠与二氧化碳:
③与酸:
氢氧化铜与稀硫酸:
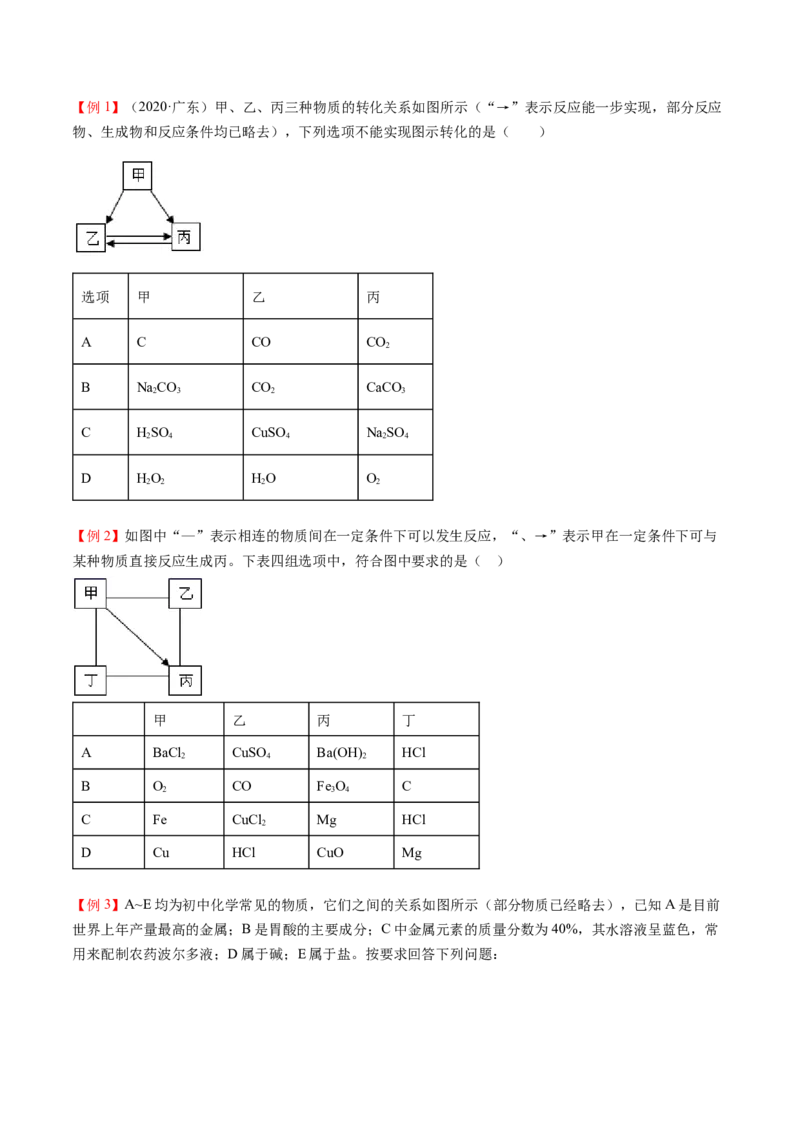
3.盐
①排前金属与可溶盐:
用金属Fe置换出CuSO4溶液中的Cu:
②可溶盐与可溶碱
CuSO 和2NaOH反应制得‘波尔多液’:
4
③盐与酸:
用CaCO 和稀盐酸反应制取CO:
3 2
④可溶盐可溶盐:
用CaCl 来鉴别纯碱:
2
经典例题
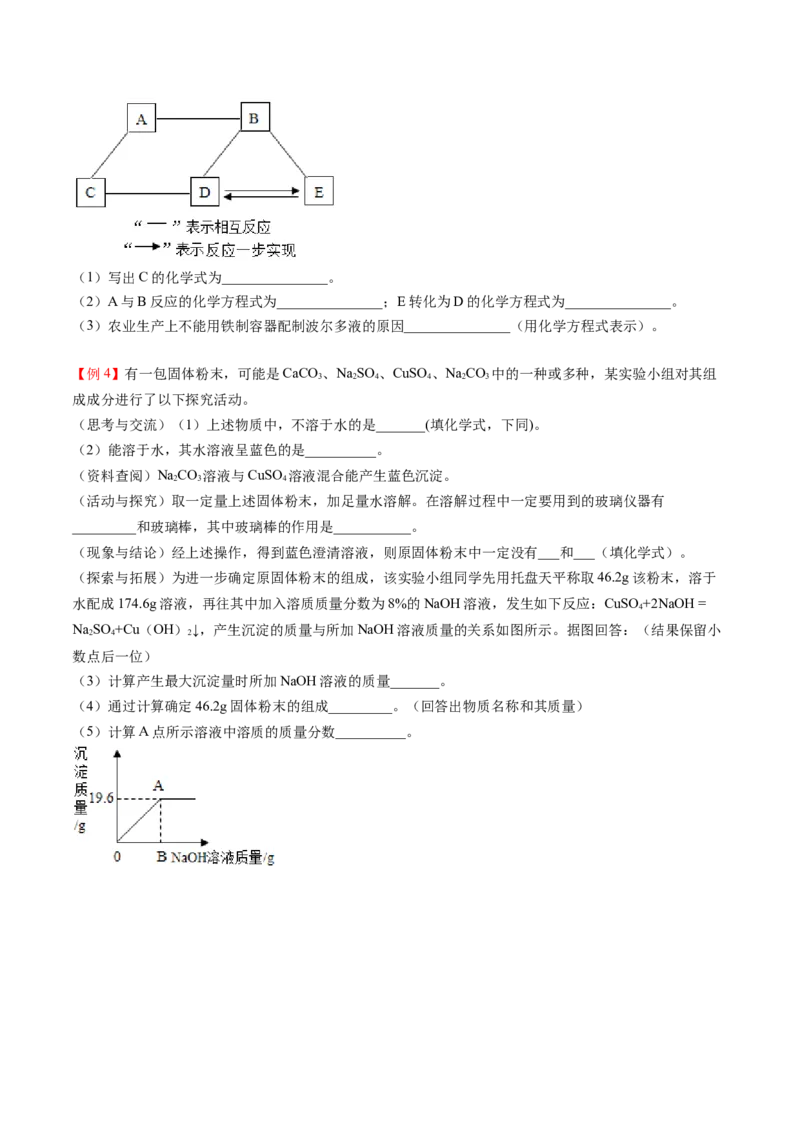
酸、碱、盐之间的转化【例1】(2020·广东)甲、乙、丙三种物质的转化关系如图所示(“→”表示反应能一步实现,部分反应
物、生成物和反应条件均已略去),下列选项不能实现图示转化的是( )
选项 甲 乙 丙
A C CO CO
2
B NaCO CO CaCO
2 3 2 3
C HSO CuSO NaSO
2 4 4 2 4
D HO HO O
2 2 2 2
【例2】如图中“—”表示相连的物质间在一定条件下可以发生反应,“、→”表示甲在一定条件下可与
某种物质直接反应生成丙。下表四组选项中,符合图中要求的是( )
甲 乙 丙 丁
A BaCl CuSO Ba(OH) HCl
2 4 2
B O CO Fe O C
2 3 4
C Fe CuCl Mg HCl
2
D Cu HCl CuO Mg
【例3】A~E均为初中化学常见的物质,它们之间的关系如图所示(部分物质已经略去),已知A是目前
世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为40%,其水溶液呈蓝色,常
用来配制农药波尔多液;D属于碱;E属于盐。按要求回答下列问题:(1)写出C的化学式为_______________。
(2)A与B反应的化学方程式为_______________;E转化为D的化学方程式为_______________。
(3)农业生产上不能用铁制容器配制波尔多液的原因_______________(用化学方程式表示)。
【例4】有一包固体粉末,可能是CaCO 、NaSO 、CuSO 、NaCO 中的一种或多种,某实验小组对其组
3 2 4 4 2 3
成成分进行了以下探究活动。
(思考与交流)(1)上述物质中,不溶于水的是_______(填化学式,下同)。
(2)能溶于水,其水溶液呈蓝色的是__________。
(资料查阅)NaCO 溶液与CuSO 溶液混合能产生蓝色沉淀。
2 3 4
(活动与探究)取一定量上述固体粉末,加足量水溶解。在溶解过程中一定要用到的玻璃仪器有
_________和玻璃棒,其中玻璃棒的作用是___________。
(现象与结论)经上述操作,得到蓝色澄清溶液,则原固体粉末中一定没有___和___(填化学式)。
(探索与拓展)为进一步确定原固体粉末的组成,该实验小组同学先用托盘天平称取46.2g该粉末,溶于
水配成174.6g溶液,再往其中加入溶质质量分数为8%的NaOH溶液,发生如下反应:CuSO +2NaOH =
4
NaSO +Cu(OH)↓,产生沉淀的质量与所加NaOH溶液质量的关系如图所示。据图回答:(结果保留小
2 4 2
数点后一位)
(3)计算产生最大沉淀量时所加NaOH溶液的质量_______。
(4)通过计算确定46.2g固体粉末的组成_________。(回答出物质名称和其质量)
(5)计算A点所示溶液中溶质的质量分数__________。专项训练
【训1】下列盐的用途中,错误的是( )
A.用含亚硝酸钠的工业盐制香肠 B.用碳酸钙做补钙剂
C.用氯化钠配制生理盐水 D.用碳酸氢钠做焙制糕点的发酵粉
【训2】下列关于NaCO 的认识,正确的是( )
2 3
A.组成:含有氧元素,所以是氧化物
B.性质:与碳酸性质相似,受热易分解
C.用途:俗名纯碱、显碱性,可用作洗涤剂
D.生产:可由钠单质与二氧化碳化合而成
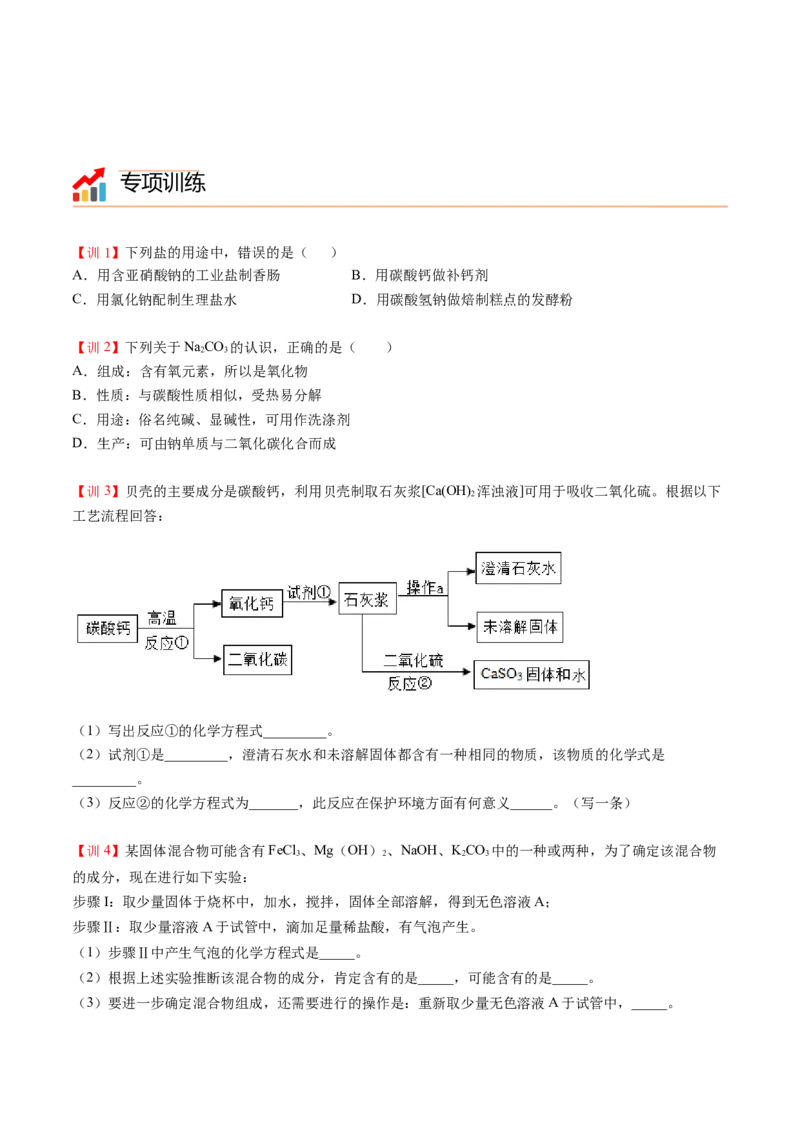
【训3】贝壳的主要成分是碳酸钙,利用贝壳制取石灰浆[Ca(OH) 浑浊液]可用于吸收二氧化硫。根据以下
2
工艺流程回答:
(1)写出反应①的化学方程式_________。
(2)试剂①是_________,澄清石灰水和未溶解固体都含有一种相同的物质,该物质的化学式是
_________。
(3)反应②的化学方程式为_______,此反应在保护环境方面有何意义______。(写一条)
【训4】某固体混合物可能含有FeCl 、Mg(OH)、NaOH、KCO 中的一种或两种,为了确定该混合物
3 2 2 3
的成分,现在进行如下实验:
步骤I:取少量固体于烧杯中,加水,搅拌,固体全部溶解,得到无色溶液A;
步骤Ⅱ:取少量溶液A于试管中,滴加足量稀盐酸,有气泡产生。
(1)步骤Ⅱ中产生气泡的化学方程式是_____。
(2)根据上述实验推断该混合物的成分,肯定含有的是_____,可能含有的是_____。
(3)要进一步确定混合物组成,还需要进行的操作是:重新取少量无色溶液A于试管中,_____。提分作业
1.下列物质的俗称、化学式及类别对应正确的是( )
A.水银—Ag—单质 B.小苏打—NaHCO —盐
3
C.火碱—Ba(OH)—碱 D.纯碱—NaCO—碱
2 2 3
2.下表中的物质、主要成分的化学式及用途三者对应关系正确的是( )
选项 物质 主要化学成分 用途
A 烧碱 NaOH 可作袋装食品的干燥剂
B 大理石 CaCO 可作建筑材料
3
C 石灰水 CaO 可改良酸性土壤
D 苏打 NaHCO 用于治疗胃酸过多症
3
3.“分类”可以使人们有序的研究物质,以下物质的分类正确的是( )
A.单质:汞、冰
B.碱:纯碱、烧碱
C.盐:小苏打、氯化铵
D.纯净物:澄清石灰水、液氧
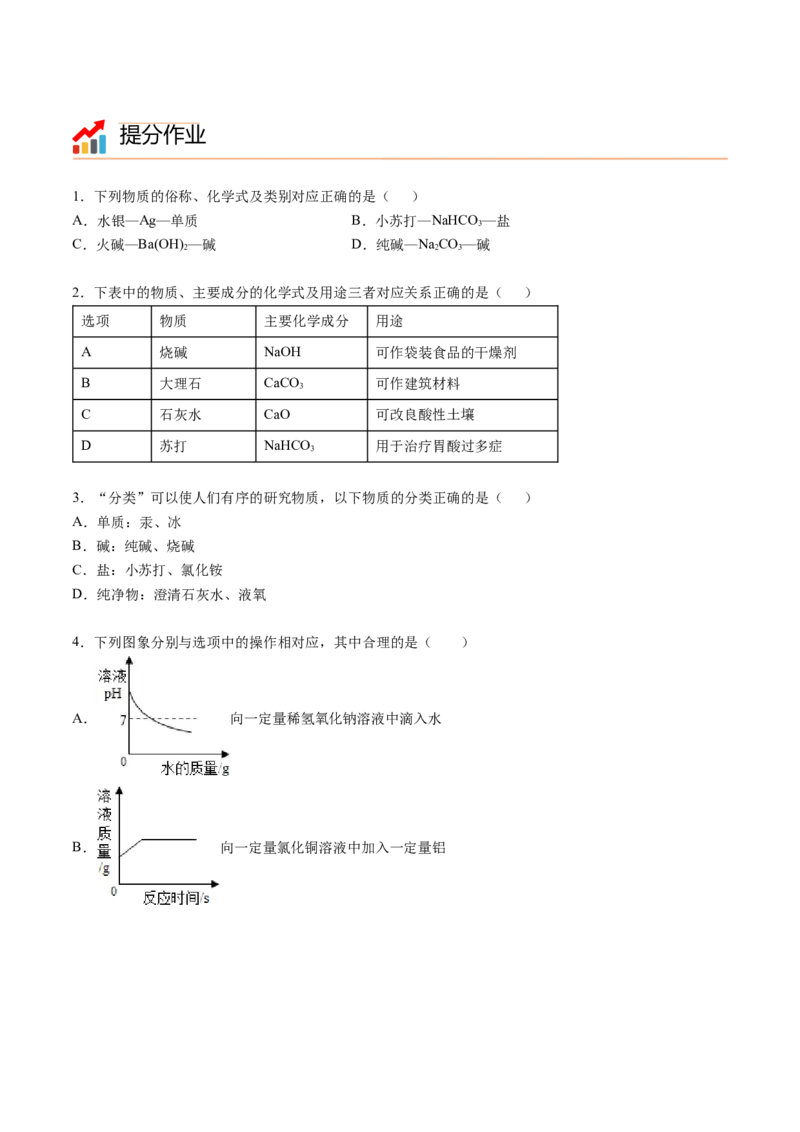
4.下列图象分别与选项中的操作相对应,其中合理的是( )
A. 向一定量稀氢氧化钠溶液中滴入水
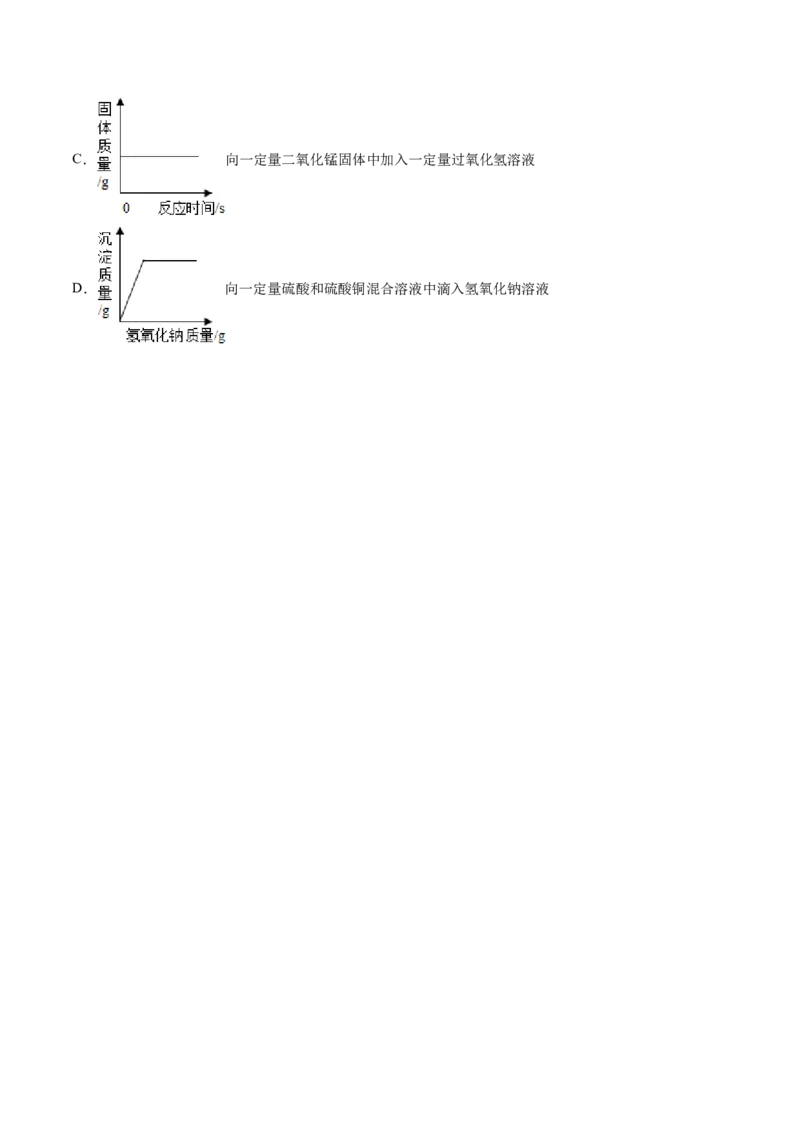
B. 向一定量氯化铜溶液中加入一定量铝C. 向一定量二氧化锰固体中加入一定量过氧化氢溶液
D. 向一定量硫酸和硫酸铜混合溶液中滴入氢氧化钠溶液