文档内容
石室中学高2026届高三下期化学定时练习
本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
注意事项:
1.答题前,务必将自己的姓名、准考证号和座位号填写在答题卡规定位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦擦干净后,再
选涂其他答案标号。
3.答非选择题时,必须使用0.5毫米黑色签字笔,将答案书写在答题卡规定的位置上。
4.所有题目必须在答题卡上作答,在试题卷上答题无效。
可能用到的相对原子质量:Li-7 S-16 Zn-65
第I卷(选择题,共45分)
一.选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是最符合题
目要求的。)
1.化学与人类的生活密切相关。下列叙述不正确的是
A.医用软膏中的“凡士林”,其主要成分是含碳原子数较多的烷烃
B.硝酸铵是一种高效氮肥,其性质稳定,可以直接施用
C.氯化镁、硫酸钙都是制作豆腐常用的凝固剂
D.聚乙烯微孔薄膜用于制造饮用水分离膜
2.下列与物质性质相关的说法正确的是
A.苯酚可用作消毒剂,因其能使蛋白质变性
B.SO 能使酸性KMnO 溶液褪色,因其具有漂白性
2 4
C.某溶液焰色试验呈黄色,说明其溶质是钠盐
D.向某溶液中滴加浓HCl,产生的气体能使品红褪色,说明该溶液中含SO 2-或HSO -
3 3
3.下列化学用语或图示正确的是
A.NaCl晶体的晶胞:
B. 二氧化硅的分子式:SiO
2
C.某物质的核磁共振氢谱图:
D.O原子的外围电子轨道表示式为:
2s 2p
4.奥司他韦是目前治疗流感的常用药物之一,其活性成分如图所示(实楔形线表示其所连接的基团在纸平面
上方,虚楔形线表示其所连接的基团在纸平面下方)。下列有关叙述正确的是
A.奥司他韦分子中含有的官能团有4种
B.1mol该有机物在镍催化下最多能与2molH 反应
2
C.该物质不存在含苯环的同分异构体
D.将分子结构中的虚、实楔形线互换,会影响药物的吸收和功效
1
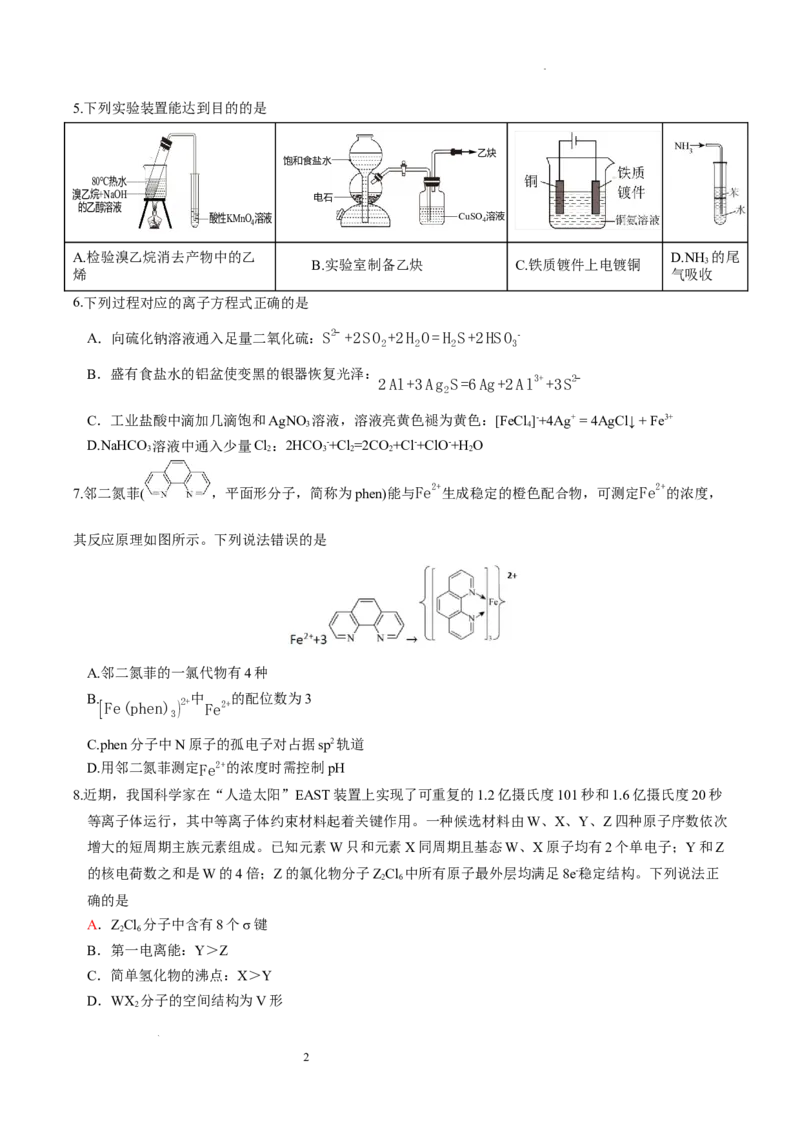
学科网(北京)股份有限公司5.下列实验装置能达到目的的是
乙炔
饱和食盐水
80℃热水
溴乙烷+NaOH
电石
的乙醇溶液
酸性KMnO
4
溶液 CuSO 4溶液
A.检验溴乙烷消去产物中的乙 D.NH 的尾
B.实验室制备乙炔 C.铁质镀件上电镀铜 3
烯 气吸收
6.下列过程对应的离子方程式正确的是
A.向硫化钠溶液通入足量二氧化硫:S2− +2SO +2H O=H S+2HSO -
2 2 2 3
B.盛有食盐水的铝盆使变黑的银器恢复光泽:
2Al+3Ag S=6Ag+2Al3++3S2−
2
C.工业盐酸中滴加几滴饱和AgNO 溶液,溶液亮黄色褪为黄色:[FeCl ]-+4Ag+ = 4AgCl↓ + Fe3+
3 4
D.NaHCO 溶液中通入少量Cl:2HCO -+Cl=2CO +Cl-+ClO-+H O
3 2 3 2 2 2
7.邻二氮菲( ,平面形分子,简称为phen)能与Fe2+生成稳定的橙色配合物,可测定Fe2+的浓度,
其反应原理如图所示。下列说法错误的是
A.邻二氮菲的一氯代物有4种
B. [Fe(phen) ) 2+ 中 Fe2+ 的配位数为3
3
C.phen分子中N原子的孤电子对占据sp2轨道
D.用邻二氮菲测定Fe2+的浓度时需控制pH
8.近期,我国科学家在“人造太阳”EAST装置上实现了可重复的1.2亿摄氏度101秒和1.6亿摄氏度20秒
等离子体运行,其中等离子体约束材料起着关键作用。一种候选材料由W、X、Y、Z四种原子序数依次
增大的短周期主族元素组成。已知元素W只和元素X同周期且基态W、X原子均有2个单电子;Y和Z
的核电荷数之和是W的4倍;Z的氯化物分子ZCl 中所有原子最外层均满足8e-稳定结构。下列说法正
2 6
确的是
A.ZCl 分子中含有8个σ键
2 6
B.第一电离能:Y>Z
C.简单氢化物的沸点:X>Y
D.WX 分子的空间结构为V形
2
2
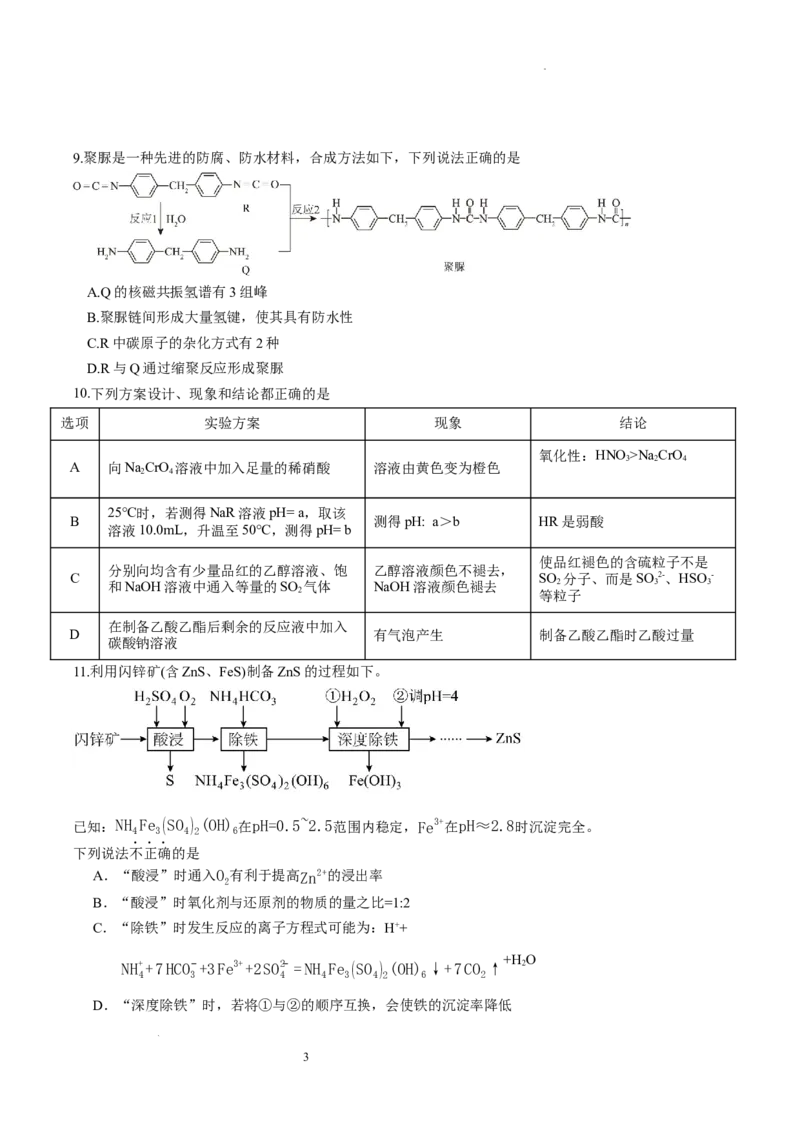
学科网(北京)股份有限公司9.聚脲是一种先进的防腐、防水材料,合成方法如下,下列说法正确的是
A.Q的核磁共振氢谱有3组峰
B.聚脲链间形成大量氢键,使其具有防水性
C.R中碳原子的杂化方式有2种
D.R与Q通过缩聚反应形成聚脲
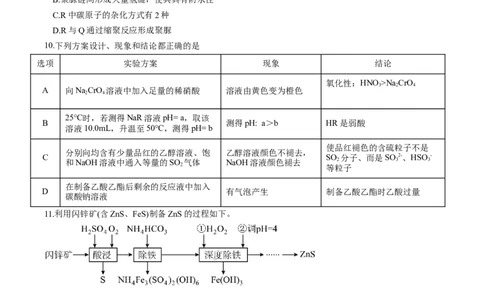
10.下列方案设计、现象和结论都正确的是
选项 实验方案 现象 结论
氧化性:HNO>Na CrO
3 2 4
A 向NaCrO 溶液中加入足量的稀硝酸 溶液由黄色变为橙色
2 4
25℃时,若测得NaR溶液pH= a,取该
B 测得pH: a>b HR是弱酸
溶液10.0mL,升温至50℃,测得pH= b
使品红褪色的含硫粒子不是
分别向均含有少量品红的乙醇溶液、饱 乙醇溶液颜色不褪去,
C SO 分子、而是SO 2-、HSO -
和NaOH溶液中通入等量的SO 气体 NaOH溶液颜色褪去 2 3 3
2 等粒子
在制备乙酸乙酯后剩余的反应液中加入
D 有气泡产生 制备乙酸乙酯时乙酸过量
碳酸钠溶液
11.利用闪锌矿(含ZnS、FeS)制备ZnS的过程如下。
已知:NH Fe (SO ) (OH) 在pH=0.5~2.5范围内稳定,Fe3+在pH≈2.8时沉淀完全。
4 3 4 2 6
下列说法不正确的是
A.“酸浸”时通入O 有利于提高Zn2+的浸出率
2
B.“酸浸”时氧化剂与还原剂的物质的量之比=1:2
C.“除铁”时发生反应的离子方程式可能为:H++
+H O
NH++7HCO−+3Fe3++2SO2− =NH Fe (SO ) (OH) ↓+7CO ↑ 2
4 3 4 4 3 4 2 6 2
D.“深度除铁”时,若将①与②的顺序互换,会使铁的沉淀率降低
3
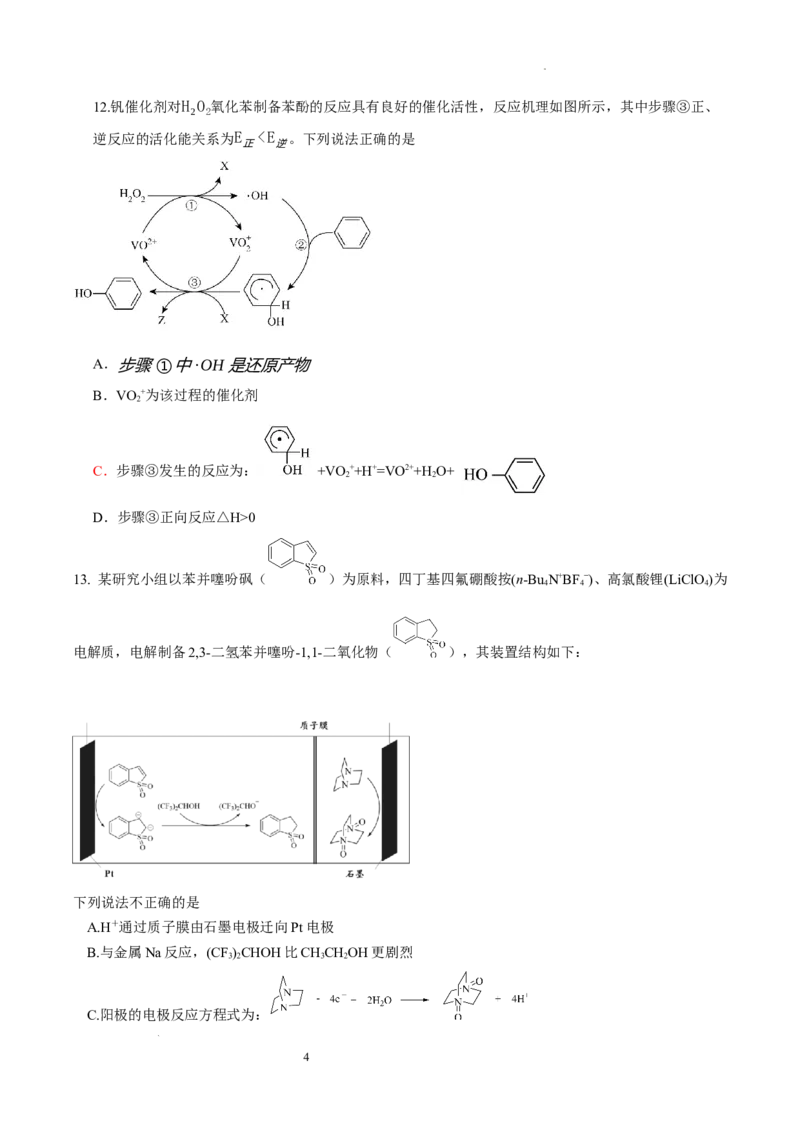
学科网(北京)股份有限公司12.钒催化剂对H O 氧化苯制备苯酚的反应具有良好的催化活性,反应机理如图所示,其中步骤③正、
2 2
逆反应的活化能关系为E 0
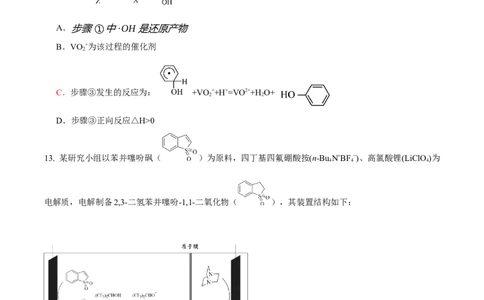
13. 某研究小组以苯并噻吩砜( )为原料,四丁基四氟硼酸按(n-Bu N+BF−)、高氯酸锂(LiClO )为
4 4 4
电解质,电解制备2,3-二氢苯并噻吩-1,1-二氧化物( ),其装置结构如下:
下列说法不正确的是
A.H+通过质子膜由石墨电极迁向Pt电极
B.与金属Na反应,(CF)CHOH比CHCHOH更剧烈
3 2 3 2
C.阳极的电极反应方程式为:
4
学科网(北京)股份有限公司D.每生成1mol ,理论上同时消耗2 mol
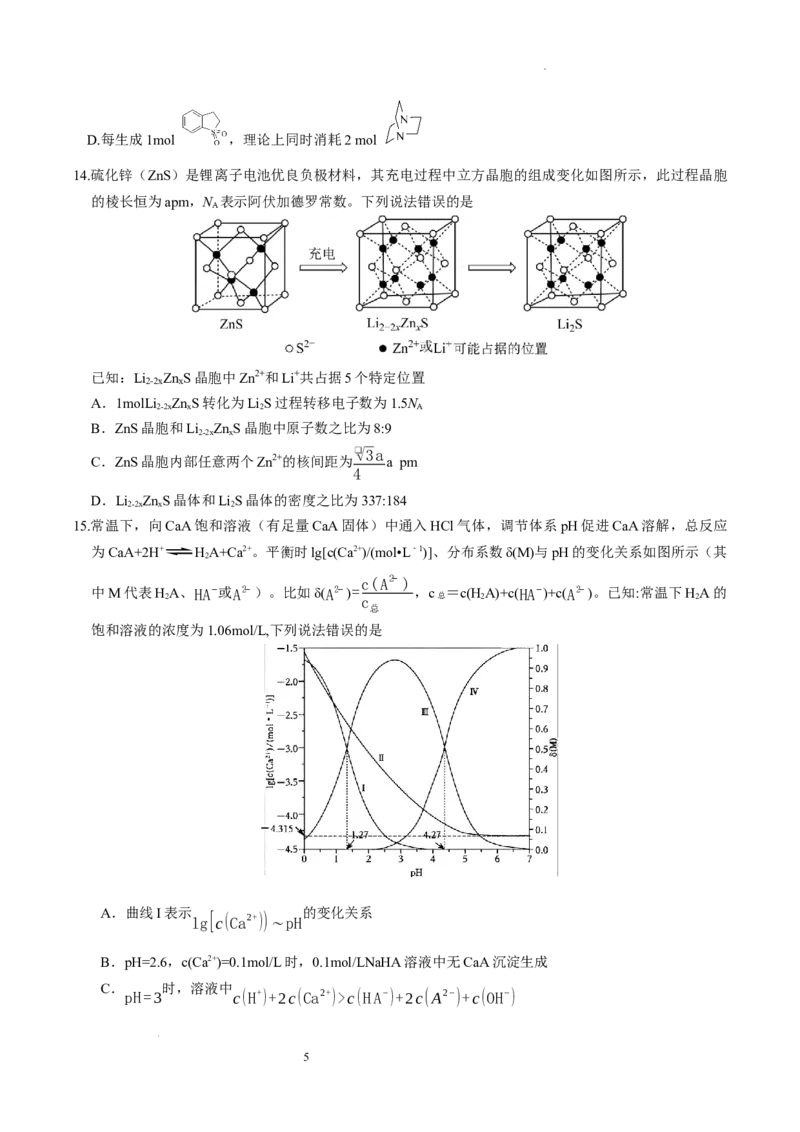
14.硫化锌(ZnS)是锂离子电池优良负极材料,其充电过程中立方晶胞的组成变化如图所示,此过程晶胞
的棱长恒为apm,N 表示阿伏加德罗常数。下列说法错误的是
A
已知:Li Zn S晶胞中Zn2+和Li+共占据5个特定位置
2-2x x
A.1molLi ZnS转化为LiS过程转移电子数为1.5N
2-2x x 2 A
B.ZnS晶胞和Li ZnS晶胞中原子数之比为8:9
2-2x x
❑√3a
C.ZnS晶胞内部任意两个Zn2+的核间距为 a pm
4
D.Li ZnS晶体和LiS晶体的密度之比为337:184
2-2x x 2
15.常温下,向CaA饱和溶液(有足量CaA固体)中通入HCl气体,调节体系pH促进CaA溶解,总反应
为CaA+2H+ HA+Ca2+。平衡时lg[c(Ca2+)/(mol•L﹣1)]、分布系数δ(M)与pH的变化关系如图所示(其
2
c(A2− )
中M代表HA、HA−或A2−)。比如δ(A2−)= ,c =c(HA)+c(HA−)+c(A2−)。已知:常温下HA的
2 c 总 2 2
总
饱和溶液的浓度为1.06mol/L,下列说法错误的是
A.曲线I表示 的变化关系
lg[c(Ca2+))∼pH
B.pH=2.6,c(Ca2+)=0.1mol/L时,0.1mol/LNaHA溶液中无CaA沉淀生成
C. 时,溶液中
pH=3 c(H+)+2c(Ca2+)>c(HA−)+2c(A2−)+c(OH−)
5
学科网(北京)股份有限公司D.在HA的饱和溶液中,c2(H+)×c(A2−)=1.06×10-5.54
2
第II 卷(非选择题,55分)
二、填空题(本题共4题,共55分)
16.(14分)茶叶中游离氨基酸是茶汤的主要成分,它对茶汤的鲜甜味有重要作用。某化学课外小组用如
下方法测定茶叶中游离氨基酸的含量。
回答下列问题:
Ⅰ.实验原理
茶叶中游离氨基酸在缓冲液中与茚三酮同时加热,α-氨基酸与茚三酮形成紫色络合物,紫色的深浅
与氨基酸含量成正相关。
O O
OH H
+ RCH(NH 2 )COOH + RCHO + NH 3 + CO 2 ↑
反应1: OH OH
O O
水合茚三酮 中间产物A
O O OH O
H
O+ + NH 3 N
OH
反应2:
O O O O
茚三酮 中间产物A 紫色
(1)反应1中水合茚三酮发生________反应(填“氧化”或“还原”)。
Ⅱ.实验步骤
步骤一:配制标准液得标准曲线
称取100g谷氨酸溶于100mL水中,稀释成如下浓度:40µg/mL、80µg/mL、160µg/mL、240µg/mL、
320µg/mL。分别取上述溶液1.0mL于25mL容量瓶中,加入0.5mL缓冲液,再加显色剂茚三酮0.5mL,定
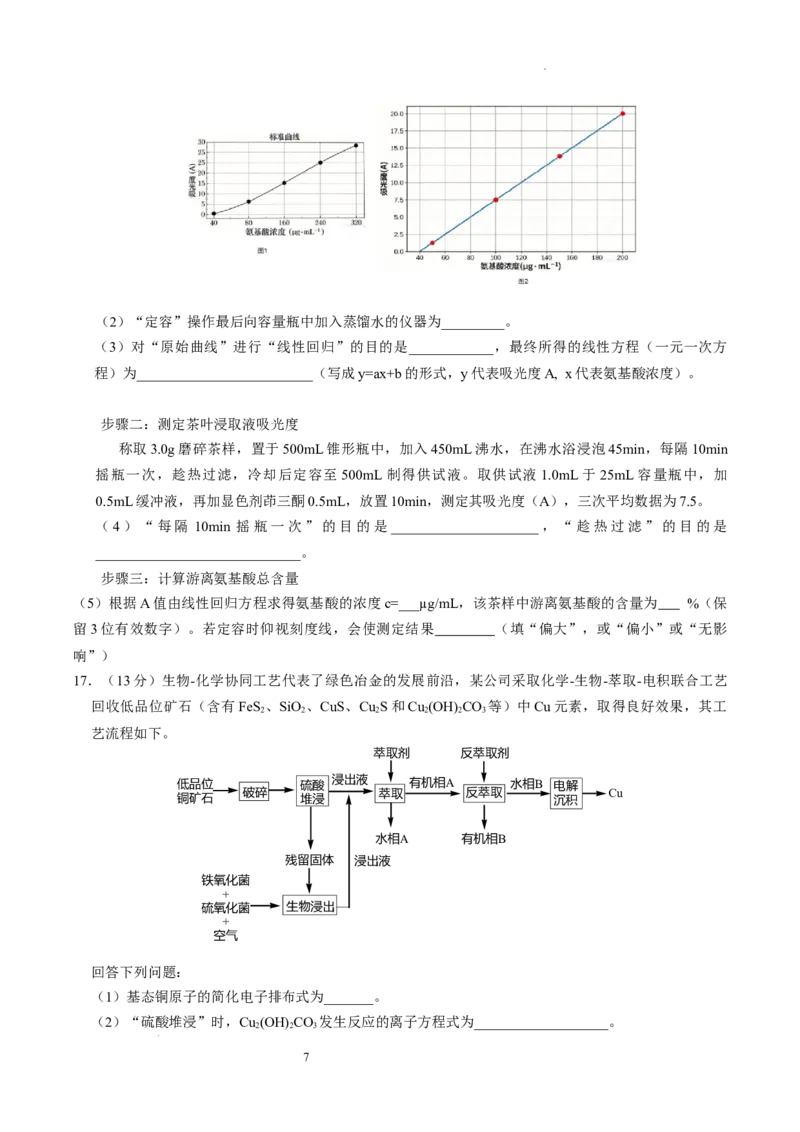
容至25mL,放置10min,测定其吸光度(A)。根据各溶液数据绘得如下原始曲线图1,对曲线进行线性
回归得到图2。
6
学科网(北京)股份有限公司(2)“定容”操作最后向容量瓶中加入蒸馏水的仪器为_________。
(3)对“原始曲线”进行“线性回归”的目的是____________,最终所得的线性方程(一元一次方
程)为_________________________(写成y=ax+b的形式,y代表吸光度A, x代表氨基酸浓度)。
步骤二:测定茶叶浸取液吸光度
称取3.0g磨碎茶样,置于500mL锥形瓶中,加入450mL沸水,在沸水浴浸泡45min,每隔10min
摇瓶一次,趁热过滤,冷却后定容至500mL制得供试液。取供试液1.0mL于25mL容量瓶中,加
0.5mL缓冲液,再加显色剂茚三酮0.5mL,放置10min,测定其吸光度(A),三次平均数据为7.5。
(4)“每隔 10min 摇瓶一次”的目的是_____________________,“趁热过滤”的目的是
_____________________________。
步骤三:计算游离氨基酸总含量
(5)根据A值由线性回归方程求得氨基酸的浓度c=___µg/mL,该茶样中游离氨基酸的含量为 %(保
留3位有效数字)。若定容时仰视刻度线,会使测定结果 (填“偏大”,或“偏小”或“无影
响”)
17.(13分)生物-化学协同工艺代表了绿色冶金的发展前沿,某公司采取化学-生物-萃取-电积联合工艺
回收低品位矿石(含有FeS 、SiO 、CuS、Cu S和Cu (OH) CO 等)中Cu元素,取得良好效果,其工
2 2 2 2 2 3
艺流程如下。
萃取剂 反萃取剂
低品位 硫酸 浸出液 有机相A 水相B 电解
破碎 萃取 反萃取 Cu
铜矿石 堆浸 沉积
水相A 有机相B
残留固体 浸出液
铁氧化菌
+
硫氧化菌 生物浸出
+
空气
回答下列问题:
(1)基态铜原子的简化电子排布式为_______。
(2)“硫酸堆浸”时,Cu (OH) CO 发生反应的离子方程式为___________________。
2 2 3
7
学科网(北京)股份有限公司(3)“残留固体”中含有FeS、Cu S以及
2 2
(4)“生物浸出”过程Fe元素转化为Fe3+,S元素转化为 ,则FeS 发生反应的离子方程式为
SO2− 2
4
__________________________。
(5)“萃取”过程可表示为2 (萃取剂)+Cu2+ 含铜螯合物+2H+,此
过程可实现 Cu2+与 Fe3+的分离,此萃取过程需调节 pH 为 2~4,请说明控制 pH 的原因
_______________,该萃取剂萃取Cu2+时长链烷基有利于萃取后有机相与水相分层,试从结构的角度解
释原因______________;“反萃取剂”的化学式为_________(填某种酸)。
(6)“电解沉积”过程(以惰性材料为阳极电极)中阳极产物为____ 。
18.(14分)氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产,硫酰氯及1,4-二(氯甲
基)苯等可通过氯化反应制备。
(1)工业上采用Deacon直接氧化法制氯气,其原理为反应a: ❑ 。
4HCl(g)+O (g)⇌ 2Cl (g)+2H O(g)
2 2 2
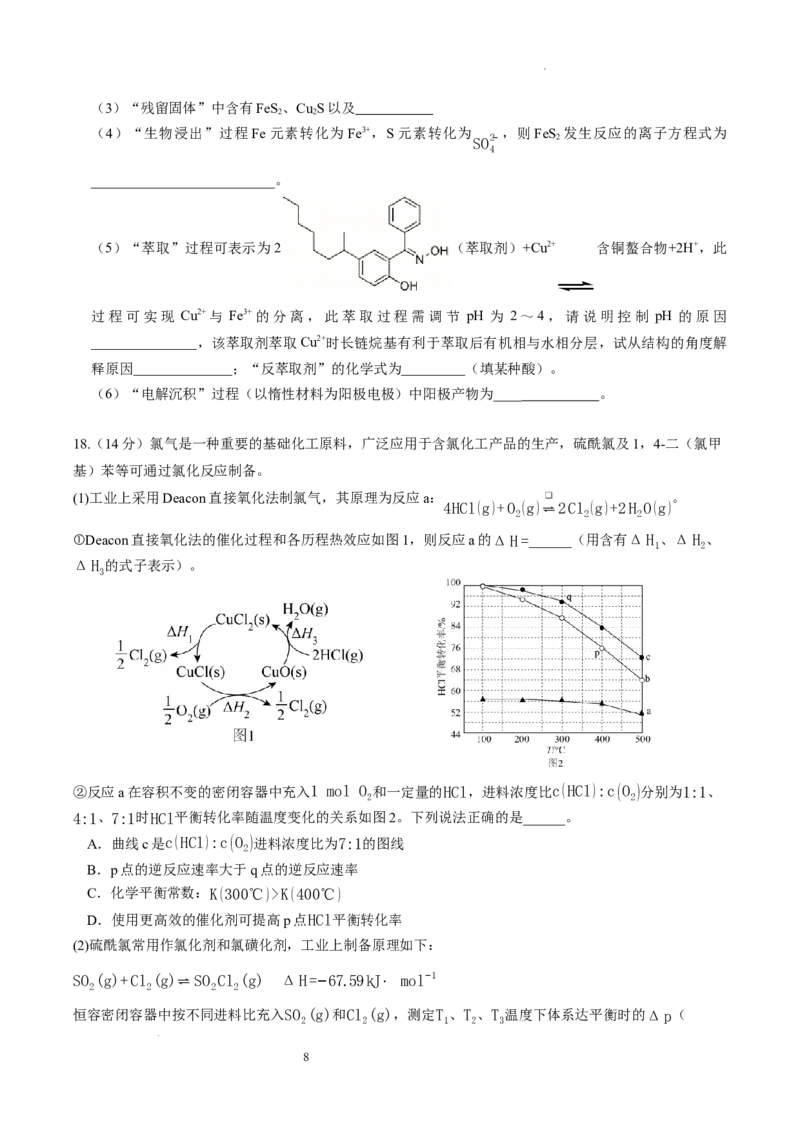
①Deacon直接氧化法的催化过程和各历程热效应如图1,则反应a的ΔH=______(用含有ΔH 、ΔH 、
1 2
ΔH 的式子表示)。
3
②反应a在容积不变的密闭容器中充入1 mol O 和一定量的HCl,进料浓度比c(HCl):c(O )分别为1:1、
2 2
4:1、7:1时HCl平衡转化率随温度变化的关系如图2。下列说法正确的是______。
A.曲线c是c(HCl):c(O )进料浓度比为7:1的图线
2
B.p点的逆反应速率大于q点的逆反应速率
C.化学平衡常数:K(300℃)>K(400℃)
D.使用更高效的催化剂可提高p点HCl平衡转化率
(2)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:
SO (g)+Cl (g)
⇌
SO Cl (g) ΔH=−67.59 kJ⋅ mol−1
2 2 2 2
恒容密闭容器中按不同进料比充入SO (g)和Cl (g),测定T 、T 、T 温度下体系达平衡时的Δp(
2 2 1 2 3
8
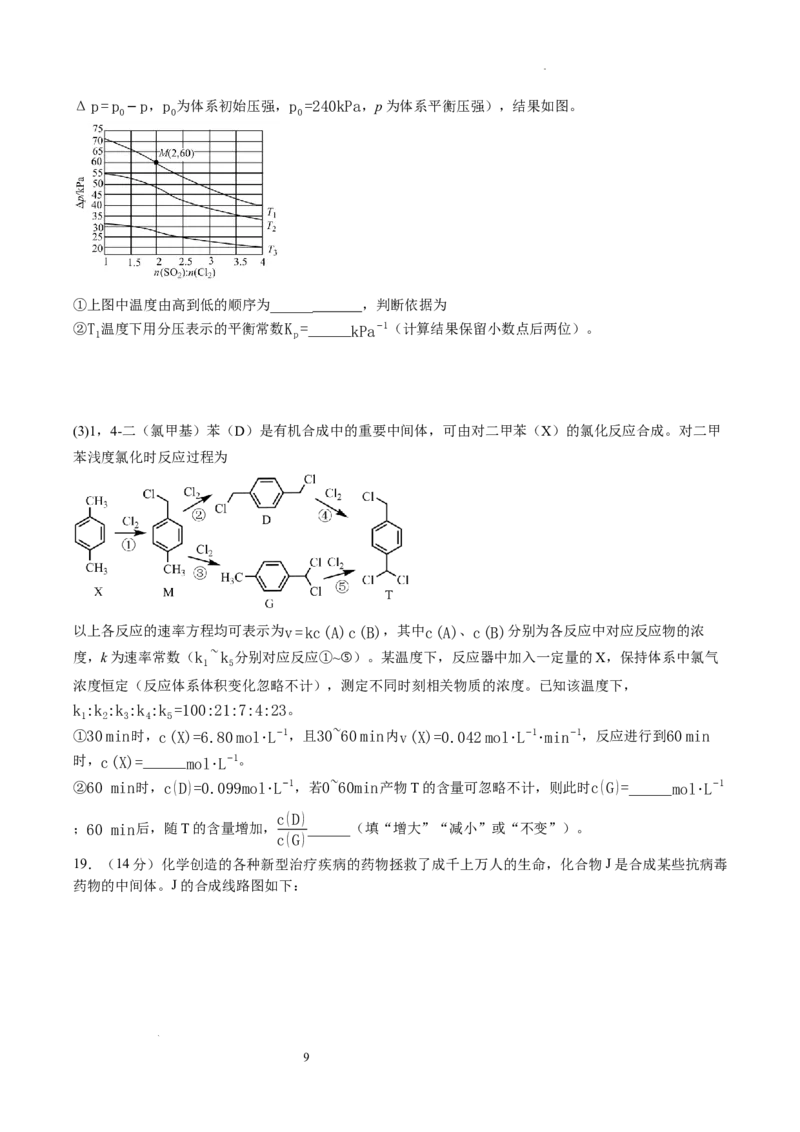
学科网(北京)股份有限公司Δp=p −p,p 为体系初始压强,p =240kPa,p为体系平衡压强),结果如图。
0 0 0
①上图中温度由高到低的顺序为______ ,判断依据为
②T 温度下用分压表示的平衡常数K =______kPa−1(计算结果保留小数点后两位)。
1 p
(3)1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲
苯浅度氯化时反应过程为
以上各反应的速率方程均可表示为v=kc(A)c(B),其中c(A)、c(B)分别为各反应中对应反应物的浓
度,k为速率常数(k ~k 分别对应反应①~⑤)。某温度下,反应器中加入一定量的X,保持体系中氯气
1 5
浓度恒定(反应体系体积变化忽略不计),测定不同时刻相关物质的浓度。已知该温度下,
k :k :k :k :k =100:21:7:4:23。
1 2 3 4 5
①30 min时,c(X)=6.80 mol∙L−1,且30~60 min内v(X)=0.042 mol∙L−1 ∙min−1,反应进行到60 min
时,c(X)=______mol∙L−1。
②60 min时,c(D)=0.099mol∙L−1,若0~60min产物T的含量可忽略不计,则此时c(G)=______mol∙L−1
c(D)
;60 min后,随T的含量增加, ______(填“增大”“减小”或“不变”)。
c(G)
19.(14分)化学创造的各种新型治疗疾病的药物拯救了成千上万人的生命,化合物J是合成某些抗病毒
药物的中间体。J的合成线路图如下:
9
学科网(北京)股份有限公司O
C
A HCHO
C H O N C 5 H 8 O
4 8 NH(CH )
3 2 B
t-BuOK
OCH F
3
D CO(OCH 3 ) 2
NaBH
C H O 4
10 12 3
H COOC COOCH
3 3 G
E
C H O
17 24 6
OCH
3 OCH
3
J 浓H 2 SO 4 (1) OH-/H O
2
C H O
14 18 3 (2) H+
COOH
COOH
COOH
OH
I OH H
已知:
O HCHO O O
(1)R1 NH(CH 3 ) 2 R1 N R1 (R 1 、R 2 表示烃基或氢)
CO(OCH )
3 2
(2)R 1 CH 2 COOR 2 R 1 CHCOOR 2
COOCH
3
OCH3 O OCH
3
(3)
R4
t-BuOK
COOR2
R
R
2
OOC COOR
3
4 COOR3
O
回答下列问题:
(1)A的结构简式为 ,其化学名称为____________。
(2)B中含氮官能团的名称为 。
(3)C与E反应生成F的化学方程式 。
(4)D转化为E的反应类型为 。
(5)D的同分异构体中:
①同时满足下列条件的共有 种(不考虑立体异构)。
10
学科网(北京)股份有限公司ⅰ.含有苯环
ⅱ.含有一个酚羟基
ⅲ.含有一个酯基
ⅳ.含有手性碳
ⅴ.含有两个甲基。
②满足上述条件的同分异构体中核磁共振氢谱显示为6组峰,且峰面积比为3:3:2:2:1:1的同分异构
体的结构简式为 。
③满足“第②小问”条件的其中一种有机物J参与如下合成路线可制备高分子化合物M:
H+/
稀硫酸 等物质的量的HCHO
有机物J C 9 H 10 O 3 C 10 H 12 O 4 (C 1H0 H [1 2 O C4 ) 1n0 H 10 O 3 ] n OH
H+/
K L M
请写出L到M的化学反应方程式____________________________________________。
11
学科网(北京)股份有限公司