文档内容
2021年陕西省中考化学试卷(副卷)
一、选择题(共9小题,每小题2分,计18分。每小题只有一个选项是符合题意的)
1.(2分)分类是学习物质的一种重要方法。下列物质属于纯净物的是( )
A.海水 B.纯碱 C.煤炭 D.空气
2.(2分)物质的性质和用途密切相关。下列物质的用途体现其化学性质的是( )
A.用石墨制作铅笔芯 B.用铜丝制作导线
C.用生石灰制作干燥剂 D.用氙气制作电光源
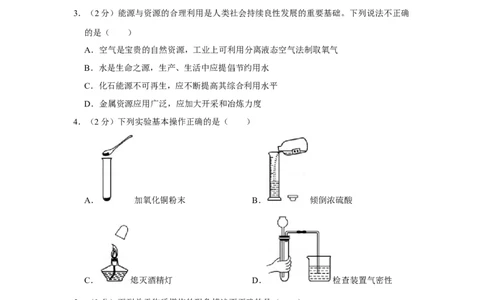
3.(2分)能源与资源的合理利用是人类社会持续良性发展的重要基础。下列说法不正确
的是( )
A.空气是宝贵的自然资源,工业上可利用分离液态空气法制取氧气
B.水是生命之源,生产、生活中应提倡节约用水
C.化石能源不可再生,应不断提高其综合利用水平
D.金属资源应用广泛,应加大开采和冶炼力度
4.(2分)下列实验基本操作正确的是( )
A. 加氧化铜粉末 B. 倾倒浓硫酸
C. 熄灭酒精灯 D. 检查装置气密性
5.(2分)下列关于物质燃烧的现象描述不正确的是( )
A.镁带在空气中燃烧,发出耀眼的白光
B.红磷在空气中燃烧,产生大量白烟
C.铁丝在氧气中燃烧,火星四射
D.木炭在氧气中燃烧,产生黄色火焰
6.(2分)对下列事实的微观解释不正确的是( )
A.固体物质很难被压缩——固体的分子间没有间隔B.酸具有一些相似的化学性质——酸溶液中都含有H+
C.CO和CO 化学性质不同——构成它们的分子不同
2
D.蔗糖在热水中溶解更快——温度越高分子运动越快
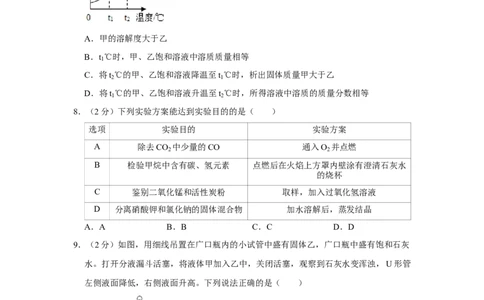
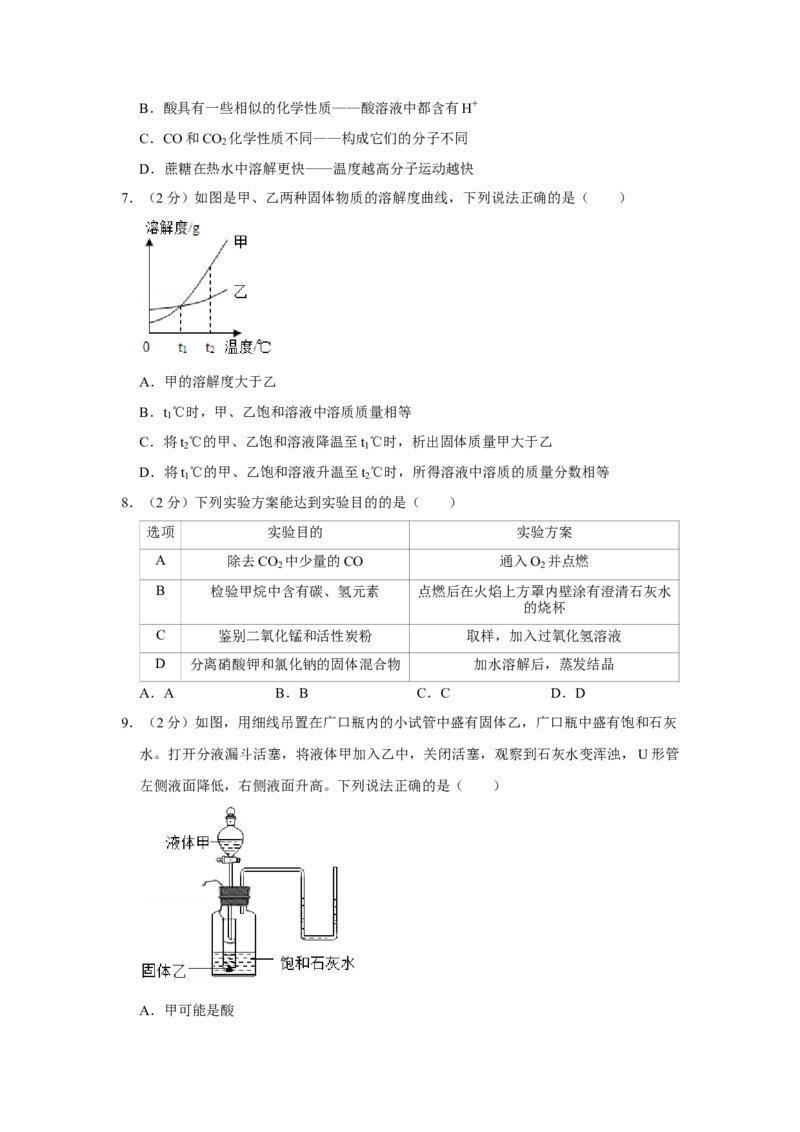
7.(2分)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
A.甲的溶解度大于乙
B.t ℃时,甲、乙饱和溶液中溶质质量相等
1
C.将t ℃的甲、乙饱和溶液降温至t ℃时,析出固体质量甲大于乙
2 1
D.将t ℃的甲、乙饱和溶液升温至t ℃时,所得溶液中溶质的质量分数相等
1 2
8.(2分)下列实验方案能达到实验目的的是( )
选项 实验目的 实验方案
A 除去CO 中少量的CO 通入O 并点燃
2 2
B 检验甲烷中含有碳、氢元素 点燃后在火焰上方罩内壁涂有澄清石灰水
的烧杯
C 鉴别二氧化锰和活性炭粉 取样,加入过氧化氢溶液
D 分离硝酸钾和氯化钠的固体混合物 加水溶解后,蒸发结晶
A.A B.B C.C D.D
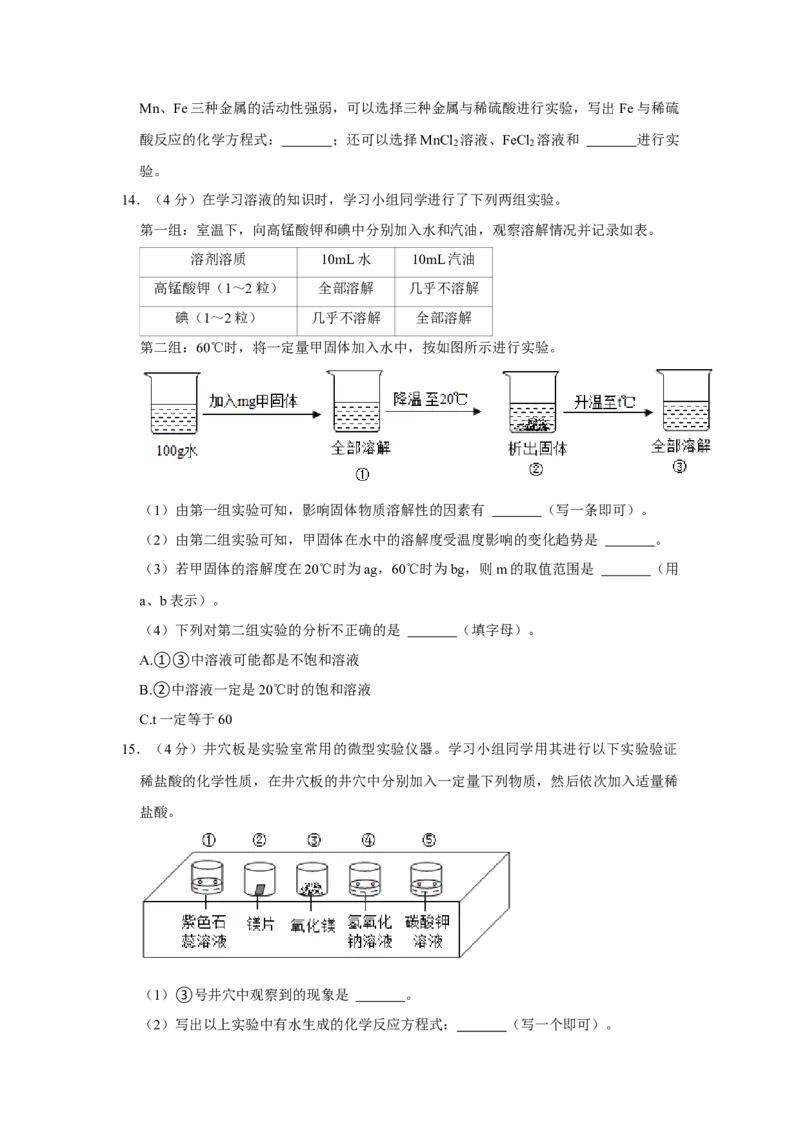
9.(2分)如图,用细线吊置在广口瓶内的小试管中盛有固体乙,广口瓶中盛有饱和石灰
水。打开分液漏斗活塞,将液体甲加入乙中,关闭活塞,观察到石灰水变浑浊,U形管
左侧液面降低,右侧液面升高。下列说法正确的是( )
A.甲可能是酸B.乙一定是盐
C.甲、乙发生的反应一定是复分解反应
D.U形管左、右两侧液面差始终保持不变
二、填空及简答题(共6小题,计24分)
10.(4分)在新冠肺炎疫情防控中,化学发挥着重要作用。
(1)最常使用的消毒剂是医用酒精。医用酒精中的溶剂是 。
(2)我国研发的新型冠状病毒灭活疫苗的辅料成分中含有氢氧化铝,其化学式为
。
(3)临床医学证明,地塞米松(化学式为C H FO )能减少新冠肺炎死亡病例。地塞
22 29 5
米松由 种元素组成,其化学式中数字“5”的含义是 。
11.(3分)第十四届全国运动会将于2021年9月在陕西隆重举行。
(1)全运会主场馆西安奥体中心是国内首个5G全覆盖的智慧场馆。生产5G芯片的主
要原料是氮化镓,镓在元素周期表中的信息如图所示,则镓原子的核外电子数为
。制取氮化镓的原理是:2Ga+2X 高温 2GaN+3H ,则X为 。
2
¯
❑
(2)陕西的“洛川苹果”“蒲城酥梨”“城固蜜桔”等水果甘甜可口、美味多汁,它
们都含有丰富的水、糖类和 ,可为运动员们提供营养佐餐。
12.(4分)水与人类的生产、生活密切相关。
(1)净化水时,除去水中难溶性固体杂质常用的操作方法是 。
(2)用井水洗衣时,当井水与肥皂粉混合搅拌后,发现泡沫很少,说明此井水为
(填“软水”或“硬水”)。
(3)实验室用电解水的方法探究水的组成,写出该反应的化学方程式: 。
13.(5分)汽车、地铁、高铁等交通工具使人们的出行更加方便快捷。
(1)汽油、天然气、甲醇、氢气等都可用作车用燃料,其中最理想的燃料是 。
(2)轻量级汽车应用较多的材料是镁合金、铝合金、碳纤维复合材料和塑料等,其中
属于有机合成材料的是 。
(3)制造地铁、高铁轨道的材料常用锰钢。已知锰的金属活动性比锌强,要验证 Zn、Mn、Fe三种金属的活动性强弱,可以选择三种金属与稀硫酸进行实验,写出Fe与稀硫
酸反应的化学方程式: ;还可以选择MnCl 溶液、FeCl 溶液和 进行实
2 2
验。
14.(4分)在学习溶液的知识时,学习小组同学进行了下列两组实验。
第一组:室温下,向高锰酸钾和碘中分别加入水和汽油,观察溶解情况并记录如表。
溶剂溶质 10mL水 10mL汽油
高锰酸钾(1~2粒) 全部溶解 几乎不溶解
碘(1~2粒) 几乎不溶解 全部溶解
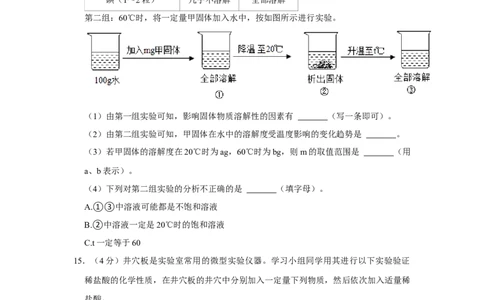
第二组:60℃时,将一定量甲固体加入水中,按如图所示进行实验。
(1)由第一组实验可知,影响固体物质溶解性的因素有 (写一条即可)。
(2)由第二组实验可知,甲固体在水中的溶解度受温度影响的变化趋势是 。
(3)若甲固体的溶解度在20℃时为ag,60℃时为bg,则m的取值范围是 (用
a、b表示)。
(4)下列对第二组实验的分析不正确的是 (填字母)。
A.①③中溶液可能都是不饱和溶液
B.②中溶液一定是20℃时的饱和溶液
C.t一定等于60
15.(4分)井穴板是实验室常用的微型实验仪器。学习小组同学用其进行以下实验验证
稀盐酸的化学性质,在井穴板的井穴中分别加入一定量下列物质,然后依次加入适量稀
盐酸。
(1)③号井穴中观察到的现象是 。
(2)写出以上实验中有水生成的化学反应方程式: (写一个即可)。(3)某同学在⑤号井穴中加入一定量稀盐酸后,想检验稀盐酸是否过量,可加入的试
剂是 (填字母)。
A.无色酚酞溶液
B.Cu(OH)
2
C.AgNO 溶液
3
三、实验及探究题(共2小题,计13分)
16.(6分)根据下列实验装置图示回答问题。
(1)写出标有字母a的仪器名称: 。
(2)写出实验室用装置甲制取氧气的化学方程式: 。实验中试管口略向下倾斜
的原因是 。
(3)同学们为验证CO 的性质设计了装置丁,塑料瓶内壁上贴的是用紫色石蕊溶液浸
2
泡过的纸花,其中c处是干燥的纸花,b、d两处是湿润的纸花。依次连接装置乙、丙、
丁进行实验时,观察到d处纸花先变红,c处不变色,b处后变红;澄清石灰水变浑浊;
蜡烛从低处到高处依次熄灭。
①上述实验现象证明了CO 具有的一些化学性质,同时也可证明CO 具有的物理性质
2 2
是 。
②装置丙的作用是 。
17.(7分)陕西东部的黄河湿地有大片盐碱地,依据资料可知,该片盐碱地的土壤中含
有的可溶性物质是Na CO 、NaCl、CaCl 、Na SO 中的一种或多种。学习小组的同学欲
2 3 2 2 4
探究某地块的土壤中可溶性物质的成分,他们利用该地块土壤的浸出液进行了以下探究。
(友情提示:把土壤样品用水充分浸泡后过滤,所得滤液即为“浸出液”)
【实验探究一】
实验 实验操作 实验现象 实验结论
① 取少量浸出液于试管中,加入 浸出液中含有Na CO ,没有
2 3
适量稀盐酸② 取少量浸出液于试管中,加入 产生白色沉淀 浸出液中含有Na SO
2 4
适量BaCl 溶液
2
【反思评价】
讨论后,同学们一致认为通过实验②无法确定浸出液中含有Na SO ,你认为理由是
2 4
(用化学方程式表示)。
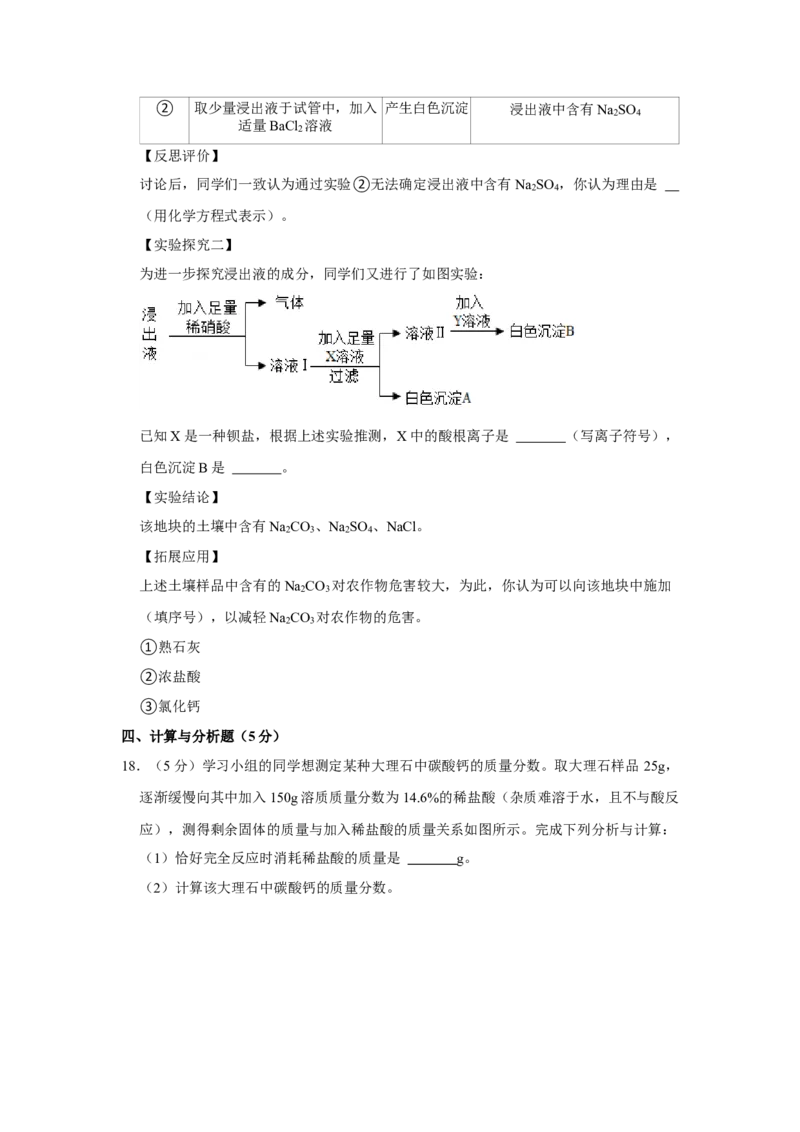
【实验探究二】
为进一步探究浸出液的成分,同学们又进行了如图实验:
已知X是一种钡盐,根据上述实验推测,X中的酸根离子是 (写离子符号),
白色沉淀B是 。
【实验结论】
该地块的土壤中含有Na CO 、Na SO 、NaCl。
2 3 2 4
【拓展应用】
上述土壤样品中含有的Na CO 对农作物危害较大,为此,你认为可以向该地块中施加
2 3
(填序号),以减轻Na CO 对农作物的危害。
2 3
①熟石灰
②浓盐酸
③氯化钙
四、计算与分析题(5分)
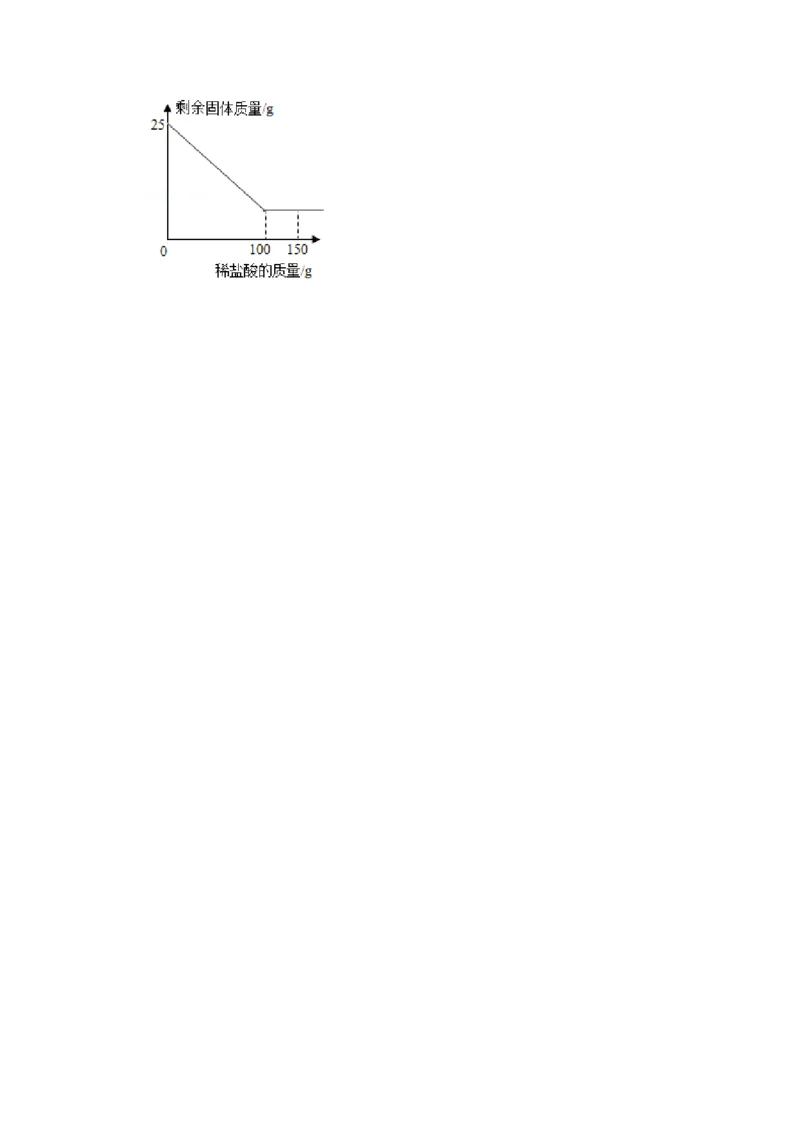
18.(5分)学习小组的同学想测定某种大理石中碳酸钙的质量分数。取大理石样品 25g,
逐渐缓慢向其中加入150g溶质质量分数为14.6%的稀盐酸(杂质难溶于水,且不与酸反
应),测得剩余固体的质量与加入稀盐酸的质量关系如图所示。完成下列分析与计算:
(1)恰好完全反应时消耗稀盐酸的质量是 g。
(2)计算该大理石中碳酸钙的质量分数。