文档内容
合肥市普通高中六校联盟2025年秋季学期期中考试
!"#$%&'()
(考试时间:75分钟 满分100分)
命题学校:合肥五中 命题教师:王晓明 审题教师:程本洁
可能用到的相对原子质量:
H:1 C:12 O:16 Na:23 Cl:35.5 Zn:65
一、选择题(本大题共15小题,每小题3分,共45分。每小题给出的四个选项中,只
有一个符合题目要求。)
1.中华优秀传统文化中蕴含着丰富的化学知识。下列说法错误的是( )
..
A.《华阳国志》:“取井火煮之,一斛水得五斗盐”——加热蒸发食盐水可得食盐
B.《汉书·枚乘传》“泰山滴水穿石”——“滴水穿石”过程中不包含化学变化
C.《肘后备急方》:“青蒿一握,以水二升渍,绞取之”——青蒿素的提取属于物理变化
D.《天工开物》:“凡石灰,经火焚炼为用”——煅烧石灰石发生了分解反应
2.下列图示中,实验操作或方法符合规范的是( )
A.溶解氯化钠固体 B.配制溶液时定容 C.收集二氧化碳气体 D.观察钠与水的反应
3.化学应用体现在生活的方方面面,下列用法不合理的是( )
...
A.用明矾净化巢湖水 B.用食醋去除水壶中水垢
C.用漂粉精漂白银耳 D.用小苏打作烘焙糕点膨松剂
4.磁流体是电子材料的新秀,它既有固体的磁性,又有液体的流动性,磁流体中分散质粒
子直径在5.5 nm~36 nm之间。下列说法不正确的是( )
...
A.磁流体属于胶体 B.磁流体中分散质粒子能通过滤纸
C.磁流体能产生丁达尔效应 D.磁流体很不稳定
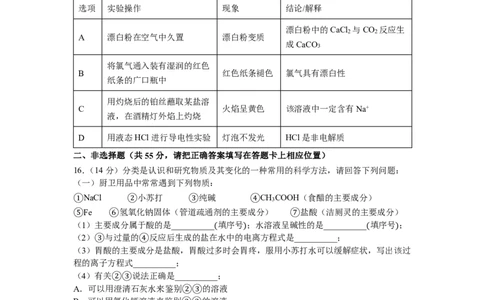
5.下列实验产生的废液中,可能大量存在的粒子组是( )
选项 实验 粒子组
A 浓盐酸与MnO 制Cl H+、Mn2+、Cl-、H O
2 2 2
B 稀硫酸与Na CO 制CO H+、Na+、SO 2-、HCO -
2 3 2 4 3
C 稀硫酸与锌粒制H H+、Zn2+、SO 2-、H
2 4 2
D Na O 加入CuSO 溶液 OH-、Na+、Cu2+、SO 2-
2 2 4 4
高一年级化学试卷 第 1 页 共6页
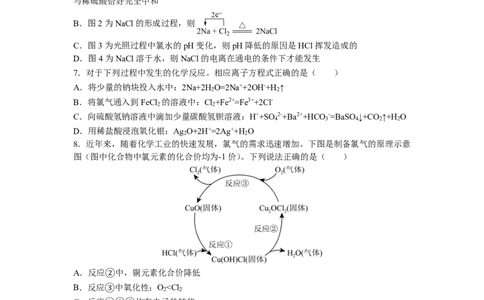
{#{QQABBQyEggigApBAAQhCAwmwCAEYkAGCAIgOwEAYoAIAAAFABAA=}#}6.下列对图示的解释正确的是( )
图1 图2 图3 图4
A.图1为向Ba(OH) 溶液中加入稀硫酸,溶液导电能力的变化,则a时刻Ba(OH) 溶液
2 2
与稀硫酸恰好完全中和
B.图2为NaCl的形成过程,则
C.图3为光照过程中氯水的pH变化,则pH降低的原因是HCl挥发造成的
D.图4为NaCl溶于水,则NaCl的电离在通电的条件下才能发生
7.对于下列过程中发生的化学反应。相应离子方程式正确的是( )
A.将少量的钠块投入水中:2Na+2H O=2Na++2OH-+H ↑
2 2
B.将氯气通入到FeCl 的溶液中:Cl +Fe2+=Fe3++2Cl-
2 2
C.向硫酸氢钠溶液中滴加少量碳酸氢钡溶液:H++SO 2-+Ba2++HCO -=BaSO ↓+CO ↑+H O
4 3 4 2 2
D.用稀盐酸浸泡氧化银:Ag O+2H+=2Ag++H O
2 2
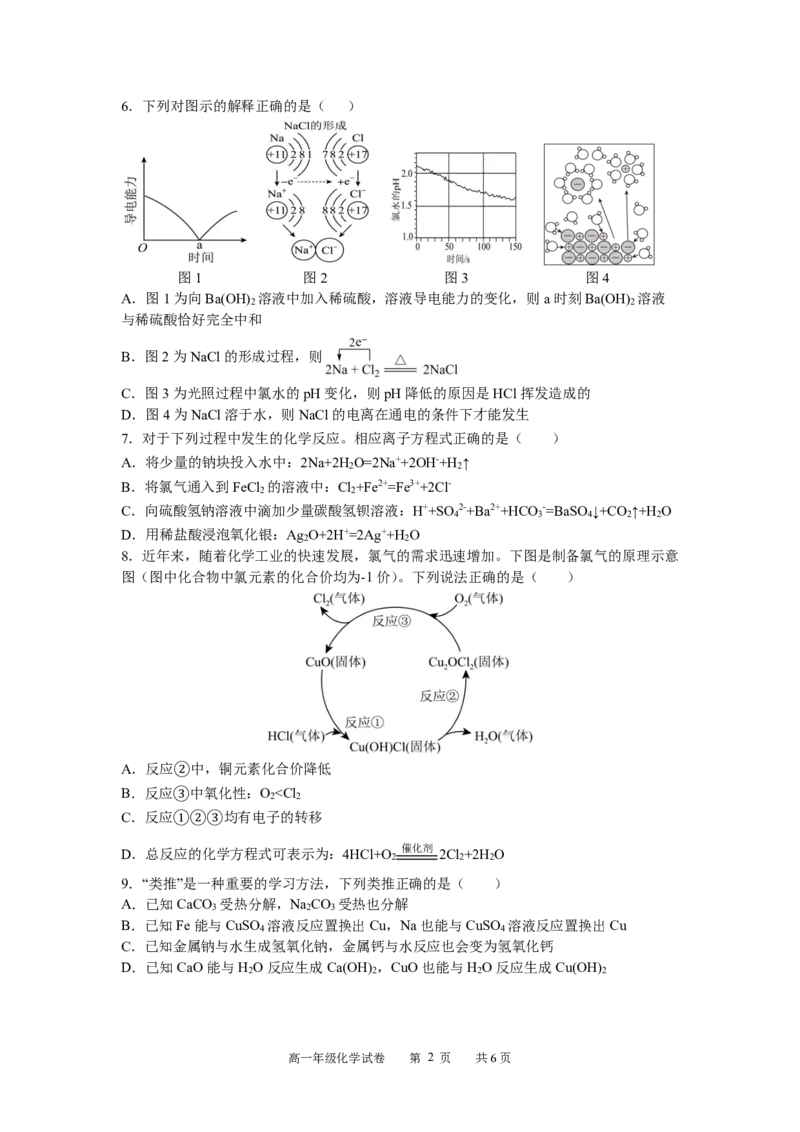
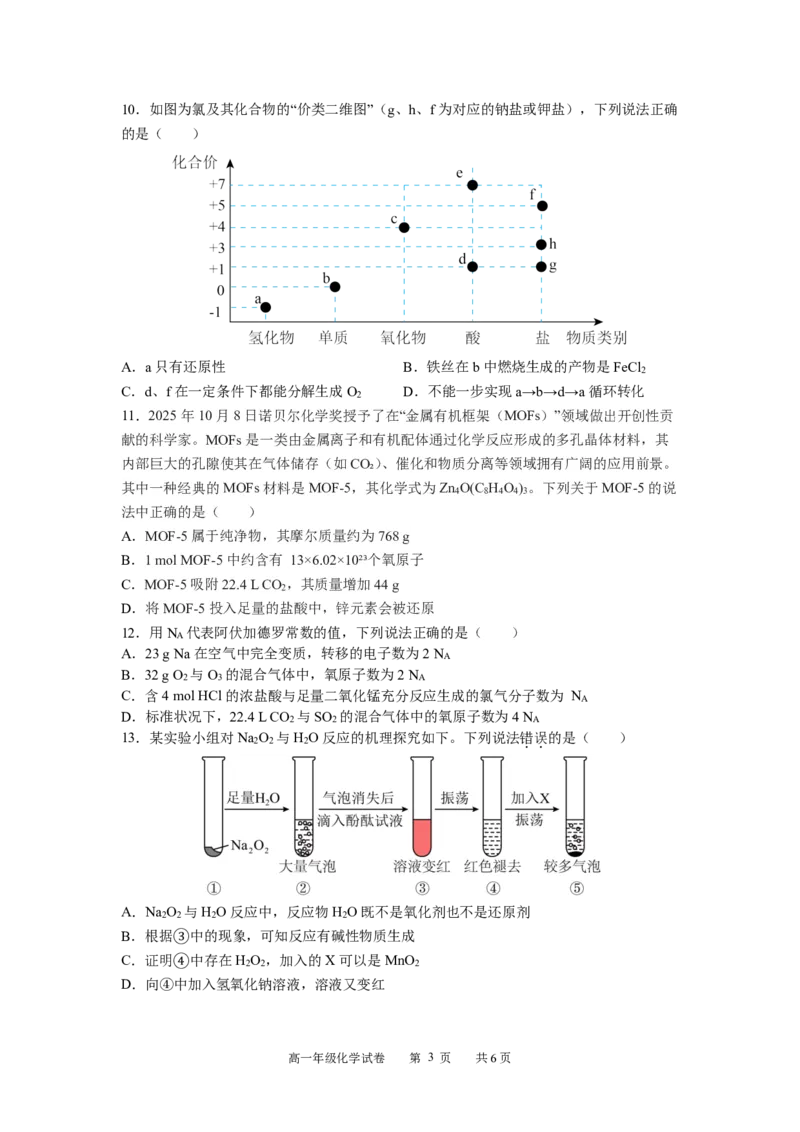
8.近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意
图(图中化合物中氯元素的化合价均为-1价)。下列说法正确的是( )
A.反应②中,铜元素化合价降低
B.反应③中氧化性:O ③
D.向③溶液中通入过量的CO ,可以使③转化为②
2
(二)1943年左右我国化学家侯德榜发明了联合制碱法(又称侯氏制碱法),对世界制碱工
业做出了巨大贡献。侯氏制碱法的主要过程如下图所示(部分物质已略去)。
饱和食盐水
高一年级化学试卷 第 4 页 共6页
{#{QQABBQyEggigApBAAQhCAwmwCAEYkAGCAIgOwEAYoAIAAAFABAA=}#}(5)分离NaHCO 固体和溶液A的操作为__________,所需的玻璃仪器有烧杯、漏斗、
3
__________。
(三)(6)NaHCO 和NaHS都属于弱酸形成的酸式盐,请写出NaHS与NaOH反应的化
3
学方程式__________。
17.(13分)过氧化钠可用于医药、印染、漂白及用作分析试剂等。工业制取过氧化钠的
流程如图:
(1)生产过程中,能用于净化空气的措施是_________。
A.将空气通过装有氢氧化钠溶液的装置 B.将空气通过装浓硫酸的装置
C.将空气通过装有碱石灰的装置 D.将空气通过装有无水硫酸铜粉末的装置
(2)反应②与反应③的反应温度不相同,下列两个反应条件中属于反应②的是______。
A.180~200℃ B.300~400℃
(3)同学甲认为,净化空气要除去CO 气体是因为CO 能与Na O、Na O 反应,请写出
2 2 2 2 2
CO 与Na O 反应的化学方程式:_______________________。
2 2 2
同学乙认为Na也能与CO 气体反应,并设计如下实验验证:
2
实验1:将燃着的Na迅速伸入装满纯净干燥CO 的集气瓶中,可以看到,Na在其中继续
2
燃烧,反应结束后,集气瓶底附着黑色颗粒,瓶壁上粘附着白色固体。
实验2:在集气瓶中加入适量蒸馏水,振荡,瓶壁白色固体全部溶解,过滤,滤纸上留下
黑色固体,滤液为无色。将干燥后的黑色固体引燃,并将产生的气体通入澄清石灰水,石
灰水变浑浊。针对白色固体的成分,该同学提出三种猜想:
猜想1:白色物质是Na O;
2
猜想2:白色物质是Na CO ;
2 3
猜想3:白色物质是Na O和Na CO 的混合物。
2 2 3
为了验证哪种猜想正确,该同学对无色滤液继续进行如下方案探究:
实验3:取少量无色滤液于试管中,向其中加入过量BaCl 溶液,溶液中出现白色沉淀。
2
实验4:静置片刻,取上层清液于试管中,滴加无色酚酞试液,无明显现象。
(4)根据以上实验,乙同学认为白色物质为__________,其理由是__________。
(5)根据以上探究,写出Na在CO 气体中燃烧的化学方程式__________。
2
(6)CaO 的性质与Na O 相似。常常在养殖水产的时候加入CaO ,其作用是________。
2 2 2 2
高一年级化学试卷 第 5 页 共6页
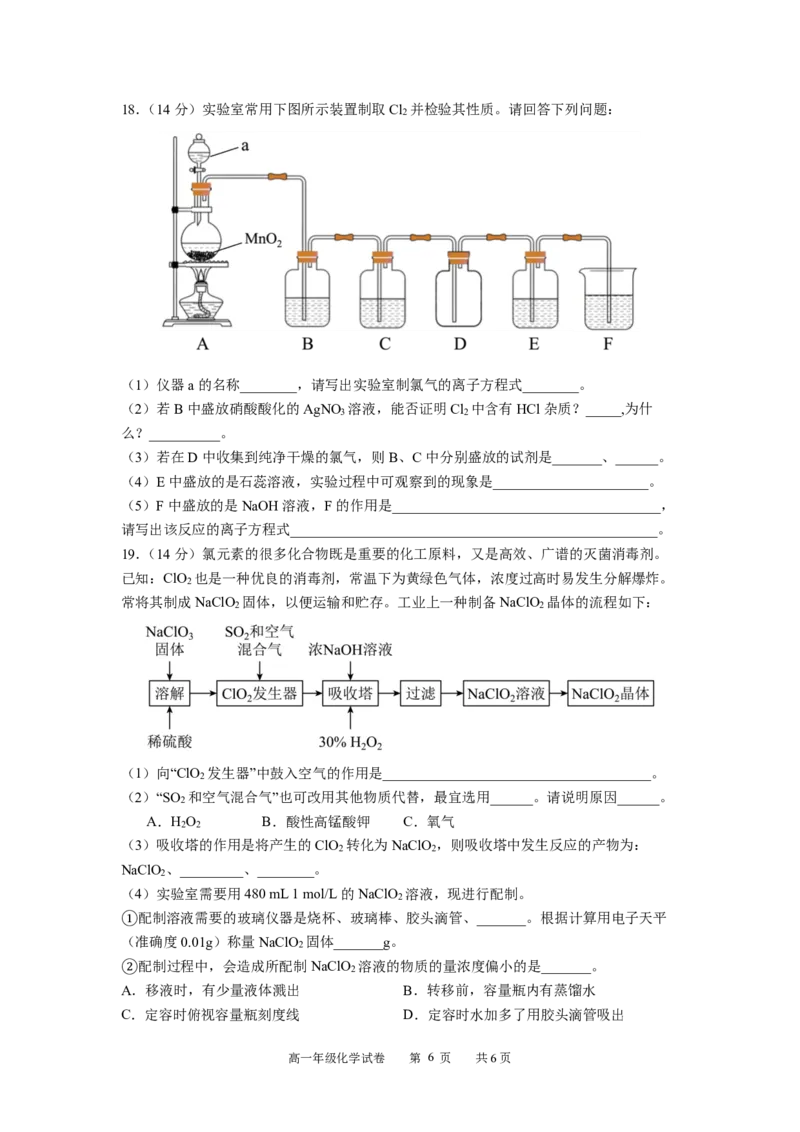
{#{QQABBQyEggigApBAAQhCAwmwCAEYkAGCAIgOwEAYoAIAAAFABAA=}#}18.(14分)实验室常用下图所示装置制取Cl 并检验其性质。请回答下列问题:
2
(1)仪器a的名称________,请写出实验室制氯气的离子方程式________。
(2)若B中盛放硝酸酸化的AgNO 溶液,能否证明Cl 中含有HCl杂质?_____,为什
3 2
么?__________。
(3)若在D中收集到纯净干燥的氯气,则B、C中分别盛放的试剂是_______、______。
(4)E中盛放的是石蕊溶液,实验过程中可观察到的现象是______________________。
(5)F中盛放的是NaOH溶液,F的作用是______________________________________,
请写出该反应的离子方程式____________________________________________________。
19.(14分)氯元素的很多化合物既是重要的化工原料,又是高效、广谱的灭菌消毒剂。
已知:ClO 也是一种优良的消毒剂,常温下为黄绿色气体,浓度过高时易发生分解爆炸。
2
常将其制成NaClO 固体,以便运输和贮存。工业上一种制备NaClO 晶体的流程如下:
2 2
(1)向“ClO 发生器”中鼓入空气的作用是______________________________________。
2
(2)“SO 和空气混合气”也可改用其他物质代替,最宜选用______。请说明原因______。
2
A.H O B.酸性高锰酸钾 C.氧气
2 2
(3)吸收塔的作用是将产生的ClO 转化为NaClO ,则吸收塔中发生反应的产物为:
2 2
NaClO 、_________、________。
2
(4)实验室需要用480 mL 1 mol/L的NaClO 溶液,现进行配制。
2
①配制溶液需要的玻璃仪器是烧杯、玻璃棒、胶头滴管、_______。根据计算用电子天平
(准确度0.01g)称量NaClO 固体_______g。
2
②配制过程中,会造成所配制NaClO 溶液的物质的量浓度偏小的是_______。
2
A.移液时,有少量液体溅出 B.转移前,容量瓶内有蒸馏水
C.定容时俯视容量瓶刻度线 D.定容时水加多了用胶头滴管吸出
高一年级化学试卷 第 6 页 共6页
{#{QQABBQyEggigApBAAQhCAwmwCAEYkAGCAIgOwEAYoAIAAAFABAA=}#}