文档内容
南充市嘉陵一中高 2024 级高一下期第一次月考试卷
化学
(满分:100 分 考试时间:75 分钟 命审题:谭剑锋)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将答题卡交回。
可能用到的相对原子质量:H1 C12 N14 O16 Na23 Ni59
第Ⅰ卷 选择题
一、本卷共16小题,每题只有 1个选项符合题意(每题 3分,共 48分)
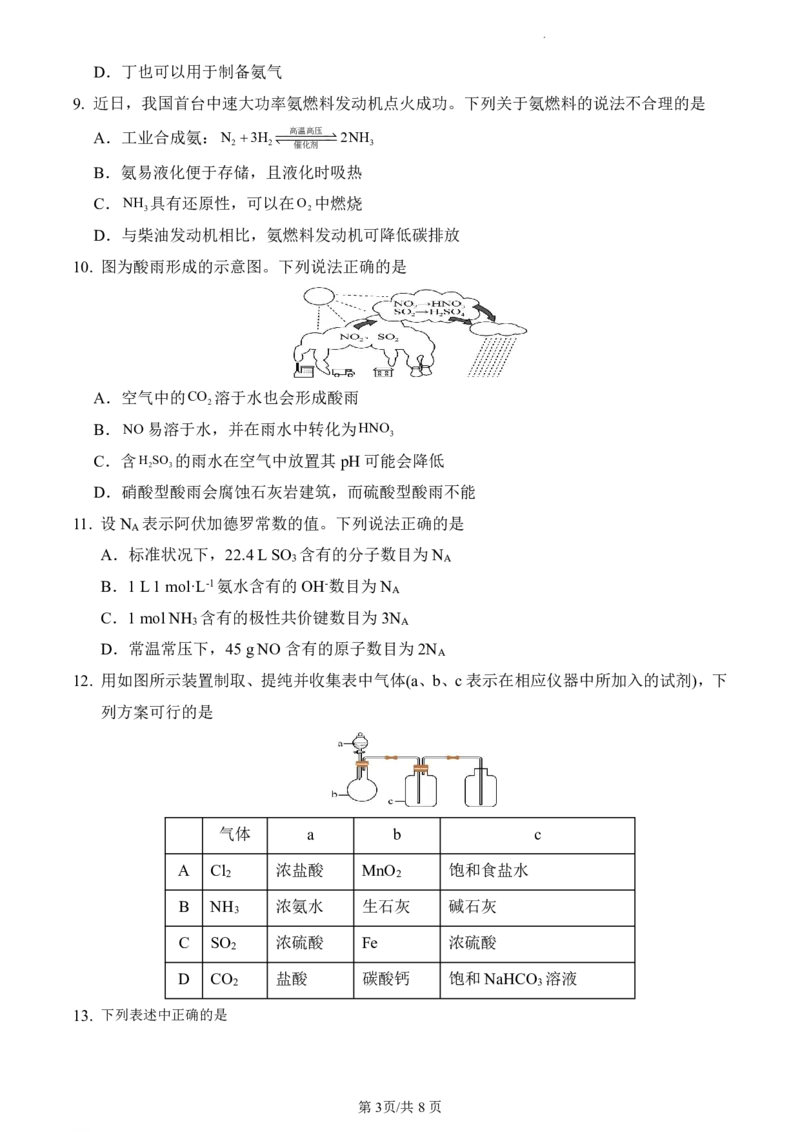
1. 很多珍贵文物都记载着中华文明的灿烂成就,具有深邃的文化寓意和极高的学术价值。下
列国宝级文物属于合金材料制成的是
选项 A B C D
文物
名称 九霄环佩木古琴 狗头兽首铜像 萧何月下追韩信图梅瓶 陶彩绘女舞俑
2.P O 常用作气体的干燥剂,易吸水转化为H PO 。下列说法不正确的是
2 5 3 4
A.P O 中P元素化合价为+5 价 B.P O 属于碱性氧化物
2 5 2 5
C.P O 能与CaO 反应 D.P O 能与NaOH 反应
2 5 2 5
3. 下列变化需加入氧化剂才能实现的是
A.MnO Mn2 B.CaCO CO
4 3 2
C.NH NO D.H O H O
3 2 2 2
4. 下列说法正确的是
A.任何化学反应都伴随着能量的变化
B.对于如图所示的过程,是吸收能量的过程
C.化学反应中能量的变化都表现为热量的变化
第1页/共8页
学科网(北京)股份有限公司D.H O(g)―→H O(l)该过程放出大量的热,所以该过程是化学变化
2 2
5. 下列物质的应用中,利用了氧化还原反应的是
A. 用石灰乳脱除烟气中的二氧化硫 B. 用“84”消毒液杀菌消毒
C. 用盐酸去除铁锈 D. 用活性炭吸附甲醛、苯等室内污染气体
6. 某同学设计如图所示实验,探究化学反应中的能量变化。
下列判断正确的是
A. 由实验可知,Ⅰ、Ⅱ、Ⅲ所涉及的反应都是放热反应
B. 将实验Ⅰ中的镁片更换为等质量的镁粉后释放出的热量增多
C. 实验Ⅲ中将玻璃搅拌器改为铜质搅拌器对实验结果没有影响
D. 实验Ⅲ中若用NaOH固体测定中和反应的反应热,则测定的ΔH偏低
7. 下列化学方程式或离子方程式书写不正确的是
A.浓硝酸加热分解的反应:
B.铁和稀硫酸溶液的反应:2Fe6H 2Fe3 3H
2
C.过量SO 和NaOH 溶液反应:SO OH HSO
2 2 3
D.过量的 Fe 和稀硝酸反应:3Fe8H 2NO 3Fe2 2NO4H O
3 2
8. 用下图装置(夹持装置已略去)进行NH 制备及性质实验,已知:NH 极易溶于水,而难溶于
3 3
CCl ,CCl 密度比水大且与水不互溶。下列说法不正确的是
4 4
A.甲中制备NH 利用了NH H O的分解反应
3 3 2
B.乙中的集气瓶内a导管短、b导管长
C.丙中的CCl 能防止倒吸
4
第2页/共8页
学科网(北京)股份有限公司D.丁也可以用于制备氨气
9. 近日,我国首台中速大功率氨燃料发动机点火成功。下列关于氨燃料的说法不合理的是
A.工业合成氨:N 3H 高 温 高 压 2NH
2 2 催化剂 3
B.氨易液化便于存储,且液化时吸热
C.NH 具有还原性,可以在O 中燃烧
3 2
D.与柴油发动机相比,氨燃料发动机可降低碳排放
10. 图为酸雨形成的示意图。下列说法正确的是
A.空气中的CO 溶于水也会形成酸雨
2
B.NO易溶于水,并在雨水中转化为HNO
3
C.含H SO 的雨水在空气中放置其pH可能会降低
2 3
D.硝酸型酸雨会腐蚀石灰岩建筑,而硫酸型酸雨不能
11. 设N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,22.4LSO 含有的分子数目为N
3 A
B.1L1mol·L-1氨水含有的OH-数目为N
A
C.1molNH 含有的极性共价键数目为3N
3 A
D.常温常压下,45gNO含有的原子数目为 2N
A
12. 用如图所示装置制取、提纯并收集表中气体(a、b、c表示在相应仪器中所加入的试剂),下
列方案可行的是
气体 a b c
A Cl 浓盐酸 MnO 饱和食盐水
2 2
B NH 浓氨水 生石灰 碱石灰
3
C SO 浓硫酸 Fe 浓硫酸
2
D CO 盐酸 碳酸钙 饱和NaHCO 溶液
2 3
13. 下列表述中正确的是
第3页/共8页
学科网(北京)股份有限公司①提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料
②化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
③氮化硅陶瓷、氧化铝陶瓷、光导纤维等属于新型无机非金属材料
④光导纤维做通讯材料有许多优点,但怕腐蚀,铺设也很不方便
⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④ C.①③⑤ D.③④⑤
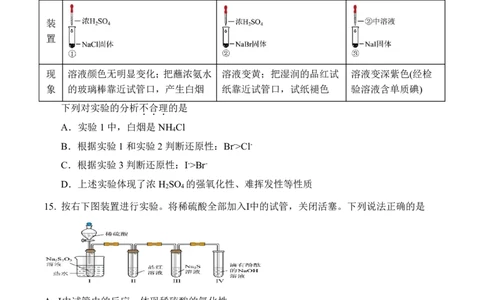
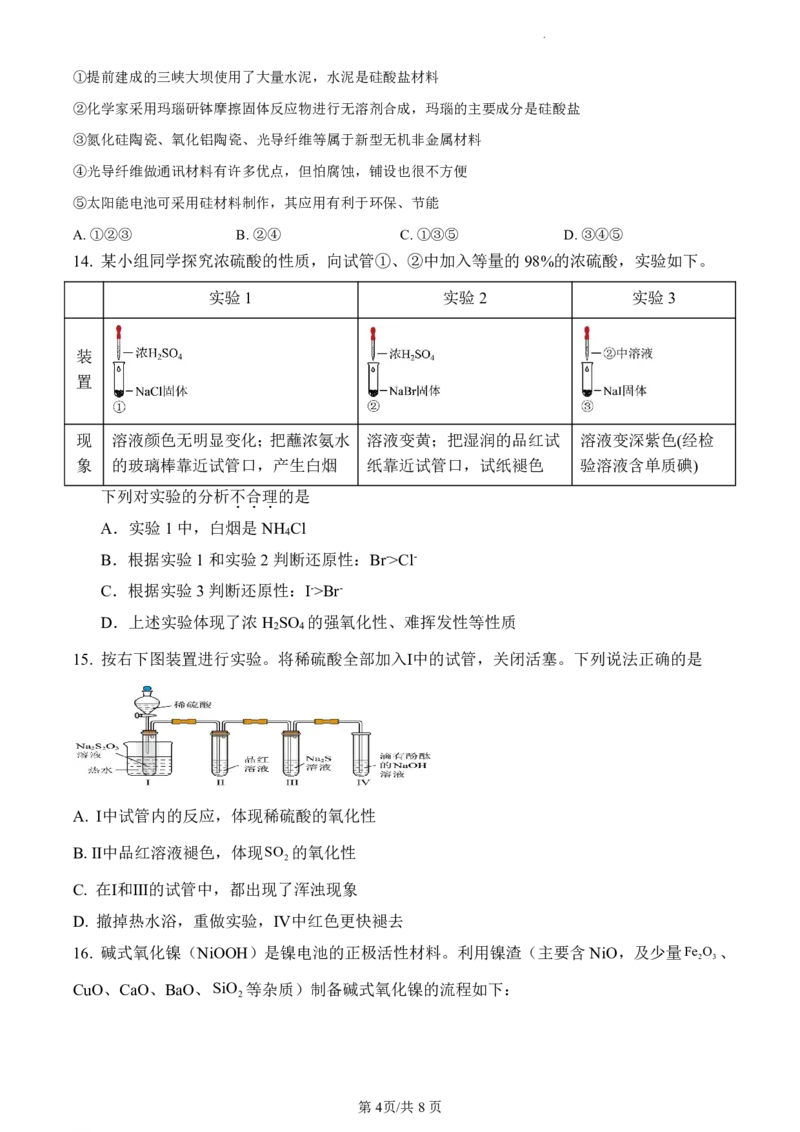
14. 某小组同学探究浓硫酸的性质,向试管①、②中加入等量的98%的浓硫酸,实验如下。
实验1 实验2 实验3
装
置
现 溶液颜色无明显变化;把蘸浓氨水 溶液变黄;把湿润的品红试 溶液变深紫色(经检
象 的玻璃棒靠近试管口,产生白烟 纸靠近试管口,试纸褪色 验溶液含单质碘)
下列对实验的分析不合理的是
...
A.实验1中,白烟是NH Cl
4
B.根据实验1和实验2判断还原性:Br->Cl-
C.根据实验3判断还原性:I->Br-
D.上述实验体现了浓H SO 的强氧化性、难挥发性等性质
2 4
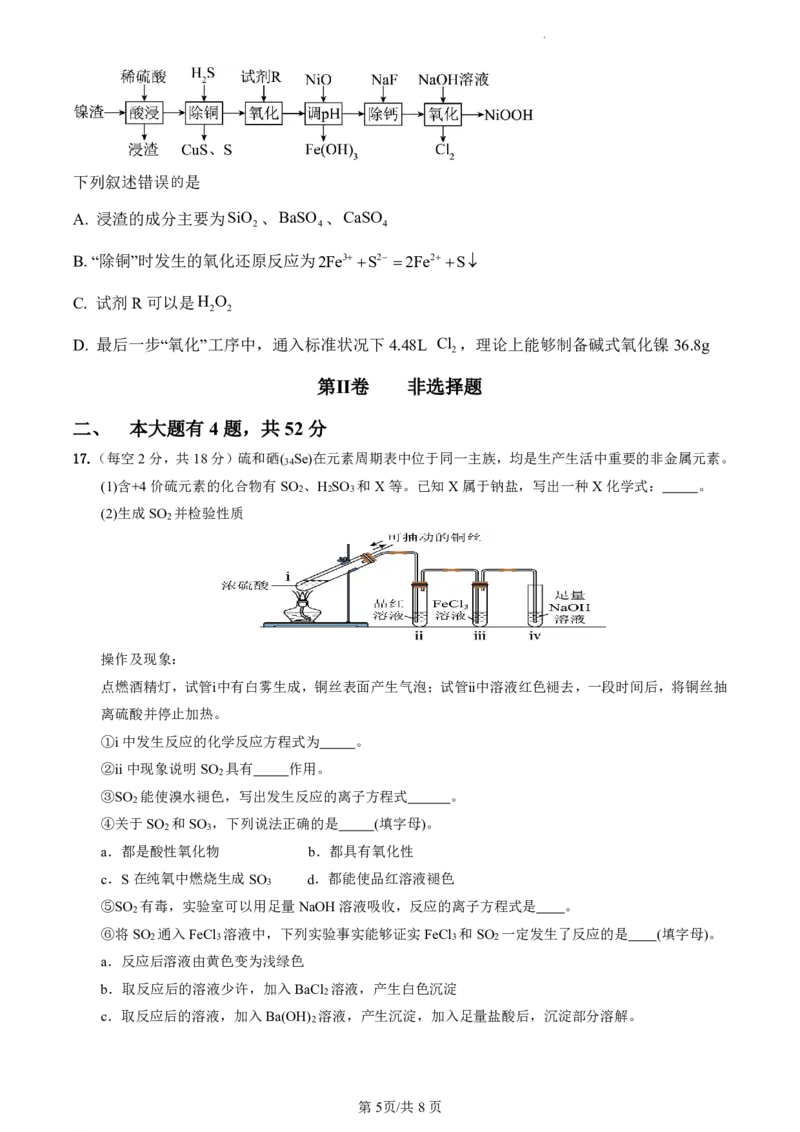
15. 按右下图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法正确的是
A. Ⅰ中试管内的反应,体现稀硫酸的氧化性
B. Ⅱ中品红溶液褪色,体现SO 的氧化性
2
C. 在Ⅰ和Ⅲ的试管中,都出现了浑浊现象
D. 撤掉热水浴,重做实验,Ⅳ中红色更快褪去
16. 碱式氧化镍(NiOOH)是镍电池的正极活性材料。利用镍渣(主要含NiO,及少量Fe O 、
2 3
CuO、CaO、BaO、SiO 等杂质)制备碱式氧化镍的流程如下:
2
第4页/共8页
学科网(北京)股份有限公司下列叙述错误的是
A. 浸渣的成分主要为SiO 、BaSO 、CaSO
2 4 4
B. “除铜”时发生的氧化还原反应为2Fe3 S2 2Fe2 S
C. 试剂R可以是H O
2 2
D. 最后一步“氧化”工序中,通入标准状况下4.48L Cl ,理论上能够制备碱式氧化镍36.8g
2
第Ⅱ卷 非选择题
二、 本大题有 4 题,共 52 分
17.(每空2分,共18分)硫和硒( Se)在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
34
(1)含+4价硫元素的化合物有SO 、H SO 和X等。已知X属于钠盐,写出一种X化学式: 。
2 2 3
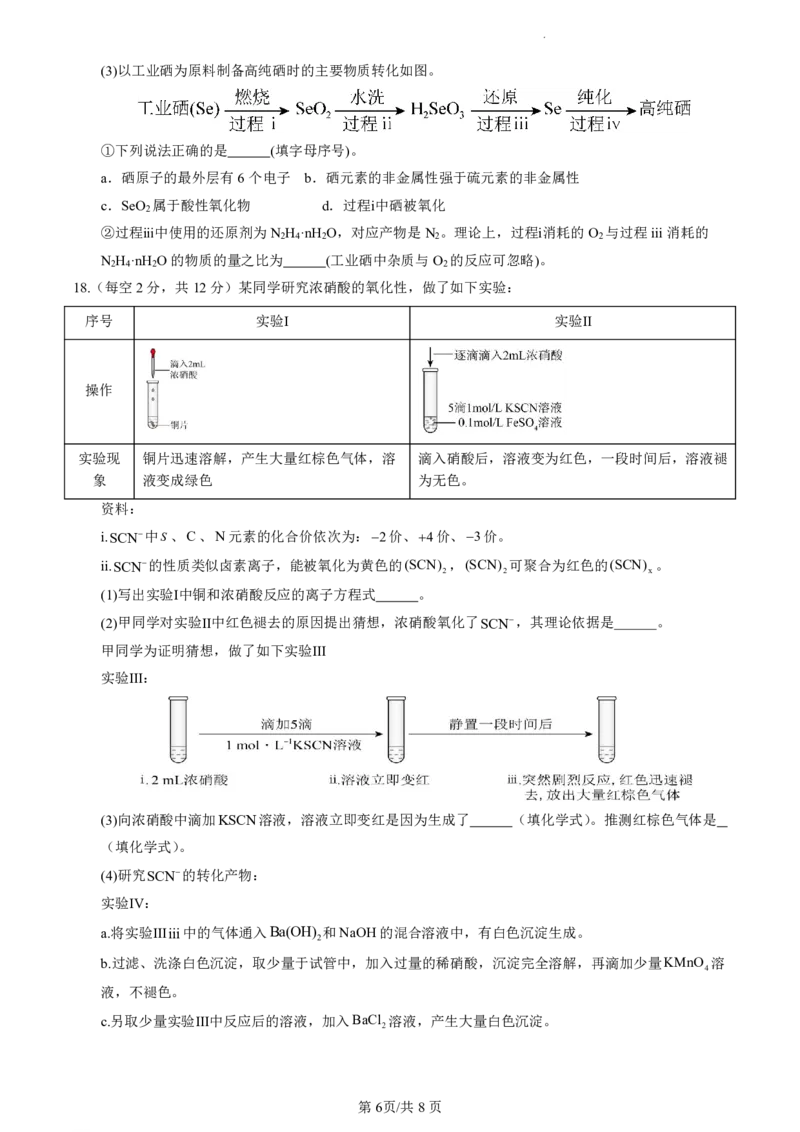
(2)生成SO 并检验性质
2
操作及现象:
点燃酒精灯,试管ⅰ中有白雾生成,铜丝表面产生气泡;试管ⅱ中溶液红色褪去,一段时间后,将铜丝抽
离硫酸并停止加热。
①i中发生反应的化学反应方程式为 。
②ii中现象说明SO 具有 作用。
2
③SO 能使溴水褪色,写出发生反应的离子方程式 。
2
④关于SO 和SO ,下列说法正确的是 (填字母)。
2 3
a.都是酸性氧化物 b.都具有氧化性
c.S在纯氧中燃烧生成SO d.都能使品红溶液褪色
3
⑤SO 有毒,实验室可以用足量NaOH溶液吸收,反应的离子方程式是 。
2
⑥将SO 通入FeCl 溶液中,下列实验事实能够证实FeCl 和SO 一定发生了反应的是 (填字母)。
2 3 3 2
a.反应后溶液由黄色变为浅绿色
b.取反应后的溶液少许,加入BaCl 溶液,产生白色沉淀
2
c.取反应后的溶液,加入Ba(OH) 溶液,产生沉淀,加入足量盐酸后,沉淀部分溶解。
2
第5页/共8页
学科网(北京)股份有限公司(3)以工业硒为原料制备高纯硒时的主要物质转化如图。
①下列说法正确的是 (填字母序号)。
a.硒原子的最外层有6个电子 b.硒元素的非金属性强于硫元素的非金属性
c.SeO 属于酸性氧化物 d.过程ⅰ中硒被氧化
2
②过程ⅲ中使用的还原剂为N H ·nH O,对应产物是N 。理论上,过程ⅰ消耗的O 与过程iii消耗的
2 4 2 2 2
N H ·nH O的物质的量之比为 (工业硒中杂质与O 的反应可忽略)。
2 4 2 2
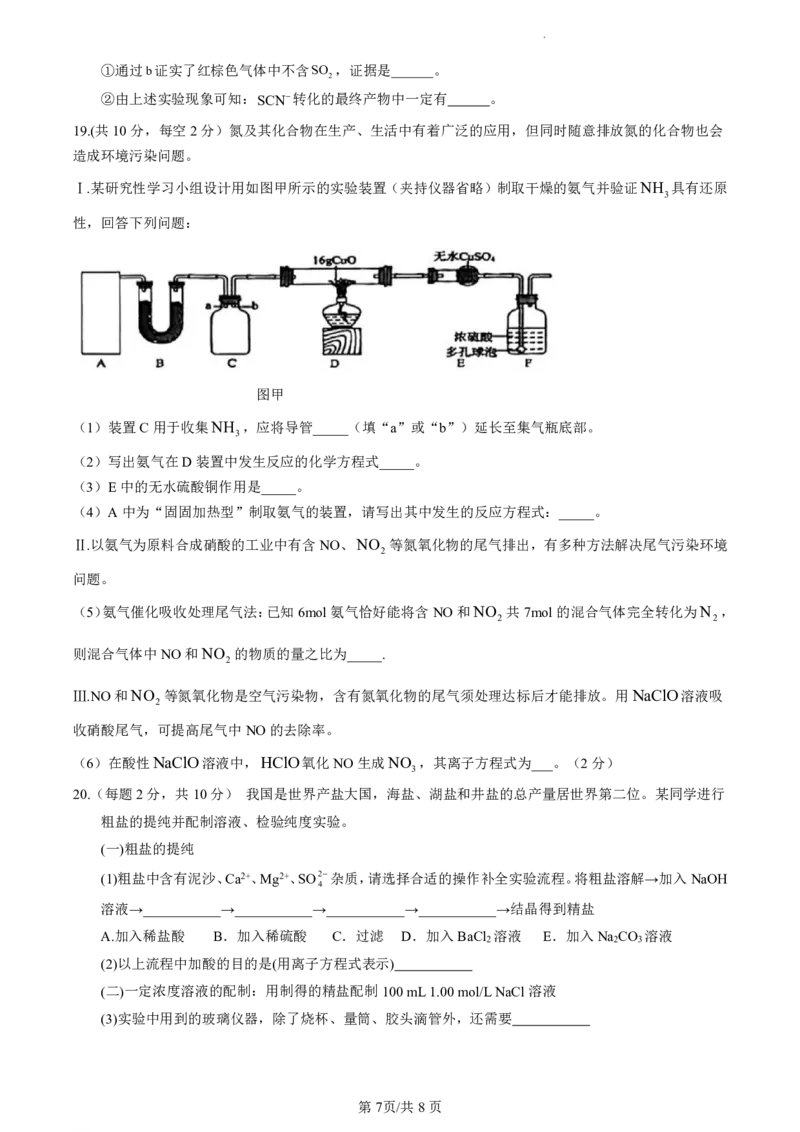
18.(每空2分,共12分)某同学研究浓硝酸的氧化性,做了如下实验:
序号 实验Ⅰ 实验Ⅱ
操作
实验现 铜片迅速溶解,产生大量红棕色气体,溶 滴入硝酸后,溶液变为红色,一段时间后,溶液褪
象 液变成绿色 为无色。
资料:
i.SCN中S、C、N元素的化合价依次为:2价、4价、3价。
ii.SCN的性质类似卤素离子,能被氧化为黄色的(SCN) ,(SCN) 可聚合为红色的(SCN) 。
2 2 x
(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式 。
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了SCN,其理论依据是 。
甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ:
(3)向浓硝酸中滴加KSCN溶液,溶液立即变红是因为生成了 (填化学式)。推测红棕色气体是
(填化学式)。
(4)研究SCN的转化产物:
实验Ⅳ:
a.将实验Ⅲiii中的气体通入Ba(OH) 和NaOH的混合溶液中,有白色沉淀生成。
2
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO 溶
4
液,不褪色。
c.另取少量实验Ⅲ中反应后的溶液,加入BaCl 溶液,产生大量白色沉淀。
2
第6页/共8页
学科网(北京)股份有限公司①通过b证实了红棕色气体中不含SO ,证据是 。
2
②由上述实验现象可知:SCN转化的最终产物中一定有 。
19.(共10分,每空2分)氮及其化合物在生产、生活中有着广泛的应用,但同时随意排放氮的化合物也会
造成环境污染问题。
Ⅰ.某研究性学习小组设计用如图甲所示的实验装置(夹持仪器省略)制取干燥的氨气并验证NH 具有还原
3
性,回答下列问题:
图甲
(1)装置C用于收集NH ,应将导管_____(填“a”或“b”)延长至集气瓶底部。
3
(2)写出氨气在D装置中发生反应的化学方程式_____。
(3)E中的无水硫酸铜作用是_____。
(4)A中为“固固加热型”制取氨气的装置,请写出其中发生的反应方程式:_____。
Ⅱ.以氨气为原料合成硝酸的工业中有含NO、NO 等氮氧化物的尾气排出,有多种方法解决尾气污染环境
2
问题。
(5)氨气催化吸收处理尾气法:已知6mol氨气恰好能将含NO和NO 共7mol的混合气体完全转化为N ,
2 2
则混合气体中NO和NO 的物质的量之比为_____.
2
Ⅲ.NO和NO 等氮氧化物是空气污染物,含有氮氧化物的尾气须处理达标后才能排放。用NaClO溶液吸
2
收硝酸尾气,可提高尾气中NO的去除率。
(6)在酸性NaClO溶液中,HClO氧化NO生成NO ,其离子方程式为___。(2分)
3
20.(每题2分,共10分) 我国是世界产盐大国,海盐、湖盐和井盐的总产量居世界第二位。某同学进行
粗盐的提纯并配制溶液、检验纯度实验。
(一)粗盐的提纯
(1)粗盐中含有泥沙、Ca2+、Mg2+、SO2杂质,请选择合适的操作补全实验流程。将粗盐溶解→加入NaOH
4
溶液→___________→___________→___________→___________→结晶得到精盐
A.加入稀盐酸 B.加入稀硫酸 C.过滤 D.加入BaCl 溶液 E.加入Na CO 溶液
2 2 3
(2)以上流程中加酸的目的是(用离子方程式表示)
(二)一定浓度溶液的配制:用制得的精盐配制100mL1.00mol/LNaCl溶液
(3)实验中用到的玻璃仪器,除了烧杯、量筒、胶头滴管外,还需要
第7页/共8页
学科网(北京)股份有限公司(4)定容时的操作:当液面离容量瓶刻度线1~2cm时, ,再将容量瓶塞盖好,反复上下颠
倒,摇匀。
(5)下列操作会使配得的NaCl溶液浓度偏低的是___________。
A.没有进行洗涤操作
B.定容时俯视容量瓶的刻度线
C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制
第8页/共8页
学科网(北京)股份有限公司