文档内容
绝密★考试结束前
2025 学年第一学期期中杭州地区(含周边)重点中学
高一年级化学学科试题
命题:萧山中学 张满满、孟红玲 审校:缙云中学 王春相 嵊州中学 陶袁燕 校稿:吕 欣
考生须知:
1.本卷满分100分,考试时间90分钟;
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字;
3.所有答案必须写在答题卷上,写在试卷上无效;
4.考试结束后,只需上交答题卷。
5.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 P-31 S-32
Cl-35.5 K-39 Ca-40 Cr-52 Fe-56 Cu-64
选择题部分
一、选择题(本大题共25小题,每小题2分,共50分。每小题列出的四个备选项中只有一个是符
合题目要求的,不选、多选、错选均不得分)
1.下列属于碱性氧化物的是
A.CO B.Na O C.Mn O D.Na O
2 2 2 2 7 2
2.实验是科学探究的重要手段。下列化学实验操作不正确的是
...
A B C D
A.液体的倾倒 B.灼烧金属钠 C.过滤 D.取用小块钠
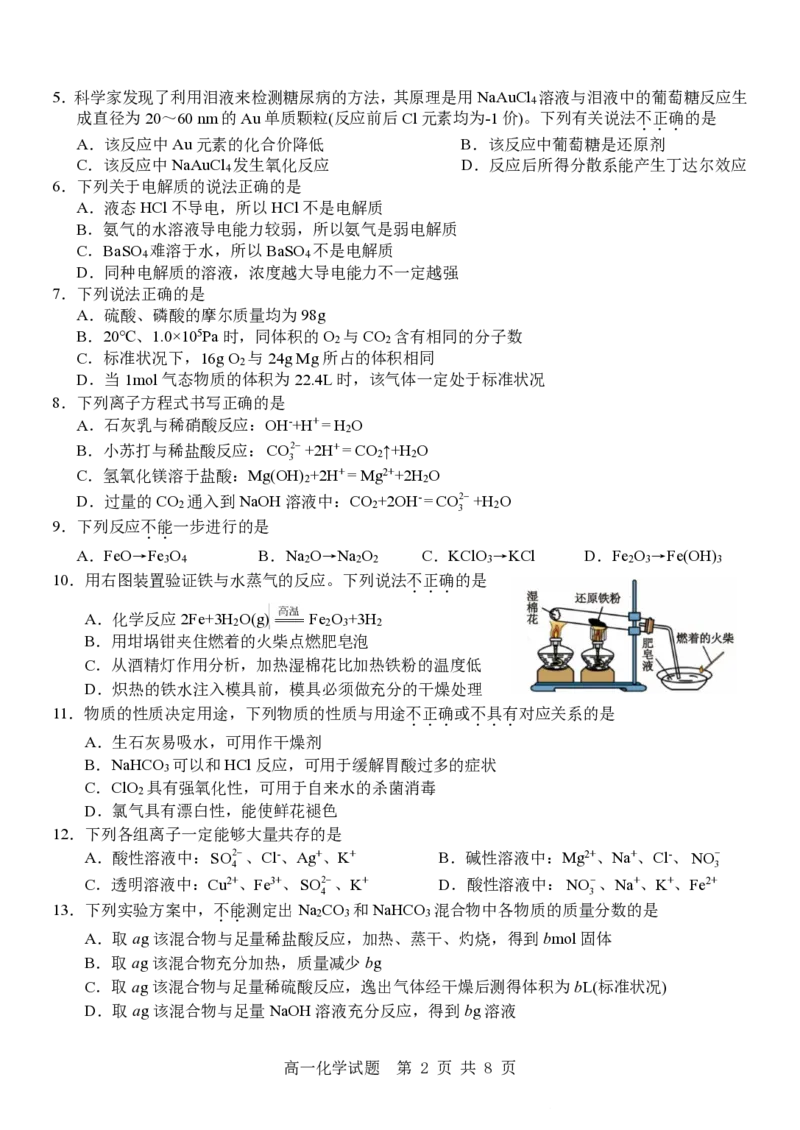
3.海洋碳循环是全球碳循环的重要组成部分,是影响全球气候变化的关键环节。如图为海洋碳循环
的简单原理图,图中没有涉及的反应类型为(钙化产物中含有Ca(HCO ) ,(CH O) 表示有机物,
.. 3 2 2 x
其中H、O元素的化合价与H O中相同)
2
A.置换反应 B.分解反应 C.离子反应 D.氧化还原反应
4.实验室中下列做法正确的是
A.含重金属离子的废液,加水稀释后可以排放
B. 表示腐蚀金属或严重灼烧皮肤、损伤眼睛的物质
C.碱液溅到皮肤上应立即用大量水冲洗,然后再涂上3%的NaHCO 溶液
3
D.实验室不慎引起金属钠着火,应立即用泡沫灭火器进行灭火
高一化学试题 第 1 页 共 8 页5.科学家发现了利用泪液来检测糖尿病的方法,其原理是用NaAuCl 溶液与泪液中的葡萄糖反应生
4
成直径为20~60 nm的Au单质颗粒(反应前后Cl元素均为-1价)。下列有关说法不正确的是
...
A.该反应中Au元素的化合价降低 B.该反应中葡萄糖是还原剂
C.该反应中NaAuCl 发生氧化反应 D.反应后所得分散系能产生丁达尔效应
4
6.下列关于电解质的说法正确的是
A.液态HCl不导电,所以HCl不是电解质
B.氨气的水溶液导电能力较弱,所以氨气是弱电解质
C.BaSO 难溶于水,所以BaSO 不是电解质
4 4
D.同种电解质的溶液,浓度越大导电能力不一定越强
7.下列说法正确的是
A.硫酸、磷酸的摩尔质量均为98g
B.20℃、1.0×105Pa时,同体积的O 与CO 含有相同的分子数
2 2
C.标准状况下,16g O 与24g Mg所占的体积相同
2
D.当1mol气态物质的体积为22.4L时,该气体一定处于标准状况
8.下列离子方程式书写正确的是
A.石灰乳与稀硝酸反应:OH-+H+ = H O
2
B.小苏打与稀盐酸反应:
高一化学试题 第 2 页 共 8 页
C O 23 − +2H+ = CO ↑+H O
2 2
C.氢氧化镁溶于盐酸:Mg(OH) +2H+ = Mg2++2H O
2 2
D.过量的CO 通入到NaOH溶液中:CO +2OH- =
2 2
C O 23 − +H O
2
9.下列反应不能一步进行的是
..
A.FeO→Fe O B.Na O→Na O C.KClO →KCl D.Fe O →Fe(OH)
3 4 2 2 2 3 2 3 3
10.用右图装置验证铁与水蒸气的反应。下列说法不正确的是
...
A.化学反应2Fe+3H O(g) Fe O +3H
2 2 3 2
B.用坩埚钳夹住燃着的火柴点燃肥皂泡
C.从酒精灯作用分析,加热湿棉花比加热铁粉的温度低
D.炽热的铁水注入模具前,模具必须做充分的干燥处理
11.物质的性质决定用途,下列物质的性质与用途不正确或不具有对应关系的是
... ...
A.生石灰易吸水,可用作干燥剂
B.NaHCO 可以和HCl反应,可用于缓解胃酸过多的症状
3
C.ClO 具有强氧化性,可用于自来水的杀菌消毒
2
D.氯气具有漂白性,能使鲜花褪色
12.下列各组离子一定能够大量共存的是
A.酸性溶液中: S O 24 − 、Cl-、Ag+、K+ B.碱性溶液中:Mg2+、Na+、Cl-、 N O −3
C.透明溶液中:Cu2+、Fe3+、SO2−、K+ D.酸性溶液中:
4
N O −3 、Na+、K+、Fe2+
13.下列实验方案中,不能测定出Na CO 和NaHCO 混合物中各物质的质量分数的是
.. 2 3 3
A.取ag该混合物与足量稀盐酸反应,加热、蒸干、灼烧,得到bmol固体
B.取ag该混合物充分加热,质量减少bg
C.取ag该混合物与足量稀硫酸反应,逸出气体经干燥后测得体积为bL(标准状况)
D.取ag该混合物与足量NaOH溶液充分反应,得到bg溶液14.下表中“方法导引”所对应的“示例”不正确的是
...
方法导引 示例
A 实验室中制取气体装置的设计 依据Cl 的性质,选择NaOH溶液进行尾气处理
2
胶体的种类有很多,按照分散剂的不同,可分为
B 分类
气溶胶、液溶胶和固溶胶
从元素价态来看,Fe O 中铁元素的化合价是+3
2 3
C 认识元素及其化合物性质的视角 价,处于铁元素的最高价态,因此Fe O 只有氧
2 3
化性,没有还原性
阿伦尼乌斯提出的电离模型很好地解释了酸、
D 模型
碱、盐溶液的某些性质
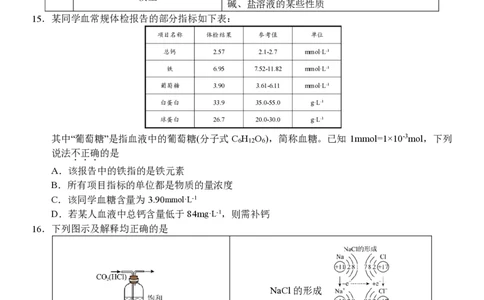
15.某同学血常规体检报告的部分指标如下表:
项目名称 体检结果 参考值 单位
总钙 2.57 2.1-2.7 mmol·L-1
铁 6.95 7.52-11.82 mmol·L-1
葡萄糖 3.90 3.61-6.11 mmol·L-1
白蛋白 33.9 35.0-55.0 g·L-1
球蛋白 26.7 20.0-30.0 g·L-1
其中“葡萄糖”是指血液中的葡萄糖(分子式 C H O ),简称血糖。已知 1mmol=1×10-3mol,下列
6 12 6
说法不正确的是
...
A.该报告中的铁指的是铁元素
B.所有项目指标的单位都是物质的量浓度
C.该同学血糖含量为3.90mmol·L-1
D.若某人血液中总钙含量低于84mg·L-1,则需补钙
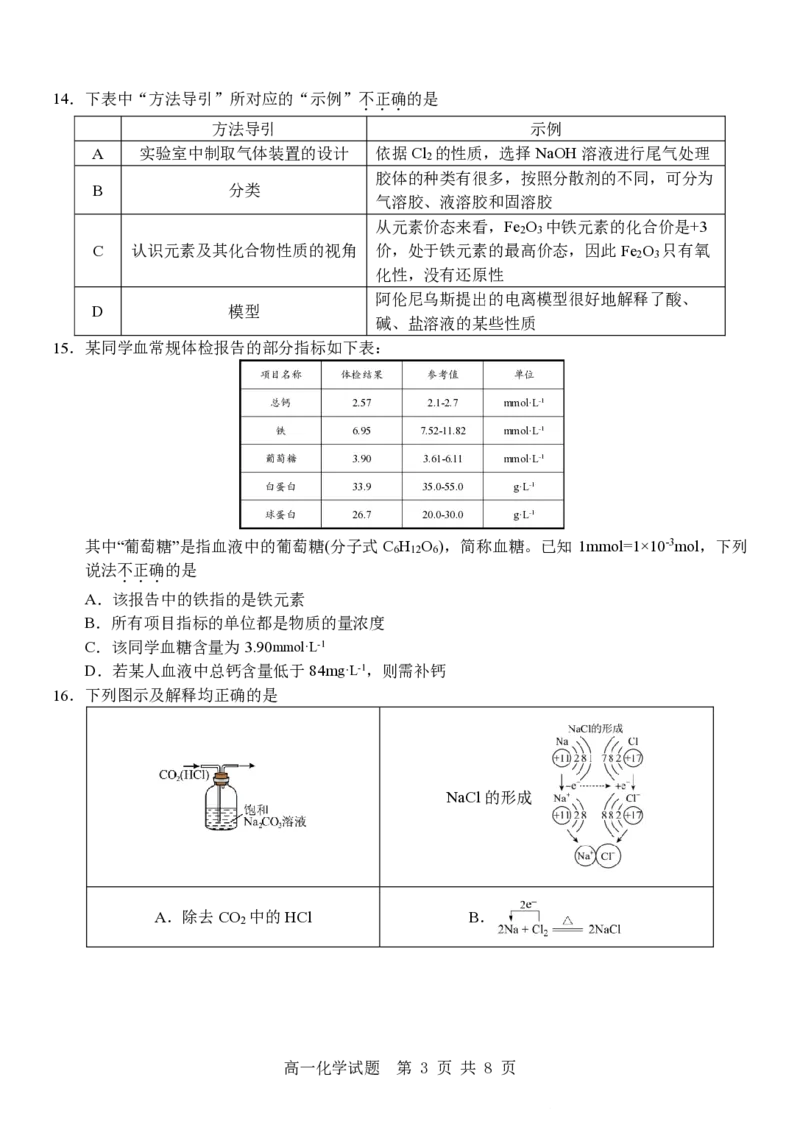
16.下列图示及解释均正确的是
NaCl的形成
A.除去CO 中的HCl B.
2
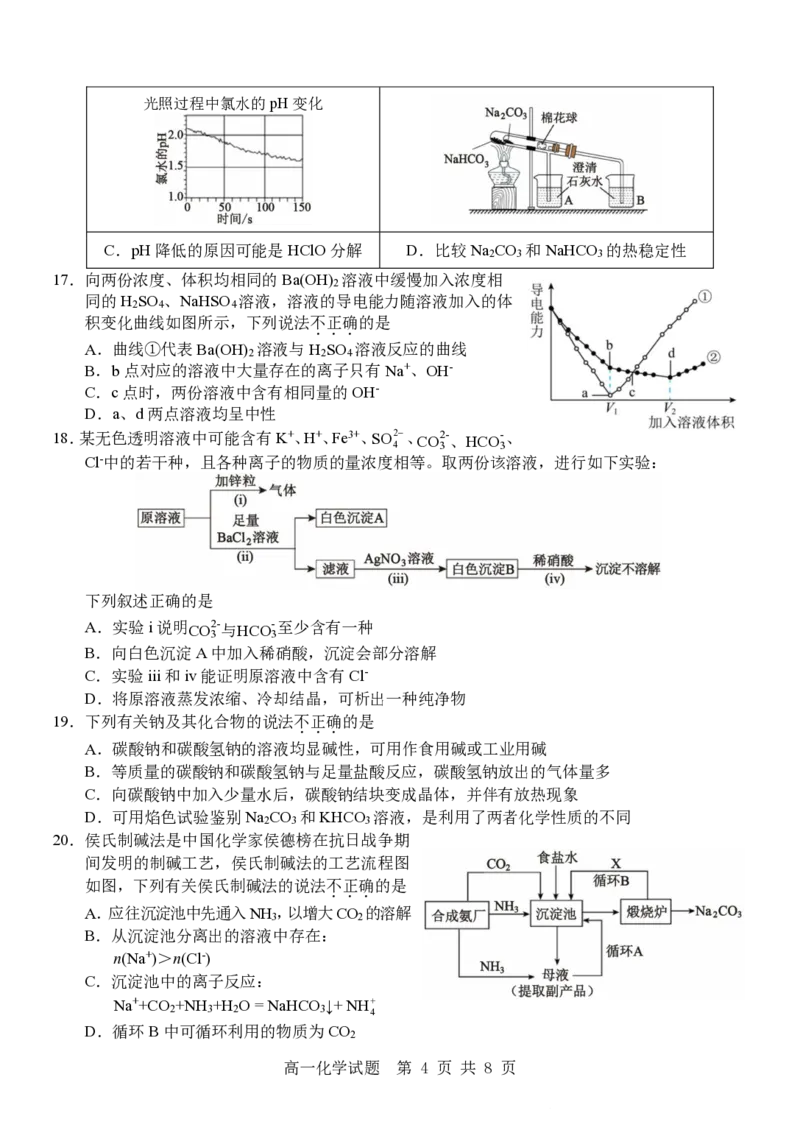
高一化学试题 第 3 页 共 8 页光照过程中氯水的pH变化
C.pH降低的原因可能是HClO分解 D.比较Na CO 和NaHCO 的热稳定性
2 3 3
17.向两份浓度、体积均相同的Ba(OH) 溶液中缓慢加入浓度相
2
同的H SO 、NaHSO 溶液,溶液的导电能力随溶液加入的体
2 4 4
积变化曲线如图所示,下列说法不正确的是
...
A.曲线①代表Ba(OH) 溶液与H SO 溶液反应的曲线
2 2 4
B.b点对应的溶液中大量存在的离子只有Na+、OH-
C.c点时,两份溶液中含有相同量的OH-
D.a、d两点溶液均呈中性
18.某无色透明溶液中可能含有K+、H+、Fe3+、
高一化学试题 第 4 页 共 8 页
S O 24 − 、CO 2-、HCO -、
3 3
Cl-中的若干种,且各种离子的物质的量浓度相等。取两份该溶液,进行如下实验:
下列叙述正确的是
A.实验i说明CO 2-与HCO -至少含有一种
3 3
B.向白色沉淀A中加入稀硝酸,沉淀会部分溶解
C.实验iii和iv能证明原溶液中含有Cl-
D.将原溶液蒸发浓缩、冷却结晶,可析出一种纯净物
19.下列有关钠及其化合物的说法不正确的是
...
A.碳酸钠和碳酸氢钠的溶液均显碱性,可用作食用碱或工业用碱
B.等质量的碳酸钠和碳酸氢钠与足量盐酸反应,碳酸氢钠放出的气体量多
C.向碳酸钠中加入少量水后,碳酸钠结块变成晶体,并伴有放热现象
D.可用焰色试验鉴别Na CO 和KHCO 溶液,是利用了两者化学性质的不同
2 3 3
20.侯氏制碱法是中国化学家侯德榜在抗日战争期
间发明的制碱工艺,侯氏制碱法的工艺流程图
如图,下列有关侯氏制碱法的说法不正确的是
...
A.应往沉淀池中先通入NH,以增大CO 的溶解
3 2
B.从沉淀池分离出的溶液中存在:
n(Na+)>n(Cl-)
C.沉淀池中的离子反应:
Na++CO +NH +H O = NaHCO ↓+NH+
2 3 2 3 4
D.循环B中可循环利用的物质为CO
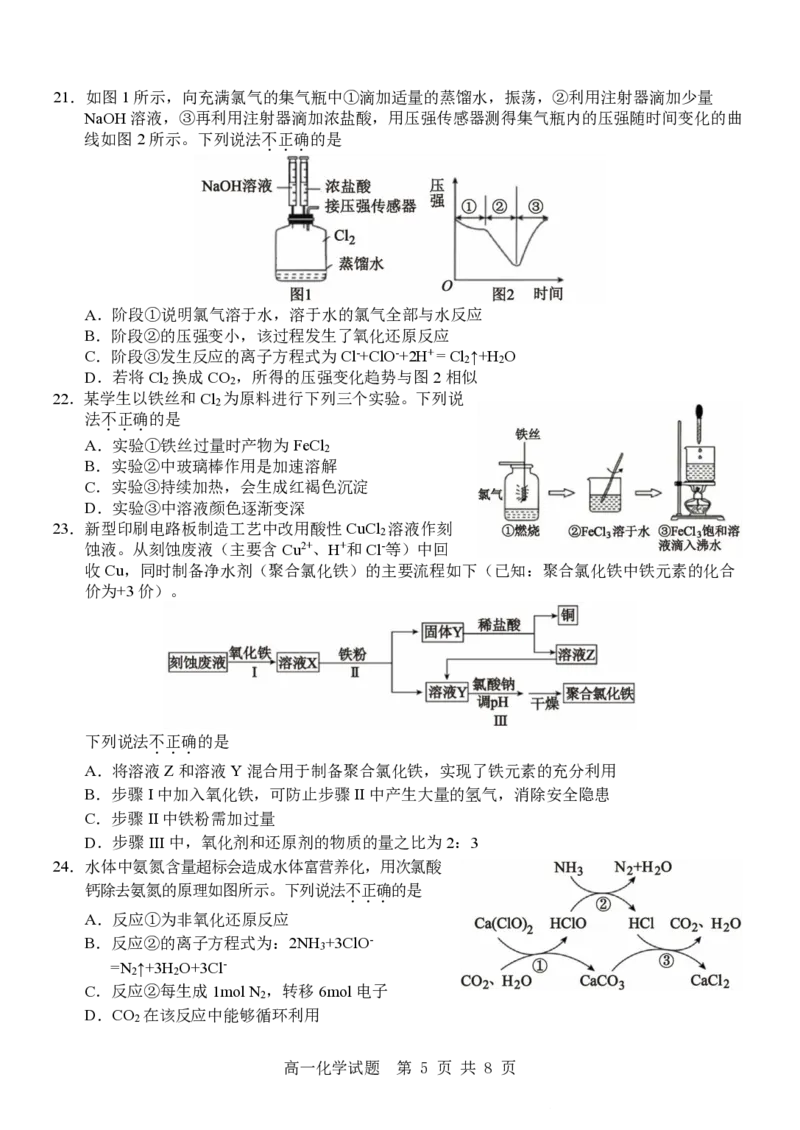
221.如图1所示,向充满氯气的集气瓶中①滴加适量的蒸馏水,振荡,②利用注射器滴加少量
NaOH溶液,③再利用注射器滴加浓盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲
线如图2所示。下列说法不正确的是
...
A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段②的压强变小,该过程发生了氧化还原反应
C.阶段③发生反应的离子方程式为Cl-+ClO-+2H+ = Cl ↑+H O
2 2
D.若将Cl 换成CO ,所得的压强变化趋势与图2相似
2 2
22.某学生以铁丝和Cl 为原料进行下列三个实验。下列说
2
法不正确的是
...
A.实验①铁丝过量时产物为FeCl
2
B.实验②中玻璃棒作用是加速溶解
C.实验③持续加热,会生成红褐色沉淀
D.实验③中溶液颜色逐渐变深
23.新型印刷电路板制造工艺中改用酸性CuCl 溶液作刻
2
蚀液。从刻蚀废液(主要含Cu2+、H+和Cl-等)中回
收Cu,同时制备净水剂(聚合氯化铁)的主要流程如下(已知:聚合氯化铁中铁元素的化合
价为+3价)。
下列说法不正确的是
...
A.将溶液Z和溶液Y混合用于制备聚合氯化铁,实现了铁元素的充分利用
B.步骤I中加入氧化铁,可防止步骤II中产生大量的氢气,消除安全隐患
C.步骤II中铁粉需加过量
D.步骤III中,氧化剂和还原剂的物质的量之比为2:3
24.水体中氨氮含量超标会造成水体富营养化,用次氯酸
钙除去氨氮的原理如图所示。下列说法不正确的是
...
A.反应①为非氧化还原反应
B.反应②的离子方程式为:2NH +3ClO-
3
=N ↑+3H O+3Cl-
2 2
C.反应②每生成1mol N ,转移6mol电子
2
D.CO 在该反应中能够循环利用
2
高一化学试题 第 5 页 共 8 页25.下列实验操作及现象和结论都正确的是
实验操作及现象 结论
一块状金属钠放置于空气中一段时间后,将所得的 钠与空气中的氧气反应生
A
固体投入水中,得到较多的气泡 成了Na O
2 2
用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的 红色褪去的可能原因之一
B 氢氧化钠稀溶液中,当滴到一定量时,红色突然褪 为氯水中的HClO具有强
去 氧化性,将酚酞氧化
C 用湿润的淀粉碘化钾试纸检验气体Y,试纸变蓝色 Y是Cl
2
为检验纯碱溶液中是否存在NaCl,向待测液中加入
D 溶液中存在NaCl
AgNO 溶液,有白色沉淀生成
3
非选择题部分
二、填空题(本大题共5小题,共50分)
26.(10分)
(1)在常温下,将Cl 通入NaOH溶液中制得漂白液的离子反应方程式为 ▲ ,该漂白
2
液的有效成分是 ▲ (填名称)。
(2)“嫦娥五号”取回的月岩的主要成分是钛酸亚铁(FeTiO ),其在熔融状态下可以导电,
3
该电离方程式为 ▲ 。
(3)“天问一号”探测器的太阳能电池板使用的材料是硅。工业上利用石英砂(主要成分为
高温
SiO )制取粗硅的反应原理是SiO +2C=Si+2CO↑。
2 2
①该反应的反应类型为 ▲ (填基本反应类型)。
②用双线桥标出该反应的电子转移的方向和数目: ▲ 。
27.(10分)实验室用浓盐酸(下图为该试剂瓶上标签的有关内容)配制稀盐酸。
名称:盐酸 溶质分子式:HCl
相对分子质量:36.5
密度:1.2 g/cm3
质量分数:36.5%
(1)用该浓盐酸配制0.2 mol·L-1的稀盐酸450mL,量筒量取浓盐酸的体积约为 ▲
mL,应选用的量筒规格为 ▲ (填5mL、10mL、25mL、50mL)。
(2)该实验中必须用到的玻璃仪器有:玻璃棒、烧杯、胶头滴管、量筒、 ▲ 。
(3)下列关于容量瓶的相关操作,正确的是 ▲ 。
(4)配制上述溶液时,其它操作都准确,下列操作会导致所配溶液的浓度偏低的是 ▲
..
(填序号)。
高一化学试题 第 6 页 共 8 页a.量筒、容量瓶洗涤后,未干燥即用来配制溶液
b.量筒量取浓盐酸时,仰视凹液面读数
c.量筒倒出浓盐酸后,用蒸馏水洗涤量筒,并将洗涤液转移至容量瓶中
d.定容时,俯视凹液面读数
e.定容时水多、超过刻度线,用胶头滴管吸出
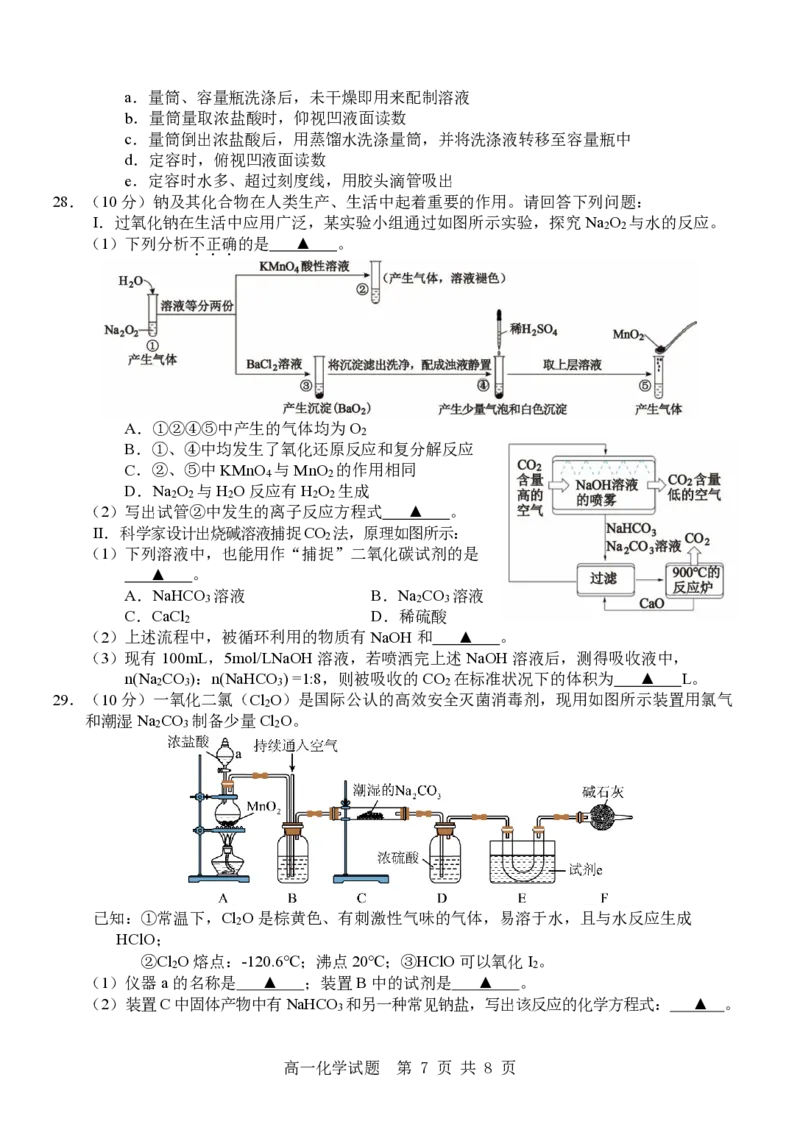
28.(10分)钠及其化合物在人类生产、生活中起着重要的作用。请回答下列问题:
Ⅰ.过氧化钠在生活中应用广泛,某实验小组通过如图所示实验,探究Na O 与水的反应。
2 2
(1)下列分析不正确的是 ▲ 。
...
A.①②④⑤中产生的气体均为O
2
B.①、④中均发生了氧化还原反应和复分解反应
C.②、⑤中KMnO 与MnO 的作用相同
4 2
D.Na O 与H O反应有H O 生成
2 2 2 2 2
(2)写出试管②中发生的离子反应方程式 ▲ 。
Ⅱ.科学家设计出烧碱溶液捕捉CO 法,原理如图所示:
2
(1)下列溶液中,也能用作“捕捉”二氧化碳试剂的是
▲ 。
A.NaHCO 溶液 B.Na CO 溶液
3 2 3
C.CaCl D.稀硫酸
2
(2)上述流程中,被循环利用的物质有NaOH和 ▲ 。
(3)现有100mL,5mol/LNaOH溶液,若喷洒完上述NaOH溶液后,测得吸收液中,
n(Na CO ):n(NaHCO ) =1:8,则被吸收的CO 在标准状况下的体积为 ▲ L。
2 3 3 2
29.(10分)一氧化二氯(Cl O)是国际公认的高效安全灭菌消毒剂,现用如图所示装置用氯气
2
和潮湿Na CO 制备少量Cl O。
2 3 2
已知:①常温下,Cl O是棕黄色、有刺激性气味的气体,易溶于水,且与水反应生成
2
HClO;
②Cl O熔点:-120.6℃;沸点20℃;③HClO可以氧化I 。
2 2
(1)仪器a的名称是 ▲ ;装置B中的试剂是 ▲ 。
(2)装置C中固体产物中有NaHCO 和另一种常见钠盐,写出该反应的化学方程式: ▲ 。
3
高一化学试题 第 7 页 共 8 页(3)装置E水槽中盛装的试剂e是 ▲ 。(填序号)
A.自来水 B.热水 C.冰水混合物 D.CCl
4
(4)装置F中碱石灰的作用是 ▲ 。
(5)为进一步探究Cl O的性质,甲同学取E中Cl O逐滴滴入淀粉-KI溶液至过量,可观察
2 2
到的实验现象为 ▲ 。
30.(10分)铁的化合物具有重要用途。
(1)铁元素是人体必不可少的元素之一,用于生成红细胞。某品牌补血剂的说明书如下表所
示,回答下列问题。
①补血剂成分中含有“维生素C”,维生素C的作用是 ▲ 。
②“开瓶后需要放冰箱冷藏,于一个月内饮用完”,以防止Fe2+发生变质。请设计实验方
案检验 Fe2+是否发生变质: ▲ [可选用的试剂有:新制氯水、KSCN 溶液、酸性
KMnO 溶液]。
4
③实验室配制FeSO 溶液后为防止空气中的氧气使其发生变质,可用液封法。下列是三种
4
液态物质的溶解氧含量如下表,其中液封效果最好的是 ▲ (填“字母”)。
选项 A B C
物质 自来水 植物油 饱和蔗糖溶液
溶解氧含量(mg/L) 4.92 3.82 0.48
(2)聚合硫酸铁{[Fe (OH) (SO ) ] }广泛用于水的净化,以FeSO ·7H O为原料,经溶解、氧
2 6-2n 4 n m 4 2
化、水解聚合等步骤,可制备聚合硫酸铁。
①将一定量的FeSO ·7H O溶于稀硫酸,在70℃下边搅拌边缓慢加入一定量的H O 溶液,
4 2 2 2
继续反应一段时间,得到红棕色黏稠液体。H O 氧化 Fe2+的离子方程式为 ▲ 。
2 2
然后稠液体在一定条件下水解聚合生成聚合硫酸铁。
②测定聚合硫酸铁样品中铁元素的质量分数:准确称取液态样品 3.000g,置于 250mL 锥
形瓶中。加入适量稀硫酸,加热,用还原剂将铁元素全部还原为Fe2+,之后将过量的还
原剂除去。然后用0.05 mol·L-1K Cr O 溶液滴定至终点(滴定过程中CrO2−与Fe2+反应
2 2 7 2 7
生成Cr3+和Fe3+),消耗K Cr O 溶液20.00mL。计算该样品中铁元素的质量分数为
2 2 7
▲ 。
高一化学试题 第 8 页 共 8 页