文档内容
源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
2025~2026 学年上学期期中考试
28 届 高一(化学)试题
命题人:李依林 审题人:陈沛华
说明: 1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题),满分 100分。
2.考试时间:75分钟。
3.将第Ⅰ卷的答案代表字母填(涂)在答题卡上。
可能用到的相对原子质量:
H 1 C 12 O 16 N 14 Na 23 Mg 24 Al 27 Cl 35.5 Ca 40 Cr 52
第Ⅰ卷 (选择题,共 42分)
一、选择题:本题共 14 小题,每小题 3分,共 42分。每小题只有一个选项符
合题意。
1. 新中国成立以来,化学与化工事业不断发展进步,始终与国同行,精准响
应国家战略需求,深刻契合时代发展脉搏。下列叙述错误的是( )
A.闵恩泽是石油化工催化领域的专家
B.徐光宪辗转回国以后为了国家的需要多次转变研究方向,先为“两弹
一星”铺就关键基石,后发展串级萃取理论实现高效分离稀土元素
C.屠呦呦首先从中药青蒿中发现抗疟有效成分并成功提取
D.赵忠贤长期从事低温和超导研究,目前廉价的室温超导体已随处可见
2. 化学强国,吾辈担当。下列关于化学学科特征的说法中,错误的是( )
A.化学是在原子、分子水平上研究物质的一门基础科学
B.可以通过化学反应创造出新的原子、分子和具有特殊性质的新物质
C.现代化学研究中理论与实验并重
D.波谱、色谱、X射线衍射等技术手段常被应用于探究物质的结构
3. 下列关于金属钠的叙述中,正确的是( )
A.钠的密度大于煤油且小于水 B.钠可以保存在细沙中
C.钠只可能在 O 中燃烧 D.钠投入CuSO 溶液会产生红色金属
2 4
高一 (化学)试题 第1页(共6页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
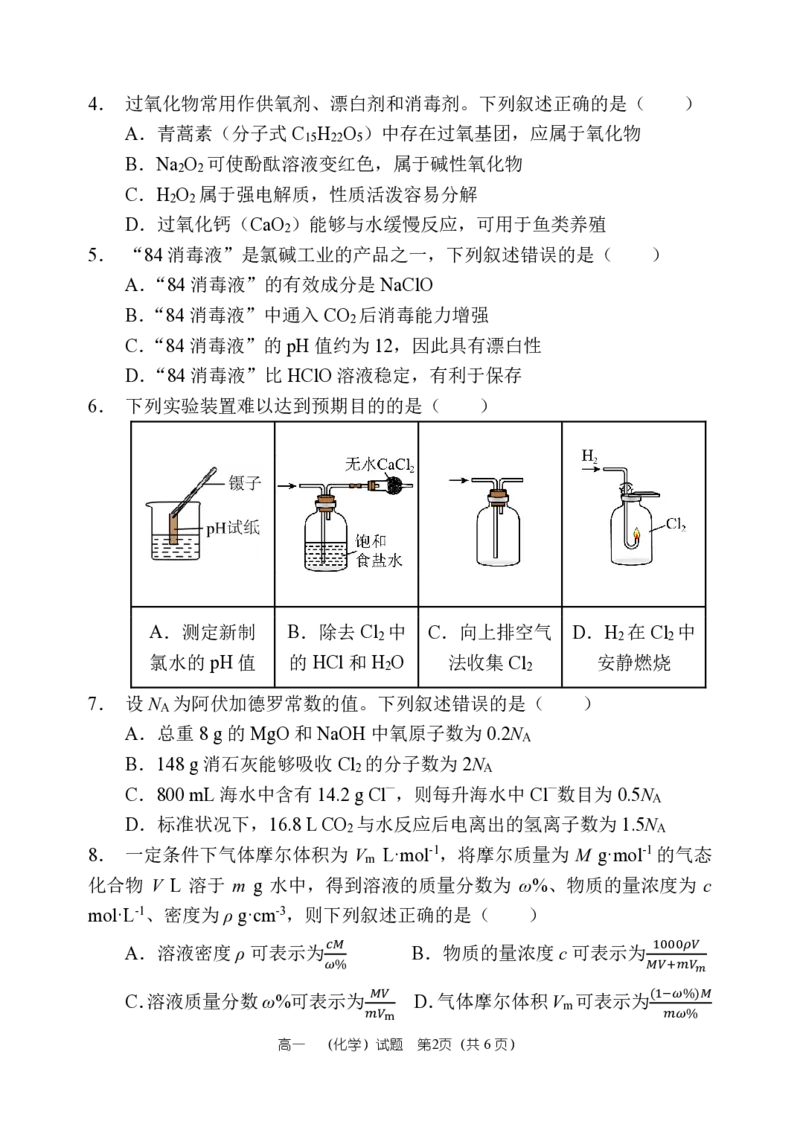
4. 过氧化物常用作供氧剂、漂白剂和消毒剂。下列叙述正确的是( )
A.青蒿素(分子式 C H O )中存在过氧基团,应属于氧化物
15 22 5
B.Na O 可使酚酞溶液变红色,属于碱性氧化物
2 2
C.H O 属于强电解质,性质活泼容易分解
2 2
D.过氧化钙(CaO )能够与水缓慢反应,可用于鱼类养殖
2
5. “84消毒液”是氯碱工业的产品之一,下列叙述错误的是( )
A.“84消毒液”的有效成分是NaClO
B.“84消毒液”中通入CO 后消毒能力增强
2
C.“84消毒液”的 pH值约为12,因此具有漂白性
D.“84消毒液”比HClO溶液稳定,有利于保存
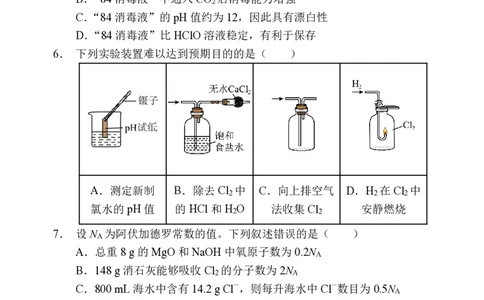
6. 下列实验装置难以达到预期目的的是( )
A.测定新制 B.除去Cl 中 C.向上排空气 D.H 在Cl 中
2 2 2
氯水的pH值 的HCl 和H O 法收集Cl 安静燃烧
2 2
7. 设N 为阿伏加德罗常数的值。下列叙述错误的是( )
A
A.总重8 g的 MgO和NaOH中氧原子数为0.2N
A
B.148 g消石灰能够吸收Cl 的分子数为 2N
2 A
C.800 mL海水中含有14.2 g Cl—,则每升海水中Cl—数目为 0.5N
A
D.标准状况下,16.8 L CO 与水反应后电离出的氢离子数为1.5N
2 A
8. 一定条件下气体摩尔体积为 V L·mol-1,将摩尔质量为 M g·mol-1的气态
m
化合物 V L 溶于 m g 水中,得到溶液的质量分数为 ω%、物质的量浓度为 c
mol·L-1、密度为ρ g·cm-3,则下列叙述正确的是( )
𝑐𝑀 1000𝜌𝑉
A.溶液密度ρ 可表示为 B.物质的量浓度c可表示为
𝜔% 𝑀𝑉+𝑚𝑉𝑚
𝑀𝑉 (1−𝜔%)𝑀
C.溶液质量分数ω%可表示为 D.气体摩尔体积V 可表示为
m
𝑚𝑉m 𝑚𝜔%
高一 (化学)试题 第2页(共6页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
9. 密闭容器内可移动的活塞两边分别充入空气和 H 与O 的混合气体且体积
2 2
比为 1:3,活塞起始位置如图所示。在室温下若将混合气体点燃,恢复至室温
后左右两室体积会变为 3:1(忽略液体体积)。则 H 和 O 的体积比为( )
2 2
空气 H 与O 混合气体
2 2
A.12:7 或15:4 B.7:12 或4:15 C.16:11或19:8 D.11:16 或 8:19
10.尖晶石是镁铝氧化物组成的矿物,主要成分为MgAl O 。其中掺杂入 Cr3+
2 4
会显红色,掺杂入Zn2+和Fe2+会显蓝色,有些颜色漂亮的可作为宝石。取一颗
7.1 g的红色尖晶石,恰好与 100 mL 一定浓度的盐酸完全反应,则该盐酸的浓
度可能是( )
A.3.5 mol·L-1 B.4.0 mol·L-1 C.4.5 mol·L-1 D.5.0 mol·L-1
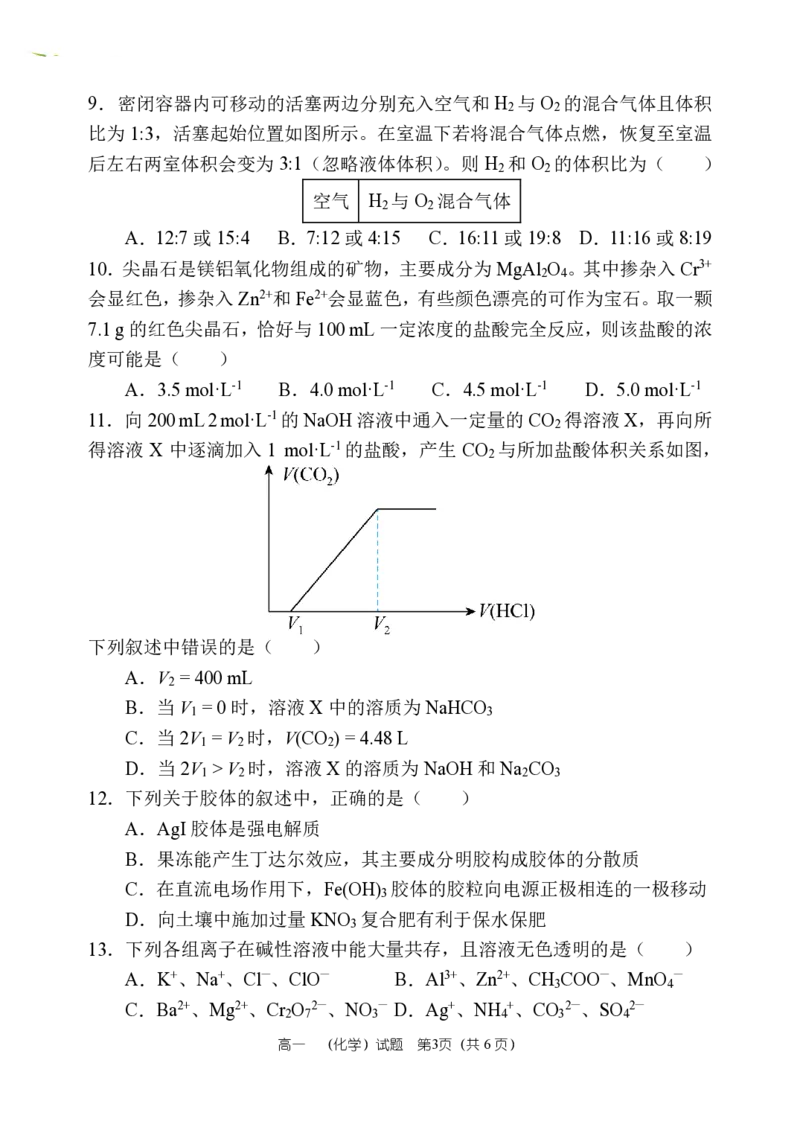
11.向200 mL 2 mol·L-1的NaOH溶液中通入一定量的 CO 得溶液 X,再向所
2
得溶液 X 中逐滴加入 1 mol·L-1的盐酸,产生 CO 与所加盐酸体积关系如图,
2
下列叙述中错误的是( )
A.V = 400 mL
2
B.当V = 0 时,溶液 X中的溶质为 NaHCO
1 3
C.当2V = V 时,V(CO ) = 4.48 L
1 2 2
D.当2V > V 时,溶液 X的溶质为 NaOH 和Na CO
1 2 2 3
12.下列关于胶体的叙述中,正确的是( )
A.AgI胶体是强电解质
B.果冻能产生丁达尔效应,其主要成分明胶构成胶体的分散质
C.在直流电场作用下,Fe(OH) 胶体的胶粒向电源正极相连的一极移动
3
D.向土壤中施加过量 KNO 复合肥有利于保水保肥
3
13.下列各组离子在碱性溶液中能大量共存,且溶液无色透明的是( )
A.K+、Na+、Cl—、ClO— B.Al3+、Zn2+、CH COO—、MnO —
3 4
C.Ba2+、Mg2+、Cr O 2—、NO — D.Ag+、NH +、CO 2—、SO 2—
2 7 3 4 3 4
高一 (化学)试题 第3页(共6页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
14.下列离子方程式正确的是( )
A.用醋酸除铁锈:Fe(OH) + 3H+ = Fe3+ + 3H O
3 2
B.侯氏制碱法的碳化反应:Na+ + NH + H O + CO = NaHCO ↓ + NH +
3 2 2 3 4
C.向Ba(OH) 溶液中加入过量的NH HSO 溶液:
2 4 4
Ba2+ + 2OH— + NH + + H+ + SO 2— = BaSO ↓ + NH ↑ + 2H O
4 4 4 3 2
D.向NaHCO 溶液中加入少量的Ca(OH) 溶液:
3 2
HCO — + Ca2+ + OH— = CaCO ↓ + 2H O
3 3 2
第Ⅱ卷 (非选择题,共 58分)
二、非选择题:本题共 4小题,共 58分。
15.(15 分) 在食品加工过程中加入膨松剂,
【名 称】××复合膨松剂
可以让食品口感变得松软酥脆。复合膨松剂 【保质期】24个月
【使用量】面粉用量的 0.5%-
产生气体速率稳定、产气分布均匀,且使用方
2.5%
便。有一复合膨松剂说明书如右图所示,其宣
【配 料】碳酸氢钠、焦磷酸二
氢二钠、碳酸钙、葡萄糖酸-δ-内
传的产品特点为“遇水发酵之后,再放入烤 酯、淀粉
【储存方法】阴凉干燥处储存
箱,遇热还会持续发酵,产生更多的气体”。
回答下列问题:
(1) 配料中属于酸式盐的是 、 ,请写出其中之一溶于水
的电离方程式 。
(2) 配料中助剂为 ,其作用是 。
(3) 已知,焦磷酸和焦磷酸盐的熔沸点较高;焦磷酸钙不溶于水,但可溶
于强酸。有实验小组计划测定复合膨松剂中钙盐的含量,但发现将复合膨松剂
溶于水后始终存在难溶物。对此有同学提出不同的猜想:
甲:焦磷酸钙不溶于水,难溶物应为焦磷酸钙。
乙: 。
① 乙同学可能的猜想是: 。
② 请给出验证甲乙两位同学猜想的合理方案: 。
③ 实验小组改进方案,用适量盐酸溶解复合膨松剂,配制成一定浓度的
溶液后取约480 mL 用于测定钙的含量。小组选取了一些玻璃仪器:烧杯、
玻璃棒,一定还需要的玻璃仪器为 、 。
高一 (化学)试题 第4页(共6页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
④ 取 14.75 g 复合膨松剂用足量盐酸溶解,逸出气体(忽略 HCl 挥发)
干燥后用碱石灰吸收,质量增加 3.52 g。最终测得样品中钙含量为 2.00 g。则
复合膨松剂中的碳酸氢钠和碳酸钙物质的量之比为 。
16.(13分) 某无色溶液中可能含有 Na+、H+、Cu2+、SO 2—、CO 2—、HCO —、
4 3 3
Cl—、NO —中的若干种离子,且各种离子的数目相等。取该溶液若干份,进行
3
如下实验:
回答下列问题:
(1) 无需进行实验,即可确定原溶液中一定不存在 (填离子符号,
下同)。
(2) 通过实验 i 可确定原溶液中一定不存在 。
(3) 实验ii、iii 是为了确定溶液中一定存在 。
(4) 白色沉淀 2 是 。甲同学认为不能依据“生成白色沉淀 2”得
出“相关离子存在”的结论,原因是 。
(5) 原溶液中一定存在的离子有 。
(6) 另取适量原溶液,向该溶液中滴加 Ba(OH) 溶液至恰好完全沉淀,该
2
反应的离子方程式为 ;向反应后的上层清液中滴加
CuSO 溶液,能观察到的现象是 。
4
17.(15分) 按要求填空
(1) 标准状况下,44.8 L CH 和SiH 的混合气体中所含氢原子数为
4 4
(设N 为阿伏加德罗常数的值)。
A
(2) 标准状况下有①6.72 L C H ;②25.6 g SO ;③0.2 mol H S;④3.01×1023
2 4 2 2
个Cl 四种气体,气体所占体积由小到大的顺序是(填序号,下同) ;
2
所含原子数由小到大的顺序是 。
高一 (化学)试题 第5页(共6页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
1
(3) 有V L Al(NO ) 溶液,若取此溶液 V L加水稀释至3V L后溶液含有
3 3
3
m g Al3+,则原溶液中NO —的物质的量浓度为 mol·L—1。
3
(4) 60 g RO 2—中,核外电子总数比质子总数多 6.02×1023个,则 R的摩尔
4
质量为 。
(5) 市售浓硝酸(ρ = 1.4 g·cm—3)的质量分数约为 69.3%,则溶液的物质
的量浓度为 mol·L—1;向1 L浓硝酸中加入 V L水使其物质的量浓度
变为之前的一半,则 V 1(选填“>”、“=”或“<”)。
(6) 一定温度下,向体积比为 11:7 的容器 X 和 Y 中分别充入等质量的气
体A和CO ,此时 X 和Y内部的压强比为 7:4,则A可能是 。
2
18.(15 分) 钠和氯元素广泛地分布于陆地和海洋中,都具有重要的生理功能
和工业价值。回答下列问题:
(1) 写出金属钠与 Cl 反应的化学方程式 ,反应的现象
2
为 。
(2) 写出HClO在光照条件下反应的化学方程式 。
(3) 写出 Na O 与 H O 反应的化学方程式 。将 39 g 过
2 2 2
氧化钠投入500 mL 0.4 mol·L-1的MgSO 中,忽略溶液体积变化,反应后各溶
4
质的浓度为 。
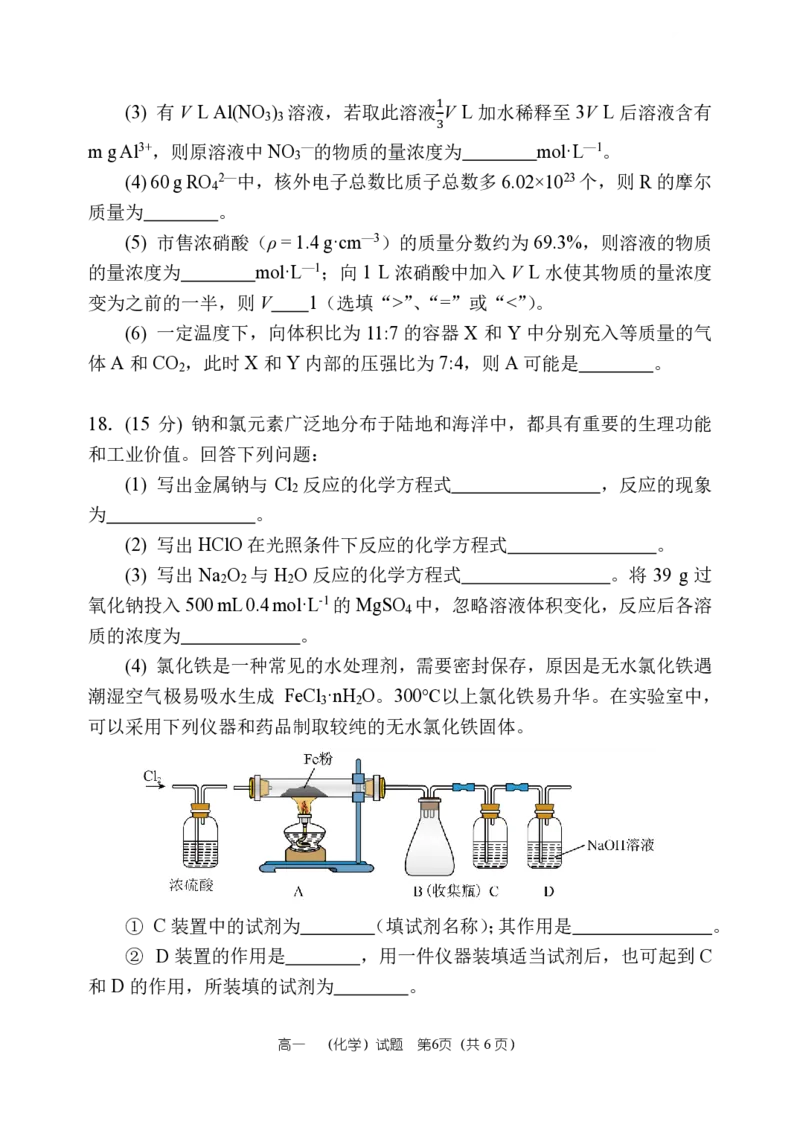
(4) 氯化铁是一种常见的水处理剂,需要密封保存,原因是无水氯化铁遇
潮湿空气极易吸水生成 FeCl ·nH O。300℃以上氯化铁易升华。在实验室中,
3 2
可以采用下列仪器和药品制取较纯的无水氯化铁固体。
① C 装置中的试剂为 (填试剂名称);其作用是 。
② D装置的作用是 ,用一件仪器装填适当试剂后,也可起到 C
和D的作用,所装填的试剂为 。
高一 (化学)试题 第6页(共6页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
2025~2026 学年上学期期中考试
28 届 高一(化学)参考答案
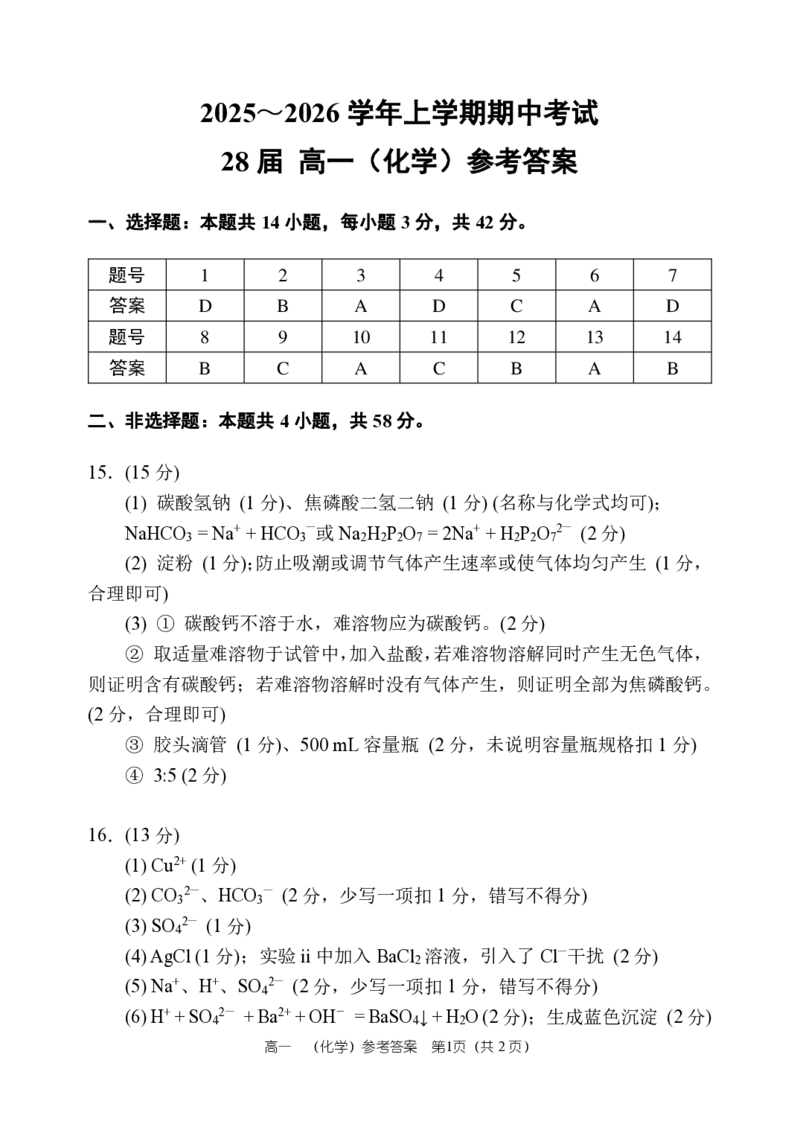
一、选择题:本题共 14 小题,每小题 3分,共 42分。
题号 1 2 3 4 5 6 7
答案 D B A D C A D
题号 8 9 10 11 12 13 14
答案 B C A C B A B
二、非选择题:本题共 4小题,共 58分。
15.(15分)
(1) 碳酸氢钠 (1 分)、焦磷酸二氢二钠 (1分) (名称与化学式均可);
NaHCO = Na+ + HCO —或Na H P O = 2Na+ + H P O 2— (2 分)
3 3 2 2 2 7 2 2 7
(2) 淀粉 (1分);防止吸潮或调节气体产生速率或使气体均匀产生 (1分,
合理即可)
(3) ① 碳酸钙不溶于水,难溶物应为碳酸钙。(2分)
② 取适量难溶物于试管中,加入盐酸,若难溶物溶解同时产生无色气体,
则证明含有碳酸钙;若难溶物溶解时没有气体产生,则证明全部为焦磷酸钙。
(2分,合理即可)
③ 胶头滴管 (1 分)、500 mL容量瓶 (2分,未说明容量瓶规格扣1分)
④ 3:5 (2分)
16.(13分)
(1) Cu2+ (1分)
(2) CO 2—、HCO — (2分,少写一项扣 1分,错写不得分)
3 3
(3) SO 2— (1分)
4
(4) AgCl (1分);实验ii 中加入BaCl 溶液,引入了 Cl—干扰 (2分)
2
(5) Na+、H+、SO 2— (2分,少写一项扣 1分,错写不得分)
4
(6) H+ + SO 2— + Ba2+ + OH- = BaSO ↓ + H O (2分);生成蓝色沉淀 (2分)
4 4 2
高一 (化学)参考答 案 第1页(共2页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
17.(15分)
(1) 8N 或4.816×1024 (2分)
A
(2) ③①②④ (2 分); ③④②① (2 分)
𝑚
(3) (2分)
3𝑉
(4) 56 g·mol—1 (2分)
(5) 15.4 mol·L—1 (2分);> (1分)
(6) CH 或其他摩尔质量相同的气体 (2分)
4
18.(15分)
点燃或Δ
(1) 2Na + Cl 2NaCl (1分);发出明亮黄光的同时产生白烟 (2分)
2
光照
(2) 2HClO 2HCl + O ↑ (2分)
2
(3) 2Na O + 2H O = 4NaOH + O ↑ (2 分);
2 2 2 2
0.2 mol·L—1 Na SO 与1.6 mol·L—1 NaOH (2分)
2 4
(4) ①浓硫酸 (1 分);防止D中的水蒸气进入 B (2分)
② 尾气处理,吸收多余的氯气 (2分);碱石灰 (1分,碱性干燥剂均可)
高一 (化学)参考答 案 第2页(共2页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
2025~2026 学年上学期期中考试
届 高一(化学)参考答案
28
一、选择题:本题共 14小题,每小题3分,共 42分。
题号 1 2 3 4 5 6 7
答案 D B A D C A D
题号 8 9 10 11 12 13 14
答案 B C A C B A B
二、非选择题:本题共 4小题,共 58分。
15.(15分)
(1) 碳酸氢钠 (1分)、焦磷酸二氢二钠 (1分)(名称与化学式均可);
NaHCO = Na+ +HCO —或Na H P O = 2Na+ +H P O 2— (2分)
3 3 2 2 2 7 2 2 7
(2) 淀粉 (1分);防止吸潮或调节气体产生速率或使气体均匀产生 (1分,
合理即可)
(3) ① 碳酸钙不溶于水,难溶物应为碳酸钙。(2分)
② 取适量难溶物于试管中,加入盐酸,若难溶物溶解同时产生无色气体,
则证明含有碳酸钙;若难溶物溶解时没有气体产生,则证明全部为焦磷酸钙。
(2分,合理即可)
③ 胶头滴管 (1分)、500mL容量瓶 (2分,未说明容量瓶规格扣1分)
④ 3:5(2分)
16.(13分)
(1) Cu2+(1分)
(2) CO 2—、HCO — (2分,少写一项扣1分,错写不得分)
3 3
(3) SO 2— (1分)
4
(4)AgCl (1分);实验ii中加入BaCl 溶液,引入了Cl—干扰 (2分)
2
(5) Na+、H+、SO 2— (2分,少写一项扣1分,错写不得分)
4
(6) H++ SO 2— + Ba2++ OH- = BaSO ↓+H O(2分);生成蓝色沉淀 (2分)
4 4 2
高一 (化学)参考答案 第1页(共2页)源泉教育秋季同步培优 咨询电话:15238939775(微信同号)
17.(15分)
(1) 8N 或 4.816×1024(2分)
A
(2) ③①②④ (2分); ③④②① (2分)
(3) (2 分)
(4) 536 g·mol—1 (2分)
(5) 15.4mol·L—1 (2分);> (1分)
(6) CH 或其他摩尔质量相同的气体 (2分)
4
18.(15分)
点燃或Δ
(1) 2Na+ Cl 2NaCl (1分);发出明亮黄光的同时产生白烟 (2分)
2
光照
(2) 2HClO 2HCl +O ↑(2分)
2
(3) 2Na O + 2H O= 4NaOH +O ↑(2分);
2 2 2 2
0.4mol·L—1Na SO 与1.2mol·L—1NaOH (2 分)
2 4
(4) ①浓硫酸 (1分);防止D 中的水蒸气进入B (2分)
② 尾气处理,吸收多余的氯气 (2分);碱石灰 (1分,碱性干燥剂均可)
高一 (化学)参考答案 第2页(共2页)