文档内容
威远中学校 2027 届高一下期半期考试
化学试题
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:
32 Cl:35.5 Fe:56
说明:本试卷共分 I 卷和 II 卷,满分 100 分,时间 75 分钟。请将答案写在答题卡对应位置。
I 卷(共 48 分)
一、选择题(本大题共 16 小题,每小题有一个选项符合题意,每小题 3 分,共 48 分)
1. 化学与环境、材料、生产、生活密切相关。下列说法错误的是
A. 在葡萄酒酿制过程中,适量添加二氧化硫可起到杀菌与保质作用
B. 硫酸钡在医疗上可被用作消化系统 X 射线检查的内服药剂,俗称“钡餐”
C. 工业制硝酸的原理是人工固氮合成 NO,NO 再经过一系列反应得到硝酸
D. 北斗导航系统所用芯片的主要成分是 Si
【答案】C
【解析】
【详解】A.二氧化硫能使蛋白质变性,并且具有还原性,可作抗氧化剂,在葡萄酒酿制过程中,添加适量
的二氧化硫可以起到杀菌抗氧化的作用,故 A 正确;
B.硫酸钡不会与胃酸反应,可用硫酸钡做“钡餐”,故 B 正确;
C.工业制硝酸的原理是人工固氮生成氨气,氨气氧化为 NO,NO 再经过一系列反应得到硝酸,故 C 错误;
D.Si 是良好的半导体材料,常用来制造芯片,北斗导航系统所用芯片的主要成分是 Si,故 D 正确;
答案选 C。
2. 下列有关化学用语使用正确的是
A. H O 的结构式为 H-O-O-H
2 2
B. 的电子式为
C. 氯的原子结构示意图为
第 1页/共 18页D. 电子式表示 形成过程:
【答案】A
【解析】
【详解】A.HO 分子中含有氢氧键、氧氧键,结构式为 H-O-O-H,A 正确;
2 2
B.氯离子是阴离子,应表示出其最外层电子,扩上中括号,标上所带负电荷,则氯化铵的电子式为
,B 错误;
C.氯为 17 号元素,原子结构示意图为 ,C 错误;
D. 镁 原 子 失 去 电 子 、 氯 原 子 得 到 电 子 形 成 离 子 化 合 物 氯 化 镁 , 表
示 为
,D 错误;
故选 A。
3. N 表示阿伏加德罗常数,下列说法错误的是
A
A. 常温常压下,46gNO 和 NO 的混合气体含有的原子数为 3N
2 2 4 A
B. 标准状况下,11.2LCl 与足量 NaOH 溶液反应转移的电子数为 0.5N
2 A
C. 40mL6mol·L-1 盐酸与足量 MnO 共热,转移的电子数为 0.12N
2 A
D. 0.5mol/LNa
2
SO
4
溶液中含有的 Na+ 浓度为 1mol/L
【答案】C
【解析】
【详解】A.NO 和 NO 的最简式为 NO ,46g NO 物质的量为 1mol,含原子数为 3N ,A 说法正确;
2 2 4 2 2 A
B.Cl 与 NaOH 溶液反应生成氯化钠、次氯酸钠和水,标准状况下,11.2LCl 物质的量为 0.5mol,反应中
2 2
转移电子数为 0.5N ,B 说法正确;
A
C.随着反应不断进行,浓盐酸变为稀盐酸反应停止,转移电子数不是 0.12N ,C 说法错误;
A
D.Na
2
SO
4
溶液浓度为 0.5mol/L,含 Na+ 浓度为 1mol/L,D 说法正确;
答案选 C。
4. 下列离子方程式书写不正确的是
A. 向 BaCl
2
溶液中通入 SO
2
气体:Ba2++SO
2
+H
2
O=BaSO
3
↓+2H+
第 2页/共 18页B. Cu 和浓 HNO
3
反应生成 NO
2
气体:Cu+4H++2 =Cu2++2NO
2
↑+2H
2
O
C. Ba(OH) 溶液中通入过量 CO:OH-+CO =
2 2 2
D. 少量碳酸氢钠溶液与足量澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
【答案】A
【解析】
详解】A.氯化钡溶液中通入二氧化硫气体,弱酸无法制强酸,两者不反应,A 错误;
B.Cu 与浓硝酸反应生成铜离子、NO 和水,离子方程式正确,B 正确;
2
C.氢氧化钡中通入过量 CO,实质为氢氧根离子与 CO 反应生成碳酸氢根离子,离子方程式正确,C 正确;
2 2
D.少量碳酸氢钠溶液与足量澄清石灰水混合,将碳酸氢根离子的系数确定为 1,一个碳酸氢根离子消耗 1
个 OH-和 1 个 Ca2+,反应生成碳酸钙沉淀和水,离子方程式正确,D 正确;
故答案选 A。
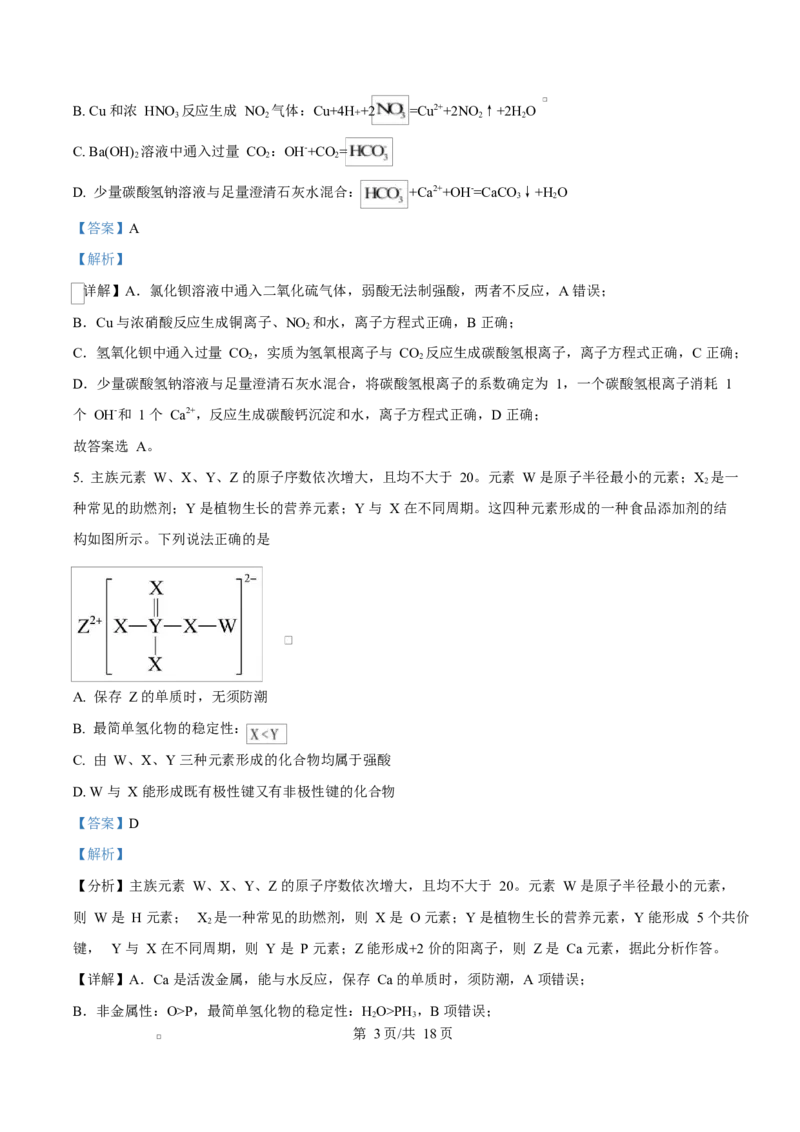
5. 主族元素 W、X、Y、Z 的原子序数依次增大,且均不大于 20。元素 W 是原子半径最小的元素;X 是一
2
种常见的助燃剂;Y 是植物生长的营养元素;Y 与 X 在不同周期。这四种元素形成的一种食品添加剂的结
构如图所示。下列说法正确的是
A. 保存 Z 的单质时,无须防潮
B. 最简单氢化物的稳定性:
C. 由 W、X、Y 三种元素形成的化合物均属于强酸
D. W 与 X 能形成既有极性键又有非极性键的化合物
【答案】D
【解析】
【分析】主族元素 W、X、Y、Z 的原子序数依次增大,且均不大于 20。元素 W 是原子半径最小的元素,
则 W 是 H 元素; X 是一种常见的助燃剂,则 X 是 O 元素;Y 是植物生长的营养元素,Y 能形成 5 个共价
2
键, Y 与 X 在不同周期,则 Y 是 P 元素;Z 能形成+2 价的阳离子,则 Z 是 Ca 元素,据此分析作答。
【详解】A.Ca 是活泼金属,能与水反应,保存 Ca 的单质时,须防潮,A 项错误;
B.非金属性:O>P,最简单氢化物的稳定性:HO>PH ,B 项错误;
2 3
第 3页/共 18页C.由 H、O、P 三种元素形成 化合物 HPO ,属于中强酸,C 项错误;
3 4
D.H 与 O 能形成既有极性键又有非极性键的化合物 HO,D 项正确;
2 2
答案选 D
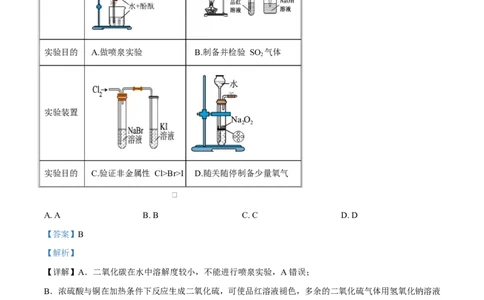
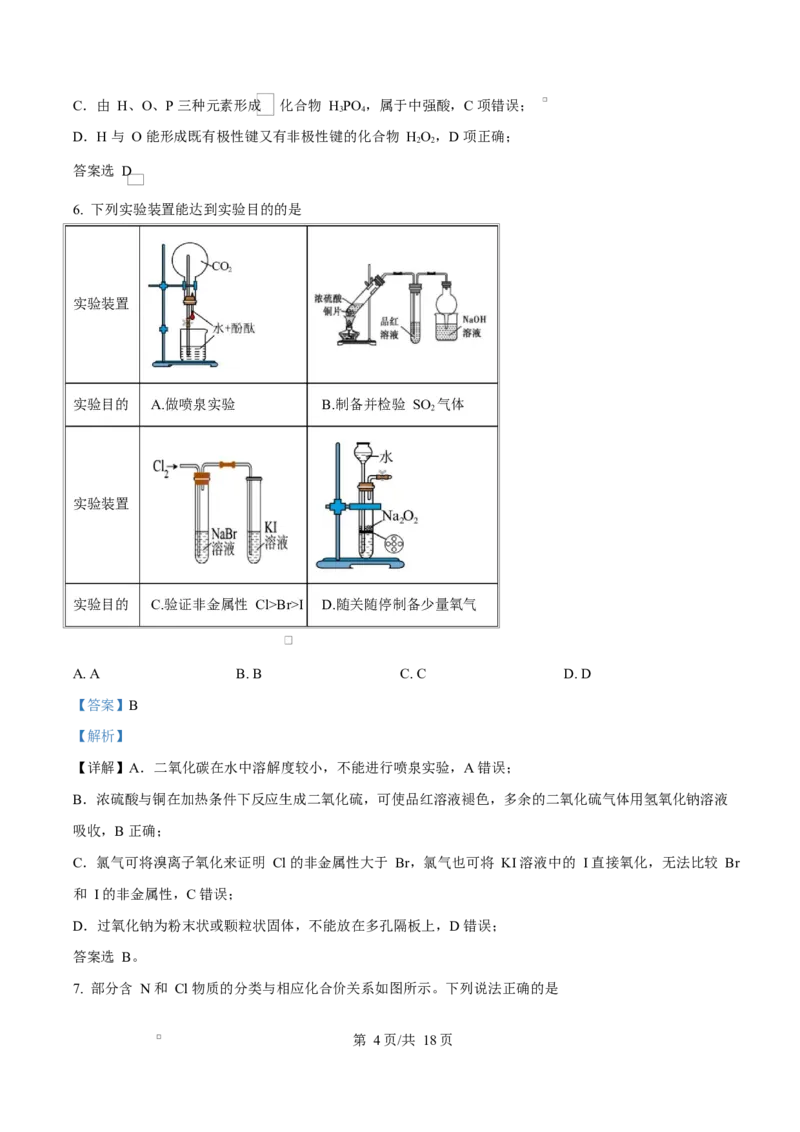
6. 下列实验装置能达到实验目的的是
实验装置
实验目的 A.做喷泉实验 B.制备并检验 SO 气体
2
实验装置
实验目的 C.验证非金属性 Cl>Br>I D.随关随停制备少量氧气
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.二氧化碳在水中溶解度较小,不能进行喷泉实验,A 错误;
B.浓硫酸与铜在加热条件下反应生成二氧化硫,可使品红溶液褪色,多余的二氧化硫气体用氢氧化钠溶液
吸收,B 正确;
C.氯气可将溴离子氧化来证明 Cl 的非金属性大于 Br,氯气也可将 KI 溶液中的 I 直接氧化,无法比较 Br
和 I 的非金属性,C 错误;
D.过氧化钠为粉末状或颗粒状固体,不能放在多孔隔板上,D 错误;
答案选 B。
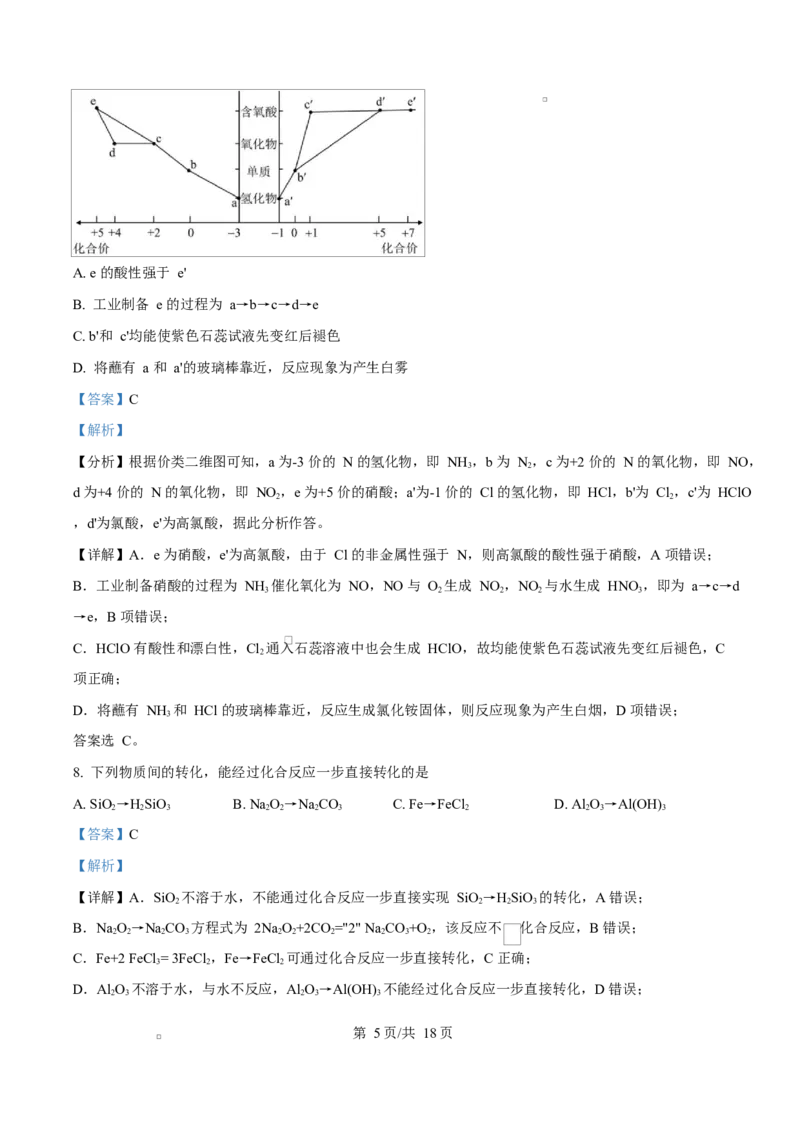
7. 部分含 N 和 Cl 物质的分类与相应化合价关系如图所示。下列说法正确的是
第 4页/共 18页A. e 的酸性强于 e'
B. 工业制备 e 的过程为 a→b→c→d→e
C. b'和 c'均能使紫色石蕊试液先变红后褪色
D. 将蘸有 a 和 a'的玻璃棒靠近,反应现象为产生白雾
【答案】C
【解析】
【分析】根据价类二维图可知,a 为-3 价的 N 的氢化物,即 NH ,b 为 N,c 为+2 价的 N 的氧化物,即 NO,
3 2
d 为+4 价的 N 的氧化物,即 NO ,e 为+5 价的硝酸;a'为-1 价的 Cl 的氢化物,即 HCl,b'为 Cl,c'为 HClO
2 2
,d'为氯酸,e'为高氯酸,据此分析作答。
【详解】A.e 为硝酸,e'为高氯酸,由于 Cl 的非金属性强于 N,则高氯酸的酸性强于硝酸,A 项错误;
B.工业制备硝酸的过程为 NH 催化氧化为 NO,NO 与 O 生成 NO ,NO 与水生成 HNO,即为 a→c→d
3 2 2 2 3
→e,B 项错误;
C.HClO 有酸性和漂白性,Cl 通入石蕊溶液中也会生成 HClO,故均能使紫色石蕊试液先变红后褪色,C
2
项正确;
D.将蘸有 NH 和 HCl 的玻璃棒靠近,反应生成氯化铵固体,则反应现象为产生白烟,D 项错误;
3
答案选 C。
8. 下列物质间的转化,能经过化合反应一步直接转化的是
A. SiO →HSiO B. Na O→NaCO C. Fe→FeCl D. Al O→Al(OH)
2 2 3 2 2 2 3 2 2 3 3
【答案】C
【解析】
【详解】A.SiO 不溶于水,不能通过化合反应一步直接实现 SiO→HSiO 的转化,A 错误;
2 2 2 3
B.NaO→NaCO 方程式为 2NaO+2CO ="2" Na CO+O ,该反应不 化合反应,B 错误;
2 2 2 3 2 2 2 2 3 2
C.Fe+2 FeCl = 3FeCl ,Fe→FeCl 可通过化合反应一步直接转化,C 正确;
3 2 2
D.Al O 不溶于水,与水不反应,Al O→Al(OH) 不能经过化合反应一步直接转化,D 错误;
2 3 2 3 3
第 5页/共 18页故答案 C。
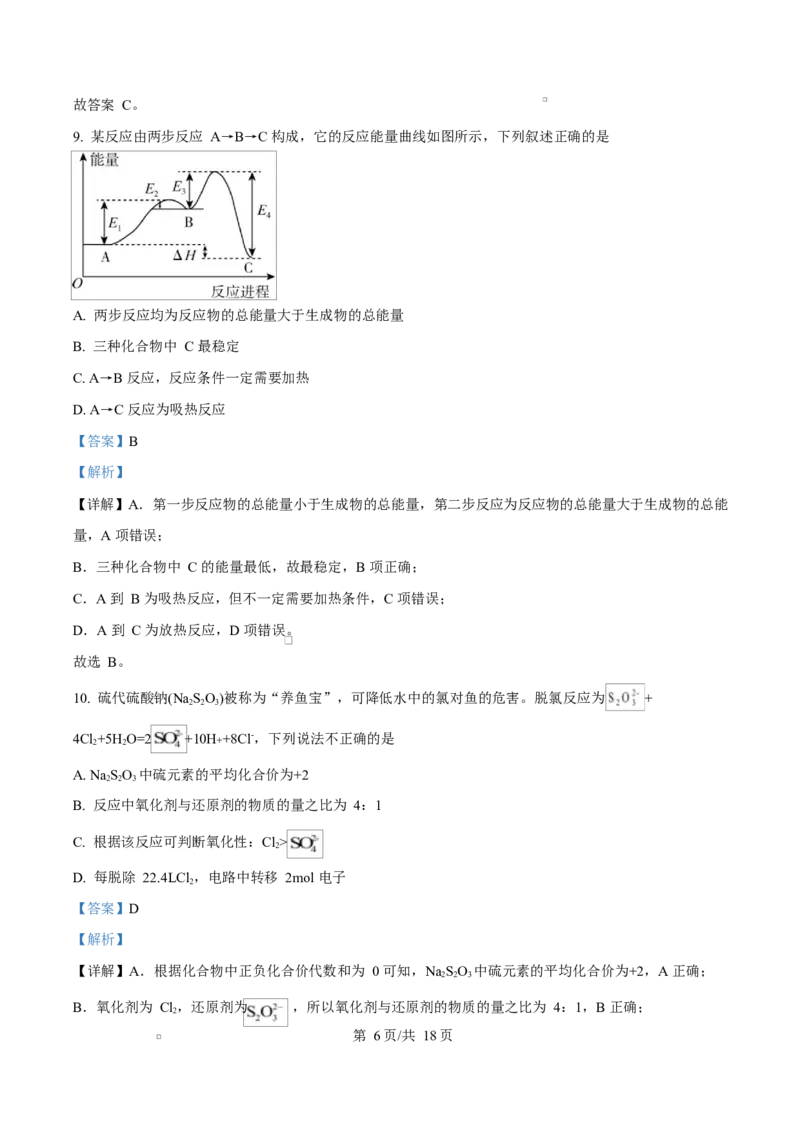
9. 某反应由两步反应 A→B→C 构成,它的反应能量曲线如图所示,下列叙述正确的是
A. 两步反应均为反应物的总能量大于生成物的总能量
B. 三种化合物中 C 最稳定
C. A→B 反应,反应条件一定需要加热
D. A→C 反应为吸热反应
【答案】B
【解析】
【详解】A.第一步反应物的总能量小于生成物的总能量,第二步反应为反应物的总能量大于生成物的总能
量,A 项错误;
B.三种化合物中 C 的能量最低,故最稳定,B 项正确;
C.A 到 B 为吸热反应,但不一定需要加热条件,C 项错误;
D.A 到 C 为放热反应,D 项错误。
故选 B。
10. 硫代硫酸钠(Na SO)被称为“养鱼宝”,可降低水中的氯对鱼的危害。脱氯反应为 +
2 2 3
4Cl
2
+5H
2
O=2 +10H++8Cl-,下列说法不正确的是
A. Na SO 中硫元素的平均化合价为+2
2 2 3
B. 反应中氧化剂与还原剂的物质的量之比为 4:1
C. 根据该反应可判断氧化性:Cl>
2
D. 每脱除 22.4LCl ,电路中转移 2mol 电子
2
【答案】D
【解析】
【详解】A.根据化合物中正负化合价代数和为 0 可知,NaSO 中硫元素的平均化合价为+2,A 正确;
2 2 3
B.氧化剂为 Cl,还原剂为 ,所以氧化剂与还原剂的物质的量之比为 4:1,B 正确;
2
第 6页/共 18页C.Cl 为氧化剂, 为氧化产物,根据氧化剂的氧化性强于氧化产物可知,氧化性:Cl> ,C 正
2 2
确;
D.没有指明在标准状况下,不能计算 22.4LCl 的物质的量,D 错误;
2
故选 D。
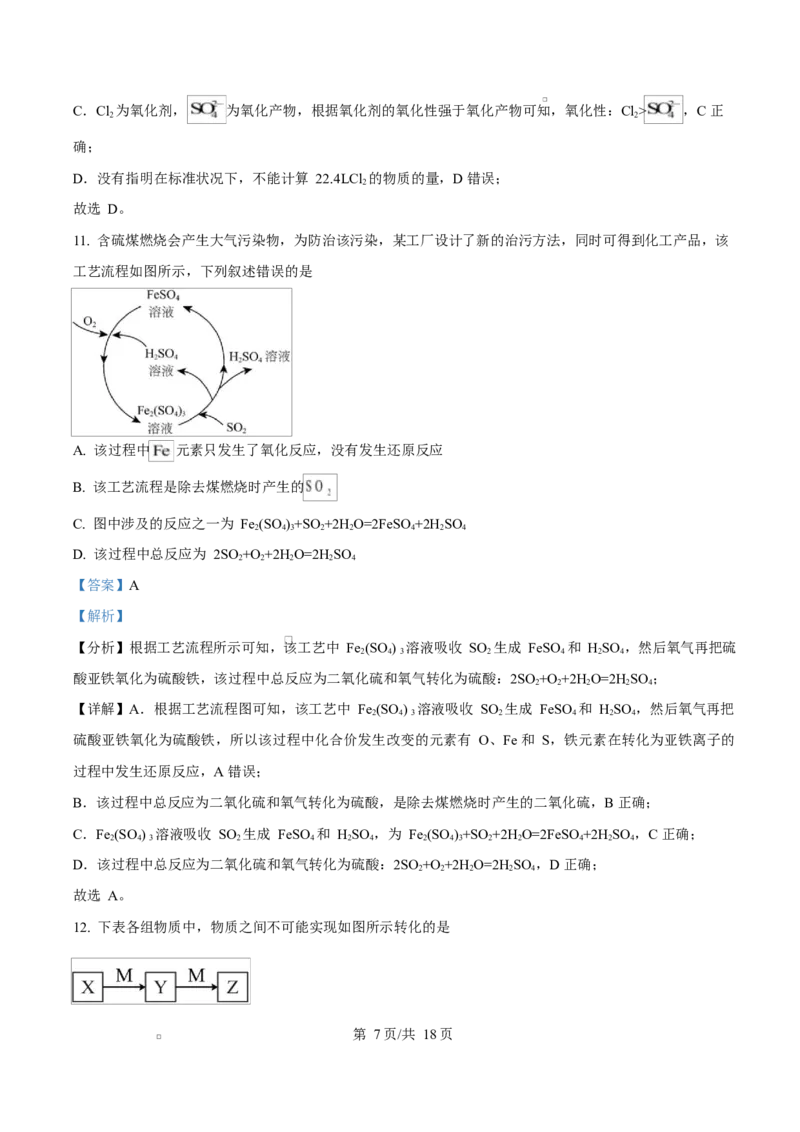
11. 含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该
工艺流程如图所示,下列叙述错误的是
A. 该过程中 元素只发生了氧化反应,没有发生还原反应
B. 该工艺流程是除去煤燃烧时产生的
C. 图中涉及的反应之一为 Fe (SO )+SO+2H O=2FeSO +2H SO
2 4 3 2 2 4 2 4
D. 该过程中总反应为 2SO +O +2H O=2HSO
2 2 2 2 4
【答案】A
【解析】
【分析】根据工艺流程所示可知,该工艺中 Fe (SO ) 溶液吸收 SO 生成 FeSO 和 HSO ,然后氧气再把硫
2 4 3 2 4 2 4
酸亚铁氧化为硫酸铁,该过程中总反应为二氧化硫和氧气转化为硫酸:2SO +O +2H O=2HSO ;
2 2 2 2 4
【详解】A.根据工艺流程图可知,该工艺中 Fe (SO ) 溶液吸收 SO 生成 FeSO 和 HSO ,然后氧气再把
2 4 3 2 4 2 4
硫酸亚铁氧化为硫酸铁,所以该过程中化合价发生改变的元素有 O、Fe 和 S,铁元素在转化为亚铁离子的
过程中发生还原反应,A 错误;
B.该过程中总反应为二氧化硫和氧气转化为硫酸,是除去煤燃烧时产生的二氧化硫,B 正确;
C.Fe (SO ) 溶液吸收 SO 生成 FeSO 和 HSO ,为 Fe (SO )+SO+2H O=2FeSO +2H SO ,C 正确;
2 4 3 2 4 2 4 2 4 3 2 2 4 2 4
D.该过程中总反应为二氧化硫和氧气转化为硫酸:2SO +O +2H O=2HSO ,D 正确;
2 2 2 2 4
故选 A。
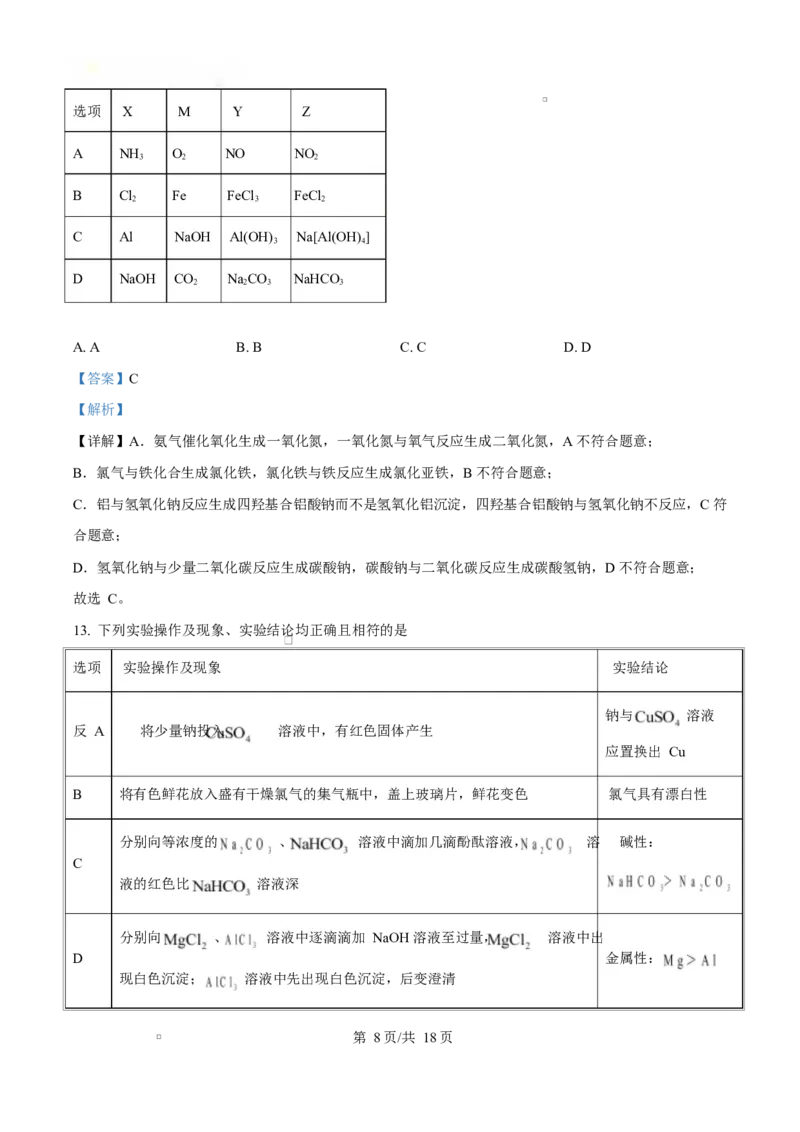
12. 下表各组物质中,物质之间不可能实现如图所示转化的是
第 7页/共 18页选项 X M Y Z
A NH O NO NO
3 2 2
B Cl Fe FeCl FeCl
2 3 2
C Al NaOH Al(OH) Na[Al(OH)]
3 4
D NaOH CO NaCO NaHCO
2 2 3 3
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.氨气催化氧化生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,A 不符合题意;
B.氯气与铁化合生成氯化铁,氯化铁与铁反应生成氯化亚铁,B 不符合题意;
C.铝与氢氧化钠反应生成四羟基合铝酸钠而不是氢氧化铝沉淀,四羟基合铝酸钠与氢氧化钠不反应,C 符
合题意;
D.氢氧化钠与少量二氧化碳反应生成碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,D 不符合题意;
故选 C。
13. 下列实验操作及现象、实验结论均正确且相符的是
选项 实验操作及现象 实验结论
钠与 溶液
反 A 将少量钠投入 溶液中,有红色固体产生
应置换出 Cu
B 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片,鲜花变色 氯气具有漂白性
分别向等浓度的 、 溶液中滴加几滴酚酞溶液, 溶 碱性:
C
液的红色比 溶液深
分别向 、 溶液中逐滴滴加 NaOH 溶液至过量, 溶液中出
D 金属性:
现白色沉淀; 溶液中先出现白色沉淀,后变澄清
第 8页/共 18页A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.钠与 溶液反应时,钠先与水反应生成氢氧化钠,氢氧化钠再与 发生复分解反应
生成氢氧化铜,故 A 错误;
B.氯气没有漂白性,将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片,鲜花变色,是因为氯气与鲜
花中的水发生反应 ,生成的 HClO 具有强氧化性而具有漂白性,故 B 错误;
C.分别向等浓度的 、 溶液中滴加几滴酚酞溶液, 溶液的红色比 溶液
深,则碱性: ,故 C 错误;
D.分别向 、 溶液中逐滴滴加 NaOH 溶液至过量, 溶液中出现白色沉淀,氢氧化镁不
能与强碱反应,氢氧化镁为强碱; 溶液中先出现白色沉淀,后变澄清,说明氢氧化铝能与强碱反应,
说明氢氧化铝具有一定的酸性,即 Al 具有一定的非金属性,故金属性: ,故 D 正确;
故选 D。
14. 溶液 X 中含有下表离子中的某 5 种,且其浓度均为 (不考虑水的电离与离子水解)。向 X 溶
液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是
阳离子 阴离子
、
、
、
、 、
、
、
、
、
、
A. X 溶液中可能含 3 种阳离子、2 种阴离子 B. X 溶液中不可能含有 或
第 9页/共 18页C. 生成的无色气体是 D. 根据电荷守恒,原溶液中一定含
【答案】A
【解析】
【分析】根据共存,OH-不能与 Fe3+、Al3+、Fe2+、Ca2+、Mg2+、 大量共存; 不能与 OH-、Fe3
+ 、Al3+大量共存; 不能与 Fe3+、Al3+、Fe2+、Ca2+、Mg2+大量共存;向 X 溶液中加入足量的稀盐酸,
阴离子种类没有发生改变,说明 X 溶液中含有 Cl-,加入稀盐酸有无色气体产生,该气体不能是 CO,气体
2
如果是 CO,则 X 溶液中含有 或 ,X 溶液与足量的稀盐酸反应,导致阴离子种类减少,因此无
2
色气体为 NO,X 溶液中含有 , 在酸中具有强氧化性,转化成 NO,X 溶液中应含有还原性离子,
即 Fe2+,X 溶液中有 5 种离子,X 溶液中离子浓度均为 0.1mol/L,溶液呈电中性,另外两种为 Mg2+和 SO 。
【详解】A.根据上述分析,含有的离子是 、Fe2+、Cl-、Mg2+、SO ,三种阴离子和两种阳离子,故
A 说法错误;
B.根据上述分析,X 溶液中一定不含有 或 ,故 B 说法正确;
C.根据上述分析,无色气体为 NO,故 C 说法正确;
D.根据电荷守恒,原溶液中一定含 ,故 D 说法正确;
故选 A。
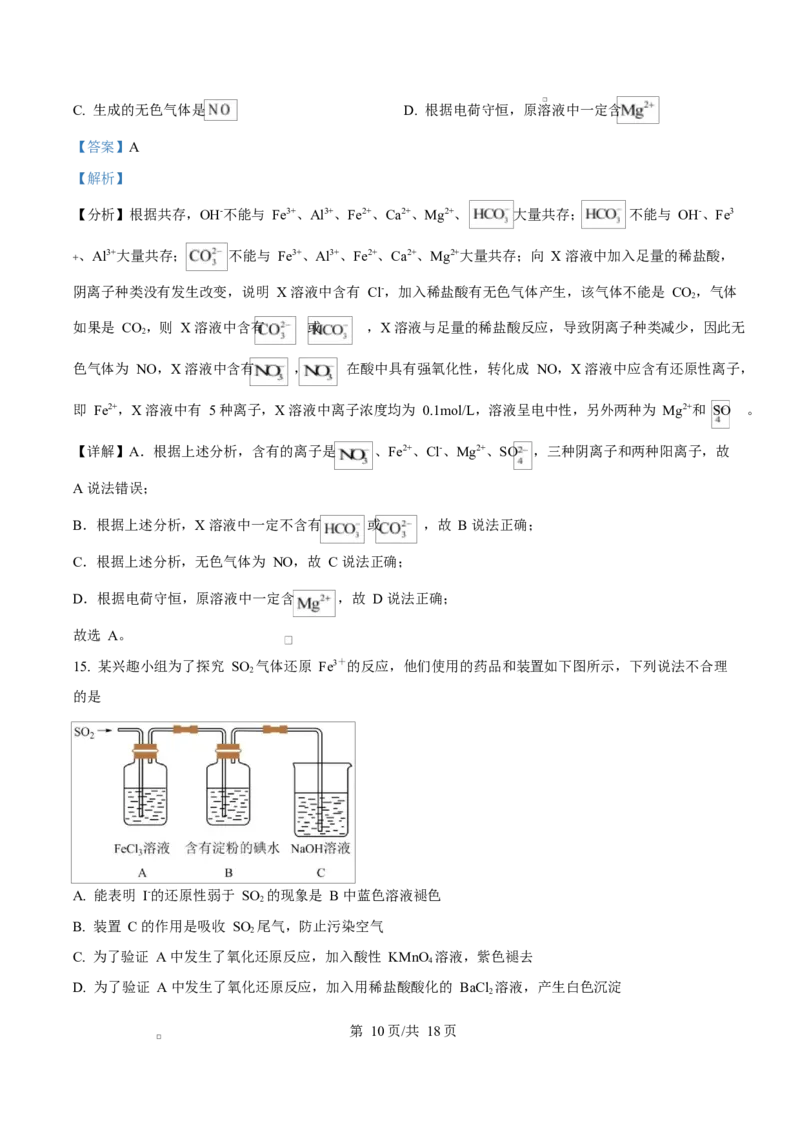
15. 某兴趣小组为了探究 SO 气体还原 Fe3+的反应,他们使用的药品和装置如下图所示,下列说法不合理
2
的是
A. 能表明 I-的还原性弱于 SO 的现象是 B 中蓝色溶液褪色
2
B. 装置 C 的作用是吸收 SO 尾气,防止污染空气
2
C. 为了验证 A 中发生了氧化还原反应,加入酸性 KMnO 溶液,紫色褪去
4
D. 为了验证 A 中发生了氧化还原反应,加入用稀盐酸酸化的 BaCl 溶液,产生白色沉淀
2
第 10页/共 18页【答案】C
【解析】
【分析】 先后通入 溶液、含淀粉的碘水中,根据溶液颜色的变化来探究 与 反应的
情况,多余的 最后通入 溶液进行吸收,防止染污空气。
【详解】A.向含有淀粉的碘水中通入 气体,会发生反应 , 被消耗,
B 中蓝色溶液褪色,证明物质的还原性强弱为 ,A 正确;
B. 是大气污染物,且是酸性气体,可以与 反应而被吸收,装置 C 可吸收 尾气,防止污染
空气,B 正确;
C.若 A 中 与 不发生反应,加入酸性 溶液时, 被 还原,溶液紫色褪去;若
A 中 与 发生反应,生成的 可使加入的 被还原,溶液紫色也褪去,因此不能验证 A
中是否发生了氧化还原反应,C 错误;
D.若 A 中发生了氧化还原反应 ,溶液中含有硫酸,当加入
用稀盐酸酸化的 溶液时,会发生反应 ,产生白色沉淀;若没有发
生氧化还原反应,由于 酸性强于 ,当向溶液中加入用稀盐酸酸化的 溶液时,不产生白色
沉淀,D 正确;
故选 C。
16. 硝酸是工业生产中不可或缺的化学品之一,通常用硝酸来制取硝酸铜溶液。为了分析制取硝酸铜溶液过
程中的原料用量和产生污染气体的情况,某中学化学兴趣小组用足量的铜与一定量的浓硝酸充分反应,得
到 6.72L(标准状况) 与 NO 的混合气体,这些气体与一定体积的 混合后通入水中,恰好被完全吸
收生成硝酸。该兴趣小组又向所得硝酸铜溶液中加 溶液, 恰好沉淀完全。下
列说法正确的是
A. 参加反应的 是 0.75mol B. 消耗氧气的体积为 3.36L
C. 此反应过程中转移了 0.3mol 的电子 D. 混合气体中含 0.15molNO
【答案】D
【解析】
第 11页/共 18页【分析】Cu 失去电子转化为得到电子转化为 6.72L (标准状况) 和 NO 的混合气体, 、NO、 与
水反应又转化为 HNO,最终 得到电子,整个过程中转移的电子的量是守恒的,铜原子失去 2 个电子转
3
化为 Cu2+,Cu2+再和 2 个 OH-结合生成 Cu(OH) ,可知转移的电子数目等于 OH-的数目,n(OH-)=0.1L×
2
6mol·L-1=0.6mol,则转移的电子的物质的量也是 0.6mol,n(Cu)=0.3mol。
【详解】A.在反应过程中 HNO 体现出了酸性和氧化性,体现酸性的硝酸,转化为了 Cu(NO ),根据 n(
3 3 2
)=2n(Cu)=0.2mol×3=0.6mol;体现氧化性的硝酸,转化为 NO 和 NO,设 n(NO )=xmol,n(NO)=ymol,
2 2
则根据转移电子守恒和物料守恒,有 x+y= ,x+3y=0.6,得 x=y=0.15mol,根据物料守恒,
则体现氧化性的 n(HNO)=n(NO)+n(NO )=0.15mol+0.15mol=0.3mol,参加反应的 HNO 是 0.6mol+
3 2 3
0.3mol=0.9mol,A 错误;
B.反应过程中转移了 0.6mol 电子,则需要 0.15molO,未指明标准状况下,无法计算体积,B 错误;
2
C.根据 A 项分析,反应过程中转移了 0.6mol 电子,C 错误;
D.根据 A 中的分析,混合气体中含 0.15molNO, D 正确;
答案选 D。
II 卷(共 52 分)
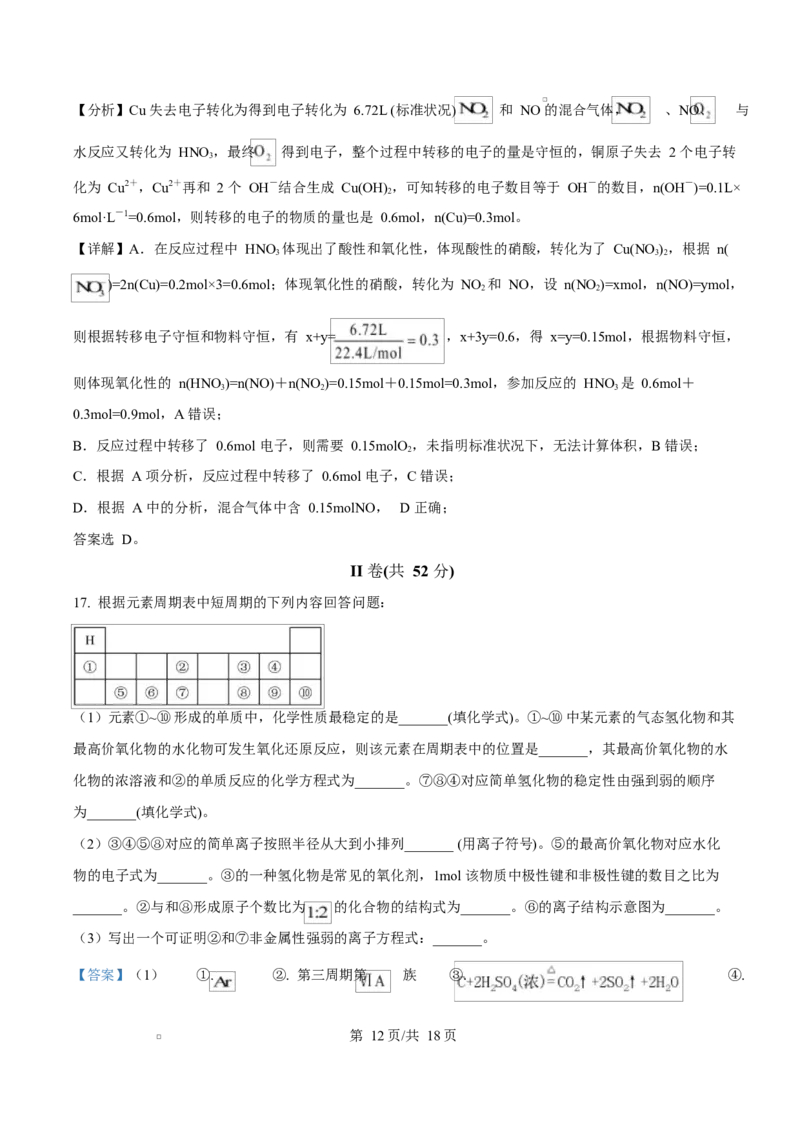
17. 根据元素周期表中短周期的下列内容回答问题:
(1)元素①~⑩形成的单质中,化学性质最稳定的是_______(填化学式)。①~⑩中某元素的气态氢化物和其
最高价氧化物的水化物可发生氧化还原反应,则该元素在周期表中的位置是_______,其最高价氧化物的水
化物的浓溶液和②的单质反应的化学方程式为_______。⑦⑧④对应简单氢化物的稳定性由强到弱的顺序
为_______(填化学式)。
(2)③④⑤⑧对应的简单离子按照半径从大到小排列_______ (用离子符号)。⑤的最高价氧化物对应水化
物的电子式为_______。③的一种氢化物是常见的氧化剂,1mol 该物质中极性键和非极性键的数目之比为
_______。②与和⑧形成原子个数比为 的化合物的结构式为_______。⑥的离子结构示意图为_______。
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:_______。
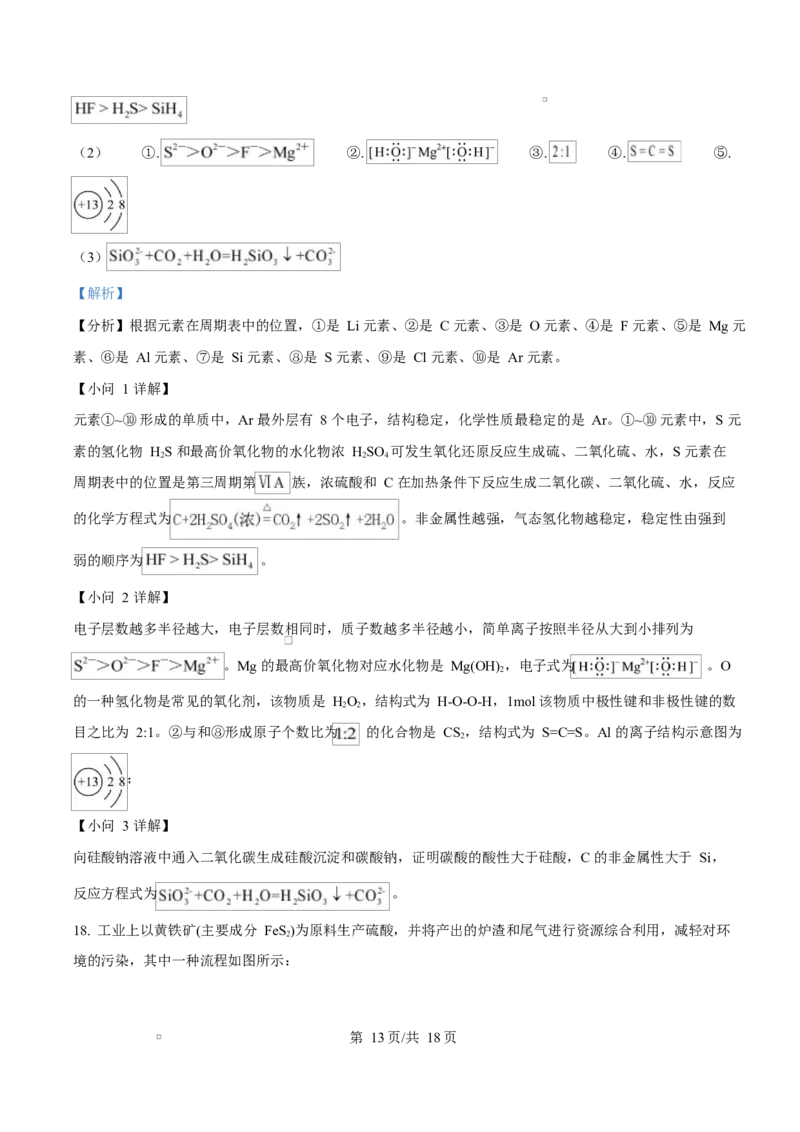
【答案】(1) ①. ②. 第三周期第 族 ③. ④.
第 12页/共 18页(2) ①. ②. ③. ④. ⑤.
(3)
【解析】
【分析】根据元素在周期表中的位置,①是 Li 元素、②是 C 元素、③是 O 元素、④是 F 元素、⑤是 Mg 元
素、⑥是 Al 元素、⑦是 Si 元素、⑧是 S 元素、⑨是 Cl 元素、⑩是 Ar 元素。
【小问 1 详解】
元素①~⑩形成的单质中,Ar 最外层有 8 个电子,结构稳定,化学性质最稳定的是 Ar。①~⑩元素中,S 元
素的氢化物 HS 和最高价氧化物的水化物浓 HSO 可发生氧化还原反应生成硫、二氧化硫、水,S 元素在
2 2 4
周期表中的位置是第三周期第 族,浓硫酸和 C 在加热条件下反应生成二氧化碳、二氧化硫、水,反应
的化学方程式为 。非金属性越强,气态氢化物越稳定,稳定性由强到
弱的顺序为 。
【小问 2 详解】
电子层数越多半径越大,电子层数相同时,质子数越多半径越小,简单离子按照半径从大到小排列为
。Mg 的最高价氧化物对应水化物是 Mg(OH) ,电子式为 。O
2
的一种氢化物是常见的氧化剂,该物质是 HO,结构式为 H-O-O-H,1mol 该物质中极性键和非极性键的数
2 2
目之比为 2:1。②与和⑧形成原子个数比为 的化合物是 CS,结构式为 S=C=S。Al 的离子结构示意图为
2
;
【小问 3 详解】
向硅酸钠溶液中通入二氧化碳生成硅酸沉淀和碳酸钠,证明碳酸的酸性大于硅酸,C 的非金属性大于 Si,
反应方程式为 。
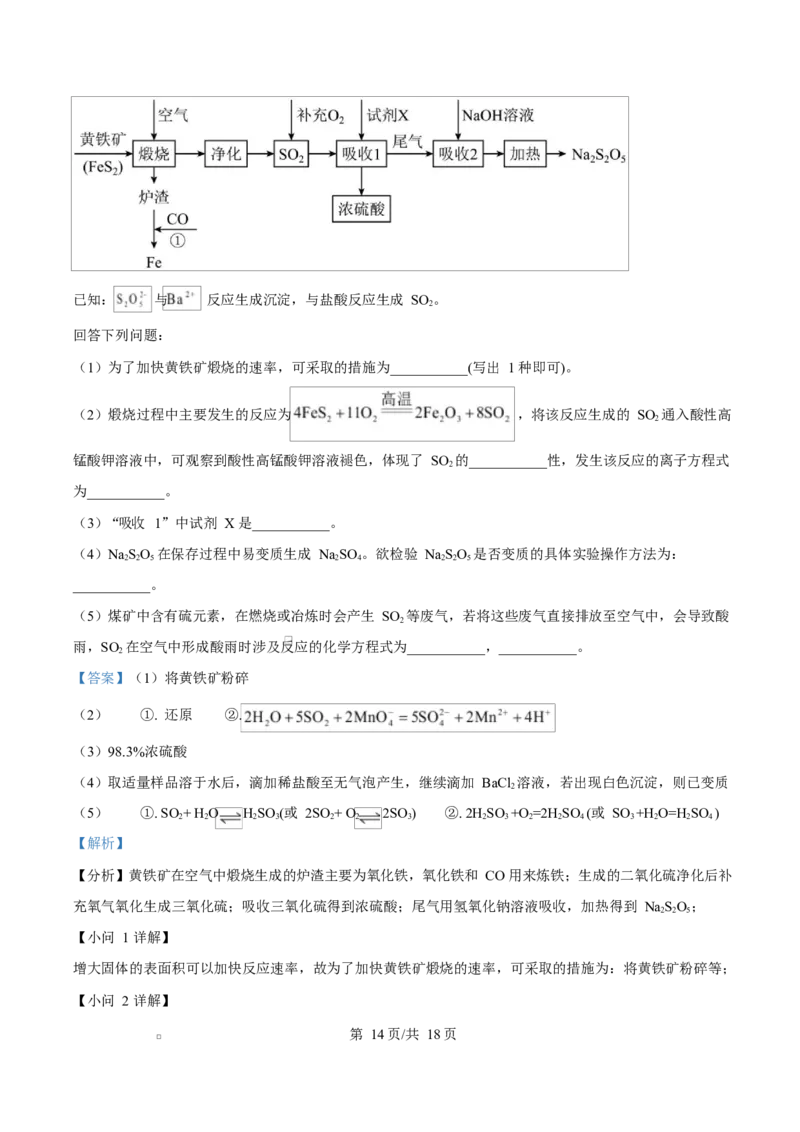
18. 工业上以黄铁矿(主要成分 FeS)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环
2
境的污染,其中一种流程如图所示:
第 13页/共 18页已知: 与 反应生成沉淀,与盐酸反应生成 SO 。
2
回答下列问题:
(1)为了加快黄铁矿煅烧的速率,可采取的措施为___________(写出 1 种即可)。
(2)煅烧过程中主要发生的反应为 ,将该反应生成的 SO 通入酸性高
2
锰酸钾溶液中,可观察到酸性高锰酸钾溶液褪色,体现了 SO 的___________性,发生该反应的离子方程式
2
为___________。
(3)“吸收 1”中试剂 X 是___________。
(4)NaSO 在保存过程中易变质生成 NaSO 。欲检验 NaSO 是否变质的具体实验操作方法为:
2 2 5 2 4 2 2 5
___________。
(5)煤矿中含有硫元素,在燃烧或冶炼时会产生 SO 等废气,若将这些废气直接排放至空气中,会导致酸
2
雨,SO 在空气中形成酸雨时涉及反应的化学方程式为___________,___________。
2
【答案】(1)将黄铁矿粉碎
(2) ①. 还原 ②.
(3)98.3%浓硫酸
(4)取适量样品溶于水后,滴加稀盐酸至无气泡产生,继续滴加 BaCl 溶液,若出现白色沉淀,则已变质
2
(5) ①. SO + H O HSO (或 2SO + O 2SO ) ②. 2HSO +O =2H SO (或 SO +H O=HSO )
2 2 2 3 2 2 3 2 3 2 2 4 3 2 2 4
【解析】
【分析】黄铁矿在空气中煅烧生成的炉渣主要为氧化铁,氧化铁和 CO 用来炼铁;生成的二氧化硫净化后补
充氧气氧化生成三氧化硫;吸收三氧化硫得到浓硫酸;尾气用氢氧化钠溶液吸收,加热得到 NaSO;
2 2 5
【小问 1 详解】
增大固体的表面积可以加快反应速率,故为了加快黄铁矿煅烧的速率,可采取的措施为:将黄铁矿粉碎等;
【小问 2 详解】
第 14页/共 18页将 SO 通入酸性高锰酸钾溶液中,酸性高锰酸钾溶液褪色,+7 价 Mn 得电子变为+2 价 Mn,SO 中+4 价 S
2 2
失电子变为+6 价 S,故 SO 体现还原性,结合电子守恒,反应为
2
;
【小问 3 详解】
三氧化硫和水反应放出热容易形成酸雾,影响三氧化硫的吸收,故吸收剂 X 为:98.3%浓硫酸;98.3%浓硫
酸可以防止酸雾的产生,提高吸收效率;
【小问 4 详解】
硫酸根离子会和钡离子生成不溶于酸的硫酸钡沉淀,故检验 NaSO 是否变质的具体实验操作方法为:取
2 2 5
适量样品溶于水后,滴加稀盐酸至无气泡产生,继续滴加 BaCl 溶液,若出现白色沉淀,则已变质;
2
【小问 5 详解】
SO 在空气中形成酸雨时涉及反应为二氧化硫和水生成亚硫酸:SO + H O HSO (或 2SO + O 2SO ),
2 2 2 2 3 2 2 3
亚硫酸容易被空气中氧气氧化为硫酸:2HSO +O =2H SO (或 SO +H O=HSO )。
2 3 2 2 4 3 2 2 4
19. 碳中和作为一种新型环保形式可推动全社会绿色发展。下图为科学家正在研究建立的一种二氧化碳新循
环体系。
(1)大气中存在温室气体 CO,写出 CO 的电子式___________。碳有多种单质,一定条件下,1mol 石墨
2 2
转化为金刚石吸收 1.85kJ 能量,则___________(填“石墨”或“金刚石”)更稳定。碳与硅同族,制备纯硅
的一种中间产物 SiHCl 遇水剧烈反应生成 HSiO、HCl 和 H,写出该反应的化学方程式:___________。
3 2 3 2
(2)过氧化氢一定条件下可发生分解:2HO(l)=2H O(l)+O(g),断裂 1 mol H O(l)中的 O-O 和 1 mol O (g)
2 2 2 2 2 2 2
中的 O=O 所需的能量依次为 142 kJ、497.3 kJ,断裂 HO(l)和 HO(l)中 1 mol H-O 键所需能量依次为 367 kJ
2 2 2
、467 kJ,则 2 mol H O(l)反应生成 2 mol H O(l)和 1 mol O (g)___________(填“吸收”或“放出”)的能量
2 2 2 2
为___________ kJ。
(3)某原电池装置如图所示。
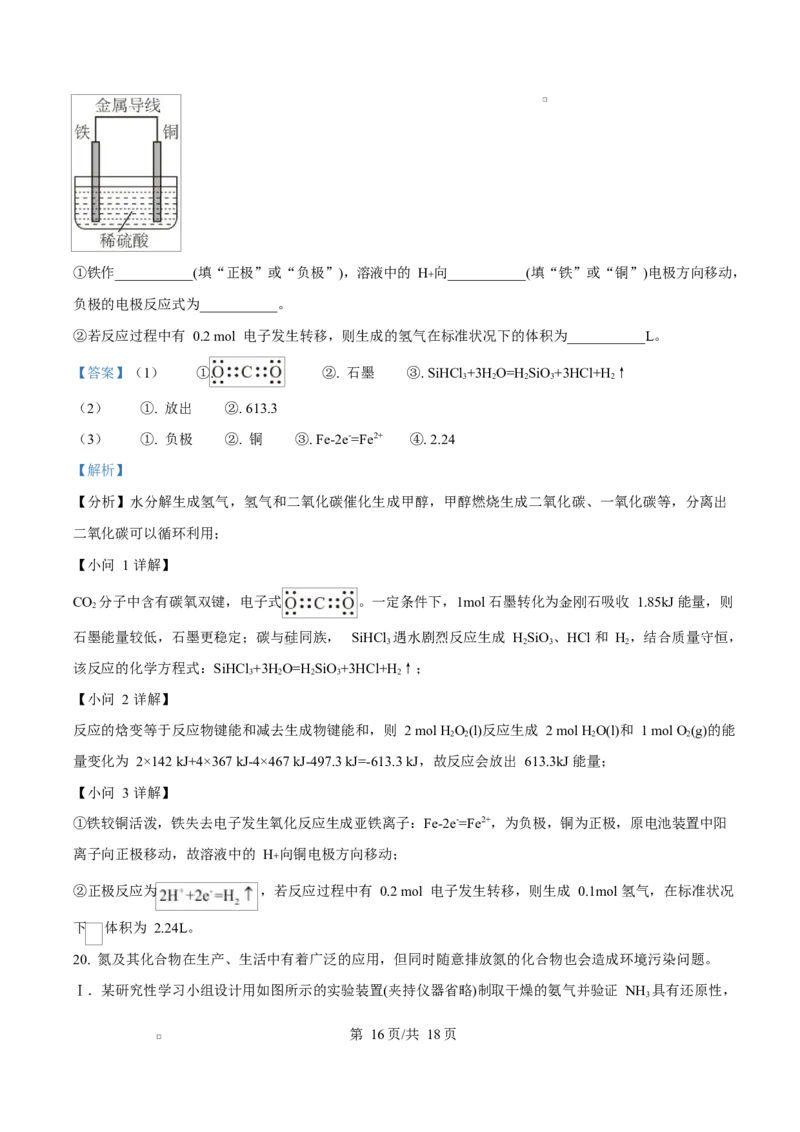
第 15页/共 18页①铁作___________(填“正极”或“负极”),溶液中的 H+ 向___________(填“铁”或“铜”)电极方向移动,
负极的电极反应式为___________。
②若反应过程中有 0.2 mol 电子发生转移,则生成的氢气在标准状况下的体积为___________L。
【答案】(1) ①. ②. 石墨 ③. SiHCl +3H O=HSiO+3HCl+H ↑
3 2 2 3 2
(2) ①. 放出 ②. 613.3
(3) ①. 负极 ②. 铜 ③. Fe-2e-=Fe2+ ④. 2.24
【解析】
【分析】水分解生成氢气,氢气和二氧化碳催化生成甲醇,甲醇燃烧生成二氧化碳、一氧化碳等,分离出
二氧化碳可以循环利用;
【小问 1 详解】
CO 分子中含有碳氧双键,电子式 。一定条件下,1mol 石墨转化为金刚石吸收 1.85kJ 能量,则
2
石墨能量较低,石墨更稳定;碳与硅同族, SiHCl 遇水剧烈反应生成 HSiO、HCl 和 H,结合质量守恒,
3 2 3 2
该反应的化学方程式:SiHCl +3H O=HSiO+3HCl+H ↑;
3 2 2 3 2
【小问 2 详解】
反应的焓变等于反应物键能和减去生成物键能和,则 2 mol H O(l)反应生成 2 mol H O(l)和 1 mol O (g)的能
2 2 2 2
量变化为 2×142 kJ+4×367 kJ-4×467 kJ-497.3 kJ=-613.3 kJ,故反应会放出 613.3kJ 能量;
【小问 3 详解】
①铁较铜活泼,铁失去电子发生氧化反应生成亚铁离子:Fe-2e-=Fe2+,为负极,铜为正极,原电池装置中阳
离子向正极移动,故溶液中的 H+ 向铜电极方向移动;
②正极反应为 ,若反应过程中有 0.2 mol 电子发生转移,则生成 0.1mol 氢气,在标准状况
下 体积为 2.24L。
20. 氮及其化合物在生产、生活中有着广泛的应用,但同时随意排放氮的化合物也会造成环境污染问题。
Ⅰ.某研究性学习小组设计用如图所示的实验装置(夹持仪器省略)制取干燥的氨气并验证 NH 具有还原性,
3
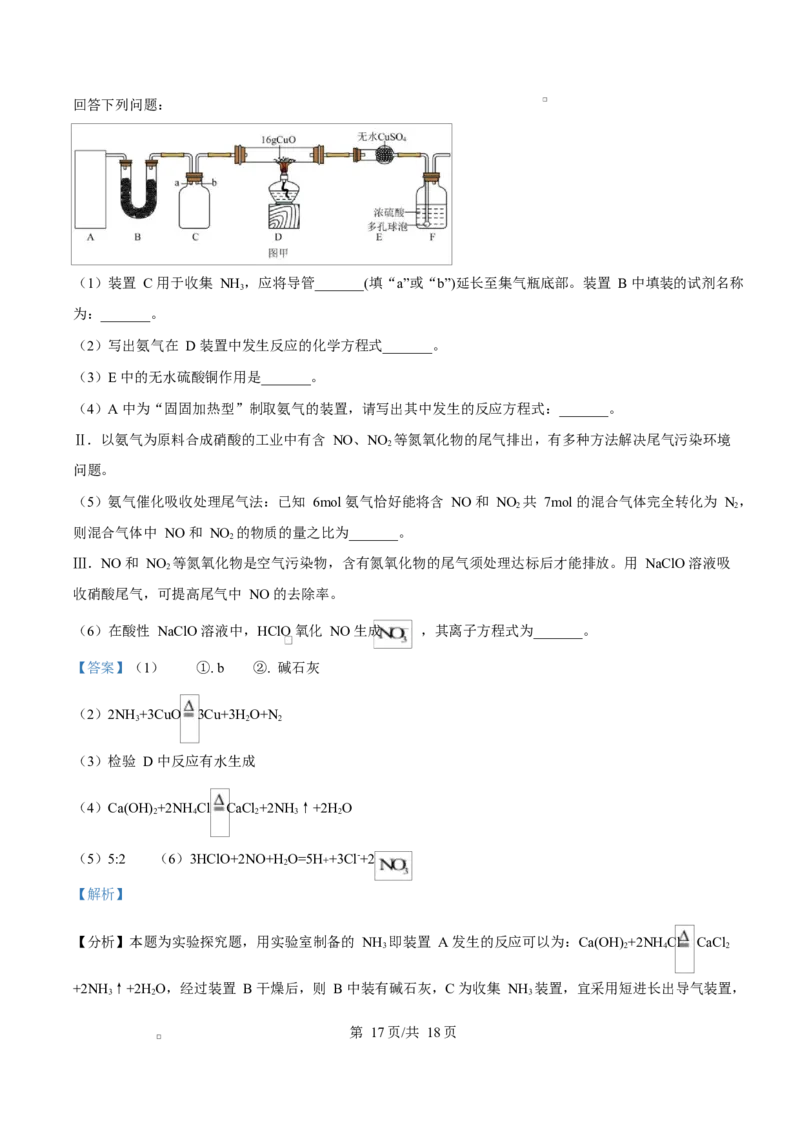
第 16页/共 18页回答下列问题:
(1)装置 C 用于收集 NH ,应将导管_______(填“a”或“b”)延长至集气瓶底部。装置 B 中填装的试剂名称
3
为:_______。
(2)写出氨气在 D 装置中发生反应的化学方程式_______。
(3)E 中的无水硫酸铜作用是_______。
(4)A 中为“固固加热型”制取氨气的装置,请写出其中发生的反应方程式:_______。
Ⅱ.以氨气为原料合成硝酸的工业中有含 NO、NO 等氮氧化物的尾气排出,有多种方法解决尾气污染环境
2
问题。
(5)氨气催化吸收处理尾气法:已知 6mol 氨气恰好能将含 NO 和 NO 共 7mol 的混合气体完全转化为 N,
2 2
则混合气体中 NO 和 NO 的物质的量之比为_______。
2
Ⅲ.NO 和 NO 等氮氧化物是空气污染物,含有氮氧化物的尾气须处理达标后才能排放。用 NaClO 溶液吸
2
收硝酸尾气,可提高尾气中 NO 的去除率。
(6)在酸性 NaClO 溶液中,HClO 氧化 NO 生成 ,其离子方程式为_______。
【答案】(1) ①. b ②. 碱石灰
(2)2NH +3CuO 3Cu+3H O+N
3 2 2
(3)检验 D 中反应有水生成
(4)Ca(OH) +2NHCl CaCl +2NH↑+2H O
2 4 2 3 2
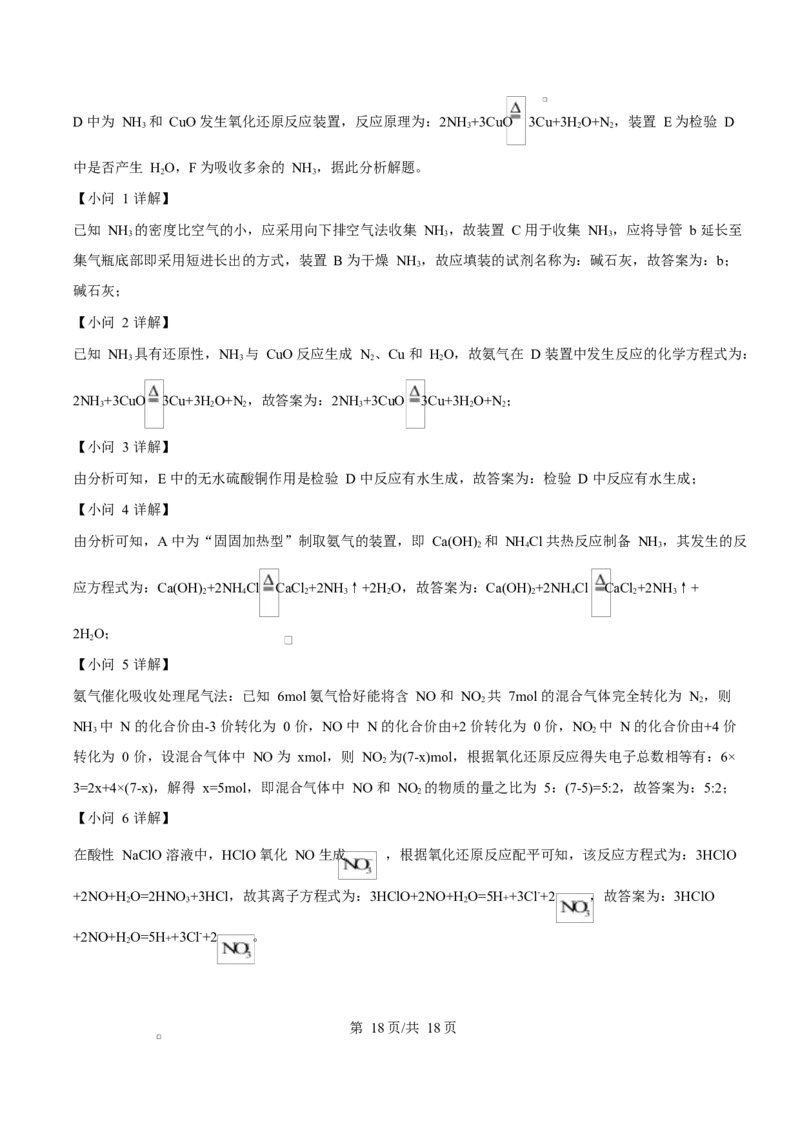
(5)5:2 (6)3HClO+2NO+H
2
O=5H++3Cl-+2
【解析】
【分析】本题为实验探究题,用实验室制备的 NH 即装置 A 发生的反应可以为:Ca(OH) +2NHCl CaCl
3 2 4 2
+2NH↑+2H O,经过装置 B 干燥后,则 B 中装有碱石灰,C 为收集 NH 装置,宜采用短进长出导气装置,
3 2 3
第 17页/共 18页D 中为 NH 和 CuO 发生氧化还原反应装置,反应原理为:2NH +3CuO 3Cu+3H O+N,装置 E 为检验 D
3 3 2 2
中是否产生 HO,F 为吸收多余的 NH ,据此分析解题。
2 3
【小问 1 详解】
已知 NH 的密度比空气的小,应采用向下排空气法收集 NH ,故装置 C 用于收集 NH ,应将导管 b 延长至
3 3 3
集气瓶底部即采用短进长出的方式,装置 B 为干燥 NH ,故应填装的试剂名称为:碱石灰,故答案为:b;
3
碱石灰;
【小问 2 详解】
已知 NH 具有还原性,NH 与 CuO 反应生成 N、Cu 和 HO,故氨气在 D 装置中发生反应的化学方程式为:
3 3 2 2
2NH +3CuO 3Cu+3H O+N,故答案为:2NH +3CuO 3Cu+3H O+N;
3 2 2 3 2 2
【小问 3 详解】
由分析可知,E 中的无水硫酸铜作用是检验 D 中反应有水生成,故答案为:检验 D 中反应有水生成;
【小问 4 详解】
由分析可知,A 中为“固固加热型”制取氨气的装置,即 Ca(OH) 和 NH Cl 共热反应制备 NH ,其发生的反
2 4 3
应方程式为:Ca(OH) +2NHCl CaCl +2NH↑+2H O,故答案为:Ca(OH) +2NHCl CaCl +2NH↑+
2 4 2 3 2 2 4 2 3
2HO;
2
【小问 5 详解】
氨气催化吸收处理尾气法:已知 6mol 氨气恰好能将含 NO 和 NO 共 7mol 的混合气体完全转化为 N,则
2 2
NH 中 N 的化合价由-3 价转化为 0 价,NO 中 N 的化合价由+2 价转化为 0 价,NO 中 N 的化合价由+4 价
3 2
转化为 0 价,设混合气体中 NO 为 xmol,则 NO 为(7-x)mol,根据氧化还原反应得失电子总数相等有:6×
2
3=2x+4×(7-x),解得 x=5mol,即混合气体中 NO 和 NO 的物质的量之比为 5:(7-5)=5:2,故答案为:5:2;
2
【小问 6 详解】
在酸性 NaClO 溶液中,HClO 氧化 NO 生成 ,根据氧化还原反应配平可知,该反应方程式为:3HClO
+2NO+H
2
O=2HNO
3
+3HCl,故其离子方程式为:3HClO+2NO+H
2
O=5H++3Cl-+2 ,故答案为:3HClO
+2NO+H
2
O=5H++3Cl-+2 。
第 18页/共 18页