文档内容
青浦一模试卷点评
单选题可能是十六个区里最简单的一个区了,一道较难题和难题也没有,不定项的最后一题
需要看清题目理解该实验的基础上再去答题,是属于选择的压轴难题。
大题的第一题题干信息量较大,但是高高拿起轻轻放下,虽然又是工厂示意图又是流程图,
但是大家别被吓到,本质就是考了一个基本概念的题,毕竟只是第一题。第二题和第一题类似,
图多字多内容多,但是难度只是适中,只是在有限时间内如何筛选出有效信息去完成题目是各位
同学需要去训练的了。第三道题最后一问和本次杨浦一模的最后一问非常像,都是文字表述题,
学会用精炼的语言给出准确答案对大家的要求不低。最后一问的读图及讨论原因是本次压轴,这
类题目属于科学实验探究相关,到了九下也会经常出现,在中考中也是属于难题。
化 学 部 分
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 K-39 Cu-64
五、选择题(本大题共17题,共20分)
21~34每题均只有1个正确选项
21.铝的元素符号是
A.Cl B.Lv C.Al D.Ag
【答案】C 考察常见元素的元素符号及名称
22.香蕉的含钾量较高,这里的“钾”是指
A.元素 B.原子 C.分子 D.单质
【答案】A 此处指的是宏观的钾元素
23.二氧化钛(TiO )是一种重要的白色颜料。TiO 中Ti的化合价为
2 2
A.-4 B.-2 C.+2 D.+4
【答案】D 氧元素为-2价 所以钛元素为+4价
24.不属于空气污染物的是
A.NO B.N C.SO D.PM
2 2 2 2.5
【答案】B B为空气中体积分数最多的气体 不是污染物25.下列物质的组成中含有原子团的是
A.MgCl B.P O C.CaO D.KNO
2 2 5 3
【答案】D D有硝酸根
26.物质名称和化学式一致的是
A.硫酸钾 K S B.氯化铁 FeCl C.氧化钠 Na O D.碳酸钠 NaCO
2 2 2 3
【答案】C A应该是 K SO B应该是 FeCl D应该是Na CO
2 4 3 2 3
27.在水中无法形成溶液的是
A.蔗糖 B.淀粉 C.硝酸钾 D.硫酸铜
【答案】B ACD都可溶于水 B形成浊液
28.一些饮品在常温时的pH范围如下,其中呈碱性的是
A.苹果汁 2.9~3.3 B.豆浆 7.4~7.9 C.牛奶 6.3~6.6 D.番茄汁 4.0~4.4
【答案】B 常温时pH>7的是碱性溶液
29.CO和CO 化学性质不同的原因是
2
A.密度不同 B.分子间隔不同 C.分子质量不同 D.分子种类不同
【答案】D 保持两者化学性质的最小微粒就是分子
30.水净化的过程中,能起到杀菌消毒作用的物质是
A.活性炭 B明矾 C.氧气 D.氯气
【答案】D AB用于吸附 C不用于水的净化
31.互为同素异形体的一组物质是
A.氮气和液氮 B.石墨和活性炭 C.红磷和白磷 D.水银和银
【答案】C 考察同素异形体的基本概念
32.物质的用途主要由其化学性质决定的是
A.镁用于制作照明弹 B.金刚石用于切割玻璃
C.干冰用于人工降雨 D.石墨用于制作电池的电极
【答案】A 镁的燃烧会发出耀眼白光 用于照明灯是该化学变化的现象
33.属于分解反应的是A.3Fe+2O Fe O B.CuO+H Cu+H O
2 3 4 2 2
C.CaCO CaO+CO ↑D.CaCO +2HCl CaCl +H O+CO ↑
3 2 3 2 2 2
【答案】C A是化合 B是置换 D是复分解
34.在某氢氧化钠溶液中加水,有关说法正确的
A.溶液颜色变浅 B.溶液变为酸性 C.溶剂的量增加 D.溶质的溶解度减小
【答案】C 溶液本身无色 碱性减弱但不会变酸性 温度不变则溶解度不变
35~37 每题均有 1~2 个正确选项
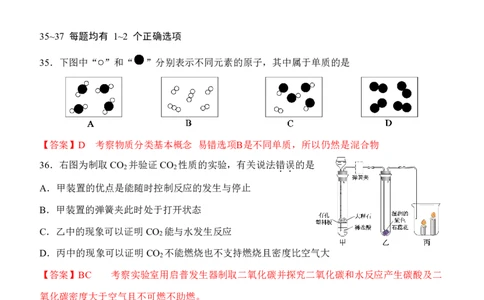
35.下图中“ ”和“ ”分别表示不同元素的原子,其中属于单质的是
【答案】D 考察物质分类基本概念 易错选项B是不同单质,所以仍然是混合物
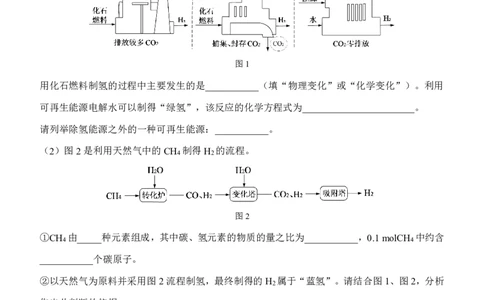
36.右图为制取CO
2
并验证CO
2
性质的实验,有关说法错
.
误
.
的是
A.甲装置的优点是能随时控制反应的发生与停止
B.甲装置的弹簧夹此时处于打开状态
C.乙中的现象可以证明CO 能与水发生反应
2
D.丙中的现象可以证明CO 不能燃烧也不支持燃烧且密度比空气大
2
【答案】BC 考察实验室用启普发生器制取二氧化碳并探究二氧化碳和水反应产生碳酸及二
氧化碳密度大于空气且不可燃不助燃。
37.利用右图装置测定空气中氧气的含量。有关说法错
.
误
.
的是
A.实验前需检查装置气密性
B.向烧杯中加水后,白磷才燃烧,说明白磷燃烧需要与氧气接触
C.白磷燃烧时,产生大量白烟
D.待锥形瓶内气体冷却至室温后,打开弹簧夹,量筒内液面由100mL
降至约80mL刻度线处【答案】BD 该反应通过加热水或者等待白磷缓慢氧化放出热量后达到着火点自燃 所以B是
温度原因 D 250ml的五分之一是50ml 所以水倒吸50ml 量筒内剩余50ml
六、简答题(共30分)
38.氢能源是最理想的绿色能源之一,有规划地开发和使用氢能源,是实现碳中和的重要措施。
(1)按照生产方式及生产过程中的碳排放情况,可将氢能源分为以下三类(见图1)。
图1
用化石燃料制氢的过程中主要发生的是___________(填“物理变化”或“化学变化”)。利用
可再生能源电解水可以制得“绿氢”,该反应的化学方程式为_______________________。
请列举除氢能源之外的一种可再生能源:___________。
(2)图2是利用天然气中的CH 制得H 的流程。
4 2
图2
①CH 由_____种元素组成,其中碳、氢元素的物质的量之比为___________,0.1molCH 中约含
4 4
___________个碳原子。
②以天然气为原料并采用图2流程制氢,最终制得的H 属于“蓝氢”。请结合图1、图2,分析
2
作出此判断的依据。_________________________________________
【答案】(1)化学变化 2H O 2H ↑+O ↑ 太阳能/风能/地热能(合理给分)
2 2 2
(2)2 1:4 6.02×1022
制氢原料是CH ,属于化石燃料;制氢过程中产生的CO 在吸附塔中被除去,碳排放量较低
4 2
39.氧气是一种常见的气体,制取氧气的方法有多种。
(1)图3为实验室制取气体的常用装置。
加热氯酸钾和二氧化锰的混合物制取氧气的化学方程式为___________________,二氧化锰的作用是_______________。若要制取一瓶干燥的氧气,可用A和______(填编号)进行组合。该实
验中选择A作为发生装置的理由是___________________________。消耗0.2mol的氯酸钾理论
上能生成_______g氧气。
图3 图4
(2)图4为家庭制取氧气的装置。
用该装置制氧气时,在反应仓中加入水和专用制氧剂,即可产生氧气。氧气能迅速从水中逸出,
是因为氧气具有_____________的物理性质。检验该装置中排出的气体为氧气的方法是________
_______________________________(写出具体操作及现象)。
【答案】(1)2KClO 2KCl+3O ↑ 催化作用/加快反应速率 B
3 2
反应物为固体,且需要加热 9.6
(2)难溶于水 将带火星的小木条放到b导管口,小木条复燃/或将燃着的小木条放到b导管
口,小木条燃烧得更旺(合理即可)
40.食盐在工农业生产中的用途非常广泛。我国在很早以前就有了关于制盐方法的记载。
(1)下表为NaCl在不同温度下的溶解度。
温度(℃) 0 10 20 40 60 80
溶解度(g/100g水) 35.7 35.8 36.0 36.6 37.3 38.4
①农业上常用溶质质量分数为16%的食盐水选种,16%的含义是____________。
②工业上常用电解饱和食盐水的方法制取氯气,反应原理为:
2NaCl+□H O 2NaOH+H ↑+Cl ↑,□内的数值为________。结合上表信息可知,20℃时,
2 2 2
饱和食盐水的溶质质量分数为__________。(2)起源于春秋战国时期的“五步产盐法”是一种古老的制盐方法,其生产流程如图5所示。
图5
①“过箩”(“箩”呈蜂窝状,有空隙)可除去卤水中的不溶性杂质,“过箩”与化学实验中_________
(填操作名称)的原理相似。“集卤蒸发”和“结晶”时都需要蒸发水,但作用不同,请分别指
出这两步中蒸发水的作用。__________________________________
②每年夏季是一年中产盐量最高的季节,请分析该季节产盐量高的原因。_____________
【答案】(1)每100 g食盐水中含食盐16 g 2 26.5%(合理给分)
(2)过滤
“集卤蒸发”时,主要是提高卤水的浓度;“结晶”时,主要是使食盐大量析出。夏天温度高,
水分蒸发快,有利于食盐的析出
41.某实验小组对氧化铜粉末与碳粉的反应展开探究。
(1)实验一:探究氧化铜粉末与碳粉反应的气体产物
【提出猜想】猜想1:CO ;猜想2:______;猜想3:CO 和CO
2 2
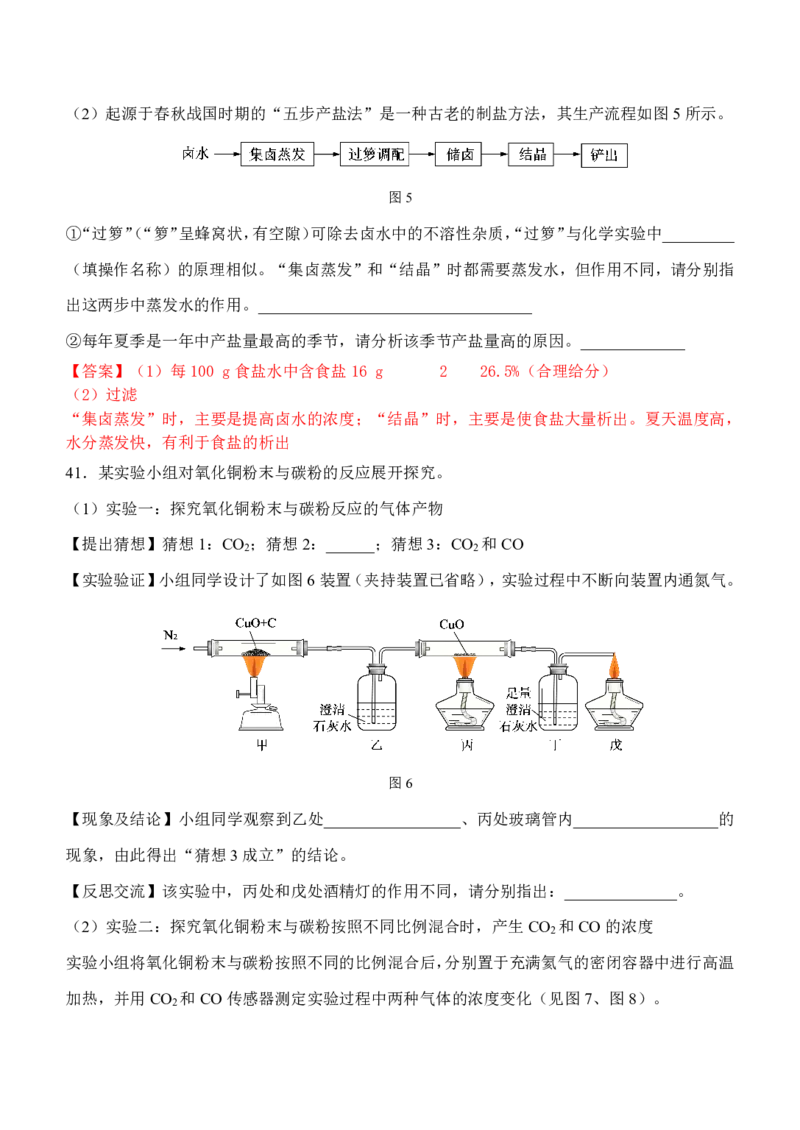
【实验验证】小组同学设计了如图6装置(夹持装置已省略),实验过程中不断向装置内通氮气。
图6
【现象及结论】小组同学观察到乙处_________________、丙处玻璃管内__________________的
现象,由此得出“猜想3成立”的结论。
【反思交流】该实验中,丙处和戊处酒精灯的作用不同,请分别指出:______________。
(2)实验二:探究氧化铜粉末与碳粉按照不同比例混合时,产生CO 和CO的浓度
2
实验小组将氧化铜粉末与碳粉按照不同的比例混合后,分别置于充满氦气的密闭容器中进行高温
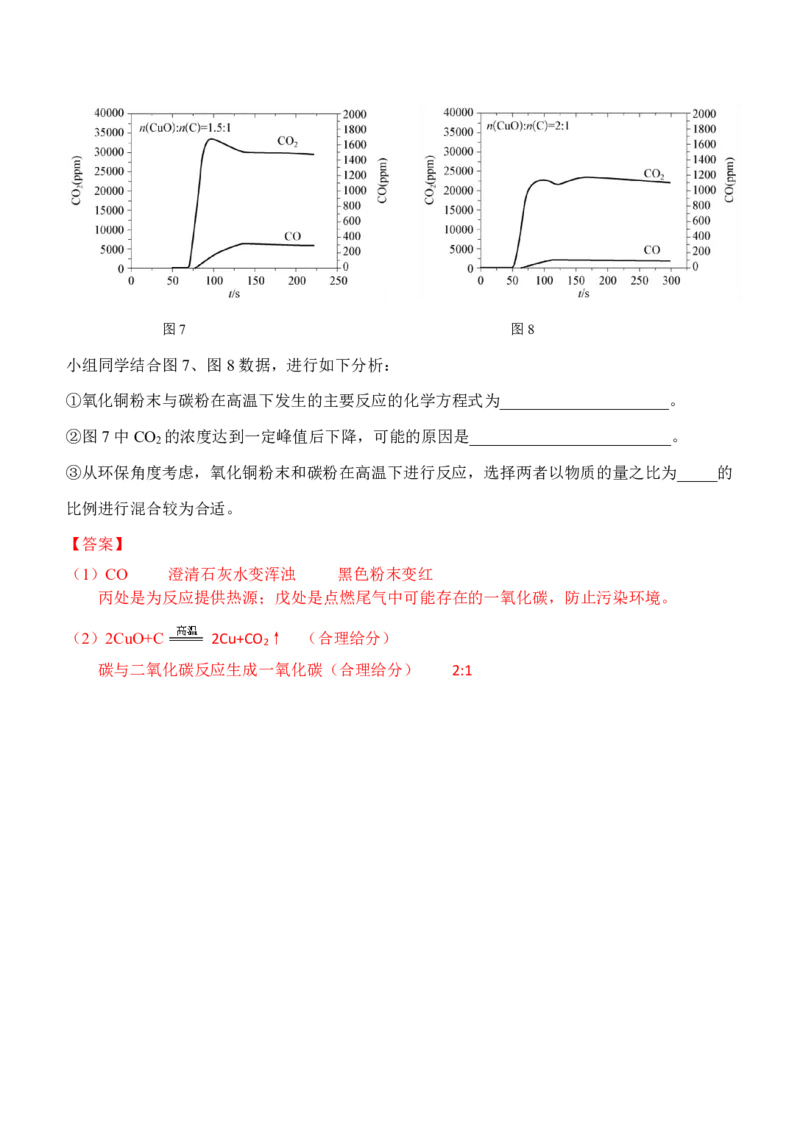
加热,并用CO 和CO传感器测定实验过程中两种气体的浓度变化(见图7、图8)。
2图7 图8
小组同学结合图7、图8数据,进行如下分析:
①氧化铜粉末与碳粉在高温下发生的主要反应的化学方程式为_____________________。
②图7中CO 的浓度达到一定峰值后下降,可能的原因是_________________________。
2
③从环保角度考虑,氧化铜粉末和碳粉在高温下进行反应,选择两者以物质的量之比为_____的
比例进行混合较为合适。
【答案】
(1)CO 澄清石灰水变浑浊 黑色粉末变红
丙处是为反应提供热源;戊处是点燃尾气中可能存在的一氧化碳,防止污染环境。
(2)2CuO+C 2Cu+CO ↑ (合理给分)
2
碳与二氧化碳反应生成一氧化碳(合理给分) 2:1