文档内容
浦东新区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2020.1
相对原子质量:H-1 C-12 O-16 Ca-40 Cu-64
六、选择题
1.地壳中含量最多的元素是( )
A. Si B. Al C. O D. Fe
2.属于物理变化的是( )
A. 蜡烛燃烧 B. 火药爆炸 C. 粮食酿酒 D. 海水晒盐
3.属于纯净物的是( )
A. 石灰水 B. 蒸馏水 C. 大理石 D. 稀盐酸
4.属于浊液的是( )
A. 糖水 B. 泥水 C. 盐水 D. 汽水
5.下列符号表示2个氢原子的是( )
A. 2H B. 2H C. H D. 2H O
2 2 2
6.硫在氧气中燃烧的现象是( )
A. 发出白光 B. 淡蓝色火焰 C. 产生白烟 D. 蓝紫色火焰
7.取用固体药品的正确操作是( )
A. B.
C. D.
8.铕(Eu)是有“工业维生素”美誉的稀土元素,EuO 中铕元素的化合价为( )
2 3
A. +1 B. +2 C. +3 D. +4
9.不属于碳元素的同素异形体的是( )
A. 金刚石 B. 石墨 C. 二氧化碳 D. C
6010.正确的化学用语是( )
A. 碳酸根:CO B. 汞原子:Ag
3
C. 氧化铁:FeO D. 胆矾:CuSO
4
11. 下列关于“酒精温度计遇热读数上升”的微观解释正确的是
A. 分子质量增大 B. 分子体积扩大 C. 分子间隔变大 D. 分子个数增多
12.水是生命之源,关于水的说法正确的是( )
A. 水是最常见的溶剂 B. 实验室废液不经处理直接排放
C. 水变成冰体积减小 D. 明矾在净水过程中起消毒作用
13.有关空气的说法错误的是( )
A. 氮气约占空气体积的 78% B. 空气质量指数反映空气质量状况
C. 空气中二氧化碳会造成酸雨 D. 分离液态空气可用于工业制氧气
14.有关燃烧和灭火的说法正确的是( )
A. 可燃物在空气中才能燃烧 B. 煤炭粉碎能使燃烧更充分
C. 降低可燃物着火点可灭火 D. 天然气燃烧符合“低碳”理念
15.过氧乙酸(C HO)是常用的消毒剂,有关过氧乙酸说法正确的是( )
2 4 3
A. 摩尔质量为 76g
B. 碳、氢、氧元素的质量比为 2:4:3
C. 一个分子中有 9 个原子
D. 0.1mol 过氧乙酸中约含6.02×1023个分子
16.已知:2KClO 2KCl+3O ,有关说法错误的是( )
3 2
A. 属于分解反应
B. 钾元素的存在形态不变
C. 从化学方程式可知氧气是无色的
D. MnO 和 KCl 的混合物可通过溶解、过滤分离
2
17.化学基本观念说法错误的是( )
A. 微粒观:金刚石由分子构成 B. 转化观:二氧化碳可转化为碳酸
C. 元素观:氧气由氧元素组成 D. 守恒观:化学反应前后元素种类不变
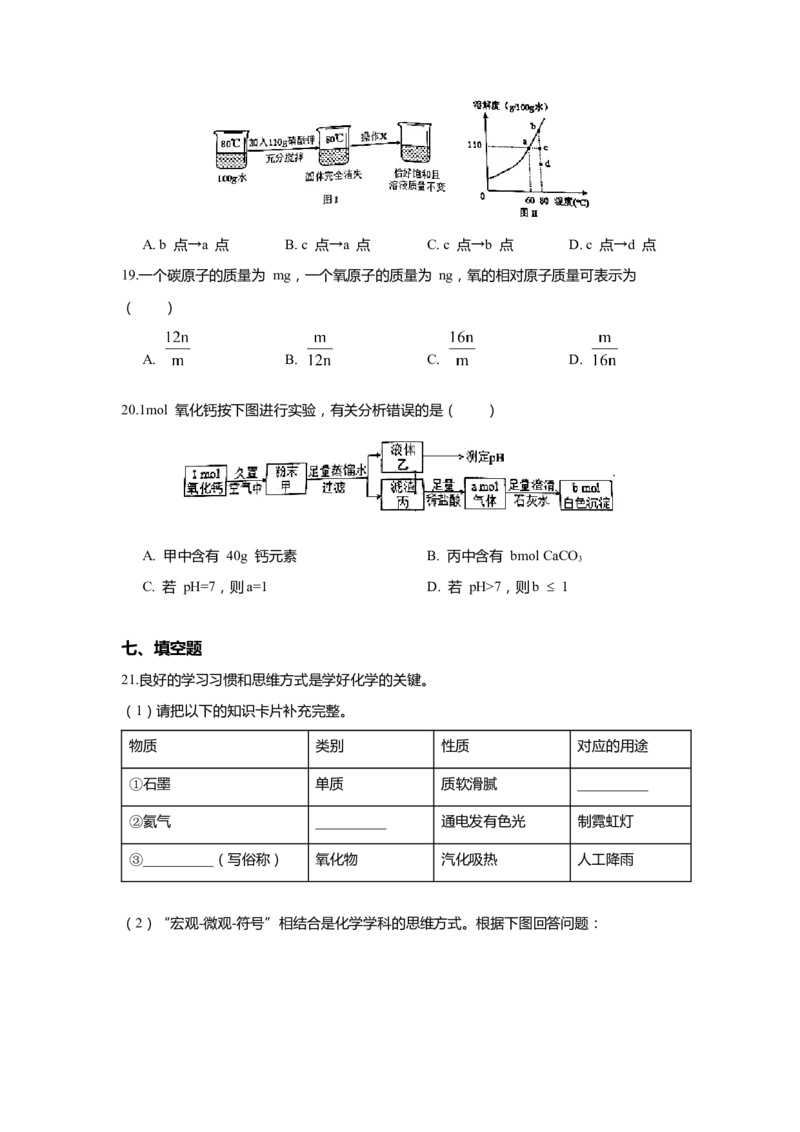
18.硝酸钾溶解度曲线如图Ⅱ所示,图Ⅰ中“操作 X”前后溶液状态变化过程可以在图Ⅱ中
表示为( )A. b 点→a 点 B. c 点→a 点 C. c 点→b 点 D. c 点→d 点
19.一个碳原子的质量为 mg,一个氧原子的质量为 ng,氧的相对原子质量可表示为
( )
A. B. C. D.
20.1mol 氧化钙按下图进行实验,有关分析错误的是( )
A. 甲中含有 40g 钙元素 B. 丙中含有 bmol CaCO
3
C. 若 pH=7,则a=1 D. 若 pH>7,则b 1
七、填空题
21.良好的学习习惯和思维方式是学好化学的关键。
(1)请把以下的知识卡片补充完整。
物质 类别 性质 对应的用途
①石墨 单质 质软滑腻 __________
②氦气 __________ 通电发有色光 制霓虹灯
③__________(写俗称) 氧化物 汽化吸热 人工降雨
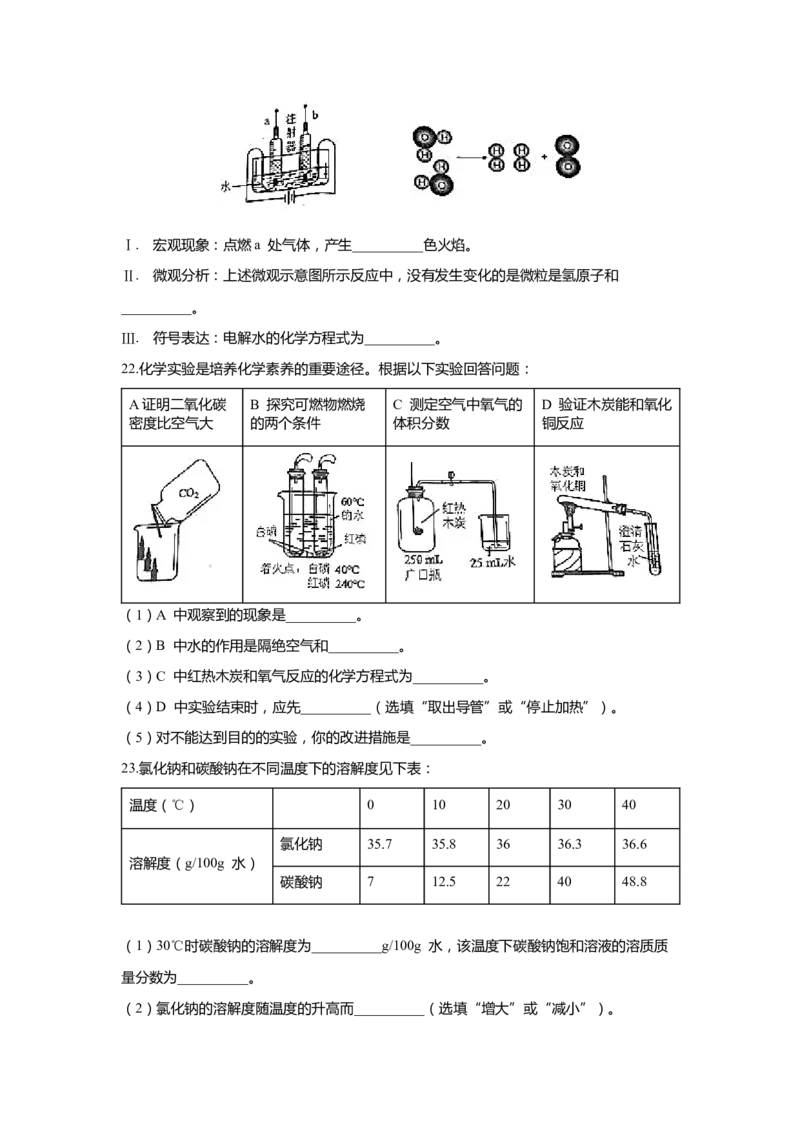
(2)“宏观-微观-符号”相结合是化学学科的思维方式。根据下图回答问题:Ⅰ. 宏观现象:点燃a 处气体,产生__________色火焰。
Ⅱ. 微观分析:上述微观示意图所示反应中,没有发生变化的是微粒是氢原子和
__________。
Ⅲ. 符号表达:电解水的化学方程式为__________。
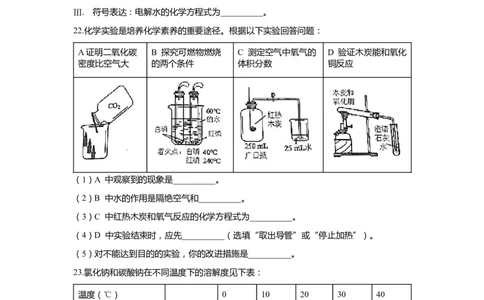
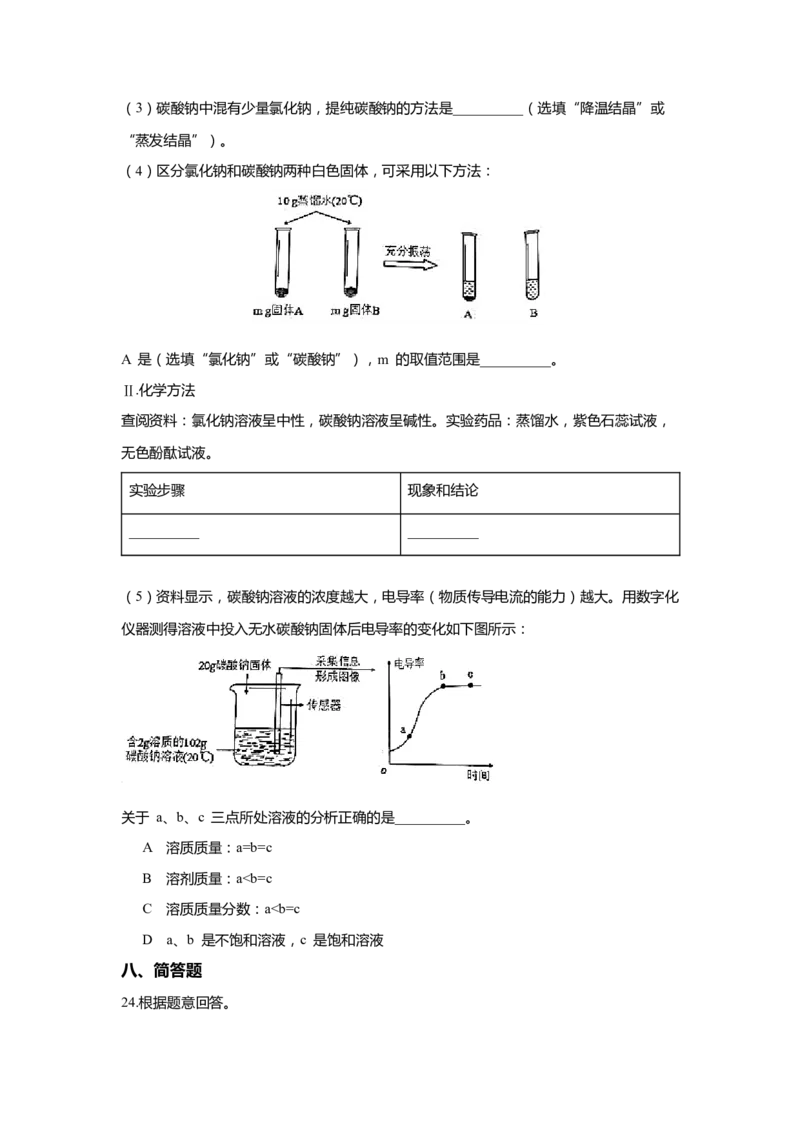
22.化学实验是培养化学素养的重要途径。根据以下实验回答问题:
A证明二氧化碳 B 探究可燃物燃烧 C 测定空气中氧气的 D 验证木炭能和氧化
密度比空气大 的两个条件 体积分数 铜反应
(1)A 中观察到的现象是__________。
(2)B 中水的作用是隔绝空气和__________。
(3)C 中红热木炭和氧气反应的化学方程式为__________。
(4)D 中实验结束时,应先__________(选填“取出导管”或“停止加热”)。
(5)对不能达到目的的实验,你的改进措施是__________。
23.氯化钠和碳酸钠在不同温度下的溶解度见下表:
温度(℃) 0 10 20 30 40
氯化钠 35.7 35.8 36 36.3 36.6
溶解度(g/100g 水)
碳酸钠 7 12.5 22 40 48.8
(1)30℃时碳酸钠的溶解度为__________g/100g 水,该温度下碳酸钠饱和溶液的溶质质
量分数为__________。
(2)氯化钠的溶解度随温度的升高而__________(选填“增大”或“减小”)。(3)碳酸钠中混有少量氯化钠,提纯碳酸钠的方法是__________(选填“降温结晶”或
“蒸发结晶”)。
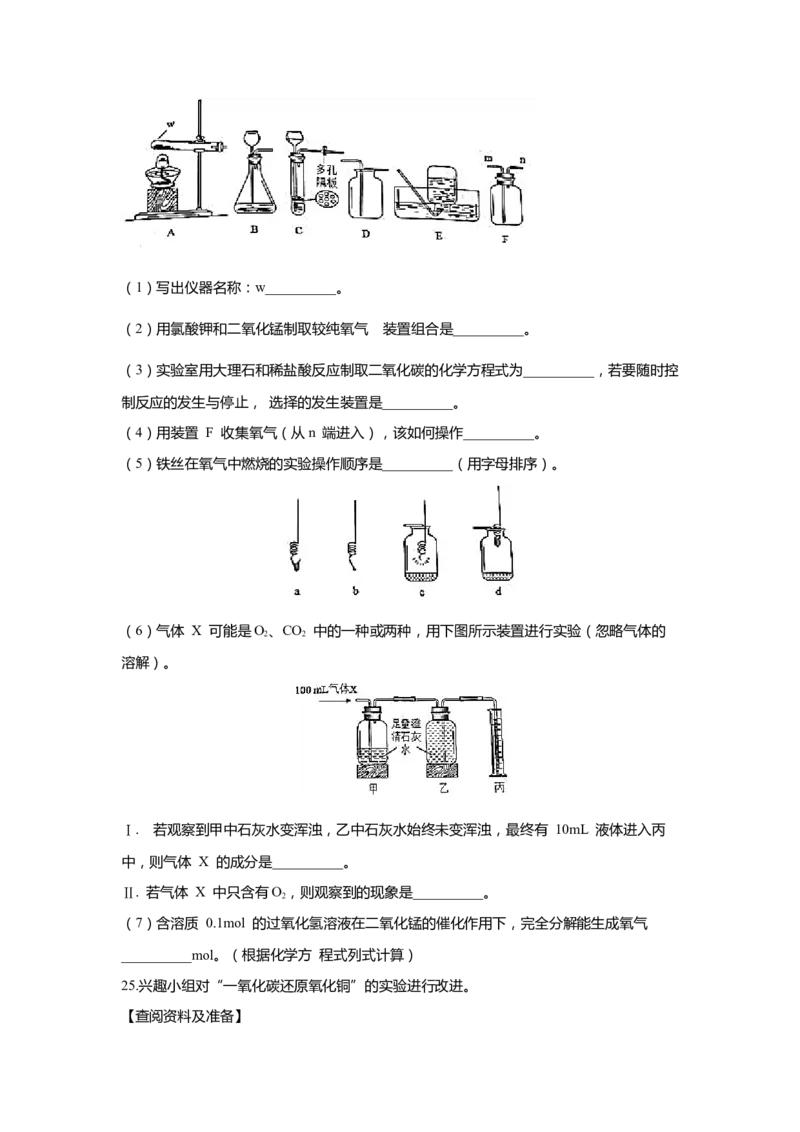
(4)区分氯化钠和碳酸钠两种白色固体,可采用以下方法:
A 是(选填“氯化钠”或“碳酸钠”),m 的取值范围是__________。
Ⅱ.化学方法
查阅资料:氯化钠溶液呈中性,碳酸钠溶液呈碱性。实验药品:蒸馏水,紫色石蕊试液,
无色酚酞试液。
实验步骤 现象和结论
__________ __________
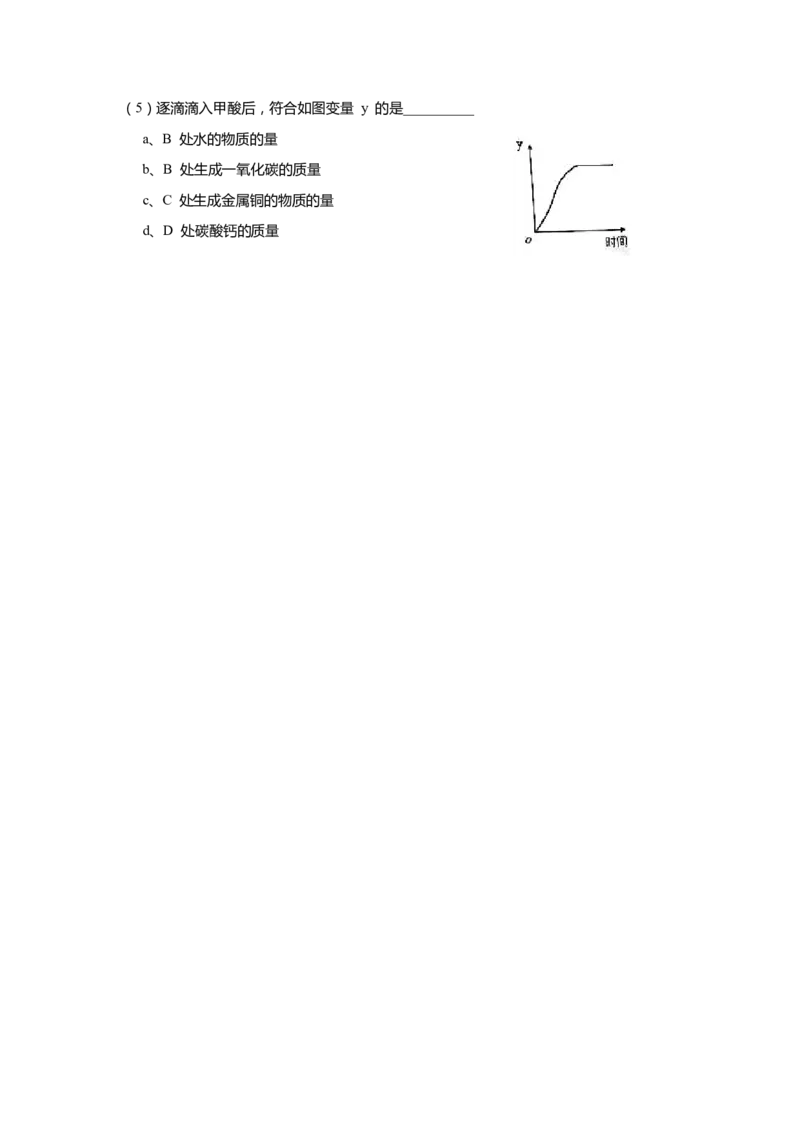
(5)资料显示,碳酸钠溶液的浓度越大,电导率(物质传导电流的能力)越大。用数字化
仪器测得溶液中投入无水碳酸钠固体后电导率的变化如下图所示:
关于 a、b、c 三点所处溶液的分析正确的是__________。
A 溶质质量:a=b=c
B 溶剂质量:ab,理由是
__________。
(4)假设装置内空气已全部排入D 处瓶中,当瓶内气体体积为 400mL 时,点燃是否发
生爆炸? 通过计算说明理由(不考虑药品的体积)__________。(5)逐滴滴入甲酸后,符合如图变量 y 的是__________
a、B 处水的物质的量
b、B 处生成一氧化碳的质量
c、C 处生成金属铜的物质的量
d、D 处碳酸钙的质量