文档内容
2025-2026学年度第一学期高中阶段联考(10月)
高一化学
时间:75分钟 满分:100分
第一卷
一、单选题 (本大题共16个小题,1-10 题每题2分,11-16每题 4分,共 44分。在每小
题列出的选项中,选出符合题目的一项)
1.分类思想方法在化学发展中起到了重大的作用,下列分类正确的是 ( )
酸 碱 盐 碱性氧化物 酸性氧化物
A HNO KOH CaCO CaO SO
3 3 2
B HCl NaOH NaHSO Na O CO
4 2
C CH COOH Cu (OH) CO CaF CO SO
3 2 2 3 2 2
D H SO Na CO NaOH SO CO
2 4 2 3 2 2
2.下列说法正确的有 ( )
①“卤水点豆腐”“黄河入海口处三角洲的形成”都与胶体的性质有关;
②在制备Fe(OH) 胶体实验中,可以长时间加热;
3
③向Fe(OH) 胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解形成棕黄色溶液;
3
④将饱和氯化铁溶液滴入NaOH溶液中,得不到Fe(OH) 胶体;
3
⑤因为胶粒比溶液中溶质粒子大,所以可以用过滤的方法把胶粒分离出来;
⑥不同品牌的墨水不能混用,与胶体聚沉有关;
⑦FeCl 溶液、云、雾、豆浆、牛奶都可以发生丁达尔现象;
3
A.①③⑤⑦ B.①③④⑥ C.①②④⑥ D.②③⑤⑦
3.下列说法正确的是( )
A.硫酸钡溶液几乎不导电,所以它是非电解质
B.氧化铝在熔融状态下能导电,则氧化铝在熔融状态下能电离产生自由移动的铝离子和氧离子
C.NaCl属于电解质,所以NaCl晶体可导电
D.SO 溶于水可导电,SO 属于电解质
3 3
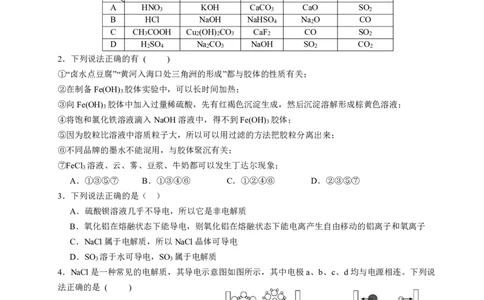
4.NaCl是一种常见的电解质,其导电示意图如图所示,其中电极a、b、c、d均与电源相连。下列说
法正确的是 ( )
A.图甲中 表示水合钠离子
B.图乙中的NaCl处于熔融状态
C.由图甲和图乙可知NaCl在任何状态下都可以导电
D.由图甲和图乙可知NaCl只有在通电条件下能电离出自由移动的离子
5.下列物质在水中的电离方程式书写正确的是 ( )
A.KClO =K+ + C l- + 3 O 2- B.NaHCO =Na++H+ + C O 2-
3 3 3
C.H SO =H 2++SO2- D.Ba(OH) =Ba2+ +2OH-
2 4 2 4 2
高一化学试卷 第1页,共4页
{#{QQABDQCAggggAoAAAQhCQQXACgOYkBGACAgOAEAUMAIBwAFABAA=}#}6.下列各组物质间的反应中,不属于离子反应的是 ( )
A.氢氧化钡溶液和盐酸的反应 B.碳酸钠溶液和氯化钙溶液的反应
C.氢气和氧化铜反应生成铜和水 D.铁和硫酸铜溶液的反应
7.在酸性溶液中能大量共存且溶液为无色透明的是( )
A.K+、MnO -、Na+、Cl- B.K+、Na+、NO -、CO 2-
4 3 3
C.Na+、K+、NO -、SO2- D.Fe3+、Na+、Cl-、SO2-
3 4 4
8.氢化钠(NaH) 可在野外用作生氢剂,NaH用作生氢剂时的化学反应原理为:NaH+H O=NaOH+H ↑。
2 2
下列有关该反应的说法中,正确的是 ( )
A.该反应属于置换反应 B.该反应属于复分解反应
C.NaH是氧化剂 D.H O中的氢元素被还原
2
9.下列离子方程式书写正确的是 ( )
A.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H ↑
2
B.BaCO 粉末加入到硫酸溶液中:BaCO +2H+=H O+Ba2++CO ↑
3 3 2 2
C.向氢氧化钠溶液中滴加NaHCO 溶液:OH-+HCO - =H O+CO 2-
3 3 2 3
D.CuSO 溶液与Ba(OH) 溶液混合:Ba2++SO2-=BaSO ↓
4 2 4 4
10.下列实验现象和结论相符的是 ( )
操作及现象 结论
A 加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体 溶液中一定含有CO 2-
3
B 加入硝酸银,产生白色沉淀 溶液中一定含有Cl-
C 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失 溶液中一定有SO2-
4
D 向溶液中滴加紫色石蕊溶液,溶液变为红色 溶液中一定有H+
A.A B.B C.C D.D
11.下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是 ( )
A.Cu(OH) 和稀H SO ;Cu(OH) 和CH COOH B.BaCl 和 Na SO ;Ba(OH) 和(NH ) SO
2 2 4 2 3 2 2 4 2 4 2 4
C.NaHCO 和HCl; Na CO 和HCl D.HNO 和Na CO ;NaHSO 和K CO
3 2 3 3 2 3 4 2 3
12.某含RO -的溶液与Na SO 溶液恰好反应完全,已知Na SO 被氧化为Na SO ,并且参加反应的RO -
3 2 3 2 3 2 4 3
与SO 2-的个数比为1∶2.则还原产物中元素R的价态是 ( )
3
A.-1价 B.+1价 C.-2价 D.+2价
13.下列变化过程中,需加入氧化剂才能实现的是 ( )
A.H O →O B.KClO →KCl C.KBr→Br D.MnO →Mn2+
2 2 2 3 2 2
14.现有下列几个离子反应,下列有关性质的比较正确的是 ( )
①Cr O2-+14H++6Cl-===2Cr3++3Cl ↑+7H O
2 7 2 2
②2Fe2++Cl ===2Fe3++2Cl-
2
③2Fe3++SO +2H O===2Fe2++SO2-+4H+
2 2 4
A.氧化性:Cr O2->Cl >Fe3+>SO2- B.氧化性:Fe3+>SO2->Cl >Cr O2-
2 7 2 4 4 2 2 7
C.还原性:SO Cr3+>Fe2+>SO
2 2
高一化学试卷 第2页,共4页
{#{QQABDQCAggggAoAAAQhCQQXACgOYkBGACAgOAEAUMAIBwAFABAA=}#}
15.一定条件下,硝酸铵受热分解的化学方程式为5NH NO 2HNO 4N 9H O,在反应中被氧化
4 3 3 2 2
与被还原的氮原子的个数之比为 ( )
A.5:3 B.5:4 C.1:1 D.3:5
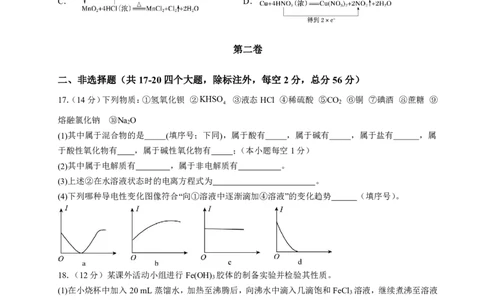
16.下列化学方程式中,表示电子转移的方向和数目不 . 正 . 确 . 的是( )
A. B.
C. D.
第二卷
二、非选择题(共 17-20四个大题,除标注外,每空 2分,总分 56分)
17.(14分)下列物质:①氢氧化钡 ②KHSO ③液态HCl ④稀硫酸 ⑤CO ⑥铜 ⑦碘酒 ⑧蔗糖 ⑨
4 2
熔融氯化钠 ⑩Na O
2
(1)其中属于混合物的是 (填序号;下同),属于酸有 ,属于碱有 ,属于盐有 ,属
于酸性氧化物有 ,属于碱性氧化物有 ;(本小题每空1分)
(2)其中属于电解质有 ,属于非电解质有 。
(3)上述②在水溶液状态时的电离方程式为 。
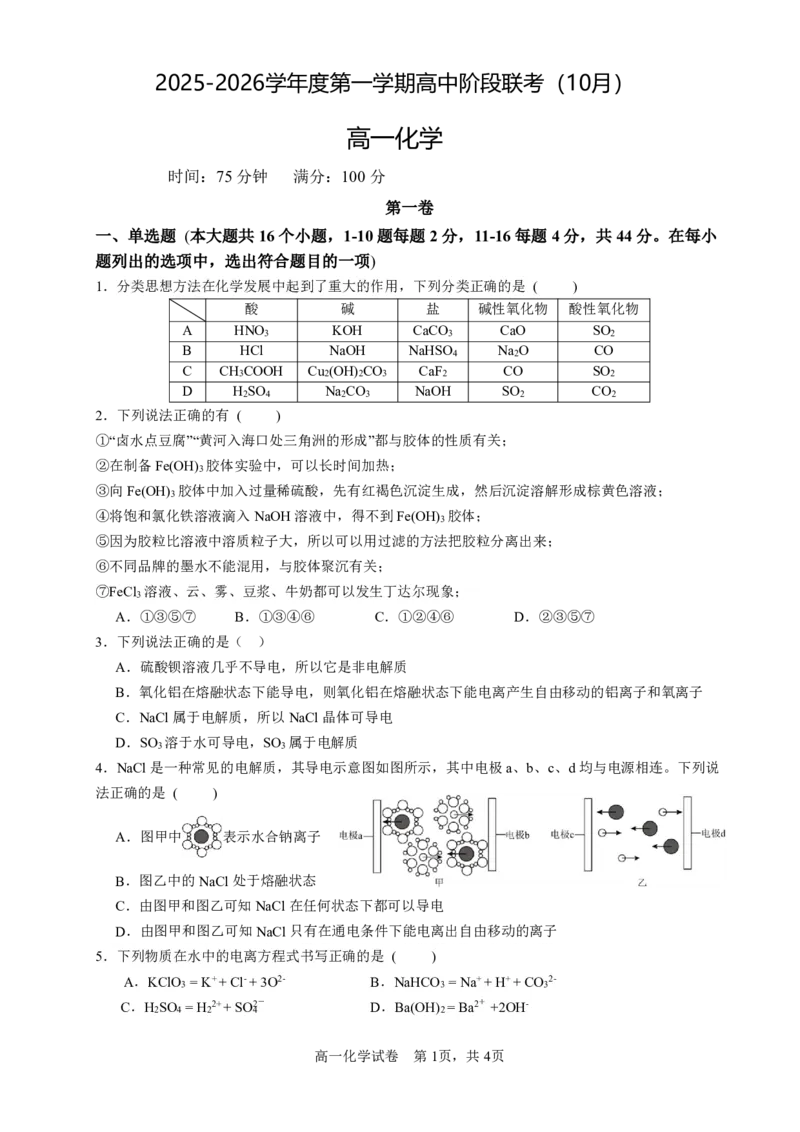
(4)下列哪种导电性变化图像符合“向①溶液中逐渐滴加④溶液”的变化趋势 (填序号)。
18.(12分)某课外活动小组进行Fe(OH) 胶体的制备实验并检验其性质。
3
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl 溶液,继续煮沸至溶液
3
呈 色,停止加热,即制得Fe(OH) 胶体。写出该反应的化学方程式 。
3
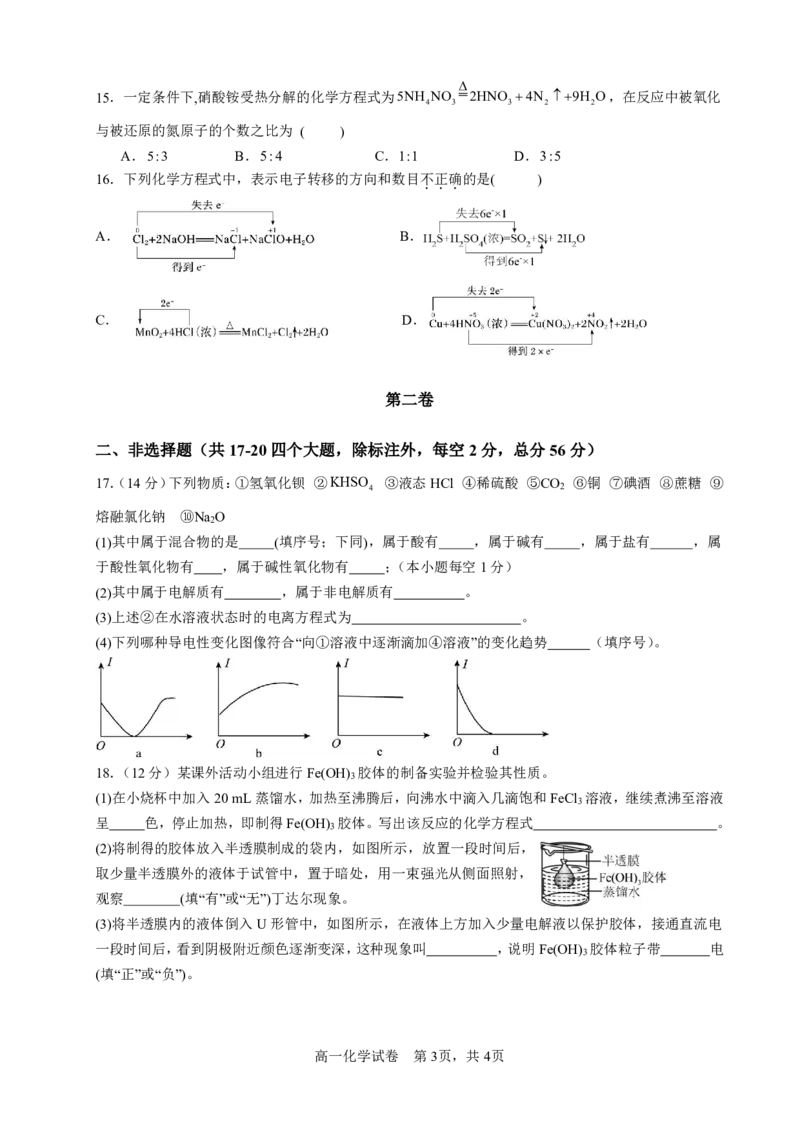
(2)将制得的胶体放入半透膜制成的袋内,如图所示,放置一段时间后,
取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,
观察 (填“有”或“无”)丁达尔现象。
(3)将半透膜内的液体倒入U形管中,如图所示,在液体上方加入少量电解液以保护胶体,接通直流电
一段时间后,看到阴极附近颜色逐渐变深,这种现象叫 ,说明Fe(OH) 胶体粒子带 电
3
(填“正”或“负”)。
高一化学试卷 第3页,共4页
{#{QQABDQCAggggAoAAAQhCQQXACgOYkBGACAgOAEAUMAIBwAFABAA=}#}(4)若向Fe(OH) 胶体中滴入硫酸直到过量,描述此过程的实验现象 。
3
19.(10分)有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl-、SO2-、CO 2-,现进行以下
4 3
实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
③取少量②中的碱性溶液,滴加Na CO 溶液,有白色沉淀产生。
2 3
(1)根据上述事实知,该溶液中肯定存在的离子有 ;肯定不存在的离子有 ;可能存在
的离子有 ;
(2)写出③中发生反应的离子方程式 。
(3)写出碳酸钙固体溶于足量稀盐酸的离子方程式 。
20.(20分)氧化还原反应是一类重要的化学反应,广泛存在于生产和生活中。
(1)高铁酸钾(K FeO )是一种新型的净水剂,可以通过下述反应制取:
2 4
2Fe3++xOH- +3ClO- =2FeO 2-+3Cl- +yH O 。
4 2
①上述反应中的x= ,y= 。
②该反应中还原剂是 (填化学符号,下同),还原产物为 。
(2) 重铬酸钾与浓盐酸反应可用于实验室制取氯气,其化学方程式为:
K Cr O +14HCl(浓)=2KCl+2CrCl +3Cl ↑+7H O
2 2 7 3 2 2
①K Cr O 中Cr的化合价为 。
2 2 7
②氧化剂与还原剂的个数比是 。
③上述反应中,每产生3分子的氯气,转移 个电子。
④将氯气通入浓氨水中发生如下反应(本小题共2分)。
请配平方程式:___Cl +___NH =___NH Cl+___N ;
2 3 4 2
(3) 误食NaNO 会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒。
2
①该过程中NaNO 表现出的性质与下列________反应中H O 表现出的性质完全相同。
2 2 2
A.5H O +2KMnO +3H SO =2MnSO +K SO +5O ↑+8H O
2 2 4 2 4 4 2 4 2 2
B.H O +2Fe2++2H+ =2Fe3++2H O
2 2 2
C.H O +H SO +2KI =2H O+I +K SO
2 2 2 4 2 2 2 4
MnO
D.2H O 2 2H O+O
2 2 2 2
②已知亚硝酸钠可以与氯化铵反应生成氮气、氯化钠和水,写出该反应的化学反应方程
式: 。
高一化学试卷 第4页,共4页
{#{QQABDQCAggggAoAAAQhCQQXACgOYkBGACAgOAEAUMAIBwAFABAA=}#}2025-2026 学年度第一学期高中阶段联考(10 月)
高一化学参考答案及评分标准
答案:
1-5 ABBBD 6-10 CCDCD 11-16 DBCAA B
17.
(1)④⑦, ③, ① , ②⑨, ⑤, ⑩,
(2)①②③⑨⑩,⑤⑧。
(3)KHSO ==K++H++SO 2-
4 4
(4)a
18.
Δ
(1) 红褐 FeCl +3H O Fe(OH) (胶体)+3HCl
3 2 3
(2) 无
(3)电泳 正
(4)先产生红褐色沉淀,后沉淀溶解,得到黄色溶液
19.
(1) H+、Ba2+、Cl- Mg2+、SO2-、CO2- Na+
4 3
(2) CO2-+Ba2+=BaCO ↓
3 3
(3) CaCO +2H+=Ca2++H O+CO ↑
3 2 2
20.
(1) ①10 5
②Fe3+ Cl-
(2) ①+6
②1:6
③6
④3 8 6 1
(3) ①BC
②NaNO +NH Cl=NaCl+N +2H O
2 4 2 2
大致评分标准:
1、2分一空,少写给1分,多写及写错不给分;
2、化学专用名词:写错别字不给分,如“饱和”写成“饱合”,“坩埚”写成“钳锅”等
3、方程式书写:
①反应物或生成物化学式书写错误或极不规范,不给分;
②少写或多写反应物、生成物,或不配平,不给分;
③化学计量数成比例扩大或缩小,扣1分;
④“=”写成“―→”或可逆符号,漏写“↑”“↓”扣1分;
⑤离子方程式写成化学方程式不给分。
⑥配平方程式时。错一空,均不给分
4、填空:要求写化学式,错写成名称不给分;要求写离子方程式写成化学方程式不给分
高一化学 参考答案 第 1 页 共 1 页
{#{QQABDQCAggggAoAAAQhCQQXACgOYkBGACAgOAEAUMAIBwAFABAA=}#}