文档内容
2024-2025 学年第二学期高一年级第一次教学质量检测
化学
(考试时间:75 分钟)
可能用到的相对原子质量:
一、选择题:本题共 16 小题,共 44 分。第 1~10 小题,每小题 2 分; 第 11~16 小题,每
小题 4 分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 广东省博物馆馆藏大量珍贵文物。下列文物主要由硅酸盐制成的是
文物
选项 A.西周信宜铜盉 B.元玉壶春瓶 C.北宋木雕罗汉像 D.白地丝绸手绘花鸟
A.A B. B C. C D. D
2. 2024 年,北斗三号全球卫星导航系统正式完成全球组网,是中国科技实力的充分体现。下列说法正
确的是
A. 控制系统的芯片是硅晶体,硅晶体用作半导体材料是因为其原子的最外层电子数多
B. 火箭推进剂发生的化学反应为 2NH + N O = 3N + 4H O,其中氢元素被氧化
2 4 2 4 2 2
C. 火箭发射时会产生大量红色的烟雾, 该现象与反应产生的 NO 有关
2
D. 火箭头部的一层特殊材料能起到保护作用,是由于其在熔化时能放出大量的热
3. “绿水青山就是金山银山”旨在引导社会各界自觉践行绿色生活,共建美丽中国。下列说法正确的是
A. 酸雨是 pH<7 的雨水
B. 豆科植物根瘤菌将氮气转化成氨的过程属于自然固氮
C. 汽车尾气中的 NO 主要来源于汽油的不充分燃烧
D. CO 、SO 、NO 均是常见的大气污染物
2 2 2
4. 化学与生产、生活密切相关。下列有关说法不正确的是
A. BaCO 可用于消化系统 X 射线检查的内服药剂
3
B. 二氧化硫可添加到葡萄酒中做防腐剂和抗氧化剂
C. 水泥制造业中会添加适量石膏,调节水泥硬化速度
D. 向燃煤中加入生石灰,可以减少酸雨的产生
5. 劳动成就梦想。下列劳动项目与所述的化学知识没有关联的是
SHIJUAN 第 1 页 共 8 页选项 劳动项目 化学知识
A 实验操作:用 SO 漂白纸浆 SO 具有漂白性
2 2
B 工业劳动:用 溶液刻蚀玻璃 是酸性氧化物
C 生产活动:用铝制容器贮运浓硝酸 铝遇浓硝酸钝化
D 家务劳动:用食醋清除水壶中的少量水垢 酸性:醋酸>碳酸
A. A B. B C. C D. D
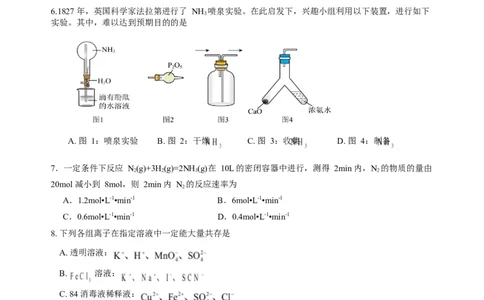
6.1827 年,英国科学家法拉第进行了 NH 喷泉实验。在此启发下,兴趣小组利用以下装置,进行如下
3
实验。其中,难以达到预期目的的是
A. 图 1:喷泉实验 B. 图 2:干燥 C. 图 3:收集 D. 图 4:制备
7.一定条件下反应 N(g)+3H(g)=2NH (g)在 10L 的密闭容器中进行,测得 2min 内,N 的物质的量由
2 2 3 2
20mol 减小到 8mol,则 2min 内 N 的反应速率为
2
A.1.2mol•L-1•min-1 B.6mol•L-1•min-1
C.0.6mol•L-1•min-1 D.0.4mol•L-1•min-1
8. 下列各组离子在指定溶液中一定能大量共存是
A. 透明溶液:
B. 溶液:
C. 84 消毒液稀释液:
D. 加入铝粉能产生氢气的溶液:
9. 下列离子方程式正确的是
A.铜和浓硝酸反应: (浓)
B. 溶液中滴加 溶液:
C. 氨水与盐酸反应:H++OH-=H
2
O
D. 二氧化氮与水反应:3NO
2
+H
2
O=2H++2NO
3
-+NO
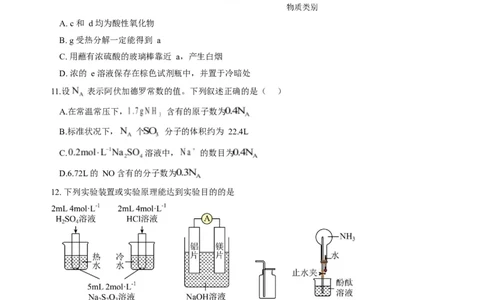
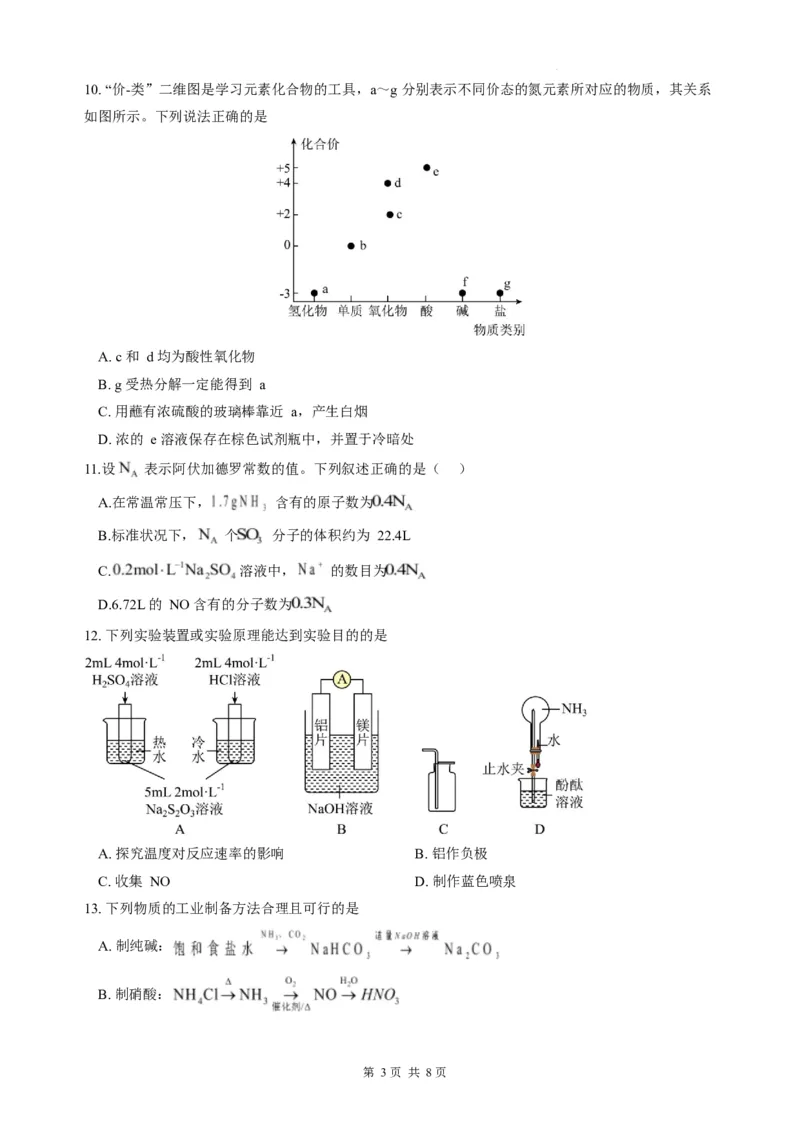
SHIJUAN 第 2 页 共 8 页10. “价-类”二维图是学习元素化合物的工具,a~g 分别表示不同价态的氮元素所对应的物质,其关系
如图所示。下列说法正确的是
A. c 和 d 均为酸性氧化物
B. g 受热分解一定能得到 a
C. 用蘸有浓硫酸的玻璃棒靠近 a,产生白烟
D. 浓的 e 溶液保存在棕色试剂瓶中,并置于冷暗处
11.设 表示阿伏加德罗常数的值。下列叙述正确的是( )
A.在常温常压下, 含有的原子数为
B.标准状况下, 个 分子的体积约为 22.4L
C. 溶液中, 的数目为
D.6.72L 的 NO 含有的分子数为
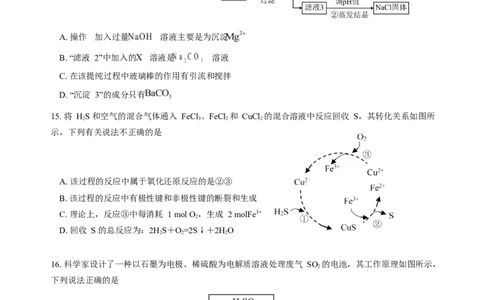
12. 下列实验装置或实验原理能达到实验目的的是
A. 探究温度对反应速率的影响 B. 铝作负极
C. 收集 NO D. 制作蓝色喷泉
13. 下列物质的工业制备方法合理且可行的是
A. 制纯碱:
B. 制硝酸:
SHIJUAN 第 3 页 共 8 页C. 制漂粉精:
D. 制高纯硅:石英砂 粗硅 纯硅
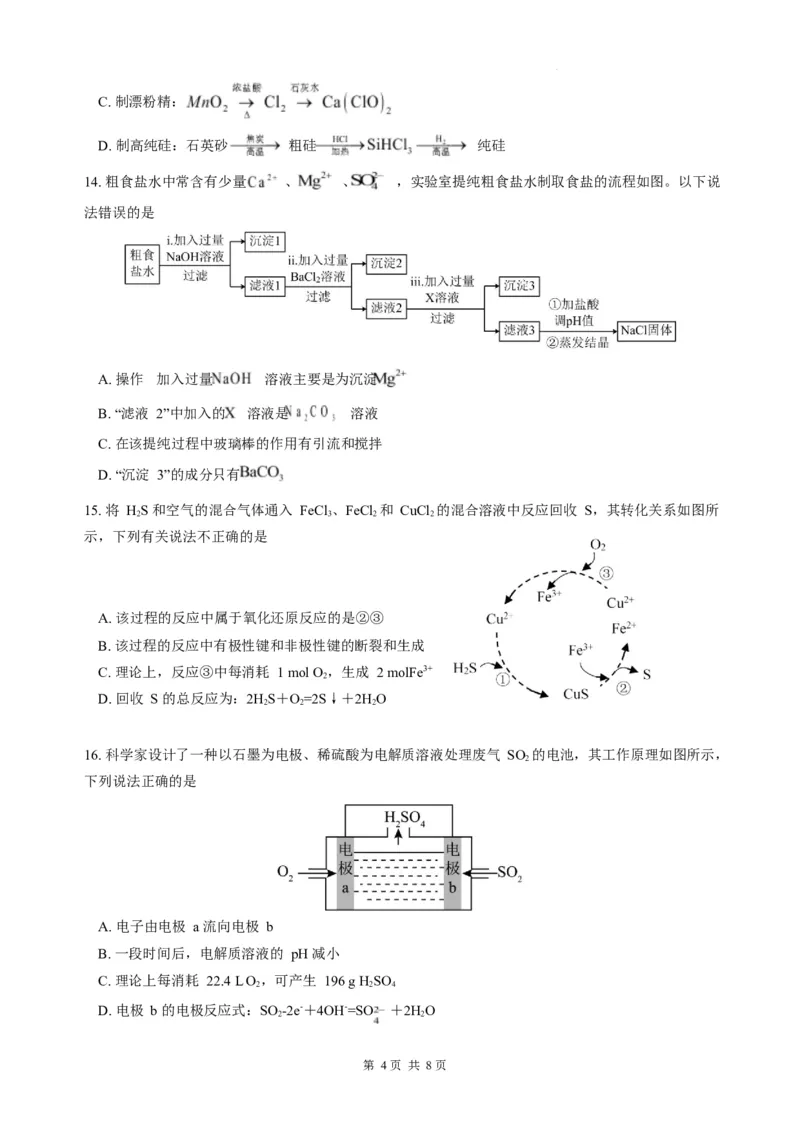
14. 粗食盐水中常含有少量 、 、 ,实验室提纯粗食盐水制取食盐的流程如图。以下说
法错误的是
A. 操作 加入过量 溶液主要是为沉淀
B. “滤液 2”中加入的 溶液是 溶液
C. 在该提纯过程中玻璃棒的作用有引流和搅拌
D. “沉淀 3”的成分只有
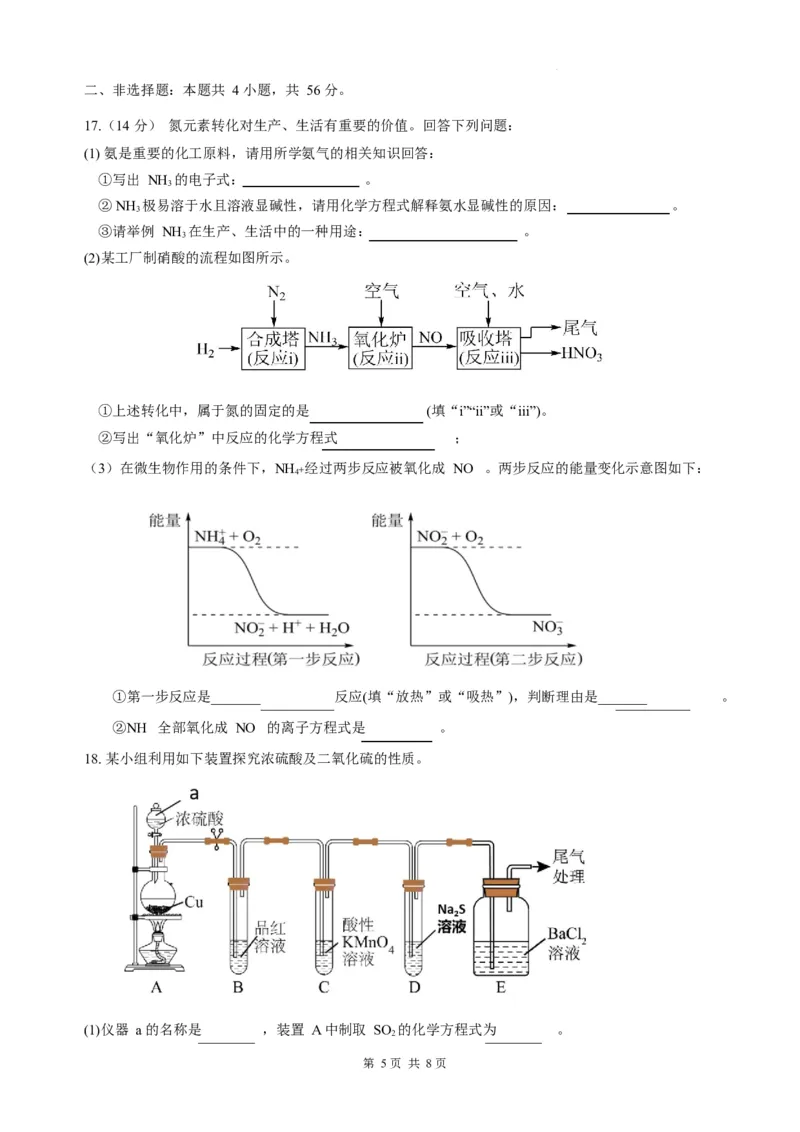
15. 将 HS 和空气的混合气体通入 FeCl 、FeCl 和 CuCl 的混合溶液中反应回收 S,其转化关系如图所
2 3 2 2
示,下列有关说法不正确的是
A. 该过程的反应中属于氧化还原反应的是②③
B. 该过程的反应中有极性键和非极性键的断裂和生成
C. 理论上,反应③中每消耗 1 mol O ,生成 2 molFe3+
2
D. 回收 S 的总反应为:2HS+O=2S↓+2HO
2 2 2
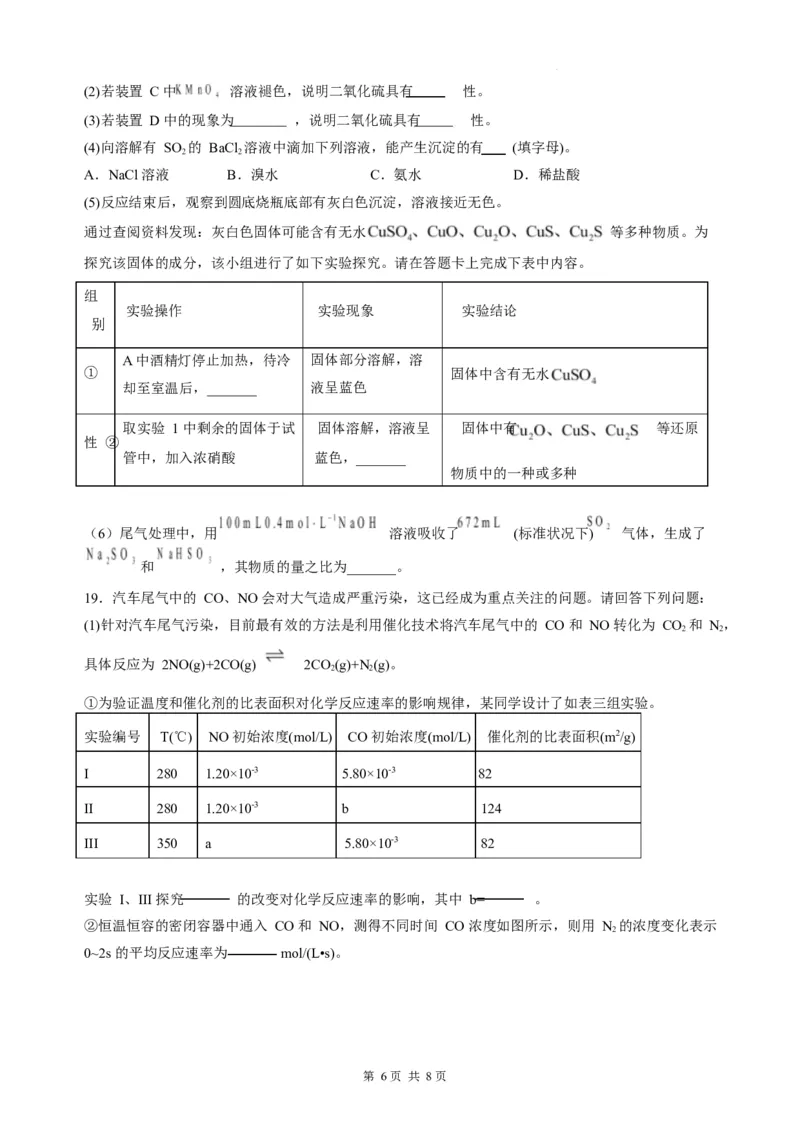
16. 科学家设计了一种以石墨为电极、稀硫酸为电解质溶液处理废气 SO 的电池,其工作原理如图所示,
2
下列说法正确的是
A. 电子由电极 a 流向电极 b
B. 一段时间后,电解质溶液的 pH 减小
C. 理论上每消耗 22.4 L O ,可产生 196 g HSO
2 2 4
D. 电极 b 的电极反应式:SO -2e-+4OH-=SO +2HO
2 2
SHIJUAN 第 4 页 共 8 页二、非选择题:本题共 4 小题,共 56 分。
17.(14 分) 氮元素转化对生产、生活有重要的价值。回答下列问题:
(1) 氨是重要的化工原料,请用所学氨气的相关知识回答:
①写出 NH 的电子式: 。
3
② NH 极易溶于水且溶液显碱性,请用化学方程式解释氨水显碱性的原因: 。
3
③请举例 NH 在生产、生活中的一种用途: 。
3
(2)某工厂制硝酸的流程如图所示。
①上述转化中,属于氮的固定的是 (填“i”“ii”或“iii”)。
②写出“氧化炉”中反应的化学方程式 ;
(3)在微生物作用的条件下,NH 4+ 经过两步反应被氧化成 NO 。两步反应的能量变化示意图如下:
①第一步反应是_______ 反应(填“放热”或“吸热”),判断理由是_______ 。
②NH 全部氧化成 NO 的离子方程式是 。
18. 某小组利用如下装置探究浓硫酸及二氧化硫的性质。
(1)仪器 a 的名称是 ,装置 A 中制取 SO 的化学方程式为 。
2
SHIJUAN 第 5 页 共 8 页(2)若装置 C 中 溶液褪色,说明二氧化硫具有 性。
(3)若装置 D 中的现象为 ,说明二氧化硫具有 性。
(4)向溶解有 SO 的 BaCl 溶液中滴加下列溶液,能产生沉淀的有 (填字母)。
2 2
A.NaCl 溶液 B.溴水 C.氨水 D.稀盐酸
(5)反应结束后,观察到圆底烧瓶底部有灰白色沉淀,溶液接近无色。
通过查阅资料发现:灰白色固体可能含有无水 等多种物质。为
探究该固体的成分,该小组进行了如下实验探究。请在答题卡上完成下表中内容。
组
实验操作 实验现象 实验结论
别
A 中酒精灯停止加热,待冷 固体部分溶解,溶
① 固体中含有无水
却至室温后,_______ 液呈蓝色
取实验 1 中剩余的固体于试 固体溶解,溶液呈 固体中有 等还原
性 ②
管中,加入浓硝酸 蓝色,_______
物质中的一种或多种
(6)尾气处理中,用 溶液吸收了 (标准状况下) 气体,生成了
和 ,其物质的量之比为_______。
19.汽车尾气中的 CO、NO 会对大气造成严重污染,这已经成为重点关注的问题。请回答下列问题:
(1)针对汽车尾气污染,目前最有效的方法是利用催化技术将汽车尾气中的 CO 和 NO 转化为 CO 和 N,
2 2
具体反应为 2NO(g)+2CO(g) 2CO(g)+N(g)。
2 2
①为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。
实验编号 T(℃) NO 初始浓度(mol/L) CO 初始浓度(mol/L) 催化剂的比表面积(m2/g)
I 280 1.20×10-3 5.80×10-3 82
II 280 1.20×10-3 b 124
III 350 a 5.80×10-3 82
实验 I、III 探究 的改变对化学反应速率的影响,其中 b= 。
②恒温恒容的密闭容器中通入 CO 和 NO,测得不同时间 CO 浓度如图所示,则用 N 的浓度变化表示
2
0~2s 的平均反应速率为 mol/(L•s)。
SHIJUAN 第 6 页 共 8 页③下列关于汽车尾气处理反应说法正确的是 。
A.给予足够的反应时间,体系中不存在 CO 和 NO
B.使用合适的催化剂可以增大反应速率
C.恒温恒容条件下,向体系中充入氦气,有利于增大反应速率
D.恒温恒容条件下,增大 NO 的量可以增大反应速率
(2)通过 NO 传感器可监测汽车尾气中 NO 含量,其工作原理如图所示:
①NiO 电极为 (填“正极”或“负极”)
②若线路中转移 2mol 电子,则该电池理论上消耗的 O 在标准状况下的体积为 L。
2
③ 电极上的电极反应式为 。
20.以高硫铝土矿(主要成分为 、 ,少量 等)为原料,生产氧化铝并获得 的部
分工艺流程如图:
(1)为了提高第一次焙烧后的烧渣在碱浸时的溶出速率,可采取的有效措施为 (任写一点)。
(2)已知:第一次焙烧的主要目的是脱硫(降低矿粉中硫化物型硫的含量),以免影响产品 的质量,
此过程中 与氧气发生了氧化还原反应: ,其中被氧化的元素
SHIJUAN 第 7 页 共 8 页有 (填元素符号);第一次焙烧结束后,硫最终主要以 (填物质的化学式)的形式存在;
(3)碱浸时发生的主要反应的离子方程式为 。
(4)第二次焙烧过程中产生了污染性气体 ,大量排放的 SO 与雨水作用生成 HSO 造成酸雨等环境
2 2 3
问题,连续测定一段时间内某雨水的 pH 结果显示 pH 随时间的增加而减小,其原因可能是_______(用
化学方程式表示)。
工业上可用双碱法脱硫法处理废气,过程如图所示,其中可循环使用的试剂是 。
(5)纯度检验:将少量磁选后的产品溶于稀硫酸中,再滴入酸性 溶液,若酸性 褪色,(填
“能”或“不能”) 说明产品中含有 FeO,理由是 。
SHIJUAN 第 8 页 共 8 页