文档内容
2022 年天津市普通高中学业水平等级性考试
化学
本试卷分为第 I 卷(选择题)和第 II 卷(非选择题)两部分,共 100 分,考试用时 60 分钟。第 I
卷 1至 4页,第 II卷 5至 8页。
答卷前,考生务必将自己的姓名、考生号、考场号和座位号填写在答题卡上,并在规定位置
粘贴考试用条形码。答卷时,考生务必将答案涂写在答题卡上,答在试卷上的无效。考试结
束后,将本试卷和答题卡一并交回。
以下数据可供解题时参考:相对原子质量:H 1 C 12 O 16 Na 23
第 I卷
注意事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净
后,再选涂其他答案标号。
2.本卷共 12题,每题 3分,共 36分。在每题所给出的四个选项中,只有一项是最符合题目
要求的。
1. 近年我国在科技领域不断取得新成就。对相关成就所涉及的化学知识理解错误的是
A. 我国科学家实现了从二氧化碳到淀粉的人工合成,淀粉是一种单糖
B. 中国“深海一号”平台成功实现从深海中开采石油和天然气,石油和天然气都是混合物
C. 我国实现了高性能纤维锂离子电池的规模化制备,锂离子电池放电时将化学能转化为电能
D. 以硅树脂为基体的自供电软机器人成功挑战马里亚纳海沟,硅树脂是一种高分子材料
【答案】A
【解析】
【详解】A.淀粉是一种多糖,故A错误;
B.石油主要是各种烷烃、环烷烃、芳香烃的混合物,天然气主要含甲烷,还有少量的其他烷烃气体,因
此天然气是混合物,故B正确;
C.锂离子电池放电属于原电池,是将化学能转化为电能,故C正确;
D.硅树脂是高聚物,属于高分子材料,故D正确。
综上所述,答案为A。
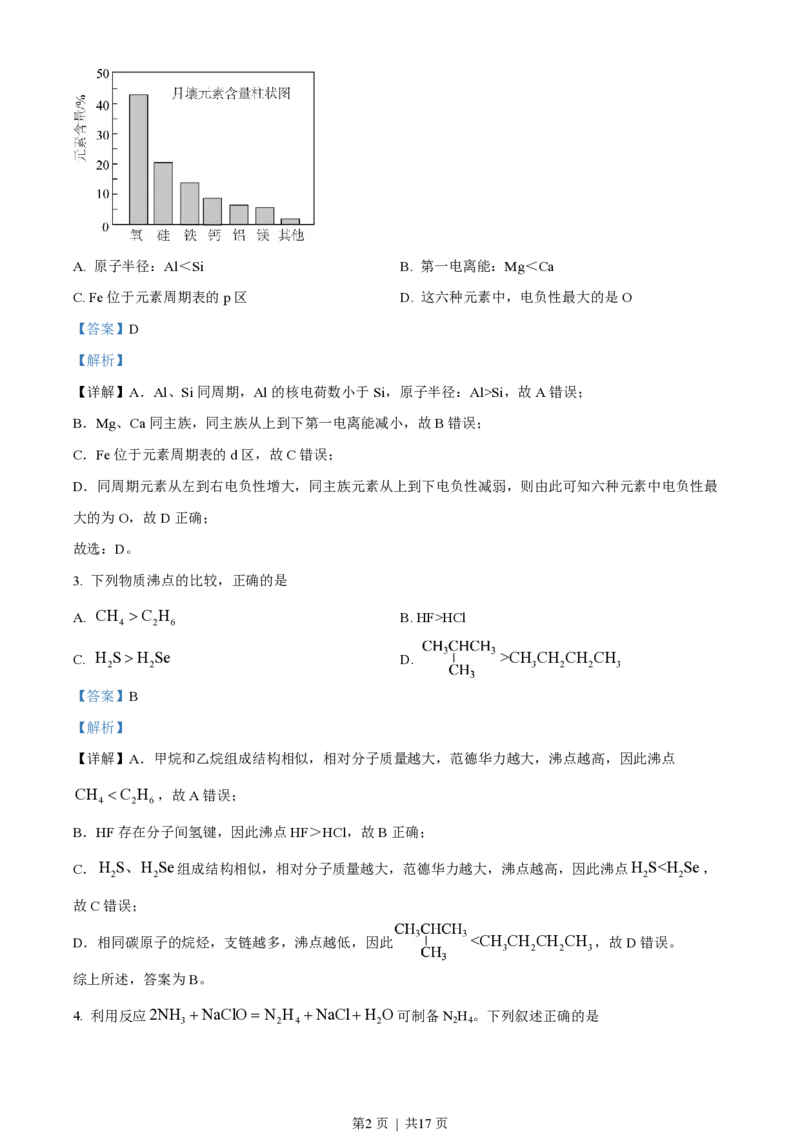
2. 嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素的说法正确的是
第1页 | 共17页A. 原子半径:Al<Si B. 第一电离能:Mg<Ca
C. Fe位于元素周期表的p区 D. 这六种元素中,电负性最大的是O
【答案】D
【解析】
【详解】A.Al、Si同周期,Al的核电荷数小于Si,原子半径:Al>Si,故A错误;
B.Mg、Ca同主族,同主族从上到下第一电离能减小,故B错误;
C.Fe位于元素周期表的d区,故C错误;
D.同周期元素从左到右电负性增大,同主族元素从上到下电负性减弱,则由此可知六种元素中电负性最
大的为O,故D正确;
故选:D。
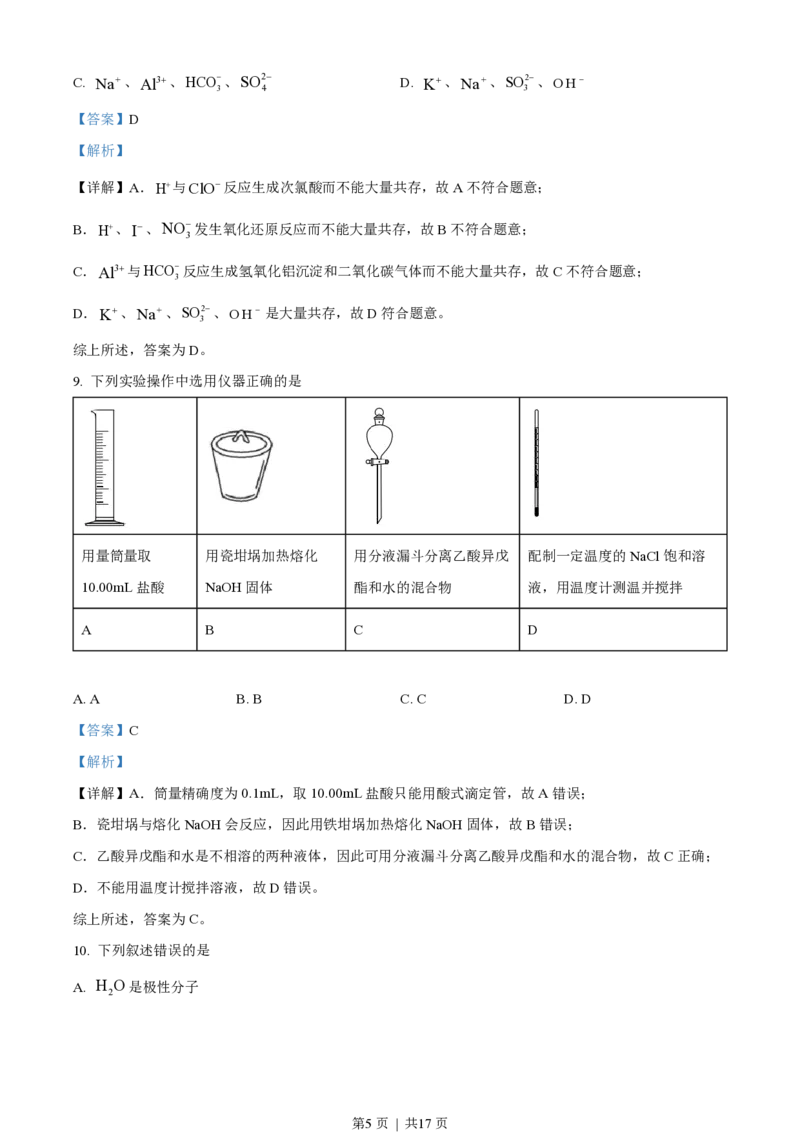
3. 下列物质沸点的比较,正确的是
A. CH >C H B. HF>HCl
4 2 6
C. H S>H Se D. >CH CH CH CH
2 2 3 2 2 3
【答案】B
【解析】
【详解】A.甲烷和乙烷组成结构相似,相对分子质量越大,范德华力越大,沸点越高,因此沸点
CH 0
2 2
②4Fe2+Laq+O g+2H Ol=4Fe3+Laq+4OH-aq ΔH =-bkJ×mol-1b>0
2 2
回答下列问题:
(1)该工艺的总反应方程式为___________。1mol H Sg 发生该反应的热量变化为___________,
2
Fe3+L在总反应中的作用是___________。
(2)研究不同配体与Fe3+所形成的配合物(A、B、C)对H S吸收转化率的影响。将配合物A、B、C分别
2
溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向三份吸收液持续通入H S,测
2
得单位体积吸收液中H 2 S吸收转化率é ë aH 2 Sù û随时间变化的曲线如图1所示。以aH 2 S 由100%降至
80%所持续的时间来评价铁配合物的脱硫效率,结果最好的是___________(填“A”、“B”或“C”)。
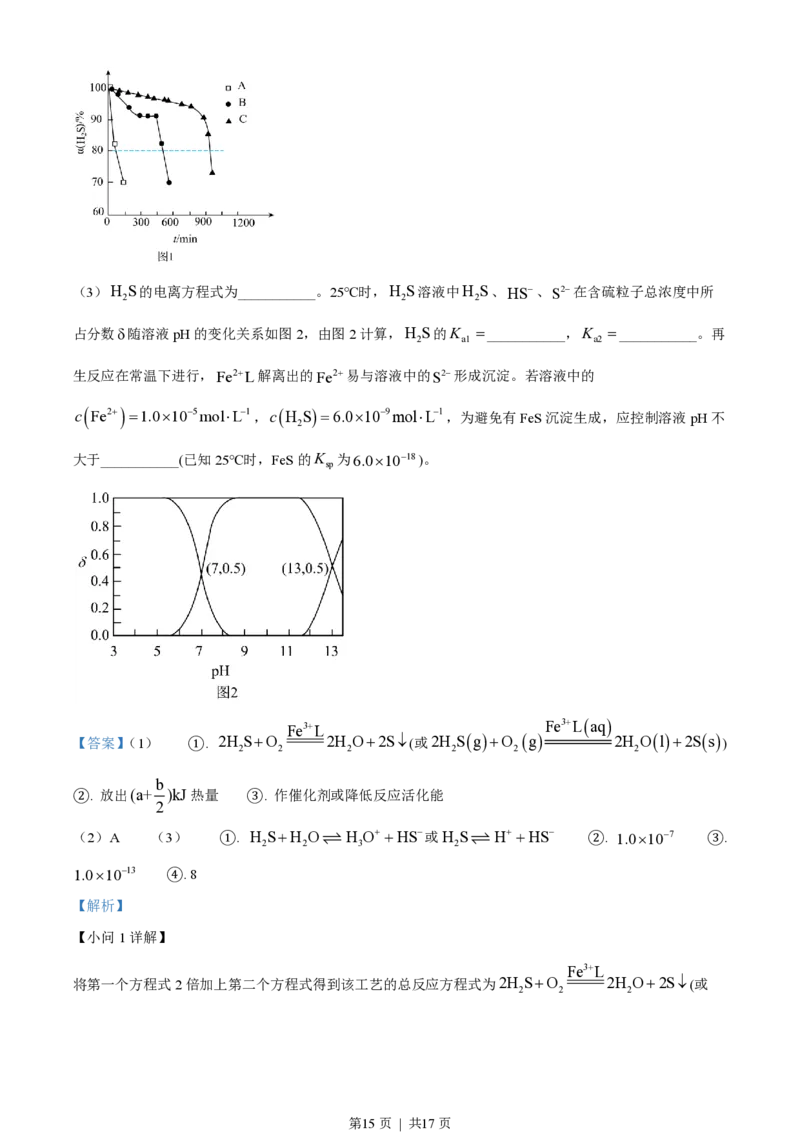
第14页 | 共17页(3)H S的电离方程式为___________。25℃时,H S溶液中H S、HS-、S2-在含硫粒子总浓度中所
2 2 2
占分数δ随溶液pH的变化关系如图2,由图2计算,H S的K =___________,K =___________。再
2 a1 a2
生反应在常温下进行,Fe2+L解离出的Fe2+易与溶液中的S2-形成沉淀。若溶液中的
c Fe2+ =1.0´10-5mol×L-1,cH S=6.0´10-9mol×L-1,为避免有FeS沉淀生成,应控制溶液pH不
2
大于___________(已知25℃时,FeS的K 为6.0´10-18)。
sp
Fe3+L
Fe3+Laq
【答案】(1) ①. 2H S+O 2H O+2S¯(或2H Sg+O g 2H Ol+2Ss )
2 2 2 2 2 2
b
②. 放出(a+ )kJ热量 ③. 作催化剂或降低反应活化能
2
(2)A (3) ①. H 2 S+H 2 O ƒ H 3 O+ +HS-或H 2 S ƒ H+ +HS- ②. 1.0´10-7 ③.
1.0´10-13 ④. 8
【解析】
【小问1详解】
Fe3+L
将第一个方程式2倍加上第二个方程式得到该工艺的总反应方程式为2H S+O 2H O+2S¯(或
2 2 2
第15页 | 共17页Fe3+Laq
2H Sg+O g 2H Ol+2Ss ),该反应的热化学方程式
2 2 2
Fe3+Laq
2H Sg+O g 2H Ol+2SsΔH =-2a+bkJ×mol-1,因此1mol H Sg 发生该反
2 2 2 2
b
应的热量变化为放出(a+ )kJ热量,Fe3+L参与了化学反应,但反应前后量没有改变,因此Fe3+L在总反
2
Fe3+L
应中的作用是作催化剂或降低反应活化能;故答案为:2H S+O 2H O+S¯(或
2 2 2
Fe3+Laq
b
2H Sg+O g 2H Ol+2Ss );放出(a+ )kJ热量;作催化剂或降低反应活化能。
2 2 2 2
【小问2详解】
根据图中信息以aH S
由100%降至80%所持续的时间来评价铁配合物的脱硫效率,A持续时间最短,
2
说明A的脱硫效率最高,因此结果最好的A;故答案为:A。
【小问3详解】
H S是二元弱酸,其电离是一步一步电离,主要以第一步电离为主,因此其电离方程式为
2
H
2
S+H
2
O
ƒ
H
3
O+ +HS-或H
2
S
ƒ
H+ +HS-;根据题意pH=7时H
2
S、HS-的所占分数相等,因此
c(HS-)×c(H+)
H S的K = =c(H+)=1.0´10-7,pH=13时HS-、S2-的所占分数相等,则
2 a1 c(H S)
2
c(S2-)×c(H+)
K == =c(H+)=1.0´10-13。再生反应在常温下进行,Fe2+L解离出的Fe2+易与溶液中
a2 c(HS-)
的S2-形成沉淀。若溶液中的c Fe2+ =1.0´10-5mol×L-1,根据
K =c(Fe2+)×c(S2-)=1.0´10-5´c(S2-)=6.0´10-18得到c(S2-)=6.0´10-13mol×L-1,根据
sp
c(S2-)×c2(H+) 6.0´10-13´c2(H+)
cH S=6.0´10-9mol×L-1和K ×K = = =1.0´10-20,得到
2 a1 a2 c(H S) 6.0´10-9
2
c(H+)=1.0´10-8mol×L-1,pH=8,因此为避免有FeS沉淀生成,应控制溶液pH不大于8;故答案为:
H
2
S+H
2
O
ƒ
H
3
O+ +HS-或H
2
S
ƒ
H+ +HS-;1.0´10-7;1.0´10-13;8。
第16页 | 共17页第17页 | 共17页