文档内容
2023 年普通高等学校招生全国统一考试
理科综合能力测试化学部分(全国甲卷)
可能用到的相对原子质量:F 19 Al 27
一、选择题:本题共 13小题,每小题 6分,共 78分。在每小题给出的四个选项中,只有一
项是符合题目要求的。(化学部分为第 7~13题)
1. 化学与生活密切相关,下列说法正确的是
A. 苯甲酸钠可作为食品防腐剂是由于其具有酸性
B. 豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C. SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D. 维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
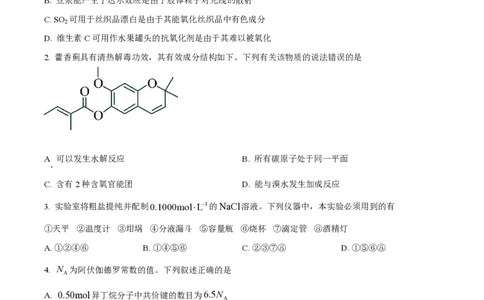
2. 藿香蓟具有清热解毒功效,其有效成分结构如下。下列有关该物质的说法错误的是
A 可以发生水解反应 B. 所有碳原子处于同一平面
.
C. 含有2种含氧官能团 D. 能与溴水发生加成反应
3. 实验室将粗盐提纯并配制0.1000mol×L-1的NaCl溶液。下列仪器中,本实验必须用到的有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A. ①②④⑥ B. ①④⑤⑥ C. ②③⑦⑧ D. ①⑤⑥⑧
4. N 为阿伏伽德罗常数的值。下列叙述正确的是
A
A. 0.50mol异丁烷分子中共价键的数目为6.5N
A
B. 标准状况下,2.24LSO 中电子的数目为4.00N
3 A
C. 1.0LpH =2的H SO 溶液中H+的数目为0.02N
2 4 A
D. 1.0L1.0mol×L-1的Na CO 溶液中CO2-的数目为1.0N
2 3 3 A
5. W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与
其K层电子数相等,WX 是形成酸雨的物质之一。下列说法正确的是
2
第1页 | 共8页A. 原子半径:X>W B. 简单氢化物的沸点:X< Z
C. Y与X可形成离子化合物 D. Z的最高价含氧酸是弱酸
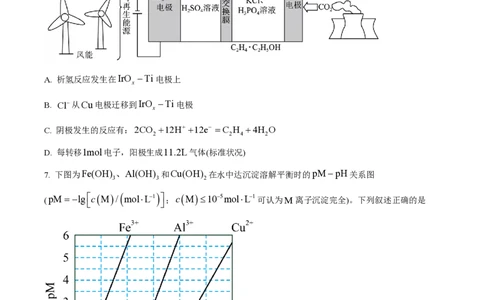
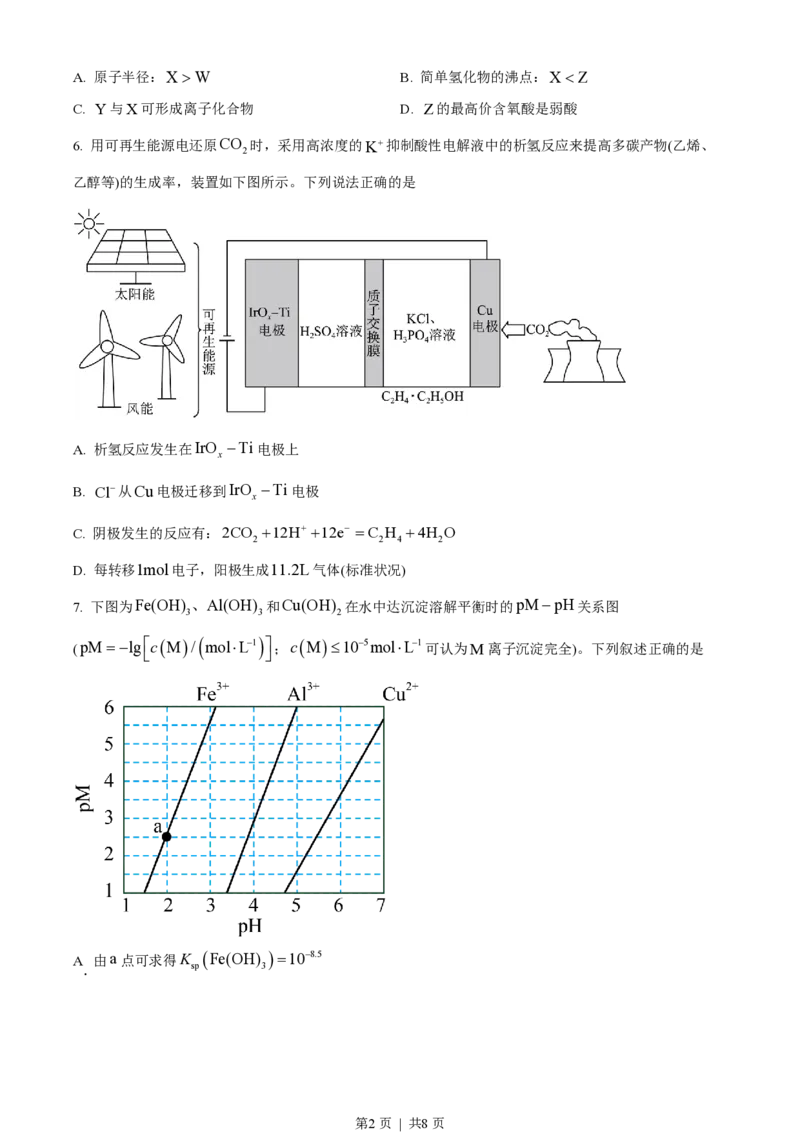
6. 用可再生能源电还原CO 时,采用高浓度的K+抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、
2
乙醇等)的生成率,装置如下图所示。下列说法正确的是
A. 析氢反应发生在IrO -Ti电极上
x
B. Cl-从Cu电极迁移到IrO -Ti电极
x
C. 阴极发生的反应有:2CO +12H+ +12e- =C H +4H O
2 2 4 2
D. 每转移1mol电子,阳极生成11.2L气体(标准状况)
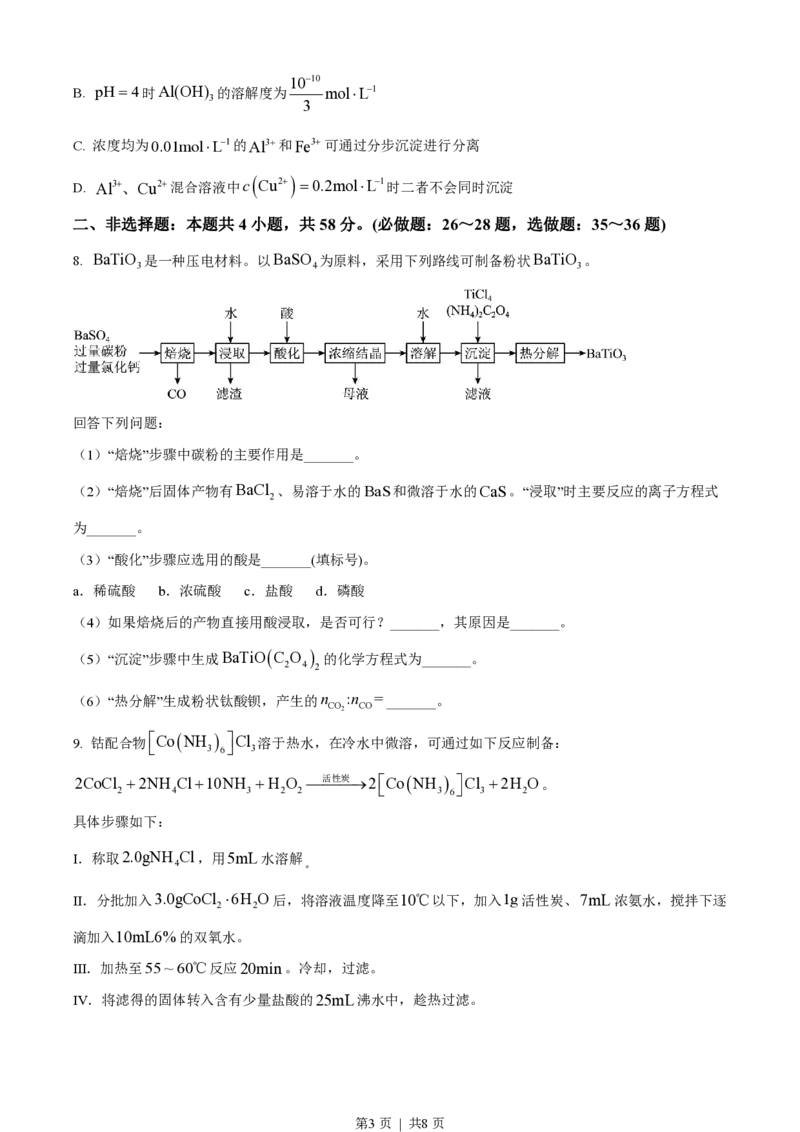
7. 下图为Fe(OH) 、Al(OH) 和Cu(OH) 在水中达沉淀溶解平衡时的pM-pH关系图
3 3 2
(pM = -lgécM/ mol×L-1ù;cM£10-5mol×L-1可认为M离子沉淀完全)。下列叙述正确的是
ë û
A 由a点可求得K Fe(OH) =10-8.5
. sp 3
第2页 | 共8页10-10
B. pH=4时Al(OH) 的溶解度为 mol×L-1
3
3
C. 浓度均为0.01mol×L-1的Al3+和Fe3+可通过分步沉淀进行分离
D. Al3+、Cu2+混合溶液中c Cu2+ =0.2mol×L-1时二者不会同时沉淀
二、非选择题:本题共 4小题,共 58分。(必做题:26~28题,选做题:35~36题)
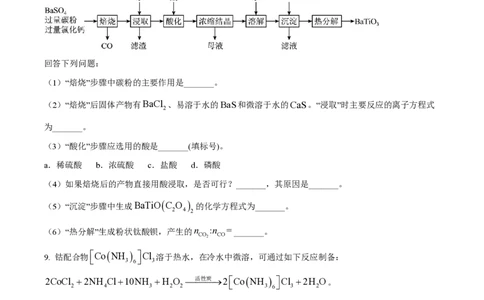
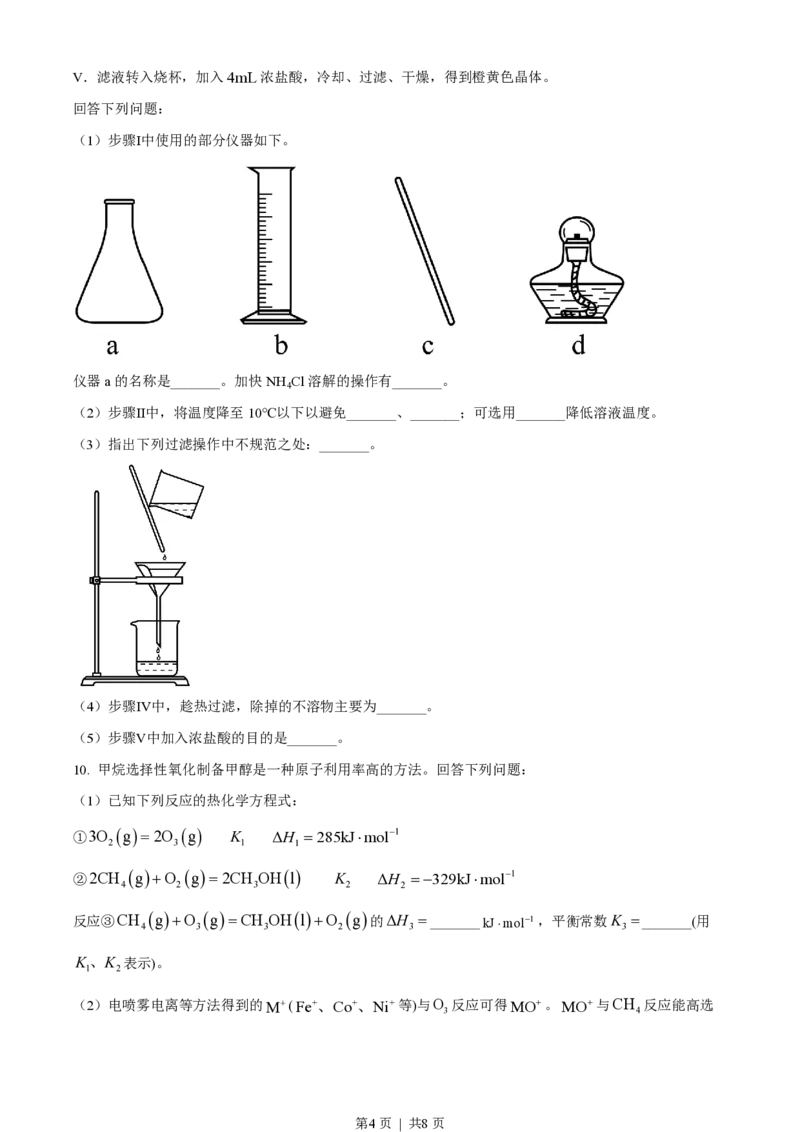
8. BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉状BaTiO 。
3 4 3
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是_______。
(2)“焙烧”后固体产物有BaCl 、易溶于水的BaS和微溶于水的CaS。“浸取”时主要反应的离子方程式
2
为_______。
(3)“酸化”步骤应选用的酸是_______(填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?_______,其原因是_______。
(5)“沉淀”步骤中生成BaTiOC O 的化学方程式为_______。
2 4 2
(6)“热分解”生成粉状钛酸钡,产生的n :n =_______。
CO CO
2
9. 钴配合物é ë CoNH 3 6 ù û Cl 3 溶于热水,在冷水中微溶,可通过如下反应制备:
2CoCl +2NH Cl+10NH +H O ¾活¾性¾炭®2éCoNH ùCl +2H O。
2 4 3 2 2 ë 3 6 û 3 2
具体步骤如下:
Ⅰ.称取2.0gNH Cl,用5mL水溶解
4 。
Ⅱ.分批加入3.0gCoCl ×6H O后,将溶液温度降至10℃以下,加入1g活性炭、7mL浓氨水,搅拌下逐
2 2
滴加入10mL6%的双氧水。
Ⅲ.加热至55~60℃反应20min。冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的25mL沸水中,趁热过滤。
第3页 | 共8页Ⅴ.滤液转入烧杯,加入4mL浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
回答下列问题:
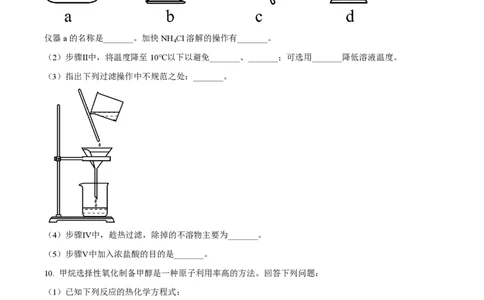
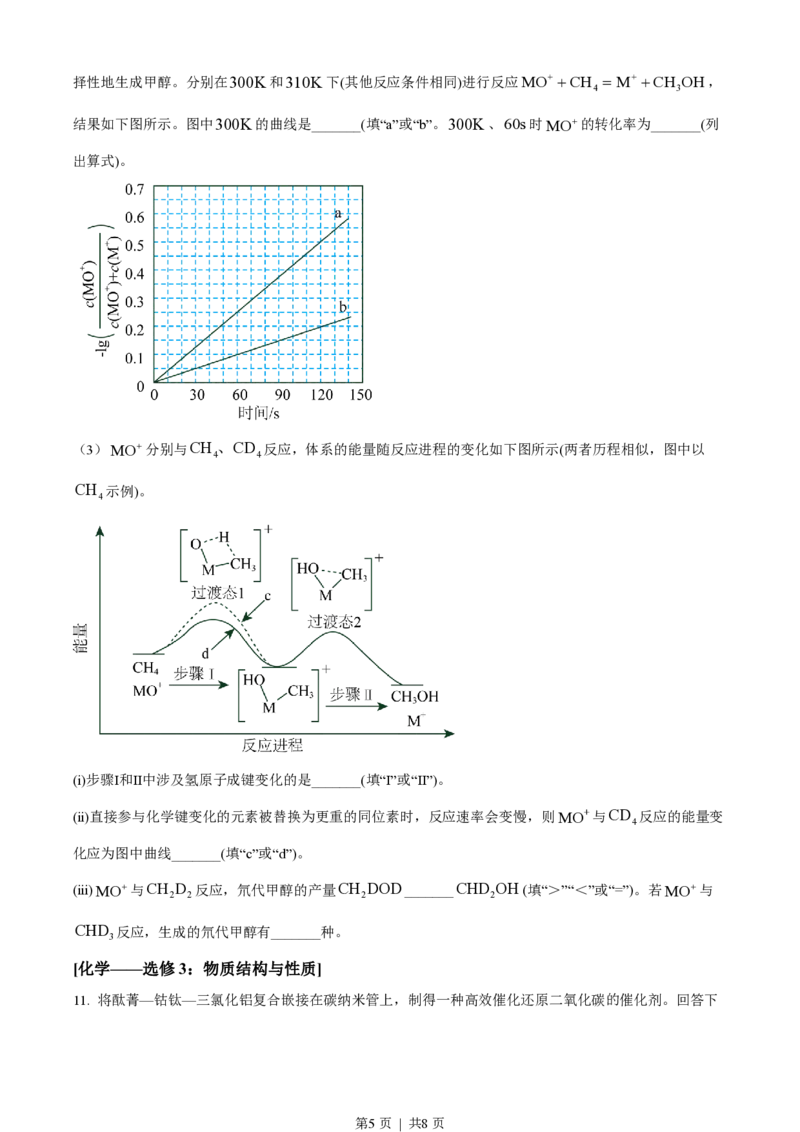
(1)步骤Ⅰ中使用的部分仪器如下。
仪器a的名称是_______。加快NH Cl溶解的操作有_______。
4
(2)步骤Ⅱ中,将温度降至10℃以下以避免_______、_______;可选用_______降低溶液温度。
(3)指出下列过滤操作中不规范之处:_______。
(4)步骤Ⅳ中,趁热过滤,除掉的不溶物主要为_______。
(5)步骤Ⅴ中加入浓盐酸的目的是_______。
10. 甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①3O g=2O g K ΔH =285kJ×mol-1
2 3 1 1
②2CH g+O g=2CH OHl K ΔH =-329kJ×mol-1
4 2 3 2 2
反应③CH g+O g=CH OHl+O g 的ΔH =_______kJ×mol-1,平衡常数K =_______(用
4 3 3 2 3 3
K、K 表示)。
1 2
(2)电喷雾电离等方法得到的M+(Fe+、Co+、Ni+等)与O 反应可得MO+。MO+与CH 反应能高选
3 4
第4页 | 共8页择性地生成甲醇。分别在300K和310K下(其他反应条件相同)进行反应MO+ +CH = M+ +CH OH,
4 3
结果如下图所示。图中300K的曲线是_______(填“a”或“b”。300K、60s时MO+的转化率为_______(列
出算式)。
(3)MO+分别与CH 、CD 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以
4 4
CH 示例)。
4
(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是_______(填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则MO+与CD 反应的能量变
4
化应为图中曲线_______(填“c”或“d”)。
(ⅲ)MO+与CH D 反应,氘代甲醇的产量CH DOD_______CHD OH(填“>”“<”或“=”)。若MO+与
2 2 2 2
CHD 反应,生成的氘代甲醇有_______种。
3
[化学——选修 3:物质结构与性质]
11. 将酞菁—钴钛—三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二氧化碳的催化剂。回答下
第5页 | 共8页列问题:
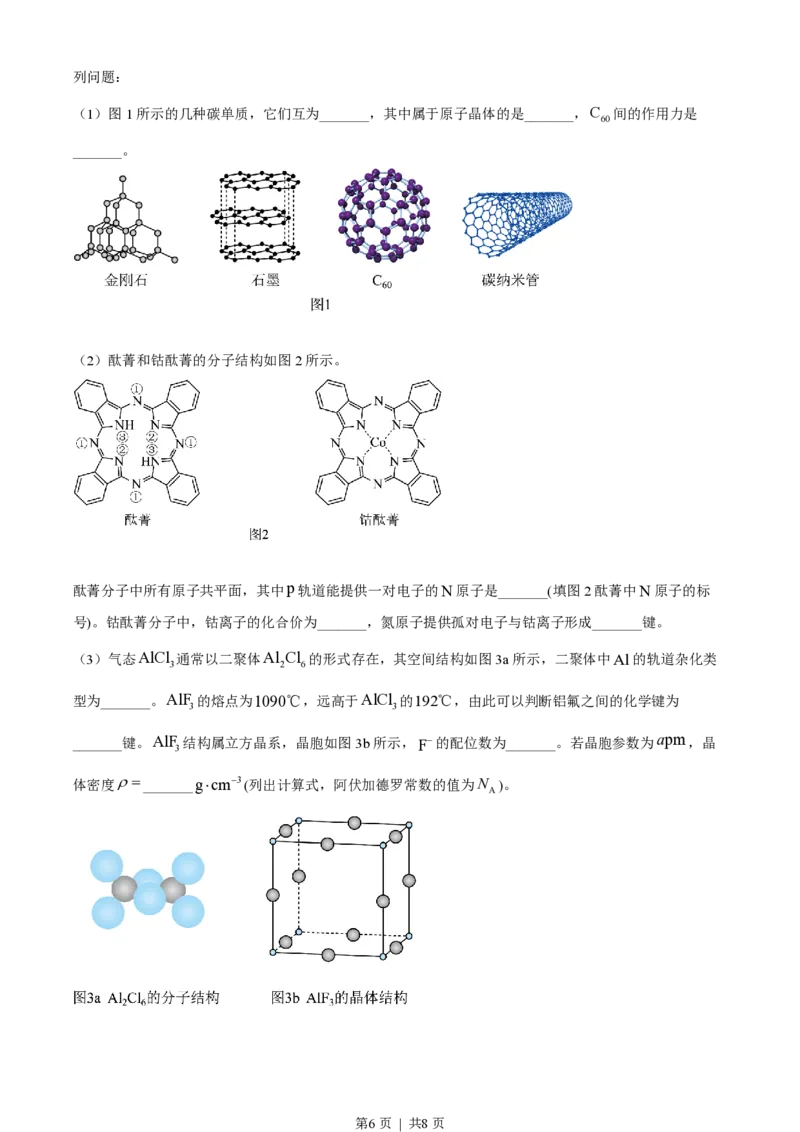
(1)图1所示的几种碳单质,它们互为_______,其中属于原子晶体的是_______,C 间的作用力是
60
_______。
(2)酞菁和钴酞菁的分子结构如图2所示。
酞菁分子中所有原子共平面,其中p轨道能提供一对电子的N原子是_______(填图2酞菁中N原子的标
号)。钴酞菁分子中,钴离子的化合价为_______,氮原子提供孤对电子与钴离子形成_______键。
(3)气态AlCl 通常以二聚体Al Cl 的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类
3 2 6
型为_______。AlF 的熔点为1090℃,远高于AlCl 的192℃,由此可以判断铝氟之间的化学键为
3 3
_______键。AlF 结构属立方晶系,晶胞如图3b所示,F-的配位数为_______。若晶胞参数为 apm ,晶
3
体密度r= _______g×cm-3(列出计算式,阿伏加德罗常数的值为N )。
A
第6页 | 共8页[化学——选修 5:有机化学基础]
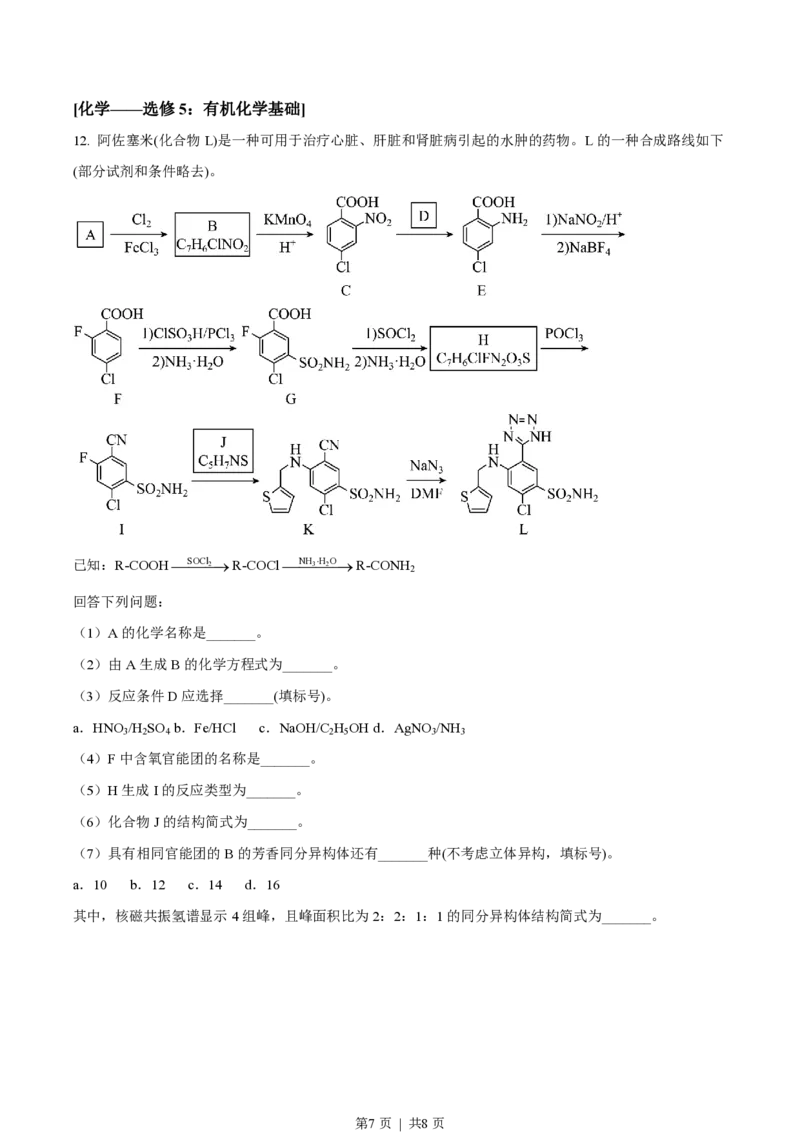
12. 阿佐塞米(化合物L)是一种可用于治疗心脏、肝脏和肾脏病引起的水肿的药物。L的一种合成路线如下
(部分试剂和条件略去)。
已知:R-COOH¾S¾OCl¾2®R-COCl¾N¾H 3¾×H
2
O¾®R-CONH
2
回答下列问题:
(1)A的化学名称是_______。
(2)由A生成B的化学方程式为_______。
(3)反应条件D应选择_______(填标号)。
a.HNO /H SO b.Fe/HCl c.NaOH/C H OH d.AgNO /NH
3 2 4 2 5 3 3
(4)F中含氧官能团的名称是_______。
(5)H生成I的反应类型为_______。
(6)化合物J的结构简式为_______。
(7)具有相同官能团的B的芳香同分异构体还有_______种(不考虑立体异构,填标号)。
a.10 b.12 c.14 d.16
其中,核磁共振氢谱显示4组峰,且峰面积比为2:2:1:1的同分异构体结构简式为_______。
第7页 | 共8页第8页 | 共8页