【2026版三维高考设计高中化学人教版培优讲义word电子版第11讲钠及其化合物
 第11讲 钠及其化合物
第11讲 钠及其化合物
课标要求
1.结合真实情境中的应用实例或通过实验探究,了解钠及其重要化合物的主要性质,了解钠在生产、生活中的应用。
2.结合实例认识钠及其化合物性质的多样性,了解通过化学反应可以探究物质性质、实现物质的转化,认识物质及其转化在自然资源综合利用中的重要价值。

考点一钠单质和其氧化物

(一)钠的性质与用途
1.钠的物理性质
|
颜色状态 |
密度 |
硬度 |
熔点 |
|
银白色固体 |
比水 ,比煤油 |
较小,能用刀切割 |
较低,低于100 ℃ |
2.从钠的原子结构认识钠的化学性质——还原性

(1)与非金属单质(如O2、Cl2)的反应(写出化学方程式)
O2(常温): ,
O2(加热):。
Cl2:。
(2)与水反应
①离子方程式:。
②钠与水反应(滴有酚酞)的实验
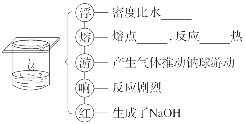
(3)与盐溶液反应

将钠放入盛有下列溶液的小烧杯中,既有气体又有白色沉淀产生的是(填序号)。
①MgSO4溶液 ②BaCl2溶液 ③饱和澄清石灰水 ④Ca(HCO3)2溶液 ⑤CuSO4溶液 ⑥浓盐酸
(4)与乙醇反应:2Na+2C2H5OH 2C2H5ONa+H2↑
2C2H5ONa+H2↑
3.钠的制取、保存与用途
|
制取 |
化学方程式为2NaCl(熔融) |
|
保存 |
通常保存在石蜡油或中 |
|
用途 |
(1)钠钾合金(室温下呈液态)用作核反应堆的传热介质。 (2)作强还原剂,熔融状态冶炼某些金属,如冶炼金属钛:4Na+TiCl4 (3)作电光源,制作高压钠灯 |

判断正误(正确的打“√”,错误的打“×”)。
(1)常温下,钠与氧气反应生成淡黄色固体。()
(2)等质量的钠与O2完全反应,无论生成Na2O,还是Na2O2,转移电子的数目均相同。()
(3)钠表面自然形成的氧化层能够保护内层金属不被空气氧化。()
(4)金属钠具有强还原性,可与TiCl4溶液反应制取金属Ti。()
(二)氧化钠和过氧化钠
1.氧化钠与过氧化钠的比较
|
物质 |
氧化钠(Na2O) |
过氧化钠(Na2O2) |
|
颜色状态 |
白色固体 |
色固体 |
|
类别 |
碱性氧化物 |
过氧化物 |
|
氧元素化合价 |
||
|
阴、阳离子个数比 |
||
|
与水反应 |
Na2O+H2O |
|
|
与CO2反应 |
Na2O+CO2 |
|
|
稳定性 |
不稳定:2Na2O+O2 |
稳定 |
|
主要用途 |
可制烧碱 |
作漂白剂、消毒剂、供氧剂 |
2.过氧化钠的强氧化性与还原性
(1)实例
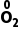
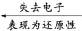 2
2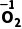
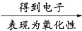
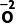 H
H
①Na2O2遇到还原剂表现极强的氧化性。
如与还原剂SO2、NO、Fe2+、S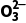 、S2-、H2S反应,又如使品红溶液褪色,使酚酞溶液先变红后褪色。
、S2-、H2S反应,又如使品红溶液褪色,使酚酞溶液先变红后褪色。
②Na2O2遇到强氧化剂表现还原性。如强氧化剂KMnO4等。
③Na2O2遇到最高价氧化物如SO3、CO2、H2O时,既表现氧化性又表现还原性。
(2)其他过氧化物的结构与性质
与过氧化钠相似,其他过氧化物也具有强氧化性、还原性等,原因是这些物质中都含有过氧键(—O—O—)。

|
一 |
钠的性质 |
1.下列关于钠的实验现象的叙述不正确的是()
|
选项 |
实验操作 |
实验现象 |
|
A |
切开一小块钠,观察切面颜色的变化 |
钠切面颜色变暗,最后呈淡黄色 |
|
B |
把一小块钠投入CuSO4溶液中 |
钠熔化成闪亮的小球,在液面上四处游动,发出“嘶嘶”的响声,产生蓝色沉淀 |
|
C |
把一小块钠投入滴有紫色石蕊溶液的冷水中 |
钠熔化成闪亮的小球,在液面上四处游动,发出“嘶嘶”的响声,反应后溶液变蓝 |
|
D |
把一小块钠迅速投入热坩埚中,继续加热坩埚片刻 |
钠熔成小球,然后剧烈燃烧,发出黄色火焰,生成淡黄色固体 |

钠露置于空气中发生的一系列变化
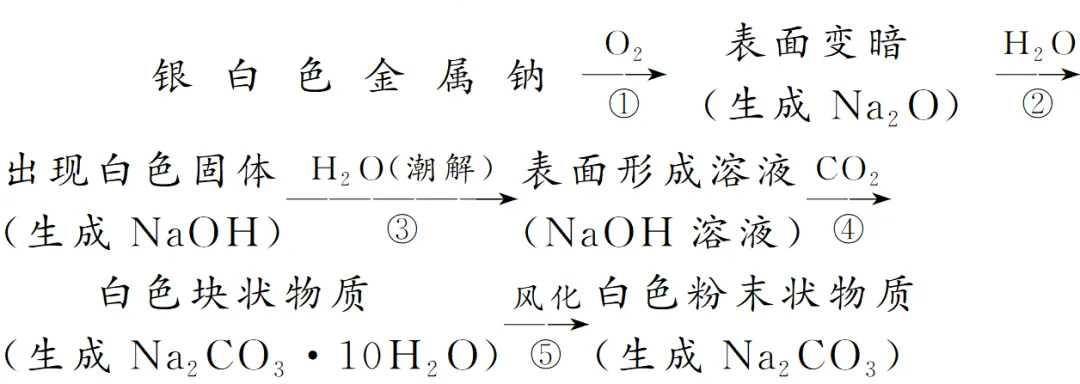
|
二 |
钠的氧化物的性质 |
2.下列关于钠的氧化物的说法正确的是()
A.Na2O2是白色固体,与冷水作用放出氧气,生成氢氧化钠
B.在Na2O2与CO2的反应中,氧化剂是Na2O2,还原剂是CO2
C.Na2O2和H2O反应时,生成0.1 mol O2转移的电子数为0.2NA
D.Na2O2能与水反应,生成NaOH,所以Na2O2是碱性氧化物
3.Na2O2具有强氧化性,可用作漂白剂。下列有关Na2O2说法正确的是()
A.Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B.过氧化钠沾到红色鲜花上,鲜花无变化
C.CO2通过Na2O2粉末后固体物质增重
D.探究金属钠在氧气中燃烧所得固体粉末的成分,可取固体粉末,加入2~3 mL蒸馏水。若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2

(1)Na2O2与CO2、H2O反应,生成1molO2,转移2mol电子。
(2)过氧化钠吸收二氧化碳、水时,Na2O2增重的质量,等于吸收与CO2、H2O等物质的量的CO、H2的质量。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风