【2026版高考一轮复习高中化学讲练测试培优版课后作业word课时作业53 定性、定量探究型综合实验
|
|
班级 姓名 考号 |
课时作业53 定性、定量探究型综合实验
(时间:30分钟 满分:90分)
非选择题(共5小题,除标注外,每空2分,共90分)
1.(16分)(2024·四川成都三模)某小组同学为探究FeSO4的性质设计了如下实验。
Ⅰ.新配制0.1 mol·L-1FeSO4溶液450 mL:
(1)配制0.1 mol·L-1FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)g,其部分实验操作示意图如图,正确的步骤顺序为(填序号)。
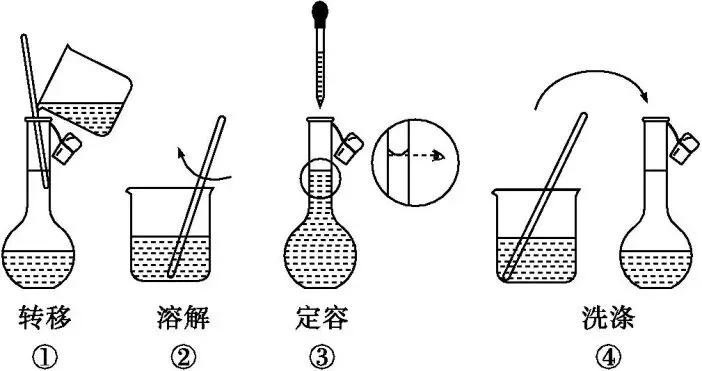
Ⅱ.取2 mL新配制的FeSO4溶液,按如图进行实验并观察到如下现象:
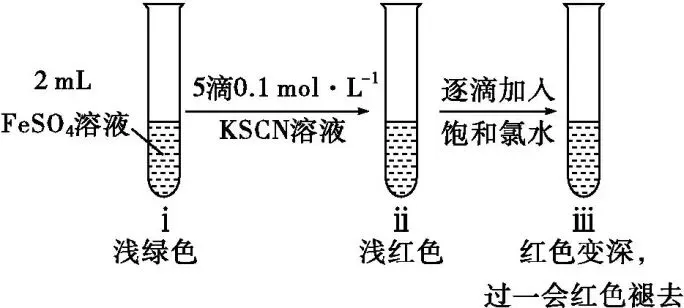
(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在(填离子符号)。
(3)ⅲ中溶液红色变深的主要原因是(用离子方程式表示)。
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN–具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
|
项目 |
猜想 |
|
甲 |
+3价铁元素又被还原成+2价铁元素 |
|
乙 |
(4)乙同学的猜想是。
为验证甲、乙两位同学的猜想,设计如下实验:将褪色后的溶液分为两等份,一份滴加KSCN溶液,呈红色;另一份加入氯化铁溶液,无明显现象,则(填“甲”或“乙”)同学猜想是正确的。
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
①丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
②丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m= ,FeSO4固体在空气氛围中加热时反应的化学方程式为。
2.(20分)碱式碳酸钴[Cox(OH)y(CO3)2]可用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示装置进行实验。
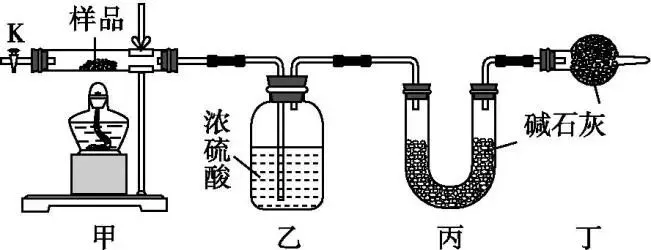
(1)请完成下列实验步骤:
①称取3.65 g样品置于硬质玻璃管内,分别称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检查装置气密性;
③加热甲装置中硬质玻璃管,当乙装置中(填实验现象),停止加热;
④打开活塞K,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是。
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的
(填字母)连接在(填装置连接位置)。
AB

CD
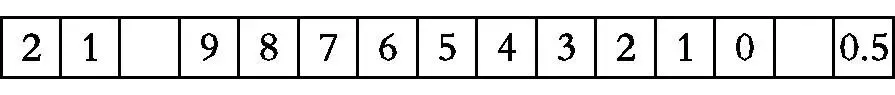
(4)若按正确装置进行实验,测得如下数据:
|
项目 |
乙装置的质量/g |
丙装置的质量/g |
|
加热前 |
80.00 |
62.00 |
|
加热后 |
80.36 |
62.88 |
则该碱式碳酸钴的化学式为。
(5)有人认为用如图所示装置进行两次实验也可以确定碱式碳酸钴的组成。
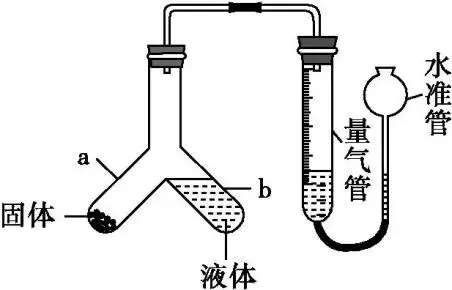
实验Ⅰ:称取一定质量的样品置于Y形管a处,加入一定体积一定物质的量浓度的足量稀硫酸于Y形管b处,量气管中盛放饱和碳酸氢钠溶液,而不用蒸馏水,其原因是
,然后通过(填操作),引发反应,测定产生的CO2的体积(假设实验条件是在室温下)。
实验Ⅱ:将实验Ⅰ中反应后的液体和足量的锌粒分别放置在另一个Y形管的a、b中,量气管中盛装蒸馏水,此时引发反应的方式与实验Ⅰ(填“相同”“不同”或“可相同也可不同”),然后测定产生H2的体积(假设实验条件是在室温下)。
两次实验结束时,读数前,先 ,再调节量气管和水准管液面持平,然后平视读数;下列实验操作有可能会使y的值偏大的是(填字母)。
A.实验Ⅰ读数时量气管液面高于水准管液面
B.实验Ⅱ实验结束时,迅速调整两侧液面持平,立即读数
C.实验Ⅱ引发反应时将稀硫酸向锌粒倾斜
3.(14分)(2025·山西大同模拟)磷化铝(AlP)通常可作为一种广谱性熏蒸杀虫剂,粮食仓储常用磷化铝熏蒸杀虫,某化学兴趣小组的同学用下述方法测定粮食中残留磷化铝的含量。C
通过网盘分享的文件:学生用书Word文档等2个文件
链接: https://pan.baidu.com/s/14v2Ty29Put0VDhBsHMMTcw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风





