
人工智能正在改变生物医药行业。过去,AI在制药领域更多是辅助性的计算工具,现在它已经直接参与到药物研发的核心工作中。根据最新统计数据,全球AI制药市场规模从2021年的7.9亿美元增长到2024年的18.2亿美元,预计2026年将达到29.9亿美元。中国市场同样增长迅速,2020年市场规模只有0.8亿元,2021年增速就达到了100%,到2025年已经突破6亿元。
本次梳理基于华创证券最新调研,围绕AI制药行业的发展现状展开,分析中美两国的政策动向、技术进展、市场需求以及产业链分工,并列举了英矽智能、晶泰科技等典型公司的业务进展。

一、中美政策持续加码,为AI制药铺平道路
AI制药行业的发展离不开政府的支持。中美两国都出台了一系列政策,推动人工智能在药物研发领域的应用。
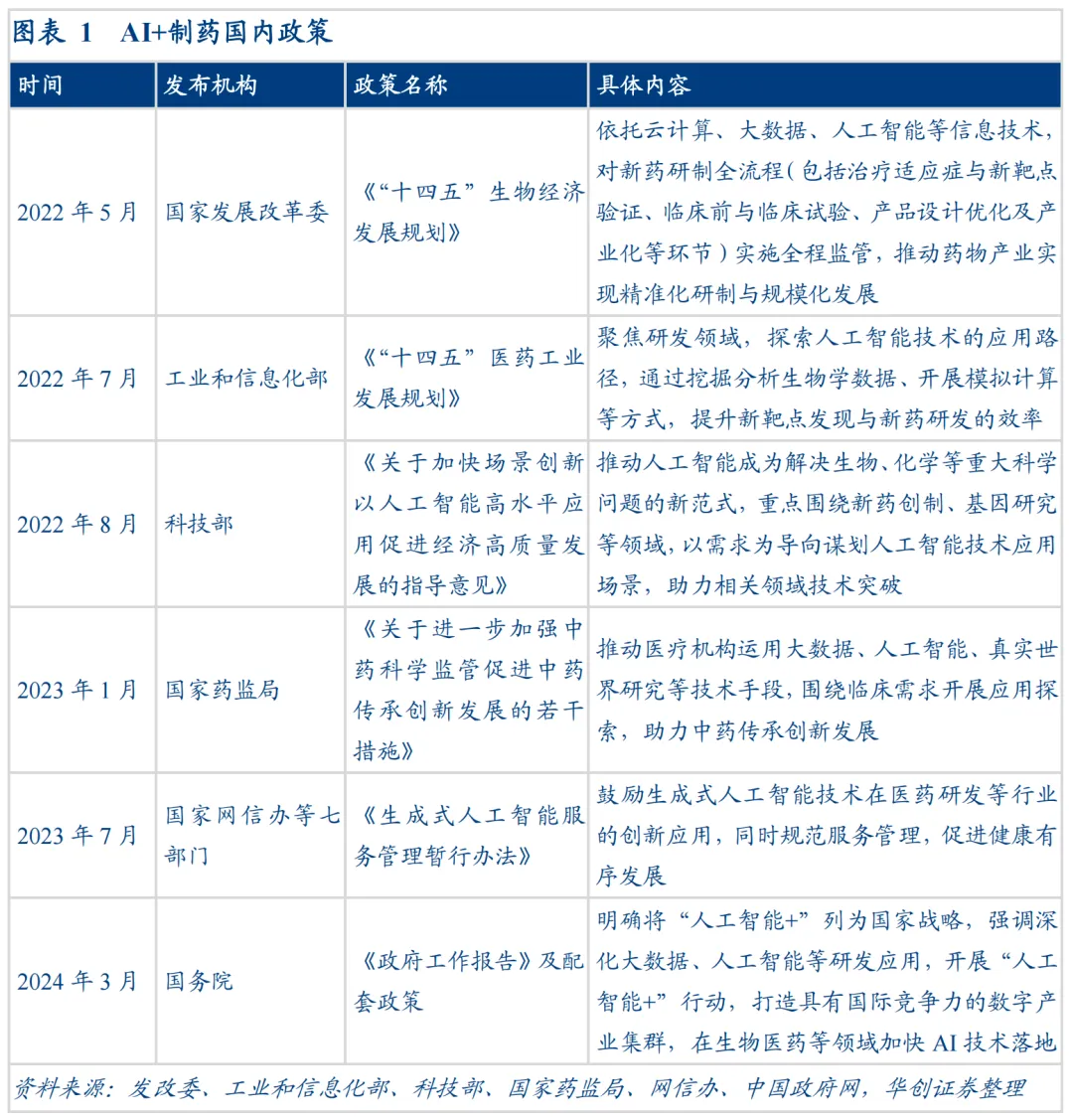
中国在政策上做了系统性的布局。2022年5月,国家发改委发布《“十四五”生物经济发展规划》,明确提出要依托云计算、大数据和人工智能技术,对新药研制的全过程实施监管,推动药物产业实现精准化研发和规模化生产。同年7月,工信部在《“十四五”医药工业发展规划》中提出,要探索人工智能的应用路径,通过挖掘生物学数据和模拟计算,提升新靶点发现和新药研发的效率。8月,科技部发布指导意见,要求推动人工智能用于解决生物、化学等重大科学问题,重点围绕新药创制等领域,以需求为导向谋划技术应用场景。到了2024年3月,“人工智能+”被写入政府工作报告,列为国家战略,生物医药领域被点名要求加快技术落地。
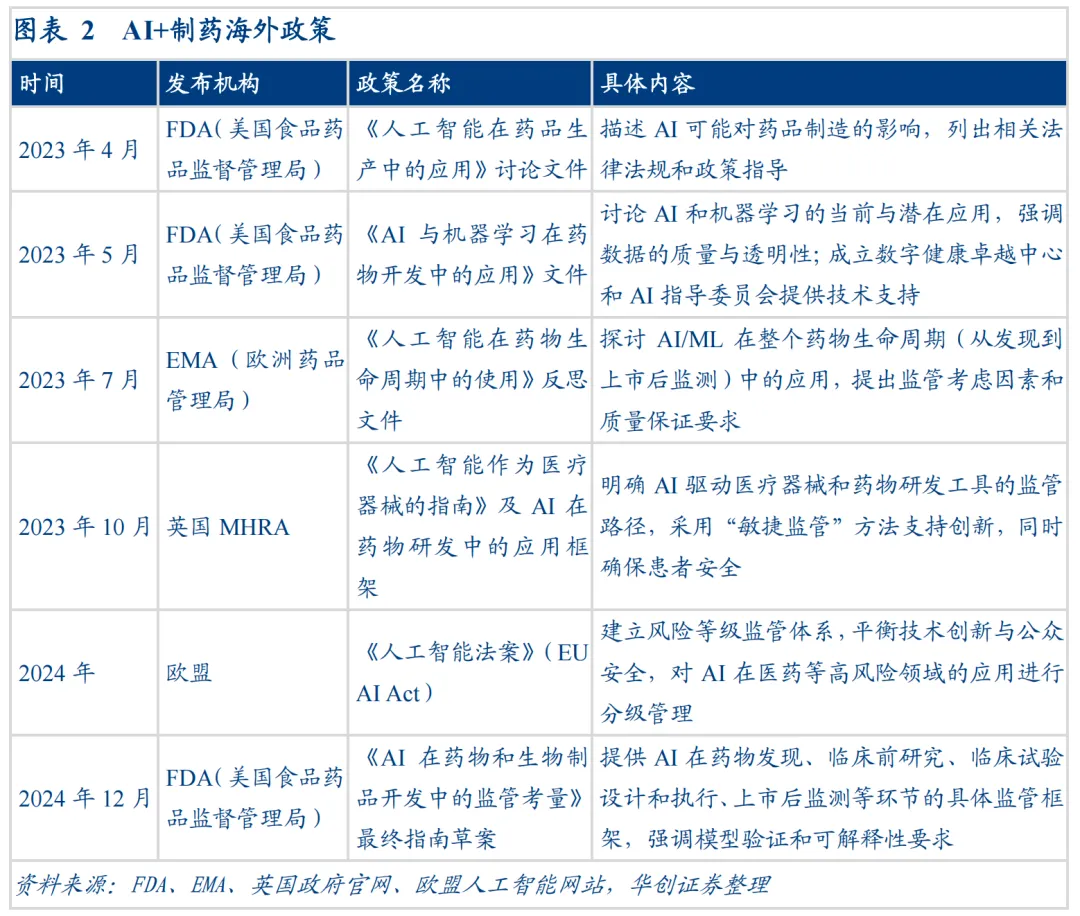
美国方面,食品药品监督管理局(FDA)在2023年密集发布了一系列监管文件。3月发布了《人工智能在药品生产中的应用》讨论文件,梳理了AI技术对药品制造环节的影响。5月又发布了《AI与机器学习在药物开发中的应用》文件,将讨论范围扩展到药物研发全链条,强调数据质量与算法透明性。FDA还专门设立了数字健康卓越中心和AI指导委员会,为行业提供技术支持。英国和欧盟也采取了类似措施,英国药品与健康产品管理局(MHRA)采用“敏捷监管”策略,欧盟则通过《人工智能法案》建立风险等级监管体系。这些全球范围内的监管框架,为AI制药的商业化应用提供了制度保障。
二、技术突破
AI制药的技术演进经历了从单一算法到多模态融合的过程。早期主要依靠深度学习在公开数据库中挖掘规律,现在则通过整合基因组学、蛋白质组学、代谢组学等数据与临床信息,构建更全面的疾病认知模型。

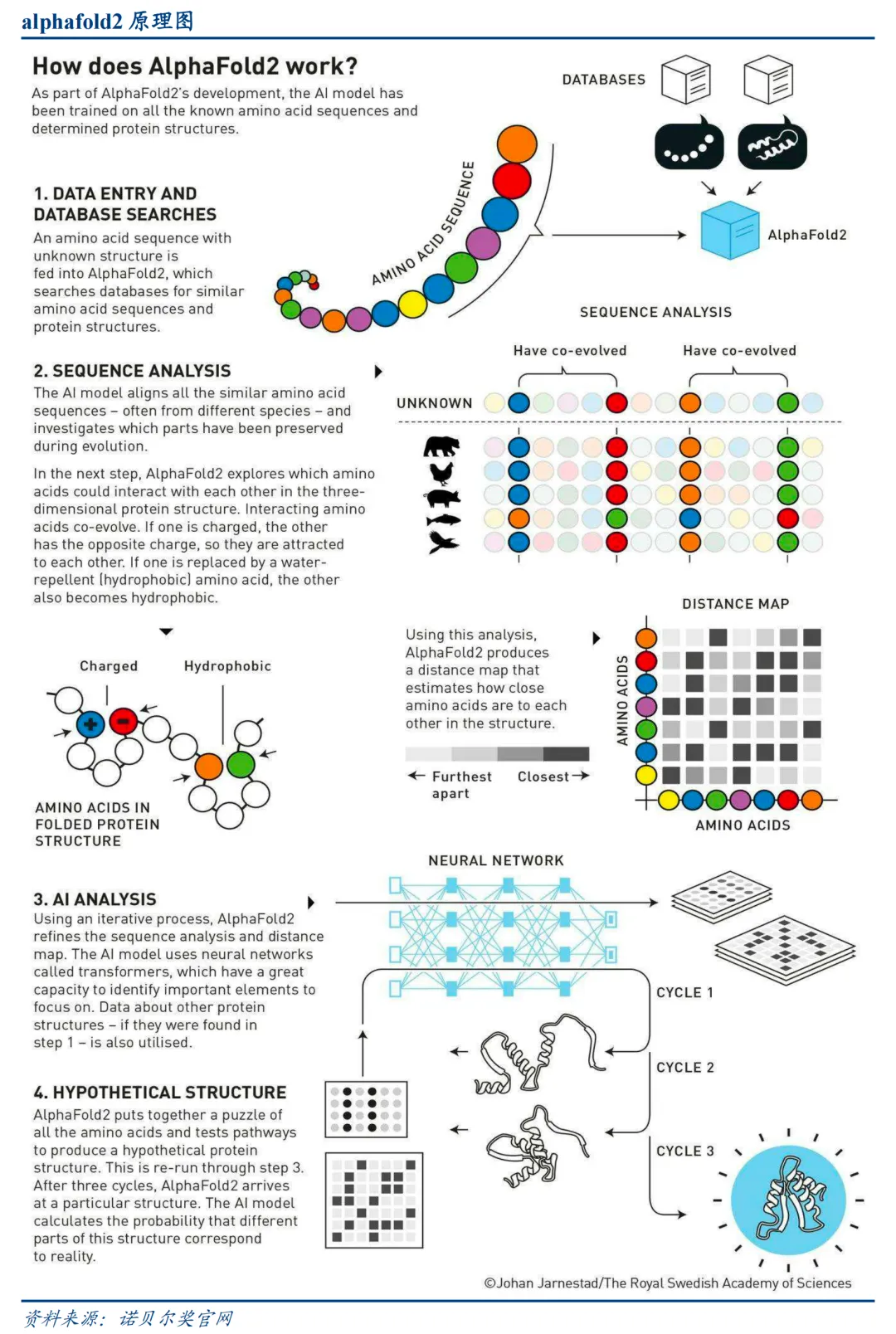
最关键的突破来自DeepMind。2020年,DeepMind推出的AlphaFold2在第14届CASP竞赛中实现了原子级精度的蛋白质结构预测,将原本需要数月甚至数年、花费数百万美元的结构解析过程压缩到了几个小时。2024年发布的AlphaFold3更进一步,引入了扩散模型架构,将预测能力扩展到蛋白质与配体、抗体与抗原等复合物的相互作用,为基于结构的药物设计提供了精细的底层工具。
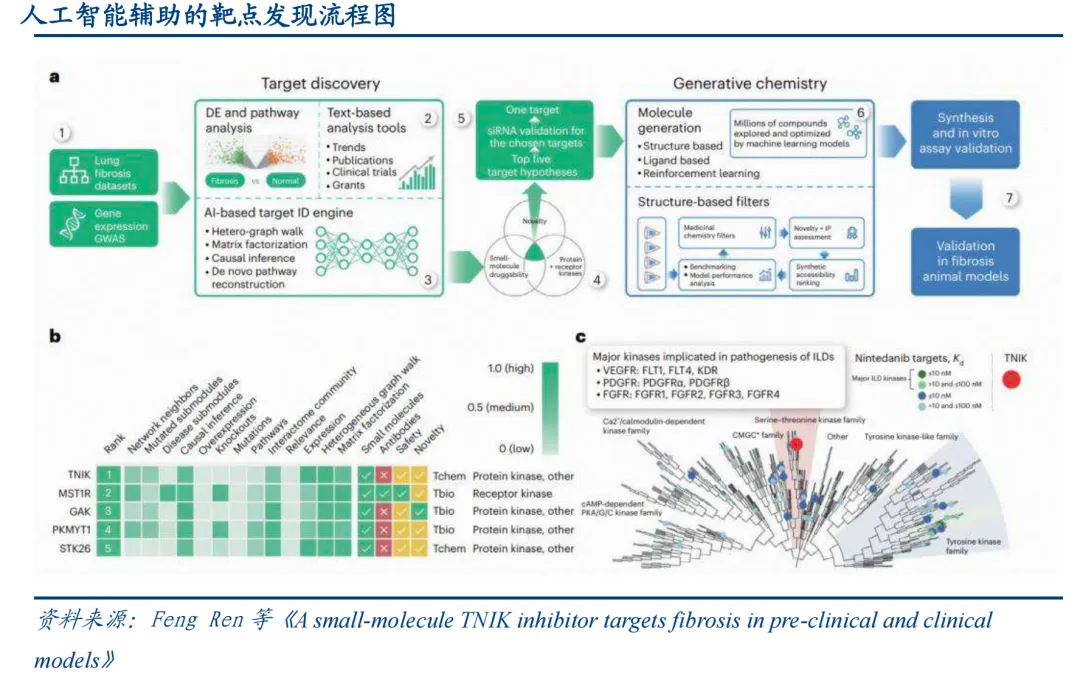
生成式AI在分子设计领域也取得了很大进展。2016年,英矽智能率先将生成对抗网络应用于靶点发现。2019年,其开发的生成式张量强化学习模型GENTRL仅用21天就完成了DDR1激酶抑制剂分子的设计、合成与体外验证,而传统研发周期通常需要一年多。基于Transformer架构的Pharma.AI平台更是将“从靶点发现到临床前候选药物确定”的全流程压缩到了18个月,传统方法平均需要4到6年。这种从“读分子”到“写分子”的转变,意味着AI不再只是分析现有数据,而是能够主动设计全新的药物分子。
三、药企面临研发困境,AI成为破局关键
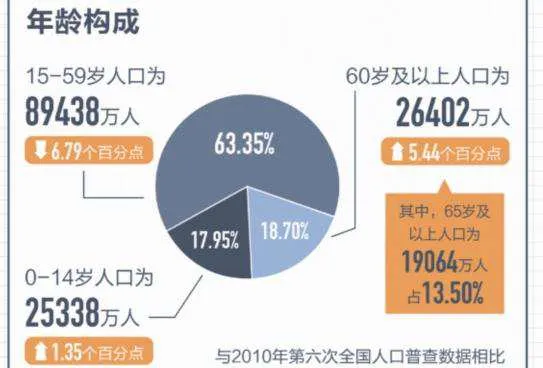
全球人口老龄化正在加速。根据联合国的预测,到2050年,全球60岁以上老年人口将增至21亿,占总人口的22%。中国第七次人口普查数据显示,60岁及以上人口占比已达到18.7%。老龄化直接推高了慢性病、恶性肿瘤、心血管疾病等老年高发疾病的患病率,制药企业需要不断推出新药来满足市场需求。
但传统新药研发面临很大的困难。业内有一个说法叫“双十定律”,意思是研发一款新药平均需要10年时间、投入10亿美元。更麻烦的是,研发回报率在持续下降。根据德勤的报告,制药行业的研发投资回报率从2010年的10.1%一路走低,虽然在2024年有所回升至4.1%左右,但仍远低于历史高点。同时,研发成本还在不断上涨,大约每九年翻一倍,这被称为“倒摩尔定律”。
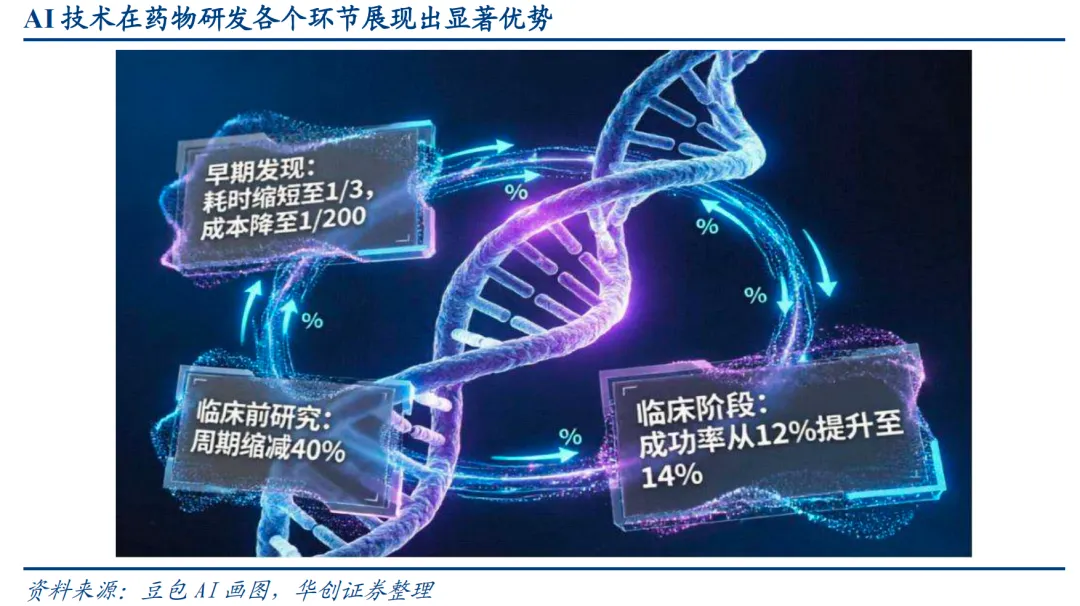
AI技术为这个困境提供了解决方案。根据英伟达公开的数据,AI在药物研发各环节都能显著缩短时间、降低成本。在早期发现阶段,耗时可以减少到原来的三分之一,成本降到原来的二百分之一。药物发现与临床前研究的整体周期可以缩短近40%。根据TechEmergence的数据,AI还能将新药研发的成功率从12%提升到约14%。这些实实在在的效率提升,正是各大药企积极拥抱AI的原因。
四、产业链分工明确,各环节参与者各有所长
AI制药产业链已经形成了比较清晰的分工体系。上游提供数据资源和算力基础设施,中游进行算法开发和药物发现,下游由药企完成临床验证和商业化。
上游的核心是数据。药物化学数据库(如ChEMBL、PubChem)、蛋白质结构数据库(如PDB)、多组学数据(基因组、蛋白质组等)以及临床数据(电子病历、临床试验结果),共同构成了训练AI模型的“原料”。但数据环节存在质量参差不齐、标准不统一、数据孤岛等问题。为此,一些头部企业开始采用“联邦学习”和“隐私计算”技术,允许多方在不共享原始数据的情况下联合训练模型。还有公司自建智能实验室,通过自动化实验产生高质量专有数据,逐步摆脱对公共数据集的依赖。算力方面,云计算平台的弹性扩容能力和GPU、TPU等专用芯片的算力提升,已经为分子动力学模拟、蛋白质结构预测等计算密集型任务提供了充足的支撑。

中游是药物研发的核心环节。科技巨头如谷歌、英伟达、亚马逊等,凭借算力和算法优势,成为底层技术标准的定义者。谷歌的AlphaFold系列以开源策略建立了事实上的行业标准。英伟达通过“芯片+软件+生态”三位一体的战略,其BioNeMo平台提供从分子生成、蛋白质设计到药物筛选的端到端服务。AI原生公司则分为两种模式。一种是AI+Biotech模式,代表公司有英矽智能、Recursion、Exscientia等,它们利用自研AI平台发现新靶点并设计分子,自建管线推进到临床阶段,最终通过药物上市或权益转让实现价值。另一种是AI+CRO/平台模式,代表公司有晶泰科技、Schrödinger、BenevolentAI等,它们不直接持有药物管线,而是向药企提供AI驱动的药物发现服务,按里程碑或服务费收费。

下游是传统药企和CXO企业。罗氏、诺华、阿斯利康等跨国药企早在2010年代就建立了内部AI团队,通过合作或收购的方式引入AI技术。碧柔罗氏旗下的基因泰克与Recursion合作,利用后者的技术在神经科学和肿瘤领域进行药物发现,还收购了拥有生成式蛋白质设计算法的初创公司Prescient Design。阿斯利康与BenevolentAI合作验证了7个新靶点并推进到临床阶段。诺华与微软合作,增强AI能力以加速药物发现。在国内,药明康德、康龙化成等CXO企业也在加速将AI工具整合到现有的药物发现服务链条中。
五、两家代表性公司的业务进展
英矽智能成立于2014年,2019年落地上海浦东,是一家由生成式AI驱动的临床阶段生物医药公司。其核心是自研的端到端平台Pharma.AI,该平台曾在18个月内完成“靶点发现→分子设计→临床前候选化合物”的全流程,如果是传统方法,则平均需要4到6年。目前,公司已建立30多条内部管线,覆盖肿瘤、免疫、纤维化、代谢等疾病领域,其中10个分子已获得临床试验许可。进展最快的抗特发性肺纤维化候选药Rentosertib(ISM001-055)已完成中国IIa期临床并取得积极数据,成为全球首个由AI独立完成靶点发现与分子设计并进入临床验证的案例。

2026年3月,英矽智能与礼来达成授权及药物研发合作。根据协议,英矽智能将获得1.15亿美元首付款,并在后续达成开发、监管及商业化里程碑后获得进一步付款,交易总价值最高可达约27.5亿美元,此外还将获得基于未来销售额的分级特许权使用费。这笔交易充分证明了大型药企对AI发现新型疗法能力的认可。
晶泰科技(晶泰控股)是另一家有代表性的公司。它融合量子物理、人工智能与云计算技术,构建了“高通量实验—高质量数据—高智能模型”的闭环。其XFEP平台在效率上实现了大幅提升,能够在无参考化合物的情况下,28天内利用主动学习成功预测关键药效团,实现特大化合物库的快速筛选。公司业务覆盖小分子、大分子药物及材料研发,为全球300多家客户提供服务。

以上,仅供参考。
扫码加入知识星球获取更多行业报告
声明:本文仅为行业研究与学术交流之用,不构成任何投资建议或操作指引。市场风险客观存在,应基于独立判断与充分调研作出决策。
点击“阅读原文”,下载所有资料
 夜雨聆风
夜雨聆风