本次我们挑选了6篇近期发表在胸部肿瘤与医学AI交叉领域的文献。这些研究涵盖了病理微环境图谱、无创生物标志物、大体标本图像识别以及真实世界工作流评估。探讨其背后的建模思路及可复现的科研方法论。
文献介绍
这6篇文献展示了研究者如何将具体的临床痛点抽象为可计算的科学问题:
文献1 (CCR): ADC target profiling in NSCLC

切入点:ADC药物靶点(TROP-2、cMET)的常规免疫组化(IHC)评估存在主观性。研究将其转化为基于全切片或组织芯片(TMA)的AI连续评分(H-score)问题,以实现定量的空间异质性分析。
文献2 (Lancet Digit Health): SuRImage for clinical stage IA LUAD

切入点:术中冰冻切片耗时较长。研究将这一流程瓶颈抽象为自然光条件下的图像分类任务,利用智能手机拍摄大体标本,预测IA期腺癌的浸润程度。
文献3 (NPJ Digit Med): Label-free pathological subtyping

切入点:常规病理制片和染色消耗时间和组织样本。研究利用自发荧光强度和荧光寿命成像(FLIM),将其转化为免染色的深度学习子型分类(腺癌 vs 鳞癌)及虚拟IHC生成任务。
文献4 (JARE): VOCs for differential diagnosis

切入点:低剂量CT(LDCT)假阳性率较高。研究切入无创检测,通过气相色谱-质谱(GC-MS)对呼出气体中的挥发性有机化合物(VOCs)进行特征筛选,构建良恶性与严重程度预测模型。
文献5 (JAMA Netw Open): Multimodal Assessment of Biological Age

切入点:早期NSCLC老年患者在接受SBRT放疗前,临床难以客观评估其实际生理负荷。研究将“衰老”抽象为面部深度学习年龄与肺功能年龄,验证其作为生存期预测指标的独立性。
文献6 (Nature Medicine): LungIMPACT RCT

切入点:AI阅片在理论上能加速诊断,但缺乏系统层面的证据。研究跳出算法准确率本身,将其设定为真实世界随机对照试验(RCT),检验“AI优先排队算法”是否能实质性缩短CT扫描和确诊的时间。
选题技巧
1. ADC 疗效评估:从 "肉眼定性" 到 "空间定量"
精准治疗时代,抗体偶联药物(ADC)的效果完全取决于靶点表达的精准度。但传统免疫组化(IHC)全靠医生在显微镜下人工判读,不仅主观性强,更无法量化亚细胞定位和肿瘤的空间异质性。研究者用 RudolfV 等病理基础模型,把这个痛点转化为图像分割与特征提取问题,建立了能独立量化细胞膜和细胞质表达的评分体系,实现了 TROP-2 和 cMET 表达的空间全景映射。这种方法把传统定性的病理观察变成了连续的定量数据,为研究靶点表达与肿瘤微环境的相互作用打下了计算基础。
2. 肺癌术中决策:跳过冰冻切片,直接看大体标本
IA 期肺腺癌的手术方式(亚肺叶切除 vs 肺叶切除)完全由术中病理决定。但传统冰冻切片不仅耗时长,还会因为制样伪影和取材局限,对 IASLC 最新的细分级系统(尤其是浸润程度和微乳头 / 实体亚型比例)判断准确率很低。SuRImage 模型另辟蹊径,把术中决策这个最紧迫的限速步骤,变成了基于智能手机自然光拍照的层级分类任务,能一次性完成浸润性识别、MIA/AIS/IAC 诊断和 IAC 细分级。它完全绕开了冰冻切片的物理延迟,尝试用宏观大体形态直接推断微观侵袭性。
3. 病理亚型鉴别:零组织消耗的 "数字染色"
非小细胞肺癌的精准治疗,第一步就是明确腺癌 / 鳞癌分型,再做后续基因检测。但多重 IHC 染色会消耗宝贵的组织样本,经常导致剩下的组织不够做分子分型。研究者用无标记自发荧光寿命成像(FLIM)结合生成对抗网络(GAN),把 "物理染色" 变成了 "虚拟染色" 任务。通过计算生成 TTF-1 和 p40 的表达图像,实现了不消耗任何组织的亚型鉴别。这相当于把依赖化学试剂的耗材过程,变成了依赖算力的信息提取过程。
4. 早期癌症筛查:多模态融合的新维度
低剂量 CT(LDCT)筛查肺癌最大的问题是假阳性率太高,导致很多不必要的侵入性检查。研究者从代谢角度切入,把肺癌早期筛查、良恶性鉴别甚至驱动基因突变预测,转化为基于气相色谱 - 质谱(GC-MS)的挥发性有机物(VOCs)分类问题。同时,基于血液 cfDNA 甲基化的多癌种早期检测(MCED)工具,也在 50 多种癌症中展现了极高的特异性。这两条技术路线内在逻辑高度一致,都在为影像学筛查提供分子层面的补充证据。
5. 预后分层:用非传统数据评估生理年龄
接受立体定向放疗(SBRT)的早期肺癌患者大多是高龄老人,且常伴有多种基础疾病。单纯的 "时序年龄" 根本无法准确反映患者的真实生理状态和治疗耐受能力。研究者把预后风险分层转化为多模态生物学年龄估计问题:用深度学习从面部照片提取 "面部年龄",结合肺功能测试得到的 "肺部年龄",构建了一个独立于传统临床变量的生存预测因子。这种思路大大拓宽了预后评估的数据维度。
6. 系统效能评估:从 "算法准确率" 到 "临床真实价值"
最后这个研究提出的问题非常尖锐:很多 AI 模型在回顾性阅片中速度惊人,但它到底能不能真正缩短患者的确诊时间?LungIMPACT 试验没有再去比拼算法准确率,而是用前瞻性随机对照试验(RCT)的金标准,去评估 "AI 优先处理胸部 X 线报告" 这个简单的流程改变,是否能切实缩短患者从检查到 CT 确诊的物理时间。它直面医疗工作流的系统性约束,探讨了技术干预在真实世界中到底能产生多大的实际价值。
多模态数据与金标准演进
在数字病理领域,除了常规的H&E和IHC切片,多重免疫荧光(mIF)正成为刻画复杂肿瘤微环境(TME)细胞表型的重要模态。以近期针对NSCLC的双中心队列研究为例,其模型训练依托了1,142例标本,并由6名资深病理医生进行独立的细胞级标注与H-score评估。这种高密度的专家标注不仅保证了“金标准”的可靠性,也为底层算法模型提供了极高精度的梯度反馈。
无标记成像技术则进一步打开了光学特征的应用空间。例如,自发荧光寿命成像(FLIM)无需外源性染料,而是直接测量组织内NADH、FAD等内源性荧光团的纳秒级衰减寿命。相比传统的荧光强度测量,FLIM对组织的代谢状态更敏感,能捕捉到更深层的微环境差异。在构建数据集时,研究者巧妙地将同一张切片退色后重新进行标准IHC染色作为真实标签,结合病理医生的盲法评估,真实建立了从光物理信号到分子病理的对应关系。此外,借助扩散模型(Diffusion models)等生成式技术,从无标记特征到标准病理图像的虚拟染色和超分重建保真度正得到进一步突破。
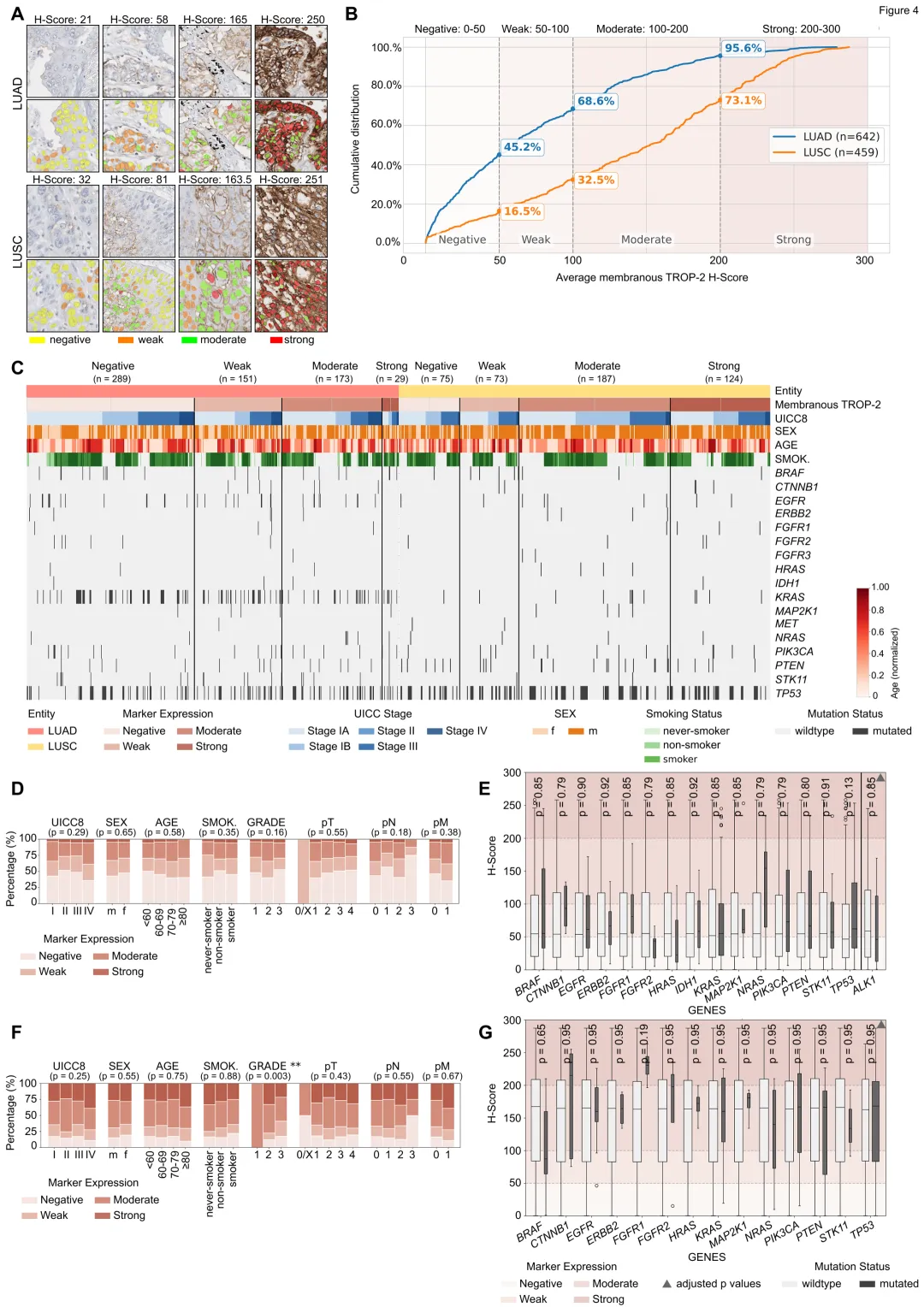
文献:ADC target profiling in NSCLC中展示 FLIM与Intensity重建虚拟IHC的对比图
基于自发荧光寿命(FLIM)特征生成的虚拟IHC图像,在TTF-1和p40阳性细胞的重建保真度上显著优于单纯的荧光强度成像,有效减少了假阳性的形态学伪影。
相比于微观切片,手术室的大体标本照片为术中诊断提供了一条低成本的路径。SuRImage研究直接使用了自然光下智能手机拍摄的大体图像。面对手机拍摄带来的色温、反光、角度等异质性噪音,研究团队在设定金标准时尤为谨慎:他们放弃了易出偏差的术中冰冻切片,直接对齐石蜡包埋(FFPE)后的最终病理诊断。这种跨尺度的标签设计,实质上是让算法跨越宏观的图像噪音,直接学习并预测肿瘤底层的微观侵袭性规律。
呼出气体的挥发性有机化合物(VOCs)测定,则提供了一个独立于局部影像的全身生理视角。在一项包含1,437例受试者的前瞻性队列中,研究通过GC-MS提取了VOCs图谱。值得注意的是其金标准的多目标设计:既包含用于良恶性分类的组织病理诊断,又纳入了长达5年的随访总生存期(OS)数据。这使得一次简单的无创呼气采集,能够同时服务于早期诊断鉴别与晚期预后风险分层。
此外,非传统生理特征的引入拓宽了临床“基线数据”的边界。例如,将患者常规的面部照片输入深度学习模型得出“面部年龄”,结合肺通气功能计算出“肺部年龄”,共同作为双模态输入特征。在确切生存时间和早期死亡事件的真实标签监督下,这类模型验证了粗颗粒度的生理老化指标与长期临床结局之间的独立关联。
最后,除了传统的生物医学数据,“系统级临床日志”也正成为一种特殊的评估基座。以LungIMPACT的真实世界研究为例,其分析的数据并非医学影像本身,而是穿透到了整个诊疗工作流:包含了影像申请时间、AI推断节点、医生阅片耗时以及最终CT执行的系统时间戳。这类系统级研究的核心门槛不在于图像特征提取,而在于必须对全流程数据中的“审查截断”和非流程性的人为干预噪音进行极其严格的清洗与界定。
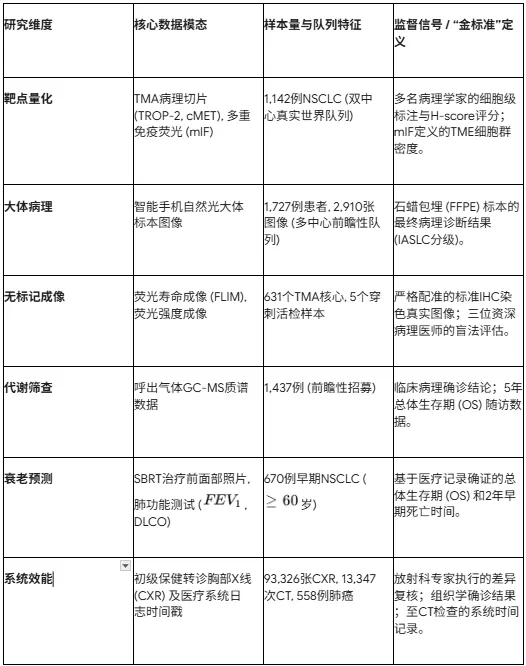
综上(详见表1),当前胸部肿瘤AI研究的核心数据模态与监督信号体系,正在经历从单一形态学,向功能学、代谢学及系统级工作流指标多维演进的过程。
思路总结
结合上述文献的演进脉络,胸部肿瘤人工智能领域仍存在大量尚未解决的科研空白,以下总结出若干可复现的科研范式与前沿选题方向,以供后续研究参考。
1. 可复现的方法论
一:多模态解耦与潜在空间对齐
整合不同尺度的异质性信息是提升预后模型鲁棒性的有效途径。可复现面部年龄与肺通气功能双模态预测的设计理念,进一步探索“大体/宏观特征”与“分子/代谢特征”的联合表征网络。例如,将手术大体病理图像与质谱分析得出的代谢物丰度信息结合。在网络架构上,可采用对比学习,强制大体形态的高维视觉特征与细胞代谢特征在多模态潜在空间中进行对齐,从而发掘尚未被人类定义的宏观形态与微观代谢的内在映射规则。此类多模态融合模型已在通过影像与临床文本联合预测中展示了优越的分类准确率。
二:面向医疗工作流重塑的实施科学
设计传统的AI研究倾向于追求测试集上AUC的边际提升,而LungIMPACT研究提供了一个评估真实临床效能的极佳模板。未来的科研选题不再局限于“开发一个精度更高的新模型”,而是将经过验证的模型置于特定的科室流转机制中,采用严格的区组随机化设计,重点评估AI干预下的卫生经济学代价、假阳性导致的系统性耗时增加以及医生的心理负荷。针对医疗管理痛点、具有明确临床转化路径的实施科学试验,正逐渐成为高水平医学综合期刊的关注焦点。
2. 尚未解决的科研空白
空白一:自发荧光功能特征的术中原位转化
尽管研究在载玻片层面证实了FLIM区分腺癌与鳞癌以及生成虚拟IHC的有效性,但离体石蜡切片的荧光衰减特性并不能完全等价于在体新鲜组织的代谢状态。如何开发基于内窥镜探头或胸腔镜的原位FLIM深度学习模型,在不进行物理切除和制片的情况下,直接实现手术视野内的组织亚型实时识别和切缘判定,是工程物理学与临床外科高度交叉的盲区。这类研究有望从根本上解决冰冻切片带来的时间延迟问题。
空白二:非结构化手术图像的通用自监督表征学习
现有的基于大体标本图像的诊断模型高度依赖庞大且精确的人工标签。在算法层面,针对手术室复杂光源条件和拍摄角度,需要开发面向大体病理图像(Gross Pathology)的掩码自编码器(Masked Autoencoders, MAE)或自监督基础模型。研究者可利用大量无标注的手术视频截图或大体标本图像进行预训练,以迫使网络学习光照无关、角度无关的鲁棒性组织纹理表征。结合近期提出的病理学特定视觉基础模型(如PLIP),开发专门针对宏观厚组织重建的算法框架,将极大降低此类研究的标注门槛。
空白三:多靶点ADC的伴随诊断模型构建与疗效预测
空间靶点量化研究已成功验证了TROP-2与cMET在微环境中的分布特征,然而,针对临床上不断涌现的新兴ADC靶点(如HER3、B7-H3、CEACAM5等)的亚细胞定位量化模型仍然缺失。未来的研究可聚焦于“靶点在细胞膜与细胞质中的共定位特征如何影响ADC的内吞效率及旁观者效应(Bystander effect)”。此外,利用AI特征工程建立病理切片特征与ADC真实世界响应队列的生存分析,开发能够精准筛选获益人群的伴随诊断模型,具有极高的转化医学价值。
空白四:特定免疫微环境(TME)的代谢逆向推演图谱目前基于VOCs的研究主要用于建立与宏观临床终点(如是否患癌、分期)的关联。一个具有深度的探索方向是:探究呼出气体的成分改变是否直接受特定TME表型的驱动。例如,肿瘤间质成纤维细胞的比例、巨噬细胞M1/M2极化状态,或T细胞的耗竭程度,是否会分泌特征性的代谢前体进入血液循环并最终被呼出。结合液体活检中的外泌体分离技术(如ASCENDx)与AI特征提取,并与单细胞测序(scRNA-seq)数据对齐,建立系统性代谢图谱与局部微环境免疫状态的直接映射,将为无创评估靶向治疗或免疫治疗的动态疗效开辟全新的评估窗口。


 夜雨聆风
夜雨聆风