点击蓝字 关注我们
前列腺癌(PCa)是中老年男性常见恶性肿瘤,中高危患者常需新辅助雄激素剥夺治疗(NADT)联合雄激素受体信号抑制剂。然而,现有指南因缺乏确切的疗效预测标志物而不常规推荐NADT,导致部分耐药患者无法及时调整治疗策略。因此,开发准确、低成本、无需分子检测的生物标志物以区分应答与非应答者至关重要。Hong Yan等中国学者利用人工智能(AI)从常规穿刺活检HE切片挖掘出13种细胞形态计量生物标志物(CMB),构建预测模型并在多个独立队列中验证其预测与预后价值。同时,通过免疫组化和患者来源类器官(PDO)证实,该模型可识别mTOR通路高活性的耐药亚群,并为联合使用mTOR抑制剂提供实验依据,为实现前列腺癌精准分层与治疗优化提供了新策略。
01
研究亮点
Research Highlights
1. 构建并验证了基于AI的13-CMB(13种细胞形态计量生物标志物)模型,仅依托常规穿刺活检HE切片,即可精准预测前列腺癌患者对NADT联合恩杂鲁胺的治疗反应,且在多中心队列中实现患者预后分层。
2. 通过患者来源类器官(PDO)实验,验证了13-CMB模型分层的NADT无应答患者对mTOR抑制剂敏感,为耐药患者提供了新的治疗方向。
3. 揭示了CMBs与肿瘤微环境、分子特征的关联,证实CMBs可预测肿瘤mTOR信号通路激活状态,为CMBs的生物学机制及临床转化提供了坚实的实验支撑。
02
研究内容
Research Content
(a) 研究队列
该研究使用四个队列:队列1(临床试验NCT02430480,n=37,中高危PCa,接受6个月NADT+恩扎卢胺),以残余肿瘤负荷0.05cm³为界分为显著应答者(ER,n=15)和不完全/无应答者(INR,n=22);队列2(n=122)和队列3(n=60)为独立医院验证队列,均为中高危及以上局限性PCa患者NADT前的穿刺活检标本(按美国国家综合癌症网络风险分级);队列4为TCGA-PRAD队列(n=396,局限性PCa)仅用于预后验证。
(b) CMBs可在NCT02430480试验队列中精准预测NADT联合恩扎卢胺治疗的疗效反应
从中高危PCa患者基线穿刺活检中鉴定出256个CMBs(图1A–B),其中13个与NADT联合恩扎卢胺治疗反应显著相关(图1F、1G,FDR<0.05)。耐药相关CMB(如CMB192)表现为收缩/立方形间质梭形细胞及免疫排斥特征;与治疗敏感相关的CMB(如CMB212)则呈现伸长梭形间质细胞及免疫友好特征,提示CMB相关间质形态可能反映癌相关成纤维细胞(CAF)功能状态及细胞外基质(ECM)和免疫拓扑差异,影响ADT敏感性。基于13个CMBs构建的LASSO模型可精准预测治疗反应(AUC:0.981,95%CI:0.979-0.983),其效能优于既往模型(图1I),表明该CMB模型可可靠地用于患者分层。
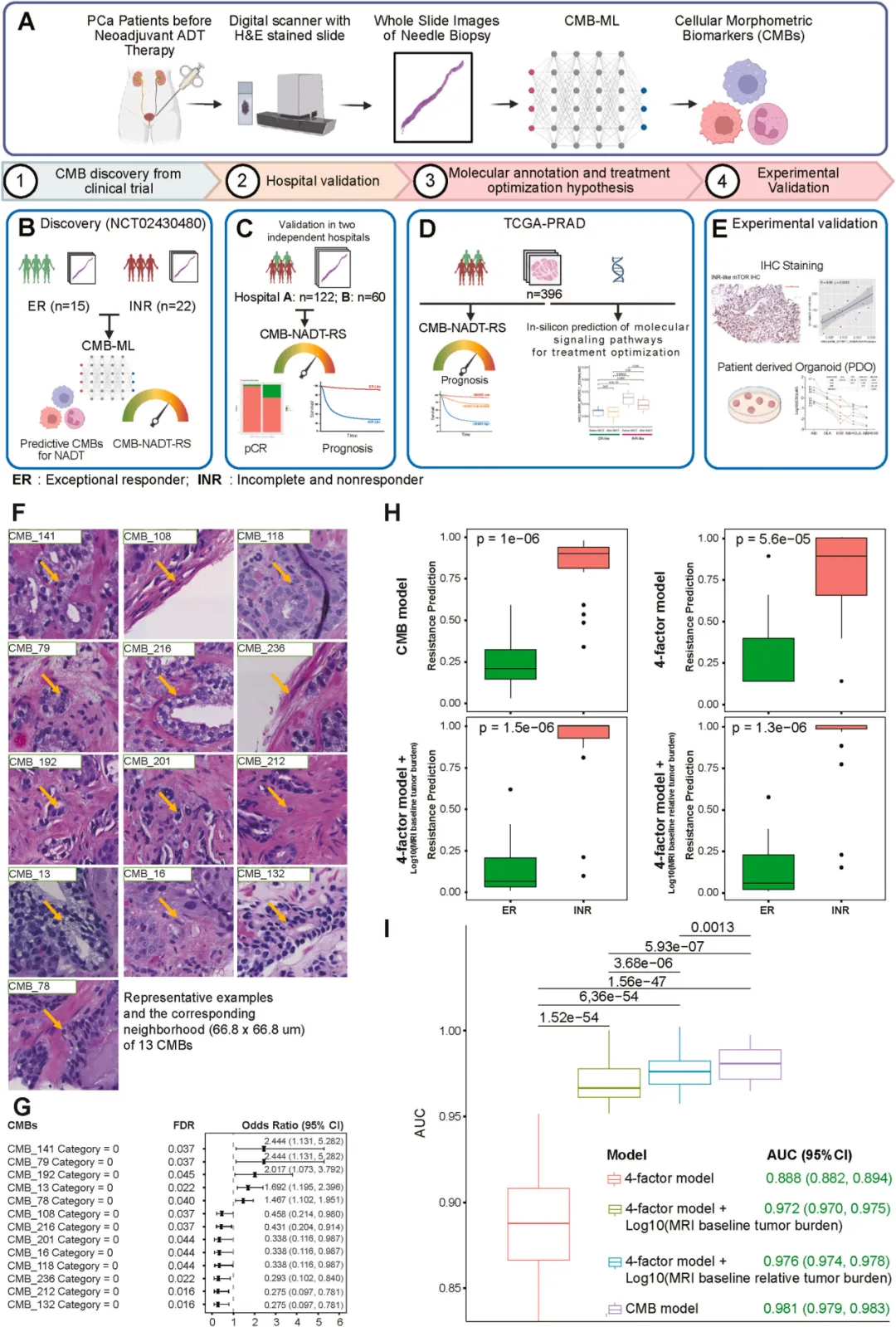
图1.(A–E)研究设计路线。(A)基于新辅助雄激素剥夺治疗(NADT)患者穿刺活检标本进行CMB挖掘的CMB-机器学习(CMB-ML)分析流程;(B)发现队列;(C)医院验证队列;(D)分子注释与治疗获益预测;(E)实验验证。(F)各CMB典型形态示例。(G)单个CMB与治疗耐药的关联性分析;(H)不同模型在显著应答组(ER)与不完全/无应答组(INR)间的预测概率比较。其中,四因子模型基于以下指标构建:导管内癌(IDC,存在导管内癌)、10q缺失(经GISTIC算法判定10号染色体长臂至少半数区域发生半合子缺失)、ERG(经免疫组化判定细胞核ERG过表达)、TP53(经GISTIC判定TP53功能缺失性改变或热点突变,包括拷贝数缺失);(I)采用80%抽样率、100次迭代的自举法对训练队列进行模型效能评估。每次迭代中,所有对比模型均基于相同数据划分进行评价。(G)中P值采用逻辑回归计算;(H)中P值采用非参数MannWhitney检验计算;(I)中P值采用配对MannWhitney非参数检验计算。缩略语:ER:显著应答者;INR:不完全应答及无应答者。(A–E)面板使用BioRender.com绘制。
(c) 锁定的CMB模型将两个独立医院队列中接受NADT治疗的前列腺癌患者分层为治疗反应与预后显著不同的亚组
为验证锁定版13-CMB模型的预测效能与临床价值,对两个分别含122例和60例接受NADT治疗的局限性前列腺癌患者的独立医院队列进行盲法评估(图2A–D)。第一个队列(n=122)中,模型将患者分为类显著应答组(ER-like,n=22)与类不完全/无应答组(INR-like,n=100),ER-like组病理完全缓解率(pCR)(p=0.0005,图2B)和无生化复发生存期(BCRFS)(p=0.024,图2C)均显著更优;第二个队列(n=60)中,模型同样分组(ER-liken=16,INRliken=44),ER-like组无生化复发生存期(BCRFS)显著更优(p=0.031,图2F),因仅1例达到pCR,两组pCR率无统计学差异(p=0.595,图2E)。合并两队列汇总分析显示,ER-like组治疗耐药评分显著更低(p<2.22×10⁻¹⁶,图2G)、pCR率更高(p=0.0004,图2H)、BCRFS更优(p=0.015,图2I)。多变量分析证实锁定模型为pCR(p=0.002,图2J)和BCRFS(p=0.032,图2K)的独立预测因子。
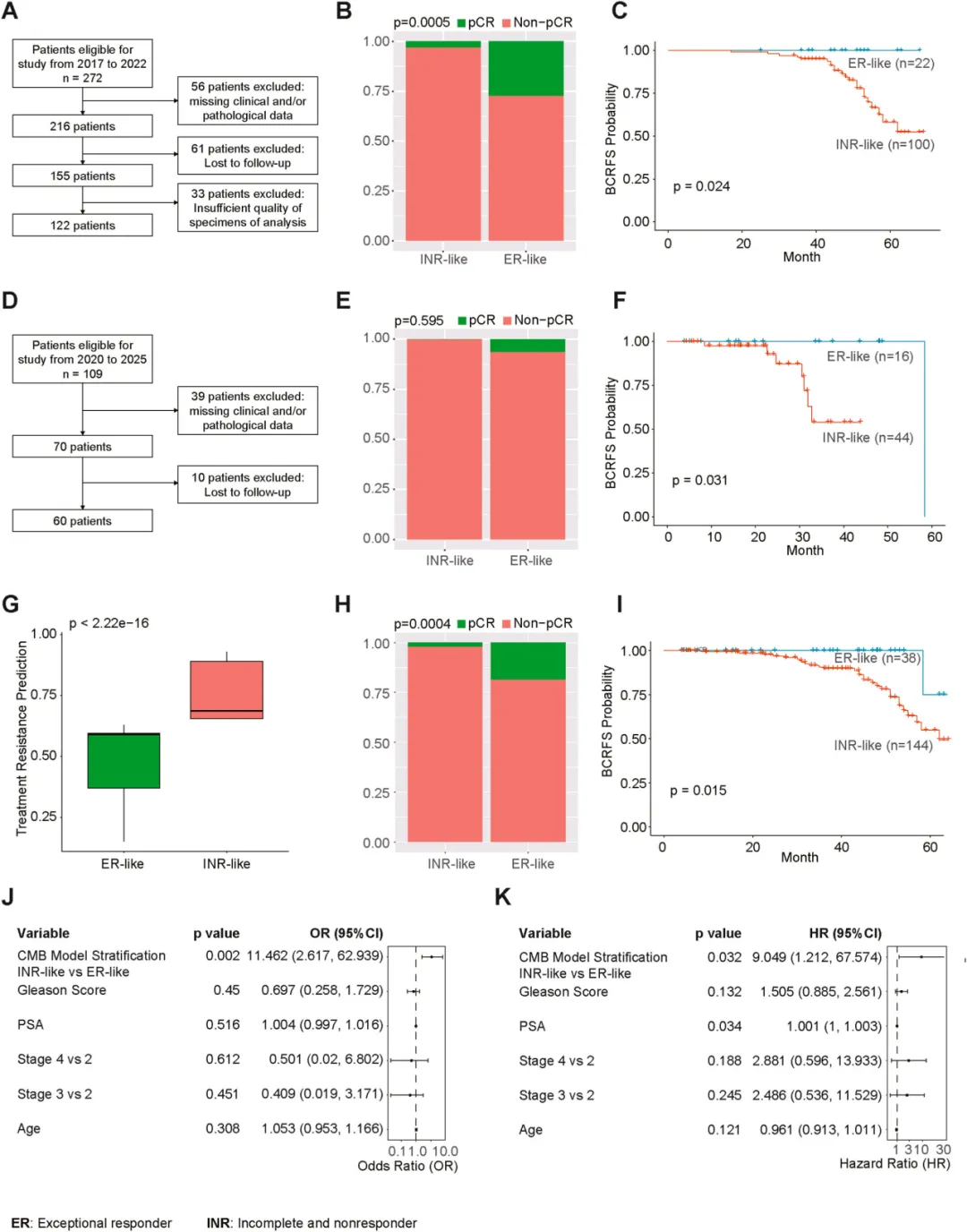
图2.(A)南京鼓楼医院患者入组流程图。(B)13CMB模型与NADT治疗反应显著相关。(C)13CMB模型与无生化复发生存期显著相关。(D)安徽医科大学第一附属医院患者入组流程图。(E)因达到病理完全缓解(pCR)的患者例数极少(仅n=1),13CMB模型与NADT治疗反应无统计学显著关联。(F)13CMB模型与无生化复发生存期显著相关。(G–K)合并分析(两个医院队列联合)结果显示:(G)类显著应答组(ERlike)与类不完全/无应答组(INRlike)之间治疗耐药评分存在显著差异;(H)13CMB模型与NADT治疗反应显著相关;(I)13CMB模型与无生化复发生存期显著相关。(J)在校正PSA、临床分期、Gleason评分和年龄后,13CMB模型是pCR的显著独立预测因子;(K)在校正PSA、临床分期、Gleason评分和年龄后,13CMB模型是无生化复发生存期的显著独立预测因子。(B、E、H)中P值采用卡方检验计算;(C、F、I)中P值采用对数秩检验(logranktest)计算;(G)中P值采用非参数MannWhitney检验计算;(J)中P值采用多因素逻辑回归计算;(K)中P值采用多因素Cox比例风险(PH)回归计算。缩略语:ER:显著应答者;INR:不完全应答及无应答者。
(d) 锁定的CMB模型将TCGA-PRAD队列中的前列腺癌患者分层为预后显著不同的亚组
为评估13-CMB模型的预后价值,将其应用于TCGA-PRAD队列(n=396),分为类显著应答组ER-like(n=252)与类不完全/无应答组INR-like(n=144)(图3A–C)。结果显示,ER-like组无进展生存期(PFS)显著更优(图3B,p=0.0017),总生存期(OS)仅呈改善趋势(图3C,p=0.054)。OS差异不显著可能与事件发生率与随访时间有限、挽救治疗及后续治疗的影响、生物学终点与治疗干预后终点的差异及TCGA队列异质性有关。
为评估13-CMB模型的临床实用性,在TCGA-PRAD队列中结合预计算的OncotypeDX和Decipher评分进行多变量分析。INR样组的两项评分均显著更高(图3D-F)。校正临床因素及基因组评分后,13-CMB模型仍是PFS的独立预后因素(图3E-G),而Decipher和OncotypeDX失去显著性。因公开评分与商业检测量纲不同,使用连续耐药评分验证,结果一致。TCGA-PRAD无NADT信息,但结合两个医院队列,13-CMB模型兼具预测NADT反应及局限性PCa预后价值。
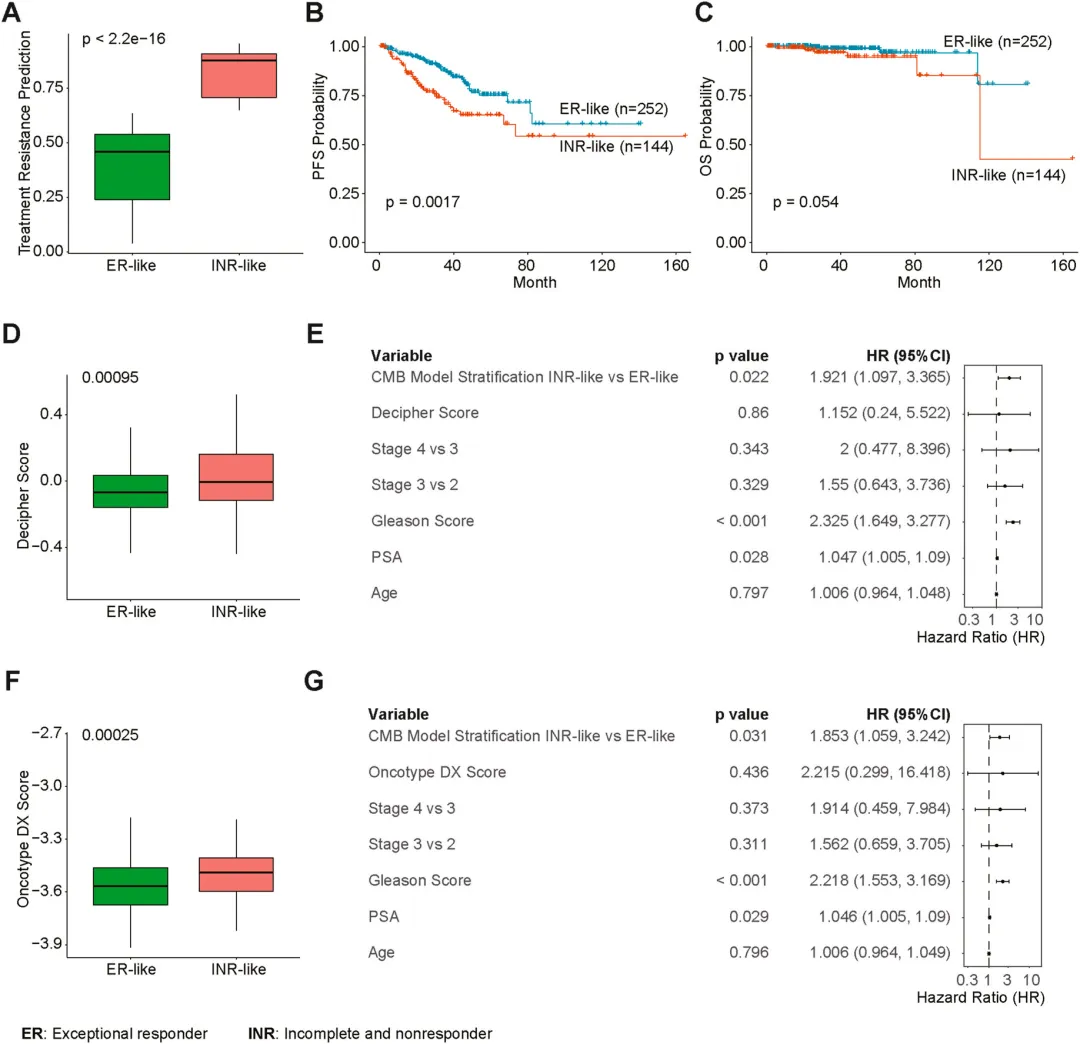
图3.(A–G)13CMB模型对TCGAPRAD队列患者进行分层后结果如下:(A)治疗耐药评分存在显著差异;(B)无进展生存期存在显著差异;(C)总生存期差异无统计学意义,仅呈趋势性差异。(D)类不完全/无应答组(INRlike)的Decipher评分显著更高;(E)在校正Decipher评分、临床分期、Gleason评分、PSA及年龄后,13CMB模型对无进展生存期仍具有显著且独立的预后价值。(F)类不完全/无应答(INRlike)的OncotypeDX评分显著更高;(G)在校正OncotypeDX评分、临床分期、Gleason评分、PSA及年龄后,13CMB模型对无进展生存期仍具有显著且独立的预后价值。(A、D、F)中P值采用MannWhitney非参数检验计算;(B、C)中P值采用对数秩检验(logrank检验)计算;(E、G)中P值采用多因素Cox比例风险(PH)回归模型计算。缩略语:ER:显著应答者;INR:不完全应答及无应答者。
(e) CMBs与肿瘤微环境显著相关
前列腺癌的肿瘤微环境(TME)对生存、治疗反应及转移至关重要。利用TCGA-PRAD队列的RNA-seq数据发现,有利的CMBs(图1G,CMB108、118、236)与TME中免疫细胞浸润呈显著负相关。PCa中免疫浸润多反映基因组不稳定性等,而非有效抗肿瘤免疫;对ADT敏感的AR依赖性、管腔分化肿瘤常呈“免疫冷”微环境。因此,该负相关可能体现肿瘤分化状态与AR依赖性,而非缺乏免疫原性。
(f) 类应答组与类无应答组在肿瘤特征、肿瘤微环境及代谢相关特征谱上存在显著差异
在TCGA-PRAD队列中,ER-like与INR-like组在肿瘤功能状态、TME及代谢重编程三方面存在显著差异(图4A、4B)。INR-like组中同源重组修复HRR(FDR=1.4×10⁻⁶)、PI3K/AKT/mTOR(FDR=0.01)、DNA损伤修复(DDR)及NK细胞(FDR=0.007)等特征评分更高,而ER-like组雌激素应答评分更高;INR-like组类固醇激素代谢与生物合成下调(FDR=0.004、0.002)。13个CMB可有效预测HRR(R=0.29)、NK细胞(R=0.29)及DDR等评分(图4B下图),且在独立医院队列中验证一致。
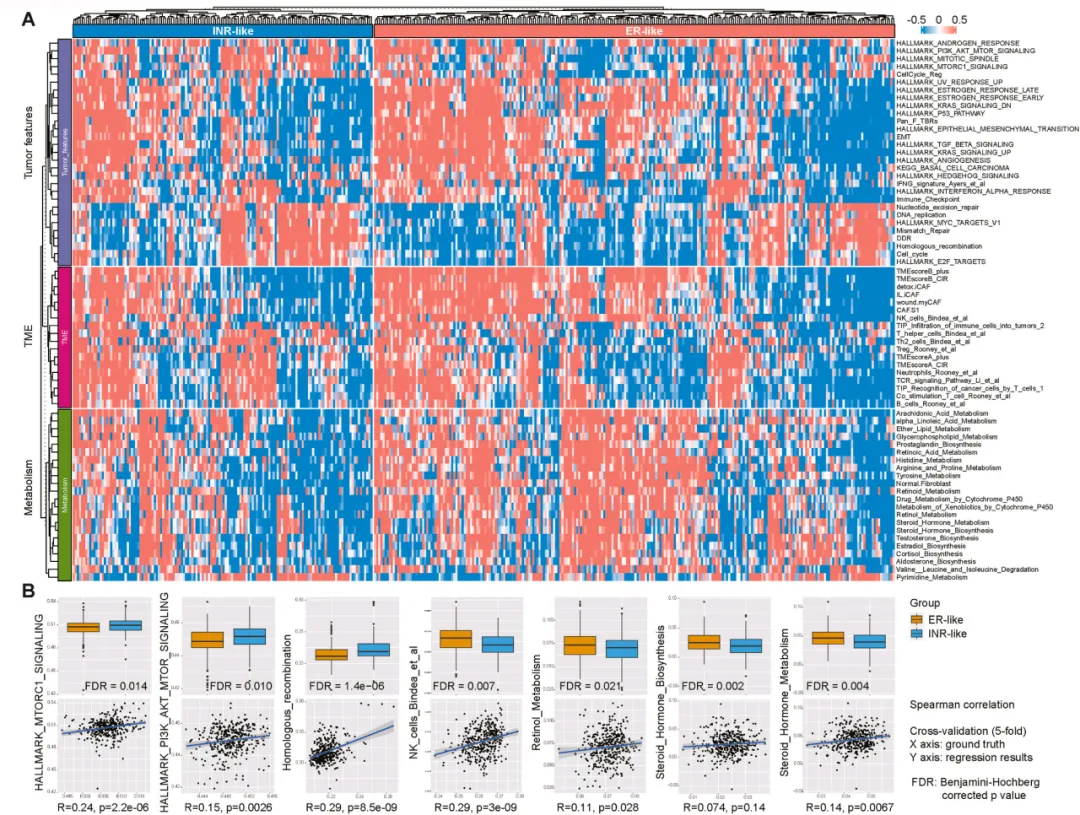
图4. 类显著应答组(ER-like)与类不完全/无应答组(INR-like)分别和肿瘤特征、肿瘤微环境(TME)及代谢相关特征基因集的关联性(A);两组间具有显著差异的特征基因集评分示例(B,上图);以及在5折交叉验证中对验证集样本上述基因集评分的预测效果(B,下图)。
(g) 类无应答组患者mTOR信号通路激活更强,对mTOR抑制剂更敏感
将CMB模型应用于20例NADT治疗前后配对标本(ER-like与INR-like各10例),发现NADT治疗后两组NK细胞增多(图5B)、EMT增强(图5C)、HRR缺陷加重(图5D),而mTOR活性不受影响(图5A),且INR-like组mTOR活性持续更高,与TCGA-PRAD结果一致(图5E)。INR-like组对mTOR抑制剂更敏感(图5G–H),并经免疫组化(IHC)验证p70S6K表达显著升高(图5M–O,p=0.03),预测评分与蛋白表达显著相关(图5L、5P),证实模型预测效能。
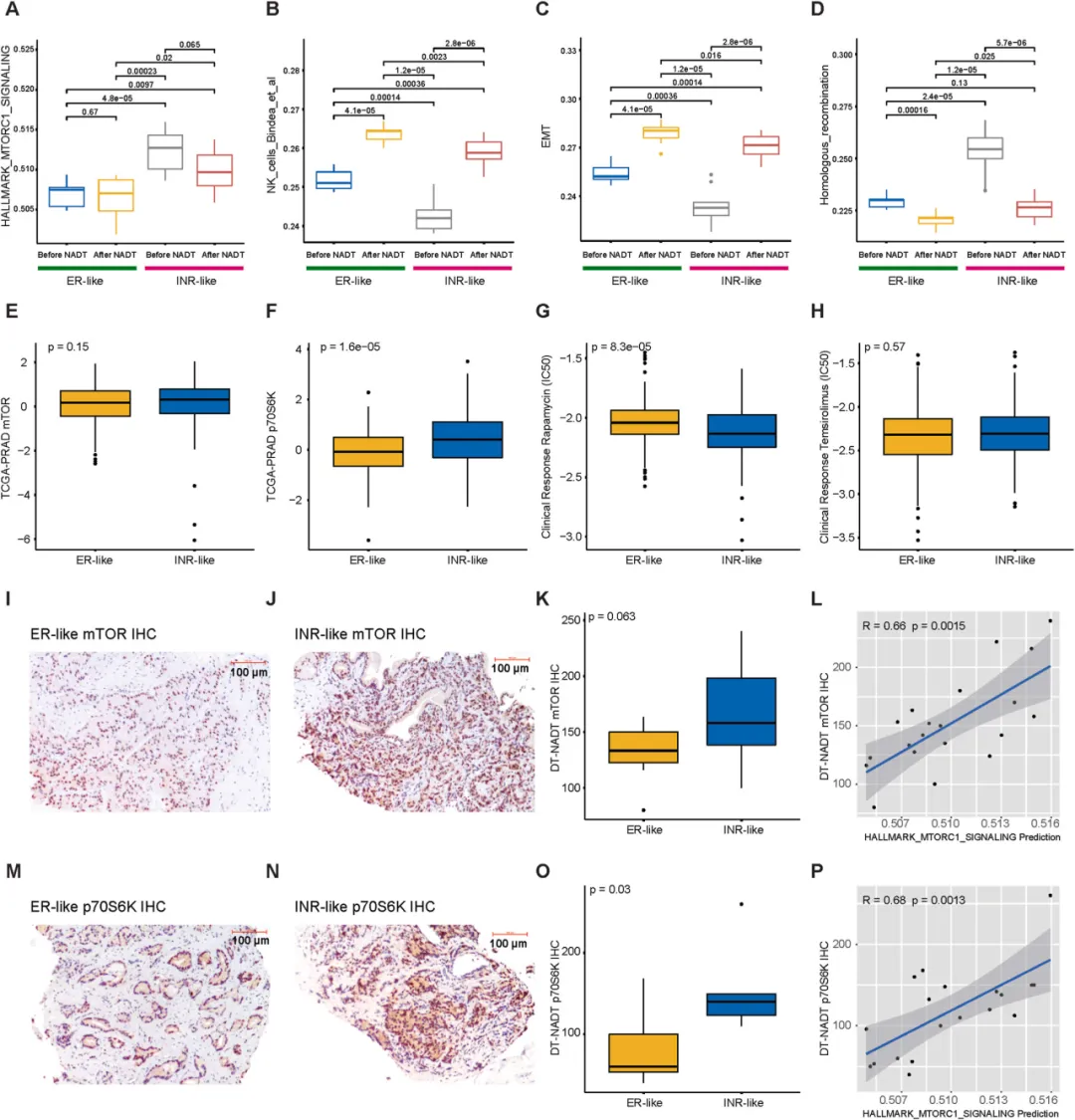
图5. 采用预先从TCGAPRAD队列构建的CMB特征模型,对独立医院队列患者在NADT治疗前后进行预测:(A)经典MTORC1信号通路(HALLMARK_MTORC1_SIGNALING)评分;(B)NK细胞评分;(C)上皮间质转化(EMT)评分;(D)同源重组修复评分。(E–F)TCGAPRAD队列中,类显著应答组(ERlike)与类不完全/无应答组(INRlike)肿瘤内pmTOR和p70S6K的蛋白表达水平。(G–H)基于TCGAPRAD队列RNAseq数据,使用pRRophetic算法预测mTOR抑制剂(雷帕霉素、替西罗莫司)在两组间的敏感性;其中INRlike组预测IC₅₀更低,提示对雷帕霉素敏感性显著更高。(I–K)独立医院队列的免疫组化(IHC)染色显示,INRlike组肿瘤中pmTOR表达呈更高趋势;(L)pmTOR蛋白表达与预测的经典MTORC1信号通路评分呈显著强相关。(M–O)独立医院队列免疫组化染色显示,INRlike组肿瘤中p70S6K表达显著更高;(P)p70S6K蛋白表达与预测的经典MTORC1信号通路评分呈显著强相关。比例尺=100μm。(A–H、O)中P值采用非参数MannWhitney检验计算;(L、P)中P值采用Spearman相关性分析计算。
(h) mTOR抑制剂在INR样肿瘤中的有效性在患者来源类器官(PDO)中得到实验证实
为验证INR样肿瘤对mTOR抑制剂的敏感性,从8例经13-CMB模型判定的INR样患者中建立PDO培养(图6A)。CMB模型显示这些肿瘤中mTOR(图6B)和DDR(图6C)活性显著升高。药物筛选包括ARPI(醋酸阿比特龙)、PARP抑制剂(奥拉帕利)、mTOR抑制剂(依维莫司)及联合方案。患者3对除奥拉帕利单药外的方案均敏感(图6D、6E)。两种联合疗法,尤其是醋酸阿比特龙+依维莫司,在宽浓度范围内细胞毒性优于单药(图6F),IC₅₀显著降低(图6G),AUC证实其整体抑制最强(图6H),而依维莫司单药效果不足,提示协同作用。这与mTOR介导的适应性耐药一致:抑制mTOR可阻断代偿程序,恢复肿瘤对雄激素阻断的敏感性。PDO实验证明,在INR-like前列腺癌耐药亚群中,mTOR抑制剂与ARPI联合应用具有明确的协同抗肿瘤效应,是克服ADT/ARPI耐药的有效策略。 该发现为针对此耐药亚群的临床试验设计提供了强有力的机制依据。
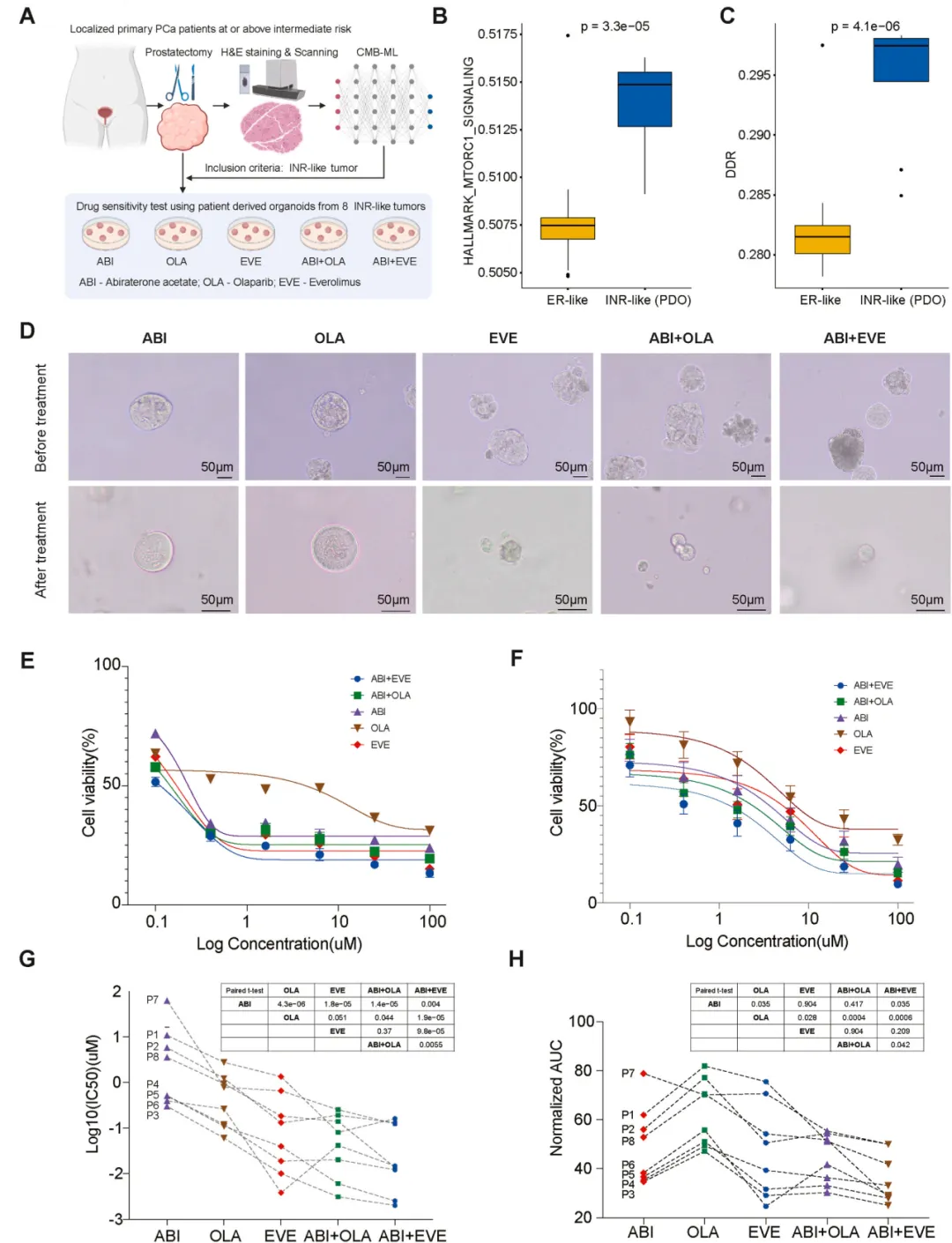
图6. mTOR抑制剂对INR-like肿瘤获益的实验验证A)基于患者来源类器官(PDO)进行药物筛选的研究设计;(B-C)PDO实验中INR-like患者的预测经典MTORC1信号通路(HALLMARK_MTORC1_SIGNALING)及DNA损伤修复信号通路(DDRSIGNALING)评分;(D-E)PDO培养模型中不同治疗方案对患者3细胞活力的影响;(F)剂量反应曲线,显示不同药物浓度(0.1–100μM)对经醋酸阿比特龙(ABI)、依维莫司(EVE)、奥拉帕利(OLA)、醋酸阿比特龙+依维莫司(ABI+EVE)及醋酸阿比特龙+奥拉帕利(ABI+OLA)处理的PDO细胞活力(%)的影响;(G-H)分别为8株患者来源前列腺癌类器官系中五种治疗方案的IC₅₀值分布(对数刻度,μM)及剂量反应的曲线下面积(AUC)。
03
讨论
Discussion
该研究开发并验证了基于AI的13-CMB模型,利用常规H&E切片即可预测NADT治疗反应,独立于基因组及组织学特征,可作为精准肿瘤学的新方法。相比商业基因组检测(Decipher、OncotypeDX),13-CMB模型更易获取、成本更低,且在多变量分析中独立预后价值显著。模型发现INR样肿瘤mTOR及DDR通路活性更高,PDO实验证实mTOR抑制剂联合ARPI可协同增效,为耐药患者提供新策略。DDR通路活性升高提示PARP抑制剂潜在获益,亦经患者来源类器官验证。
该研究局限性包括:开发队列较小、回顾性验证仅两中心、TCGA-PRAD治疗信息不完整、未直接头对头比较商业检测、IHC仅支持性证据、PDO队列小且缺乏多样性、未纳入ER样类器官、PDO缺乏微环境等。此外,临床部署需解决切片质量、扫描异质性等问题,需前瞻性多中心验证及监管审批。总之,13-CMB模型基于穿刺活检,可精准预测NADT反应、预后及mTOR抑制剂治疗获益,融合AI与数字病理学,有待更大规模前瞻性验证。
大橡科技肿瘤类器官药物评价
大橡科技依托自主创新的类器官芯片平台与标准化肿瘤类器官样本库,打造精准药物评价解决方案。平台可高度还原肿瘤微环境与异质性,突破传统模型局限,高效支持小分子、抗体、ADC、CGT等多种类型候选药物的敏感性检测与耐药机制研究,助力药企快速筛药,降低研发成本与临床转化风险;依托平台标准化培养体系与稳定的检测流程,为临床个体化用药提供精准导航,全面推动肿瘤药物研发与精准医疗落地。
小分子药物更多研究案例,点击下方链接:
客户文章解读|PARP抑制剂耐药了怎么办?中国团队最新发现,铜离子或是破局关键 GUT重磅|突破肠毒性-疗效困境!类器官共培养精准筛选小分子,革新免疫治疗副作用管理
抗体、ADC药物 更多研究案例,点击下方链接:类器官新机制:为何HER2低表达的尿路上皮癌仍对靶向治疗敏感? STTT(IF52.7)皮摩尔级锁定!PDOX模型验证抗CD155纳米抗体携药直捣肺腺癌 肿瘤克星:类器官研究为ADC药物研发按下“快进键” CGT药物 更多研究案例,点击下方链接:肿瘤显著清除!类器官与动物实验共同验证新型细胞外囊泡递送系统免疫治疗胰腺癌"鸡尾酒"CAR-T疗法:治疗异质性脑癌的新策略


扫描二维码可联系我们
小红书
客服电话/微信:18610798010

设计: Summer、Rebecca|封面: Rebecca
求点赞

求分享

求喜欢

 夜雨聆风
夜雨聆风