
在细胞分化的宏伟篇章中,一个核心谜题长久存在:驱动分化的关键转录因子(如指导血细胞生成的Spi1、Gata1等)在干细胞和祖细胞中常常以平缓、重叠的梯度表达,如同模糊的渐变信号。然而,它们最终却能够启动截然不同、高度特异的基因表达程序,精准地决定一个细胞是变成巨噬细胞还是红细胞。这个从“模糊指令”到“精确行动”的转换是如何实现的?传统上认为,增强子(基因的远程开关)通过组合不同转录因子结合位点来工作,但其精确的“决策规则”一直如黑箱般难以破译。
方法突破:用“合成增强子”文库进行系统性破解
为了自上而下地破解这套调控密码,2025年6月12日,西班牙巴塞罗那科学技术研究所LarsVelten团队在Cell 在线发表题为“Design principles of cell-state-specific enhancers in hematopoiesis”的研究论文,该研究另辟蹊径,摒弃了研究复杂天然基因组序列的传统思路。他们采用了一种“自下而上”的合成生物学方法:精心设计了包含64,400个完全合成的DNA序列的增强子文库。这些序列以随机DNA为骨架,系统地嵌入38个关键造血转录因子的结合位点,并变化其组合、排列、亲和力及拷贝数。随后,他们利用大规模平行报告基因测定技术,在从造血干细胞分化为七种不同髓系细胞的完整过程中,高通量测量了每一个合成增强子的活性。

核心发现:令人惊讶的“负协同”作用
这项大规模的“增强子功能普查”得出了颠覆直觉的核心发现:转录因子结合位点之间的相互作用并非简单的叠加激活,而普遍存在“负协同”效应。即,某些单独存在时能强力激活基因的“谱系决定因子”结合位点(如Spi1或Gata1的位点),当它们彼此组合时,活性反而相互抵消甚至转为抑制。这种“负协同”作用对转录因子的表达比例极为敏感,使得增强子仅在其中某一个因子占绝对主导的细胞状态下才会被特异性激活,从而将连续的转录因子浓度梯度,“翻译”成了离散的、细胞状态特异性的“开/关”信号。
相反,一些在干细胞中高表达的“干细胞因子”(如Runx1、Meis1)的结合位点,本身单独作用时表现为抑制子,但却能在特定组合下“允许”或支持激活。这套由激活与抑制性相互作用共同构成的复杂规则,如同一套精密的布尔逻辑电路,确保了基因在正确的时间、正确的细胞中被精确开启。
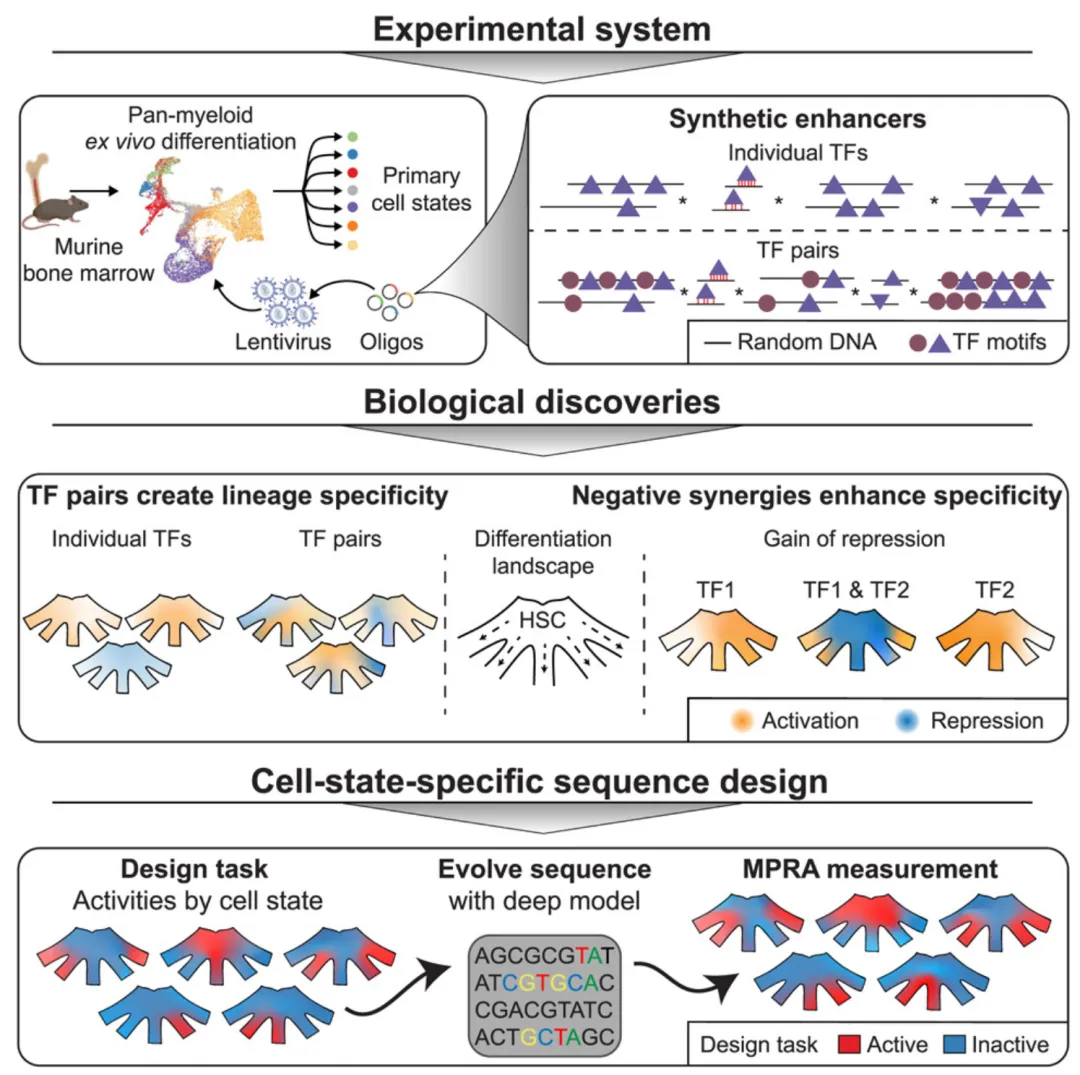
文章模式图(图源自Cell )
验证与应用:从规则解读到智能设计
研究团队进一步证明,这套从合成序列中总结出的规则同样适用于预测天然基因组中增强子的功能。更具开创性的是,他们反向运用这些规则,成功实现了增强子的“理性设计”——通过计算自动生成具有用户指定活性模式(例如,仅在特定祖细胞亚群中活跃)的全新DNA序列。这标志着对基因调控元件的理解,从“解读”迈向了“编写”的新阶段。
科学意义与前景
这项研究不仅为理解细胞分化、再生乃至癌变(癌细胞常异常共表达本应互斥的程序)提供了普适性的调控逻辑框架,其建立的“设计原则”和合成筛选平台,更将为合成生物学、细胞命运重编程及靶向基因调控疗法的开发提供强大的新工具。它向我们展示,生命在分子层面实现精准调控的智慧,往往蕴藏在看似复杂的相互作用所形成的、具有鲁棒性的逻辑关系之中。
参考消息:
https://www.cell.com/cell/fulltext/S0092-8674(25)00449-0

iMedicines,专注于生物医学科研报道。
投稿事宜:ilovehainan@foxmail.com
觉得本文好看,请点这里!
 夜雨聆风
夜雨聆风