

My Happy Time
点击蓝字 关注我们
课题设计、论文指导、实验委托等服务,可在公众号咨询!我们在文末拆解了这篇文献的可复制的科研套路,同时设置了几个小问题,大家一起来看看吧~

这篇发表于npj Digital Medicine(IF=15.1)的研究,来自惠州市第一人民医院肿瘤中心团队。研究通过整合单细胞 RNA 测序、空间转录组和 bulk 去卷积技术,首次揭示低级别乳腺癌中CXCR4⁺成纤维细胞等三类细胞的免疫抑制作用,为免疫治疗耐药提供了全新机制解释。

01
研究背景
乳腺癌是全球女性发病率和死亡率最高的恶性肿瘤,肿瘤微环境(TME)异质性是导致治疗耐药和转移的核心原因,但低级别肿瘤的免疫逃逸机制认识不足。近年来单细胞和空间转录组技术的发展,为系统解析 TME 提供了可能,但目前仍缺乏跨肿瘤分级的全面时空图谱。
02
研究思路
这篇文章的核心思路我们完全可以模仿。首先数据全是公开的——GEO单细胞+空间转录组+TCGA bulk验证,零自产测序。
分析分四步:①scRNA-seq聚类15个大群,基质/髓系/淋巴细胞分别亚群再分群;②空间转录组用CARD验证各亚群定位;③锁定三个低级别富集亚群(CXCR4+成纤维、IGKC+髓系、CLU+内皮),用NicheNet/CellChat解通讯、TIDE预测免疫治疗响应;④TCGA bulk用BisqueRNA反卷积验证预后。
全套工具全是免费R包和在线平台,换个癌种、换套公开数据就能复用,适合想做多组学整合又不想花钱测序的朋友~
03
结果
1
乳腺癌 TME 单细胞全景图谱乳腺癌 TME 单细胞全景与分级特异性亚群
研究整合 59 例 scRNA-seq 数据进行无监督聚类,对基质、免疫细胞二次分群并做功能富集。
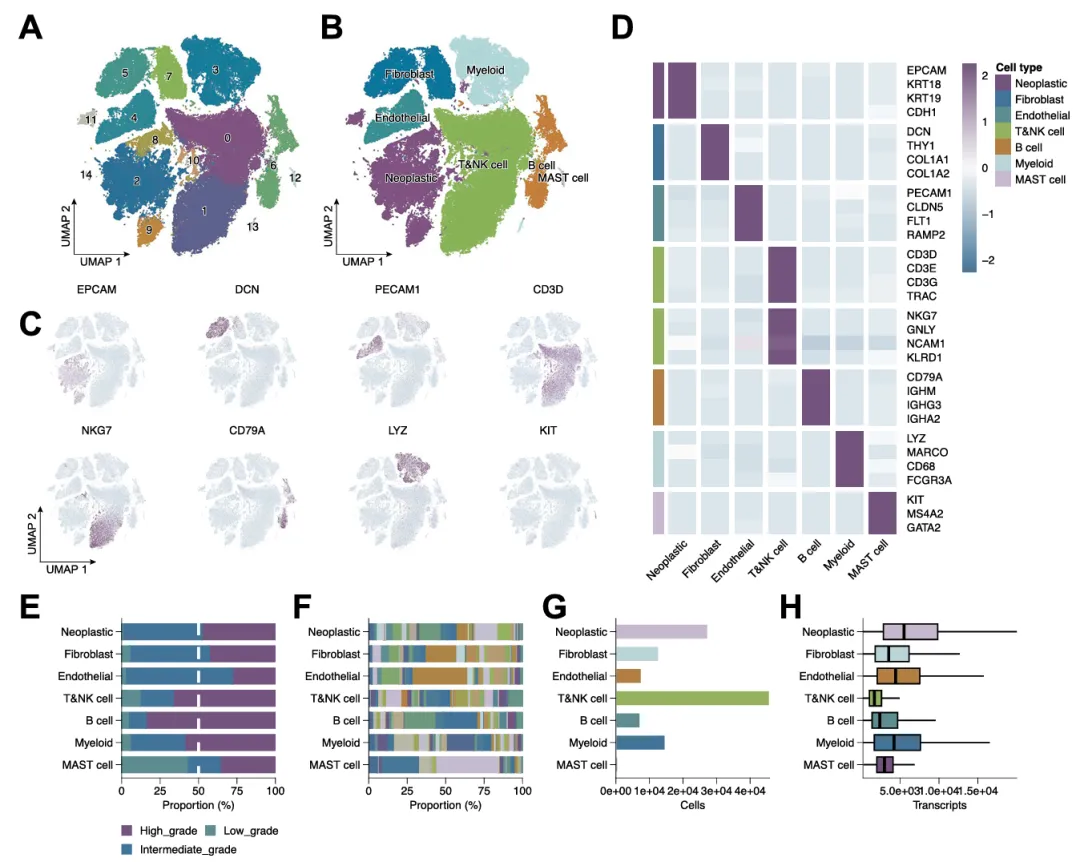

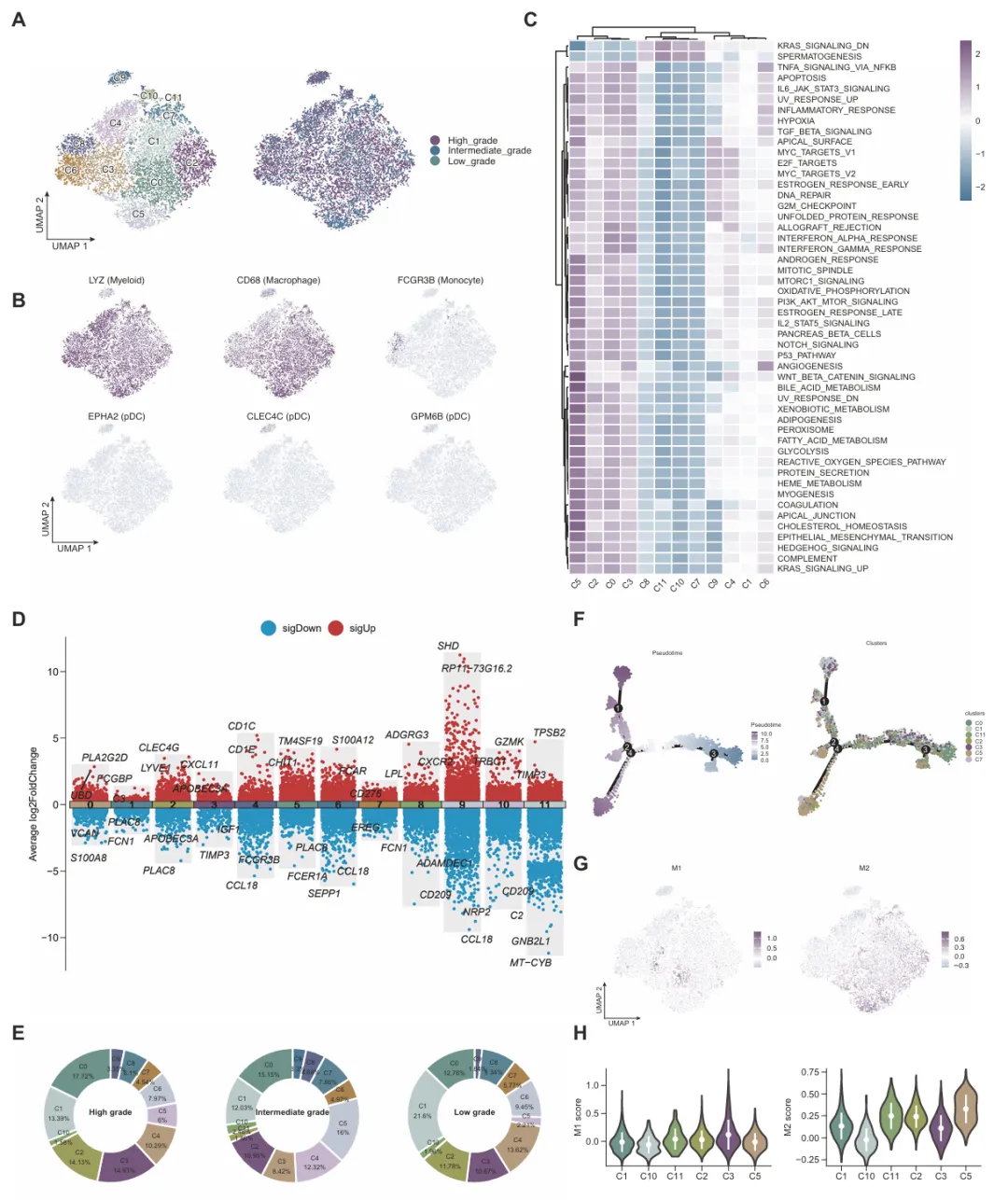
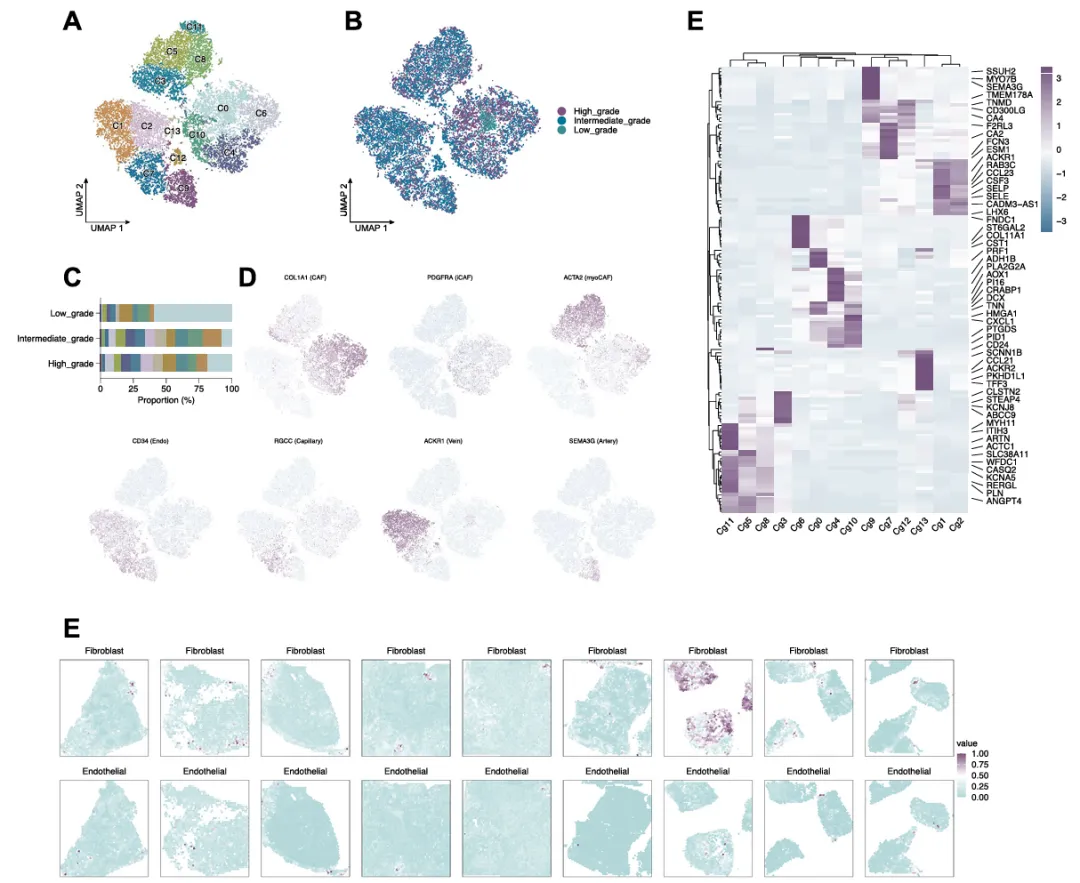
左右滑动
鉴定出 15 个主要细胞群,同时发现F3_CXCR4⁺成纤维细胞、M1_IGKC⁺髓系细胞、E4_CLU⁺内皮细胞特异性富集于低级别肿瘤。
这表明,乳腺癌 TME 存在高度异质性,低级别肿瘤拥有独特的基质 - 免疫微环境。
2
空间转录组解析细胞分布与通讯网络
随后,研究又用 9 例空间转录组数据结合 CARD 去卷积,通过 CellChat 构建配体 - 受体互作网络。
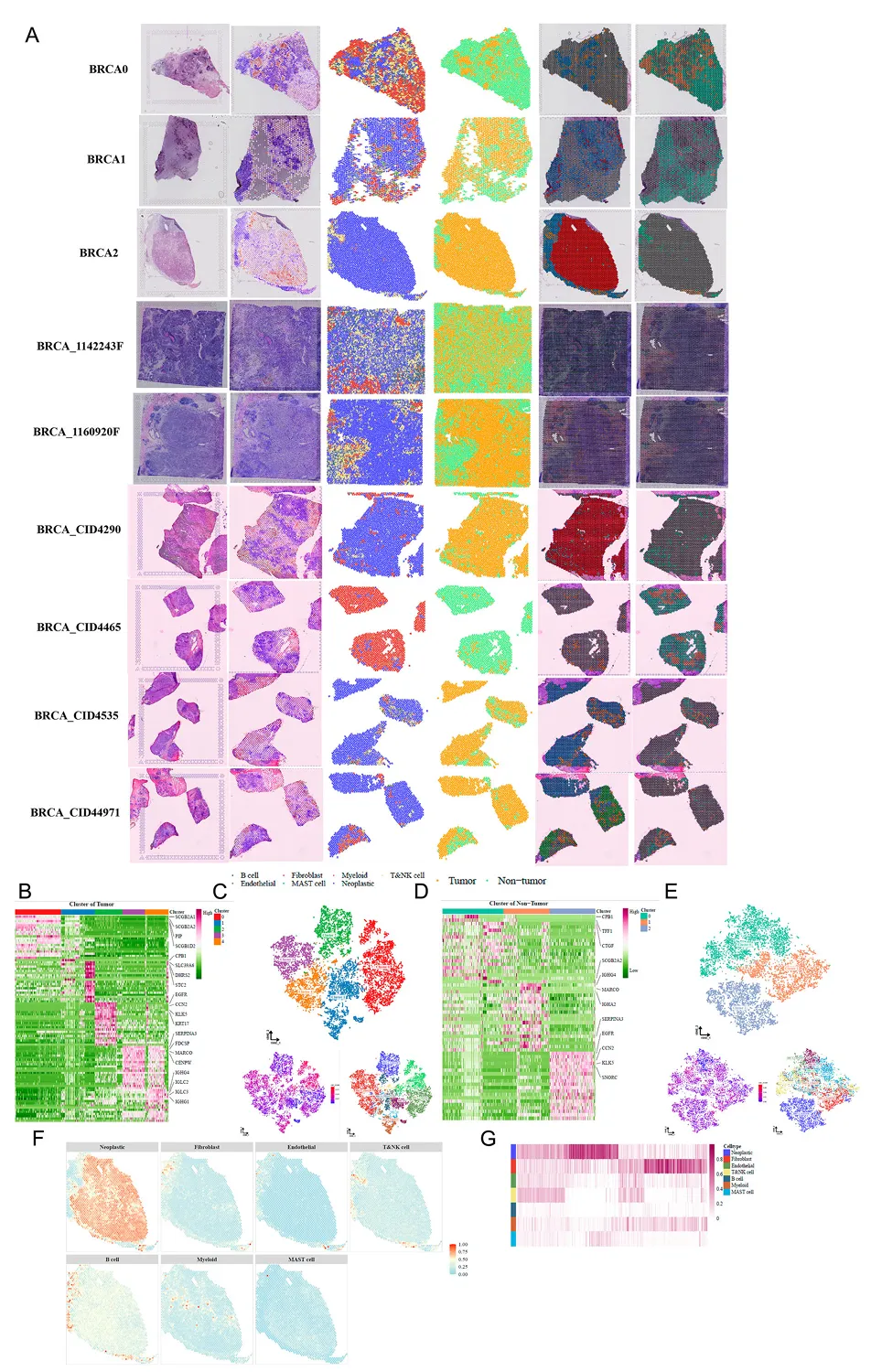
上下滑动
结果发现,肿瘤与免疫细胞形成明显空间分区,高级别肿瘤信号网络更复杂,MDK 和 Galectin 信号通路显著激活。
这表明,细胞空间分布和通讯重编程共同驱动肿瘤进展与免疫逃逸。
3
低级别亚型的免疫治疗悖论与临床验证
最后,研究用 TIDE 算法预测免疫治疗响应,基于单细胞参考对 TCGA-BRCA 进行去卷积并构建复合评分。
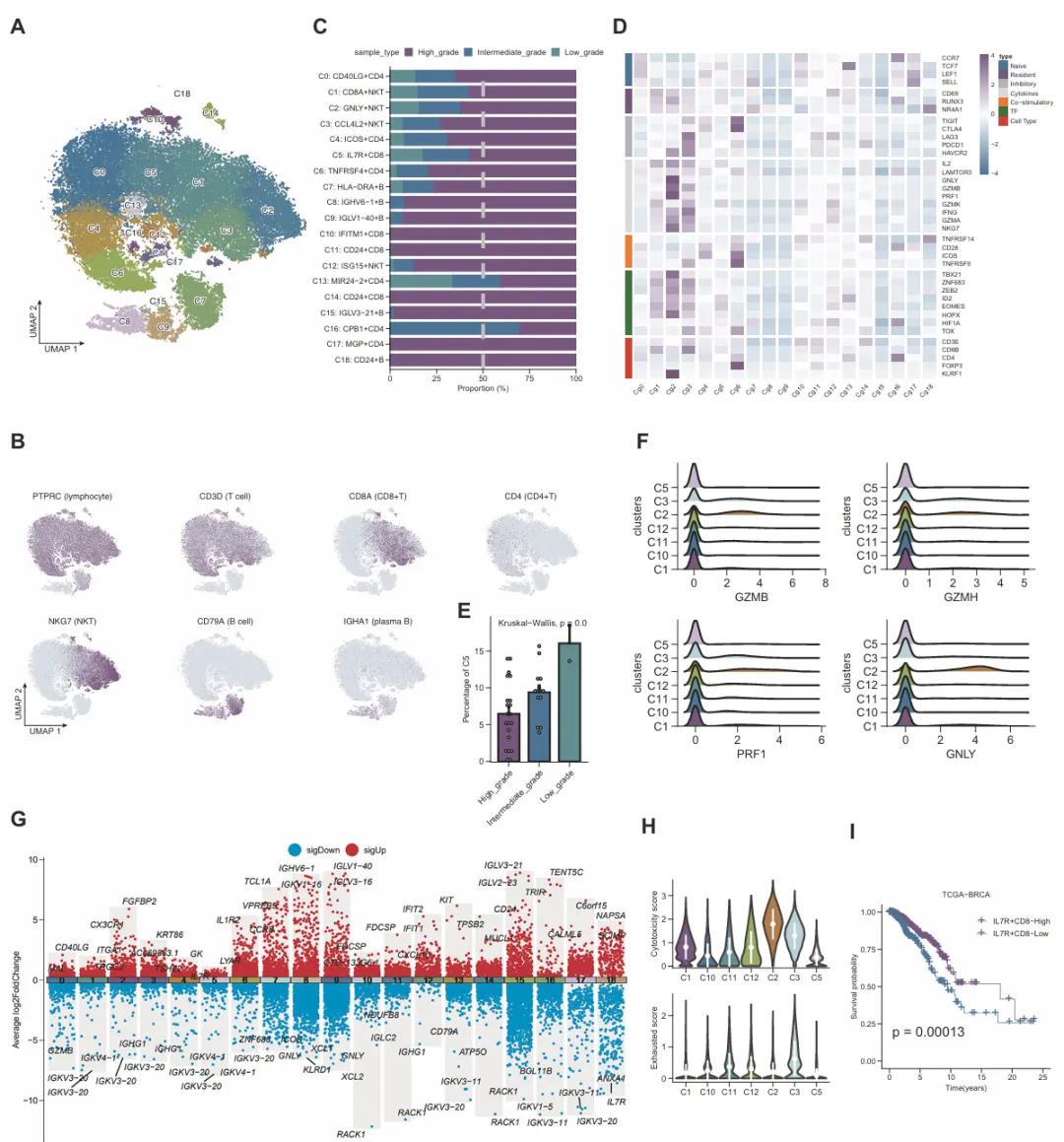
结果发现低级别富集亚型虽与良好预后相关,但显著关联免疫检查点抑制剂耐药,复合评分可同时预测预后和治疗响应。
这直接表明了该评分可作为乳腺癌精准分层的新型生物标志物。
04
讨论
这篇文章为“多组学整合的肿瘤微环境图谱”提供了可复用的高端模板,可带来以下启发:
一、“单细胞+空间+bulk反卷积”三组学整合范式:
scRNA-seq做细胞亚群发现和功能注释,空间转录组验证空间定位,TCGA bulk RNA-seq用BisqueRNA反卷积验证临床预后——三组学环环相扣,全部数据来自GEO和TCGA公开数据库,零实验成本即可构建完整的多组学证据链,可迁移至任何有公开数据的癌种。
二、TIDE免疫治疗预测为文章增加转化医学维度:
研究发现低级别富集亚群虽与良好预后相关,但TIDE预测却显示与免疫治疗不响应相关,这种“好预后但耐药”的反差叙事极具创新性。
任何做肿瘤微环境亚群分析的研究,只需在最后加一个TIDE预测,就能为文章增加“免疫治疗生物标志物”的转化医学卖点。
三、NicheNet+CellChat双工具解析细胞通讯:
研究先用NicheNet预测低级别富集亚群的配体-受体信号,再用CellChat量化整体通讯网络,发现高级别肿瘤中MDK和Galectin信号增强。
这种“靶向亚群通讯预测+全局通讯网络比较”的双层次分析策略,可在任何单细胞研究中提升机制深度和图表丰富度。
 你在临床中遇到过低级别乳腺癌却快速进展的病例吗?
你在临床中遇到过低级别乳腺癌却快速进展的病例吗?
 你还想了解哪些肿瘤的单细胞空间转录组研究?
你还想了解哪些肿瘤的单细胞空间转录组研究?
 告诉我你想看的高分文献方向(比如肿瘤免疫、多组学整合、生物标志物等),下期优先安排解析!
告诉我你想看的高分文献方向(比如肿瘤免疫、多组学整合、生物标志物等),下期优先安排解析!
在最末,我们还列出了往期推荐,同样拆解科研套路
感兴趣的可以来看看~


免费一对一线上交流,解决切实困难。
国家级、省市级等课题方案设计,
高分、高区SCI方案定制化设计。
生信统计分析、基础实验服务。
精准对接需求,定制科研方案。小助理:keti198
获取文献原文,可添加小助理~
往期推荐|
队列研究拿下1区TOP!UKB公开数据+多状态模型,首都医团队锁定心肾代谢共病预测指标!
 夜雨聆风
夜雨聆风