
点击蓝字 关注我们

在再生医学与生物创新药领域,细胞外囊泡(EVs)凭借独特的生物运载特性、低免疫原性及优异的组织修复能力,已成为全球生物医药重点研发方向。但长期以来,行业存在显著发展短板:全球范围内尚未形成统一、可落地、适配药物研发的标准化质量评价体系。
2026年,该项行业僵局迎来根本性突破。
中国食品药品检定研究院牵头整合国内顶尖科研力量,在国际细胞外囊泡学会(ISEV)顶级期刊 Journal of Extracellular Vesicles(JEV)发布干细胞源性细胞外囊泡治疗产品质量评价综述。该文献构建了适配国内产业环境、贴合药监审评逻辑的EVs药物全链条质控框架。
国家级监管机构定标、权威质控框架落地、产业化逻辑纳入行业标准,多重行业信号明确,标志着中国细胞外囊泡产业正式迈入质控可控、指标可评、产业化落地的标准化发展新阶段。


作为国家级药品生物制品质量检定权威机构,中检院发布的学术成果具备极强的监管指导性,是国内生物药审评审批的核心参考依据。本次顶刊综述发布,被界面新闻、经济观察报等权威行业媒体评定为:国内首套具备临床落地效力的细胞外囊泡药物官方质控框架。
过往全球EVs产业研发模式粗放,质控逻辑混乱,检测方法缺乏统一标准。多数研发主体缺乏系统化质控思维,生产工艺优化、临床试验申报均依赖经验摸索,研发试错成本居高不下。
本次综述创新性搭建全生命周期质量评价体系,质控节点贯穿细胞库建立、细胞培养、囊泡分离纯化、理化表征检测、杂质分析、生物效价评定、安全性验证、制剂稳定性管控、成品放行及批间一致性核查全流程。
文献明确九大核心关键质量属性(CQAs),涵盖物种溯源与标志物鉴定、粒径分布与Zeta电位、外源微生物污染、颗粒浓度、残留核酸与宿主蛋白、生物活性效价、免疫原性与促瘤风险、制剂理化参数等硬性审评指标。同时明确差异化质控原则:摒弃一刀切式固化标准,依据产品适应症、细胞来源、生产工艺、作用机理及风险等级,定制个性化质控方案。
该体系补齐了国内EVs药物研发的质控短板,打通临床申报核心卡点。中国经济新闻网专业评价:本次发布的质控框架完善了国内细胞外囊泡药物监管逻辑,同时为全球干细胞源性EVs药物研发提供了成熟的中国技术方案。
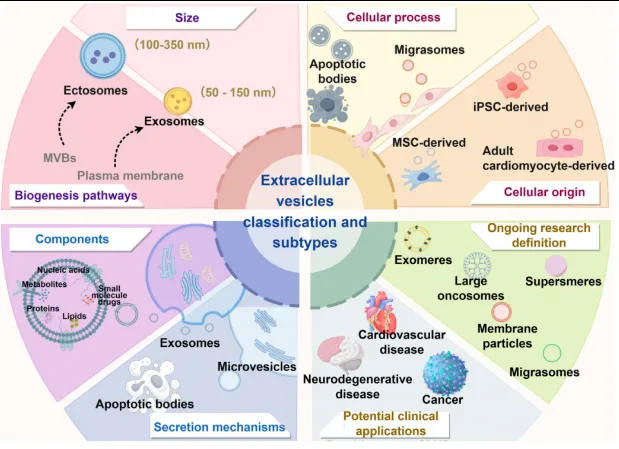

本次权威综述由中检院主导,联合多家顶尖科研机构共同完成,兼顾学术严谨性与工业落地性。标准体系能够贴合产业化生产要求,核心源于科研团队深耕EVs质量评价领域,深度结合国内生物医药产业化实操经验。
① 联动国家级监管平台,完善国标体系
本次研究团队长期配合中检院、国家药监局药品审评中心(CDE)开展监管科学研究。2024年,团队参与国家级重点专项,深耕干细胞及其衍生物创新药研发与监管评价技术;同步参与药物监管科学国家重点实验室专项课题,填补国内细胞外囊泡质量评价体系空白,助力行业标准从理论搭建到落地成型。
② 依托工业化生产数据,优化质控边界
药物级行业标准不能局限于实验室理论研究,必须适配规模化工业生产。目前国内头部生物医药企业已建成GMP标准化生产车间,搭建自动化纯化、单囊泡级别表征、多维活性检测技术平台,实现细胞外囊泡规模化、标准化生产。
科研团队整合国内大量工业化生产真实数据,将生产工艺痛点、杂质控制难点、质量波动边界纳入标准编制体系,实现质控标准科研严谨性与产业落地性双向统一。北京科技报刊文指出:本土产业化实操数据,是本次国家级质控框架成型的核心产业支撑。
③ 统一合规逻辑,降低行业研发试错成本
本次顶刊发文向产业端与资本市场释放关键信号:国内头部生物医药企业现行质控体系,已高度契合未来国家级审评标准。合规研发主体在自研管线推进、CRO/CDMO技术服务过程中,可有效规避合规风险,压缩申报周期,构建适配国内药监逻辑的研发通道。
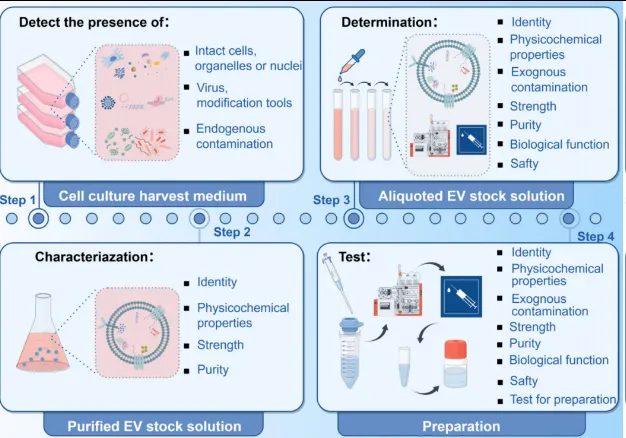

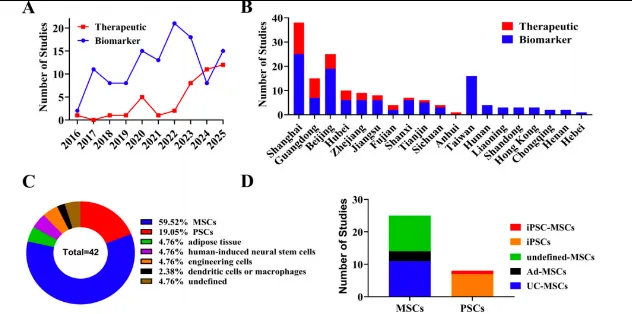
文献公开临床统计数据显示,截至2025年9月,国内机构在ClinicalTrials.gov平台注册的EVs相关研究共计161项,其中治疗类研究42项,整体研发规模仅次于美国,位列全球第二位。
行业增速态势显著:2016至2022年,国内治疗性细胞外囊泡研究仅11项;2023至2025年三年间,相关研究数量增长至此前三倍。从研发管线结构来看,95%的治疗管线采用天然干细胞源性囊泡,其中间充质干细胞(MSCs)占比达60%;国内研发产业高度集中,主要聚集于北京、上海、广东三大生物医药产业集群。
新华网行业分析指出:当前全球尚无获批上市的细胞外囊泡治疗药物,国内凭借标准先行、产业成熟、临床储备充足的优势,有望在生物创新药赛道实现弯道超车。

生物医药产业研发周期漫长、技术门槛严苛,细胞外囊泡作为新兴生物治疗载体,发展之路兼具挑战与机遇。
回望行业发展历程,国内细胞外囊泡产业从早期技术乱象、质控缺失的无序阶段,逐步走向国家定标、合规研发、规范生产的成熟阶段;从技术跟跑国外,到自主搭建国家级质控框架、输出中国行业标准,本土产业完成了关键性的蜕变升级。
道阻且长,行则将至。期待全行业坚守药品研发底线,以权威质控标准为依托、以核心技术为驱动力、以临床患者为核心导向,持续优化生产工艺、严控产品质量。聚力推动国产细胞外囊泡药物走出实验室、落地临床应用,助力中国生物创新药产业高质量发展,早日为全球患者提供全新的治疗方案。
文章来源与参考文献
Na, T. et al. Quality Evaluation Considerations for Stem Cell-Derived Extracellular Vesicles-Based Therapeutic Products in China. J Extracell Vesicles 15, e70297, 2026.
中国食品药品检定研究院:《干细胞外囊泡药物质量评价体系研究公告》,2026.
新华网:《瞭望 | 打造创新药发展加速器》,2026-04-08.
界面新闻:《药品级外囊泡质控行业白皮书观察》,2026-04.
经济观察报:《生物医药新规落地,外囊泡行业加速出清》,2026-03.
中国经济新闻网:《干细胞外囊泡临床研究进展报告》,2026-05-09.
北京科技报:《生物医药行业质控体系发展研究》,2025-01.


 夜雨聆风
夜雨聆风