文档内容
专练 19 氮及其化合物
授课提示:对应学生用书37页
一、选择题
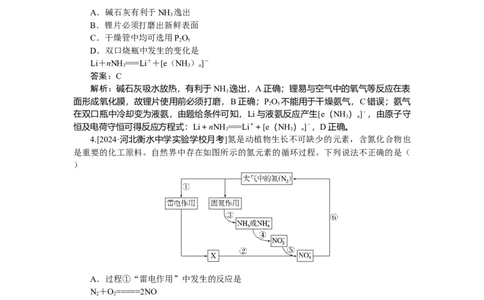
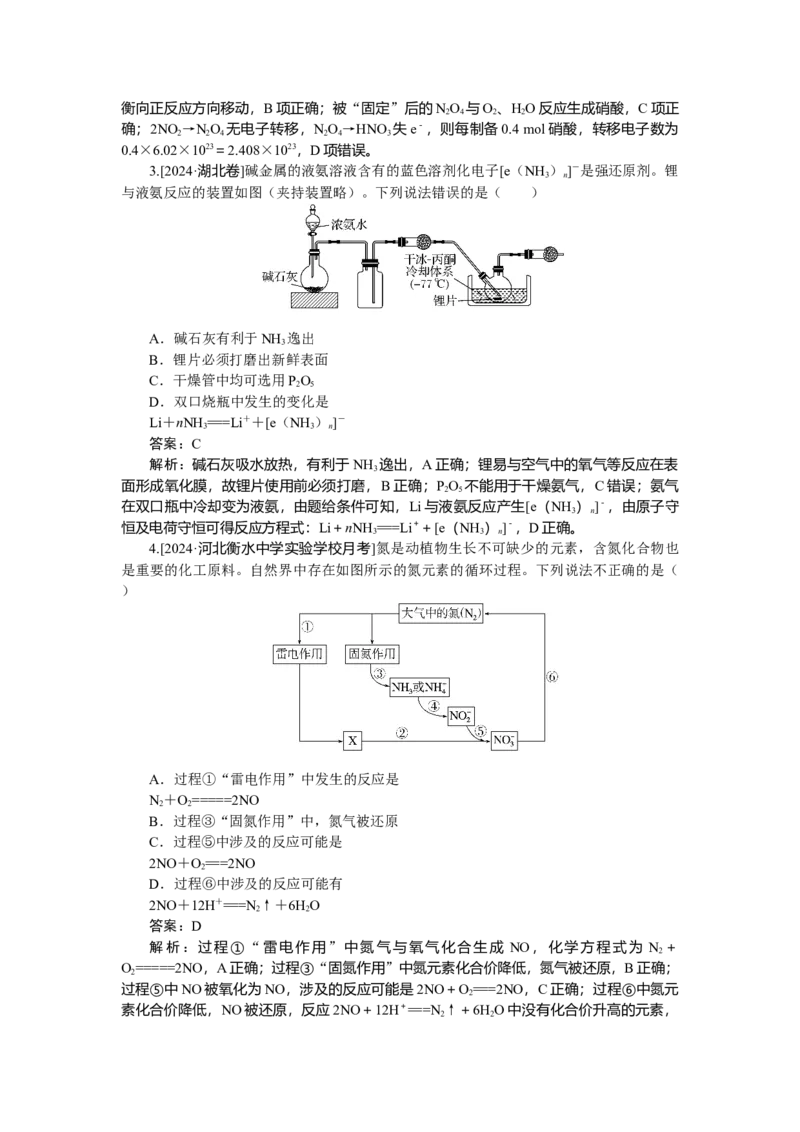
1.[2024·黑龙江省实验中学月考]价-类二维图是学习元素化合物的工具,a~g分别表
示氮元素的不同价态所对应的物质,其关系如图所示。下列说法正确的是( )
A.f属于强电解质
B.a可经过转化,最终制备出e
C.通常情况下b可与O 反应转化为d,造成空气污染
2
D.可用湿润的蓝色石蕊试纸检验g
答案:B
解析:由图可知,a为NH ,b为N ,c为NO,d为NO ,e为HNO ,f为NH ·H O,
3 2 2 3 3 2
g 为 含 NH 的 盐 。 NH ·H O 是 弱 碱 , 属 于 弱 电 解 质 , A 项 错 误 ; 经 过
3 2
NH →NO→NO →HNO,最终可以制备出硝酸,B项正确;氮气可与O 在放电或高温条件
3 2 3 2
下反应生成NO,不能直接生成NO ,C项错误;检验NH应用湿润的红色石蕊试纸,D项
2
错误。
2.[2022·北京卷]某MOFs多孔材料孔径大小和形状恰好将NO“固定”,能高选择性
2 4
吸附NO 。废气中的NO 被吸附后,经处理能全部转化为HNO。原理示意图如下。
2 2 3
已知:2NO
2
(g) ⇌N
2
O
4
(g) ΔH<0
下列说法不正确的是( )
A.温度升高时不利于NO 吸附
2
B.多孔材料“固定”N
2
O
4
,促进2NO 2⇌N
2
O
4
平衡正向移动
C.转化为HNO 的反应是2NO+O+2HO===4HNO
3 2 4 2 2 3
D.每获得0.4 mol HNO 时,转移电子的数目为6.02×1022
3
答案:D
解析:2NO
2
(g)⇌N
2
O
4
(g)为放热反应,升高温度,平衡向逆反应方向移动,不利
于NO
2
吸附,A项正确;N
2
O
4
被“固定”后,N
2
O
4
的浓度减小,2NO
2
(g)⇌N
2
O
4
(g)平衡向正反应方向移动,B项正确;被“固定”后的NO 与O 、HO反应生成硝酸,C项正
2 4 2 2
确;2NO →NO 无电子转移,NO→HNO 失e-,则每制备0.4 mol硝酸,转移电子数为
2 2 4 2 4 3
0.4×6.02×1023=2.408×1023,D项错误。
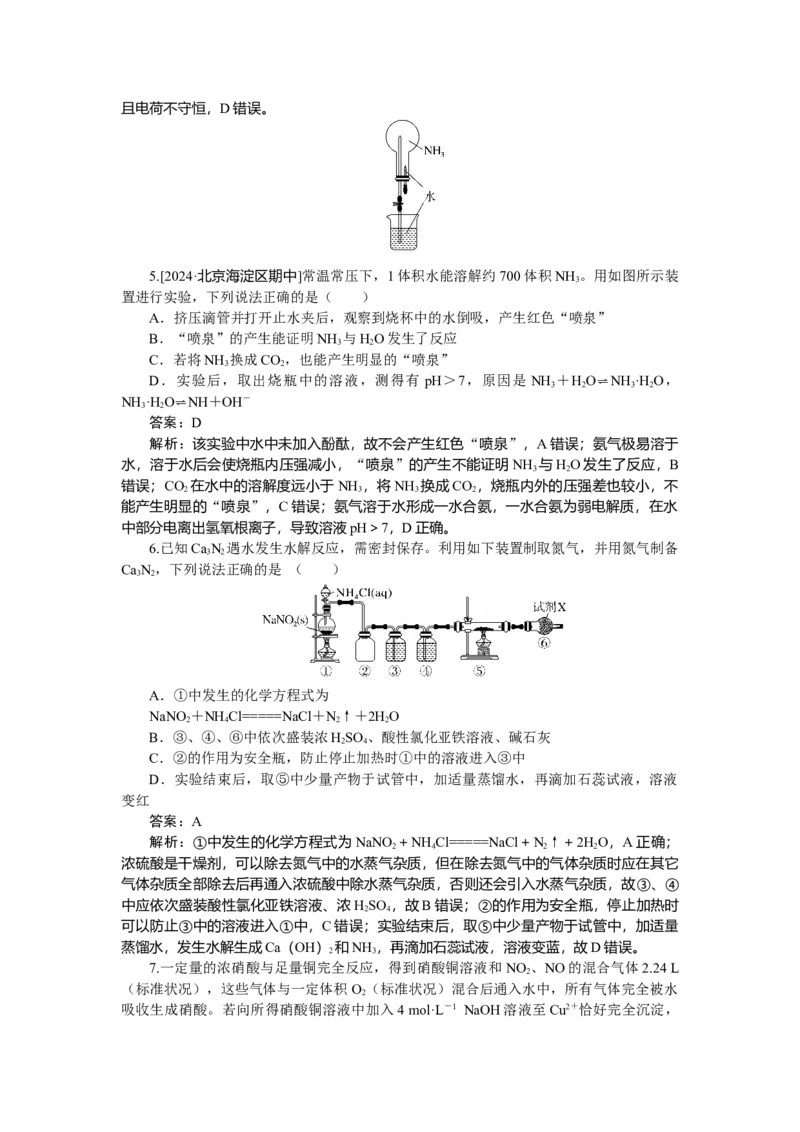
3.[2024·湖北卷]碱金属的液氨溶液含有的蓝色溶剂化电子[e(NH )]-是强还原剂。锂
3 n
与液氨反应的装置如图(夹持装置略)。下列说法错误的是( )
A.碱石灰有利于NH 逸出
3
B.锂片必须打磨出新鲜表面
C.干燥管中均可选用PO
2 5
D.双口烧瓶中发生的变化是
Li+nNH ===Li++[e(NH )]-
3 3 n
答案:C
解析:碱石灰吸水放热,有利于NH 逸出,A正确;锂易与空气中的氧气等反应在表
3
面形成氧化膜,故锂片使用前必须打磨,B正确;PO 不能用于干燥氨气,C错误;氨气
2 5
在双口瓶中冷却变为液氨,由题给条件可知,Li与液氨反应产生[e(NH ) ]-,由原子守
3 n
恒及电荷守恒可得反应方程式:Li+nNH ===Li++[e(NH )]-,D正确。
3 3 n
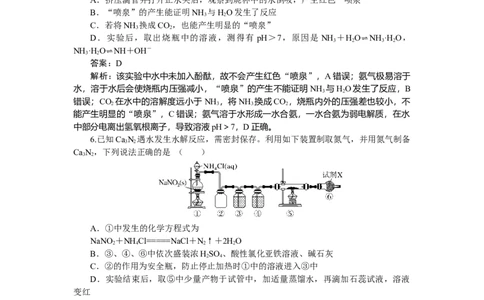
4.[2024·河北衡水中学实验学校月考]氮是动植物生长不可缺少的元素,含氮化合物也
是重要的化工原料。自然界中存在如图所示的氮元素的循环过程。下列说法不正确的是(
)
A.过程①“雷电作用”中发生的反应是
N+O=====2NO
2 2
B.过程③“固氮作用”中,氮气被还原
C.过程⑤中涉及的反应可能是
2NO+O===2NO
2
D.过程⑥中涉及的反应可能有
2NO+12H+===N ↑+6HO
2 2
答案:D
解析:过程①“雷电作用”中氮气与氧气化合生成 NO,化学方程式为 N +
2
O=====2NO,A正确;过程③“固氮作用”中氮元素化合价降低,氮气被还原,B正确;
2
过程⑤中NO被氧化为NO,涉及的反应可能是2NO+O===2NO,C正确;过程⑥中氮元
2
素化合价降低,NO被还原,反应2NO+12H+===N ↑+6HO中没有化合价升高的元素,
2 2且电荷不守恒,D错误。
5.[2024·北京海淀区期中]常温常压下,1体积水能溶解约700体积NH 。用如图所示装
3
置进行实验,下列说法正确的是( )
A.挤压滴管并打开止水夹后,观察到烧杯中的水倒吸,产生红色“喷泉”
B.“喷泉”的产生能证明NH 与HO发生了反应
3 2
C.若将NH 换成CO,也能产生明显的“喷泉”
3 2
D.实验后,取出烧瓶中的溶液,测得有 pH>7,原因是 NH
3
+H
2
O⇌NH
3
·H
2
O,
NH
3
·H
2
O⇌NH+OH-
答案:D
解析:该实验中水中未加入酚酞,故不会产生红色“喷泉”,A错误;氨气极易溶于
水,溶于水后会使烧瓶内压强减小,“喷泉”的产生不能证明NH 与HO发生了反应,B
3 2
错误;CO 在水中的溶解度远小于NH ,将NH 换成CO ,烧瓶内外的压强差也较小,不
2 3 3 2
能产生明显的“喷泉”,C错误;氨气溶于水形成一水合氨,一水合氨为弱电解质,在水
中部分电离出氢氧根离子,导致溶液pH>7,D正确。
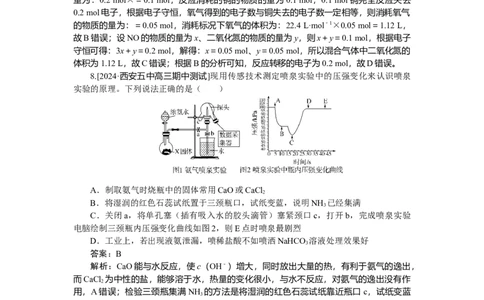
6.已知Ca N 遇水发生水解反应,需密封保存。利用如下装置制取氮气,并用氮气制备
3 2
Ca N,下列说法正确的是 ( )
3 2
A.①中发生的化学方程式为
NaNO +NH Cl=====NaCl+N↑+2HO
2 4 2 2
B.③、④、⑥中依次盛装浓HSO 、酸性氯化亚铁溶液、碱石灰
2 4
C.②的作用为安全瓶,防止停止加热时①中的溶液进入③中
D.实验结束后,取⑤中少量产物于试管中,加适量蒸馏水,再滴加石蕊试液,溶液
变红
答案:A
解析:①中发生的化学方程式为NaNO +NH Cl=====NaCl+N↑+2HO,A正确;
2 4 2 2
浓硫酸是干燥剂,可以除去氮气中的水蒸气杂质,但在除去氮气中的气体杂质时应在其它
气体杂质全部除去后再通入浓硫酸中除水蒸气杂质,否则还会引入水蒸气杂质,故③、④
中应依次盛装酸性氯化亚铁溶液、浓HSO ,故B错误;②的作用为安全瓶,停止加热时
2 4
可以防止③中的溶液进入①中,C错误;实验结束后,取⑤中少量产物于试管中,加适量
蒸馏水,发生水解生成Ca(OH) 和NH ,再滴加石蕊试液,溶液变蓝,故D错误。
2 3
7.一定量的浓硝酸与足量铜完全反应,得到硝酸铜溶液和NO 、NO的混合气体2.24 L
2
(标准状况),这些气体与一定体积O (标准状况)混合后通入水中,所有气体完全被水
2
吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50 mL,下列说法正确的是( )
A.参加反应的硝酸是0.3 mol
B.消耗氧气的体积为1.68 L
C.混合气体中含NO 2.24 L
2
D.此反应过程中转移的电子为0.3 mol
答案:A
解析:标况下2.24 L混合气体的物质的量为0.1 mol;50 mL 4 mol·L-1的氢氧化钠溶液
中氢氧化钠的物质的量为:4 mol·L-1×0.05 L=0.2 mol。铜离子恰好沉淀时,反应后的溶
质为硝酸钠,根据钠离子守恒可知硝酸钠中硝酸根离子的物质的量为 0.2 mol,根据氮原子
守恒可得硝酸的物质的量为0.1 mol+0.2 mol=0.3 mol,故A正确;生成氢氧化铜的物质的
量为:0.2 mol×=0.1 mol,反应消耗的铜的物质的量为0.1 mol,0.1 mol铜完全反应失去
0.2 mol电子,根据电子守恒,氧气得到的电子数与铜失去的电子数一定相等,则消耗氧气
的物质的量为:=0.05 mol,消耗标况下氧气的体积为:22.4 L·mol-1×0.05 mol=1.12 L,
故B错误;设NO的物质的量为x、二氧化氮的物质的量为y,则x+y=0.1 mol,根据电子
守恒可得:3x+y=0.2 mol,解得:x=0.05 mol、y=0.05 mol,所以混合气体中二氧化氮的
体积为1.12 L,故C错误;根据B的分析可知,反应转移的电子为0.2 mol,故D错误。
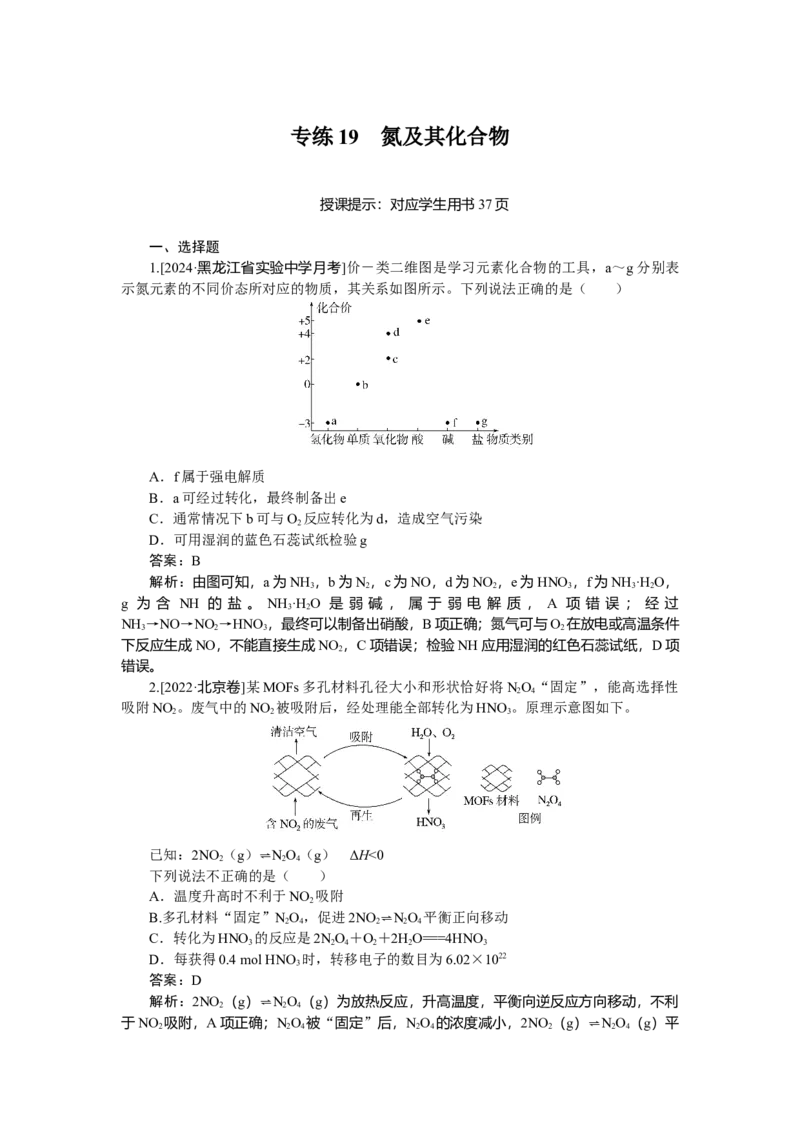
8.[2024·西安五中高三期中测试]现用传感技术测定喷泉实验中的压强变化来认识喷泉
实验的原理。下列说法正确的是( )
A.制取氨气时烧瓶中的固体常用CaO或CaCl
2
B.将湿润的红色石蕊试纸置于三颈瓶口,试纸变蓝,说明NH 已经集满
3
C.关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验
电脑绘制三颈瓶内压强变化曲线如图2,则E点时喷泉最剧烈
D.工业上,若出现液氨泄漏,喷稀盐酸不如喷洒NaHCO 溶液处理效果好
3
答案:B
解析:CaO能与水反应,使c(OH-)增大,同时放出大量的热,有利于氨气的逸出,
而CaCl 为中性的盐,能够溶于水,热量的变化很小,与水不反应,对氨气的逸出没有作
2
用,A错误;检验三颈瓶集满NH 的方法是将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝
3
色,证明 NH 已收集满,B正确;三颈瓶内气体与外界大气压压强之差越大,其反应速率
3
越快,C点压强最小、大气压不变,所以大气压和C点压强差最大,则喷泉越剧烈,C错
误;盐酸显酸性,碳酸氢钠溶液显碱性,氨水溶液显碱性,因此氨气在酸性溶液中的吸收
效率高于碱性溶液中的吸收效率,D错误。
二、非选择题
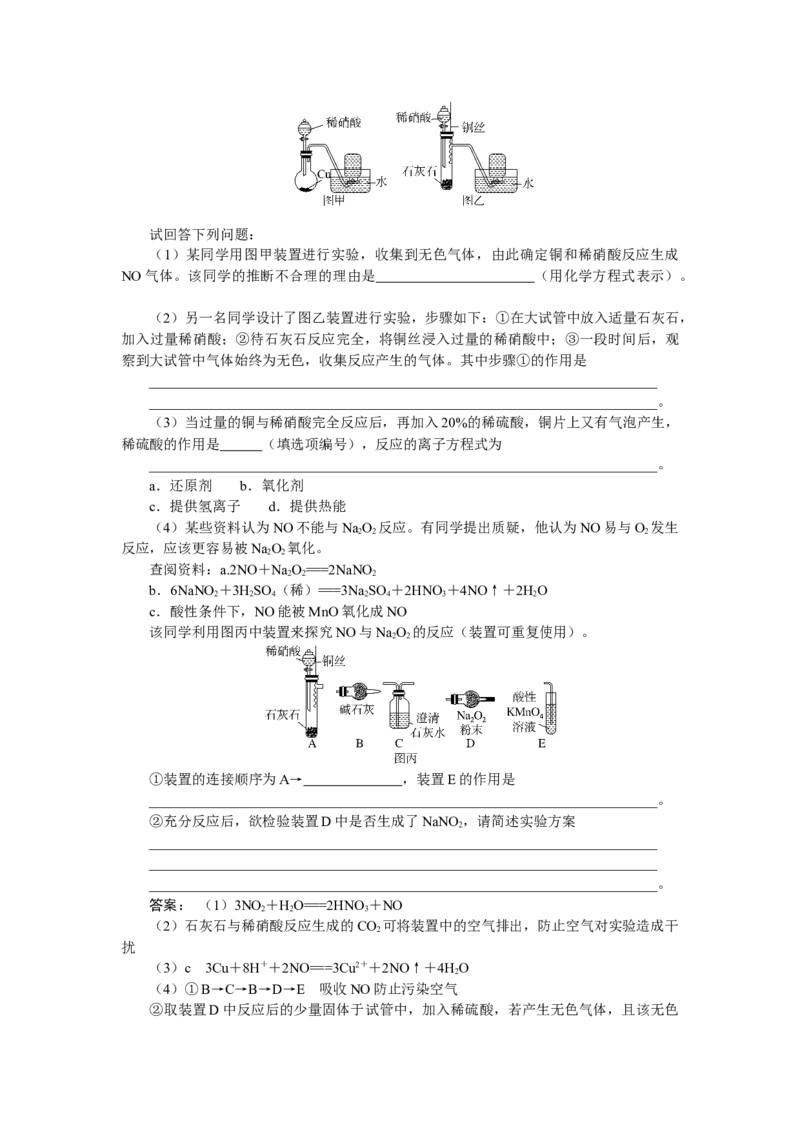
9.某研究性学习小组的同学为了制取NO并探究其性质,进行了如下实验。试回答下列问题:
(1)某同学用图甲装置进行实验,收集到无色气体,由此确定铜和稀硝酸反应生成
NO气体。该同学的推断不合理的理由是 (用化学方程式表示)。
(2)另一名同学设计了图乙装置进行实验,步骤如下:①在大试管中放入适量石灰石,
加入过量稀硝酸;②待石灰石反应完全,将铜丝浸入过量的稀硝酸中;③一段时间后,观
察到大试管中气体始终为无色,收集反应产生的气体。其中步骤①的作用是
________________________________________________________________________
________________________________________________________________________。
(3)当过量的铜与稀硝酸完全反应后,再加入20%的稀硫酸,铜片上又有气泡产生,
稀硫酸的作用是 (填选项编号),反应的离子方程式为
________________________________________________________________________。
a.还原剂 b.氧化剂
c.提供氢离子 d.提供热能
(4)某些资料认为NO不能与NaO 反应。有同学提出质疑,他认为NO易与O 发生
2 2 2
反应,应该更容易被NaO 氧化。
2 2
查阅资料:a.2NO+NaO===2NaNO
2 2 2
b.6NaNO +3HSO (稀)===3Na SO +2HNO+4NO↑+2HO
2 2 4 2 4 3 2
c.酸性条件下,NO能被MnO氧化成NO
该同学利用图丙中装置来探究NO与NaO 的反应(装置可重复使用)。
2 2
①装置的连接顺序为A→ ,装置E的作用是
________________________________________________________________________。
②充分反应后,欲检验装置D中是否生成了NaNO ,请简述实验方案
2
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
答案: (1)3NO +HO===2HNO +NO
2 2 3
(2)石灰石与稀硝酸反应生成的CO 可将装置中的空气排出,防止空气对实验造成干
2
扰
(3)c 3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
(4)①B→C→B→D→E 吸收NO防止污染空气
②取装置D中反应后的少量固体于试管中,加入稀硫酸,若产生无色气体,且该无色气体在试管口上方变为红棕色,则证明生成了NaNO
2
解析:(1)由于NO 能与水发生反应:3NO +HO===2HNO +NO,所以题图甲装置
2 2 2 3
中即使有NO 生成,集气瓶中收集到的也是无色的NO,故该同学的推断不合理。
2
(2)由于2NO+O===2NO,利用石灰石与稀硝酸反应生成的CO 能将装置中的空气
2 2 2
排出,从而防止空气对实验造成干扰。
(3)铜过量时,溶液中的HNO 完全反应,生成Cu(NO ) ,在溶液中加入稀硫酸,
3 3 2
提供H+,N继续氧化Cu。
(4)①根据实验目的,装置的连接顺序为NO发生装置A→气体净化装置(包括除去
CO 的装置B、检验CO 是否除尽的装置C和干燥装置B)→NO与NaO 的反应装置D→
2 2 2 2
尾气处理装置E。②可利用查阅资料b中的反应检验装置D中是否生成了NaNO 。
2