文档内容
专练 25 元素周期表及其应用
授课提示:对应学生用书49页
一、选择题
1.[2024·全国甲卷]W、X、Y、Z为原子序数依次增大的短周期元素。W和X原子序
数之和等于Y-的核外电子数,化合物W+[ZY]-可用作化学电源的电解质。下列叙述正确
6
的是( )
A.X和Z属于同一主族
B.非金属性:X>Y>Z
C.气态氢化物的稳定性:Z>Y
D.原子半径:Y>X>W
答案:A
解析:N和P均位于第ⅤA族,A正确;同周期元素从左到右,元素的非金属性逐渐
增强,同主族元素从上到下,元素的非金属性逐渐减弱,故非金属性:F>N>P,B错误;
元素的非金属性越强,对应的简单气态氢化物越稳定,非金属性:F>P,故稳定性:
HF>PH ,C 错误;同周期主族元素从左到右,原子半径逐渐减小,故原子半径:
3
Li>N>F,D错误。
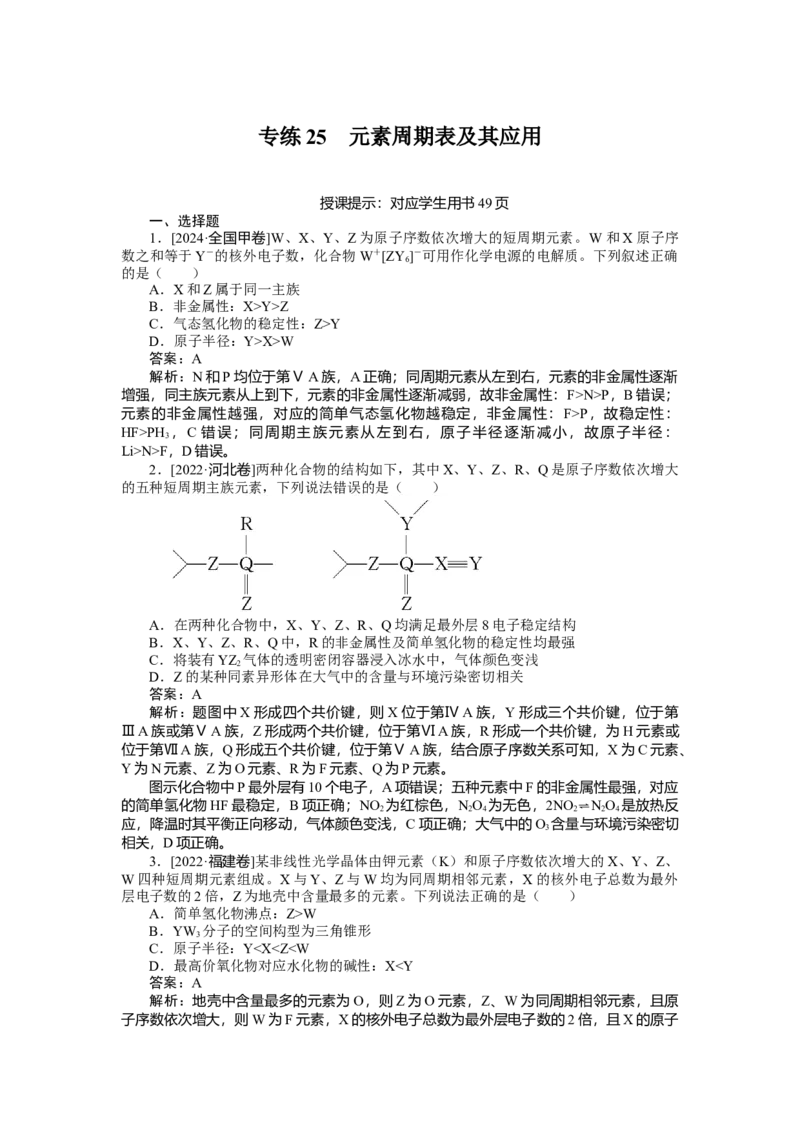
2.[2022·河北卷]两种化合物的结构如下,其中X、Y、Z、R、Q是原子序数依次增大
的五种短周期主族元素,下列说法错误的是( )
A.在两种化合物中,X、Y、Z、R、Q均满足最外层8电子稳定结构
B.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强
C.将装有YZ 气体的透明密闭容器浸入冰水中,气体颜色变浅
2
D.Z的某种同素异形体在大气中的含量与环境污染密切相关
答案:A
解析:题图中X形成四个共价键,则X位于第ⅣA族,Y形成三个共价键,位于第
ⅢA族或第ⅤA族,Z形成两个共价键,位于第ⅥA族,R形成一个共价键,为H元素或
位于第ⅦA族,Q形成五个共价键,位于第ⅤA族,结合原子序数关系可知,X为C元素、
Y为N元素、Z为O元素、R为F元素、Q为P元素。
图示化合物中P最外层有10个电子,A项错误;五种元素中F的非金属性最强,对应
的简单氢化物HF最稳定,B项正确;NO
2
为红棕色,N
2
O
4
为无色,2NO 2⇌N
2
O
4
是放热反
应,降温时其平衡正向移动,气体颜色变浅,C项正确;大气中的O 含量与环境污染密切
3
相关,D项正确。
3.[2022·福建卷]某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、
W四种短周期元素组成。X与Y、Z与W均为同周期相邻元素,X的核外电子总数为最外
层电子数的2倍,Z为地壳中含量最多的元素。下列说法正确的是( )
A.简单氢化物沸点:Z>W
B.YW 分子的空间构型为三角锥形
3
C.原子半径:YHF,A正确;BF 中B原子
2 3
的价层电子对数为3+×(3-3×1)=3,无孤电子对,则BF 的空间构型为平面三角形,
3
B 错误;同周期主族元素从左到右原子半径逐渐减小,则原子半径大小顺序为
Be>B>O>F,C错误;碱性:Be(OH)>H BO,D错误。
2 3 3
4.
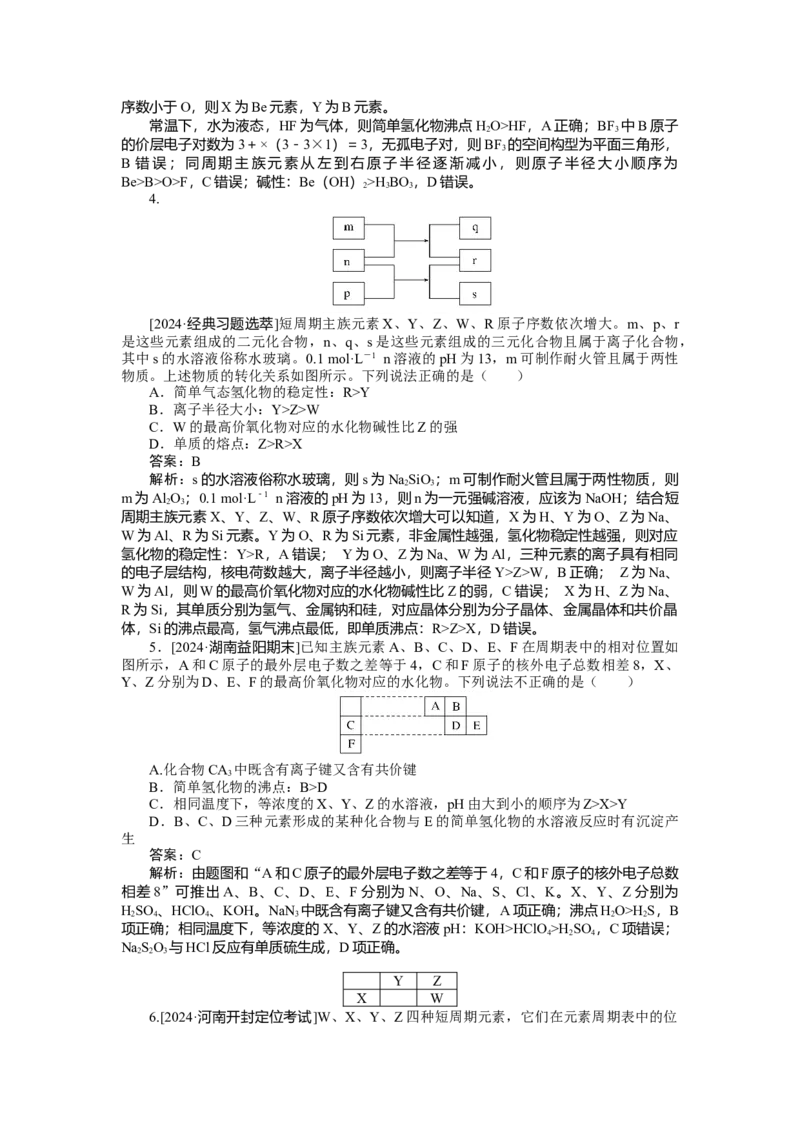
[2024·经典习题选萃]短周期主族元素X、Y、Z、W、R原子序数依次增大。m、p、r
是这些元素组成的二元化合物,n、q、s是这些元素组成的三元化合物且属于离子化合物,
其中s的水溶液俗称水玻璃。0.1 mol·L-1 n溶液的pH为13,m可制作耐火管且属于两性
物质。上述物质的转化关系如图所示。下列说法正确的是( )
A.简单气态氢化物的稳定性:R>Y
B.离子半径大小:Y>Z>W
C.W的最高价氧化物对应的水化物碱性比Z的强
D.单质的熔点:Z>R>X
答案:B
解析:s的水溶液俗称水玻璃,则s为NaSiO ;m可制作耐火管且属于两性物质,则
2 3
m为Al O ;0.1 mol·L-1 n溶液的pH为13,则n为一元强碱溶液,应该为NaOH;结合短
2 3
周期主族元素X、Y、Z、W、R原子序数依次增大可以知道,X为H、Y为O、Z为Na、
W为Al、R为Si元素。Y为O、R为Si元素,非金属性越强,氢化物稳定性越强,则对应
氢化物的稳定性:Y>R,A错误; Y为O、Z为Na、W为Al,三种元素的离子具有相同
的电子层结构,核电荷数越大,离子半径越小,则离子半径Y>Z>W,B正确; Z为Na、
W为Al,则W的最高价氧化物对应的水化物碱性比Z的弱,C错误; X为H、Z为Na、
R为Si,其单质分别为氢气、金属钠和硅,对应晶体分别为分子晶体、金属晶体和共价晶
体,Si的沸点最高,氢气沸点最低,即单质沸点:R>Z>X,D错误。
5.[2024·湖南益阳期末]已知主族元素A、B、C、D、E、F在周期表中的相对位置如
图所示,A和C原子的最外层电子数之差等于4,C和F原子的核外电子总数相差8,X、
Y、Z分别为D、E、F的最高价氧化物对应的水化物。下列说法不正确的是( )
A.化合物CA 中既含有离子键又含有共价键
3
B.简单氢化物的沸点:B>D
C.相同温度下,等浓度的X、Y、Z的水溶液,pH由大到小的顺序为Z>X>Y
D.B、C、D三种元素形成的某种化合物与E的简单氢化物的水溶液反应时有沉淀产
生
答案:C
解析:由题图和“A和C原子的最外层电子数之差等于4,C和F原子的核外电子总数
相差8”可推出A、B、C、D、E、F分别为N、O、Na、S、Cl、K。X、Y、Z分别为
HSO 、HClO 、KOH。NaN 中既含有离子键又含有共价键,A项正确;沸点HO>HS,B
2 4 4 3 2 2
项正确;相同温度下,等浓度的X、Y、Z的水溶液pH:KOH>HClO >H SO ,C项错误;
4 2 4
NaSO 与HCl反应有单质硫生成,D项正确。
2 2 3
Y Z
X W
6.[2024·河南开封定位考试]W、X、Y、Z四种短周期元素,它们在元素周期表中的位置如图所示,其中W元素的原子序数为Z元素原子序数的两倍,则下列说法正确的是(
)
A.X、Z、Y三种元素对应原子的半径依次减小
B.X位于元素周期表中的第3周期第ⅣA族
C.HYO 的酸性强于HWO,故W元素的非金属性弱于Y
3 2 3
D.X和Y可分别与Z形成XZ 和YZ,它们的结构和化学性质相似
2 2
答案:B
解析:由于该四种元素均是短周期元素,W元素的原子序数为Z元素原子序数的两倍,
且W与Z同主族,原子序数相差8,故Z为O,W为S,则X为Si,Y为N。同周期主族
元素的原子半径从左到右依次减小,同主族元素的原子半径从上到下依次增大,故半径:r
(X)>r(Y)>r(Z),A错误; X为硅,位于元素周期表中第三周期第ⅣA族,B正确;
比较元素非金属性的强弱时应比较其最高价氧化物对应的水化物的酸性强弱,C错误;
SiO 和NO 的结构和化学性质均不相似,D错误。
2 2
7.[2024·湖北鄂东南省级示范高中期中]门捷列夫曾经说过:“从积累的事实得出结论
就是理论;而理论使我们能够预见事实”。2016年IUPAC确认了四种新元素,其中一种为
Mc,中文名“镆”。元素Mc可由反应:Am+Ca―→Mc+3n得到。下列有关说法正确的
是( )
A.Mc原子的质子数为115
B.287Mc与288Mc互为同素异形体
C.Ca原子的中子数为20
D.Mc元素位于元素周期表中第ⅥA族
答案:A
解析:Mc质子数为115,质量数为281,A项正确;287Mc与288Mc互为同位素,B项
错误;Ca原子的中子数为41-20=21,C项错误;Mc元素原子序数为115,位于元素周
期表中第ⅤA族,D项错误。
8.
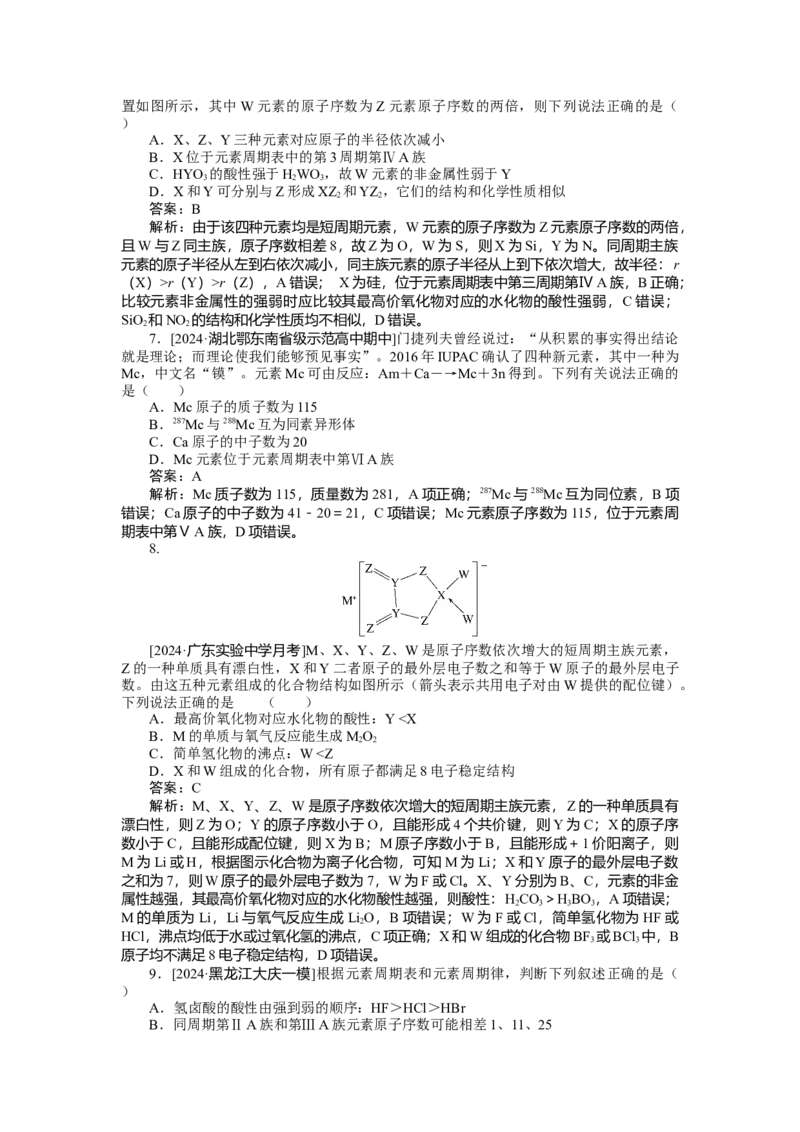
[2024·广东实验中学月考]M、X、Y、Z、W是原子序数依次增大的短周期主族元素,
Z的一种单质具有漂白性,X和Y二者原子的最外层电子数之和等于W原子的最外层电子
数。由这五种元素组成的化合物结构如图所示(箭头表示共用电子对由W提供的配位键)。
下列说法正确的是 ( )
A.最高价氧化物对应水化物的酸性:Y Y>Z>M>X
B.N的一种氧化物可用作油漆和涂料
C.氢化物的沸点:Z小于M
D.工业上制备W单质的方法为电解熔融的W的氧化物
答案:D
解析:由题意可知X为H,W原子核外电子数是M原子最外层电子数的2倍,则M
为O元素,W为Mg元素,Y、Z分别为C、N元素;N是用量最多的金属元素,则N为
Fe。同周期主族元素自左而右原子半径减小, 同主族元素自上而下原子半径增大,故原子
半径Mg>C>N>O>H,A正确;Fe O 可用作油漆和涂料,B正确;NH 的沸点小于HO,C
2 3 3 2
正确;工业上制备Mg单质的方法为电解熔融的MgCl ,D错误。
2
二、非选择题
13.[2024·江西红色七校联考]短周期元素W、X、Y、Z、M原子序数依次增大,元素
W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,Z与M同主族,Z2-
电子层结构与氖原子相同。
(1)M在元素周期表中的位置是 。
(2)化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl 溶液,溶液
3
变血红色;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸变蓝的气体。p
的化学式为__________________________________________________________________。
(3)由X、Y、Z三种元素可组成摩尔质量为84 g·mol-1的物质q,且q分子中三种元
素的原子个数之比为1∶1∶1。已知q分子中各原子均达到8电子稳定结构,且分子中不含
双键,但含极性键和非极性键,q分子的结构式为 。
(4)(XY) 的性质与Cl 相似,(XY) 与NaOH溶液常温下反应的离子方程式为
2 2 2
。
(5)常温下,1 mol Z 能与Y的最简单氢化物反应,生成一种常见的盐和1 mol Z ,
3 2
该反应的化学方程式为_________________________________________________________。
答案:(1)第三周期第ⅥA 族 (2)NH SCN
4
(3) N≡C—O—O—C≡N
(4)(CN)+2OH-===CN-+CNO-+HO
2 2
(5)2NH +4O===NHNO +4O+HO
3 3 4 3 2 2
解析:元素W的一种核素的中子数为0,W是H元素;X的原子最外层电子数是次外
层的2倍,X是C元素;Z2-电子层结构与氖相同,Z是O元素;M是S元素。W、X、
Y、Z、M的原子序数依次增大,Y是N元素。
(1)S位于元素周期表中第三周期第ⅥA族;
(2)化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl 溶液,溶液
3
变血红色p中含有SCN-;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸
变蓝的气体,p中含有NH。p的化学式为NH SCN。(3)由X、Y、Z三种元素可组成摩
4
尔质量为84 g·mol-1的物质q,且q分子中三种元素的原子个数之比为1∶1∶1。已知q分
子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子
的结构式为N≡C—O—O—C≡N。(4)(CN) 的性质与Cl 相似,根据氯气与氢氧化钠
2 2
反应,(CN) 与NaOH溶液反应的离子方程式为(CN) +2OH-===CN-+CNO-+
2 2
HO。(5)常温下,1 mol O 能与氨气反应,生成一种常见的盐NH NO 和1 mol O ,该反
2 3 4 3 2
应的化学方程式为:2NH +4O===NHNO +4O+HO。
3 3 4 3 2 2