文档内容
二○一○年福州市初中毕业会考、高级中等学校招生考试
班级 姓名 座号
一、选择题(本题包含l0小题,每小题3分,共30分。)
1.生活离不开化学,下列生活习惯或做法合理的是( )
A.菜刀用后洗净擦干 B.废旧电池随意丢弃
C.霉变大米洗净后继续食用 D.尽可能多吃含微量元素的保健品
2.我国饮用矿泉水的基本类别是碳酸水、硅酸水和锶水。此外还有锌、锂、溴、碘及硒矿泉
水等,这里的锌、锂、溴、碘、硒是指( )
A.原子 B.分子 C.元素 D.单质
3.图l所示实验主要说明( )
A.分子很小 B.分子间有间隔
C.分子不断运动 D.分子可以分成原子
4.尿素[CO(NH)]是一种常见的化学肥料,它属于( )
2 2
A.钾肥 B.磷肥 C.氮肥 D.复合肥
5.下列物质的用途利用其化学性质的是( )
A.石墨作铅笔芯 B.金刚石作钻头 C.干冰作致冷剂 D.天然气作燃料
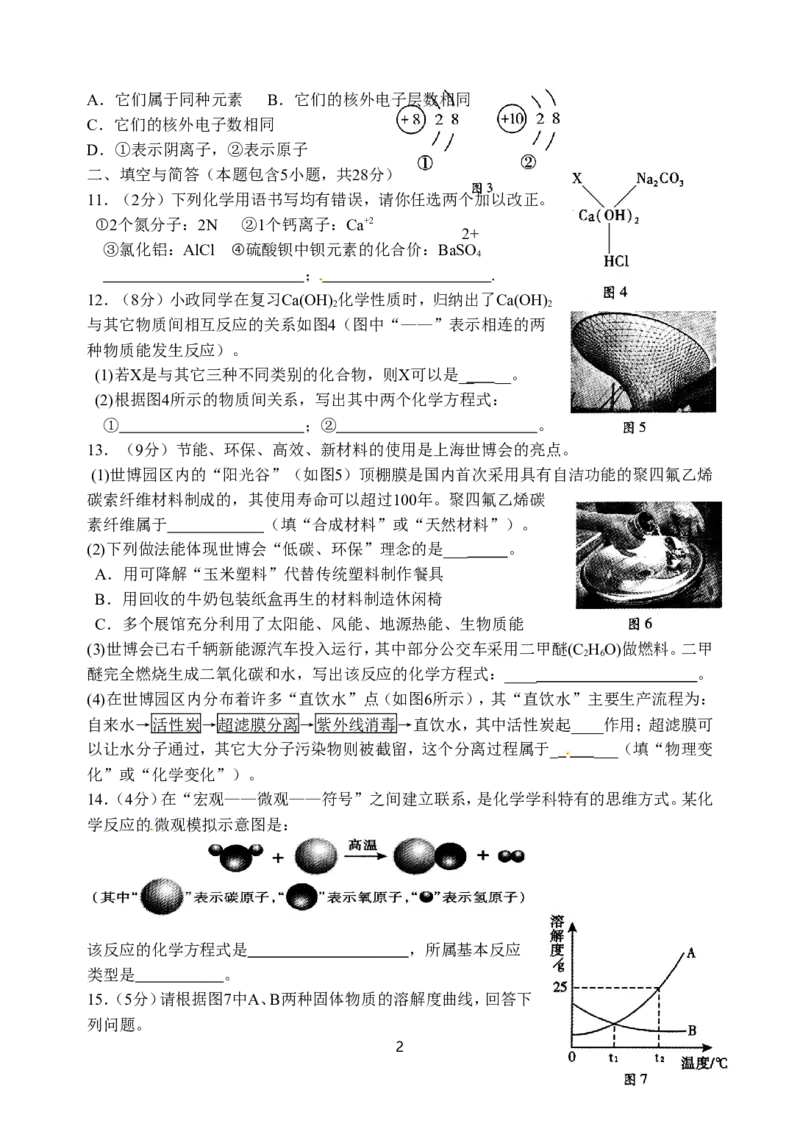
6.下列实验操作正确的是( )
7.下列人体体液中,酸性最强的是( )
A B C D
体液 唾液 血液 胆汁 胃液
pH范围 6.6 -7.1 7. 35 -7.45 6.8 -7.4 0.8 -1.5
8.英国科技人员研制出自动灭火陶瓷砖,砖里压入了一定量的氦气和二氧化碳。这种砖砌
成的房屋发生火灾时,在高温烘烧下,砖会裂开并喷出氦气和二氧化碳,从而抑制和扑灭火
焰。自动灭火陶瓷砖的灭火原理是( )
A.清除可燃物 B.使燃烧物与氧气隔绝
C.降低燃烧物的着火点 D.使燃烧物的温度降低到着火点以下
9.当空气受SO 严重污染时,可通过飞机喷洒X粉末,使空气中的SO 含量明显降低,该过程
2 2
发生的反应是2X +2SO+O=2CaSO +2CO。X的化学式是( )
2 2 4 2
A.CaO B.CaCO C.Ca(OH) D.NaCO
3 2 2 3
10.从图3所示的两种微粒结构示意图中,所获取信息不正确的是( )
1A.它们属于同种元素 B.它们的核外电子层数相同
C.它们的核外电子数相同
D.①表示阴离子,②表示原子
二、填空与简答(本题包含5小题,共28分)
11.(2分)下列化学用语书写均有错误,请你任选两个加以改正。
①2个氮分子:2N ②1个钙离子:Ca+2
2+
③氯化铝:AlCl ④硫酸钡中钡元素的化合价:BaSO
4
; .
12.(8分)小政同学在复习Ca(OH) 化学性质时,归纳出了Ca(OH)
2 2
与其它物质间相互反应的关系如图4(图中“——”表示相连的两
种物质能发生反应)。
[来源:学§科§网Z§X§X§K]
(1)若X是与其它三种不同类别的化合物,则X可以是__ __。
(2)根据图4所示的物质间关系,写出其中两个化学方程式:
① ;② 。
13.(9分)节能、环保、高效、新材料的使用是上海世博会的亮点。
(1)世博园区内的“阳光谷”(如图5)顶棚膜是国内首次采用具有自洁功能的聚四氟乙烯
碳索纤维材料制成的,其使用寿命可以超过100年。聚四氟乙烯碳
素纤维属于 (填“合成材料”或“天然材料”)。
(2)下列做法能体现世博会“低碳、环保”理念的是___ 。
A.用可降解“玉米塑料”代替传统塑料制作餐具
B.用回收的牛奶包装纸盒再生的材料制造休闲椅
C.多个展馆充分利用了太阳能、风能、地源热能、生物质能
(3)世博会已右千辆新能源汽车投入运行,其中部分公交车采用二甲醚(C HO)做燃料。二甲
2 6
醚完全燃烧生成二氧化碳和水,写出该反应的化学方程式:____ 。
(4)在世博园区内分布着许多“直饮水”点(如图6所示),其“直饮水”主要生产流程为:
自来水→活性炭→超滤膜分离→紫外线消毒→直饮水,其中活性炭起____作用;超滤膜可
以让水分子通过,其它大分子污染物则被截留,这个分离过程属于_ ___(填“物理变
化”或“化学变化”)。
14.(4分)在“宏观——微观——符号”之间建立联系,是化学学科特有的思维方式。某化
学反应的微观模拟示意图是:
该反应的化学方程式是 ,所属基本反应
类型是 。
15.(5分)请根据图7中A、B两种固体物质的溶解度曲线,回答下
列问题。
2(l)在____℃时,A、B两种物质溶解度相同。
(2) t ℃时,100g水中溶解 gA物质恰好达到饱和,该饱和溶液中溶质的质量分数为_
2
___,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水 g。
(3)将t℃时A、B两种物质的饱和溶液降温至t℃(其它条件不变),溶质的质量分数保持不
2 1
变的是 。
三、实验与探究(本题包含2小题,共29分)
16.(17分)实验室部分仪器或装置如图8所示,请回答下列问题
(l)写出指定仪器的名称:A ,B________。
(2)若要组装一套二氧化碳的发生和收集装置,可选择图8中的_______。(填标号)实验室制
取二氧化碳的化学方程式为 _______________________ _。用该装置还可
以制取的气体是 ,应选择的药品是_______________ 。
(3)若用高锰酸钾制取氧气,你认为还需增加的仪器是___ _,写出用高锰
酸钾制取氧气的化学方程式: __ __。用图9所示装置收集氧气,
氧气应从____(填“a”或“b”)端导入。
(4)要鉴别氧气和二氧化碳,可选择 。
A.无色酚酞溶液 B.紫色石蕊溶液 C.澄清石灰水 D.燃着的木条
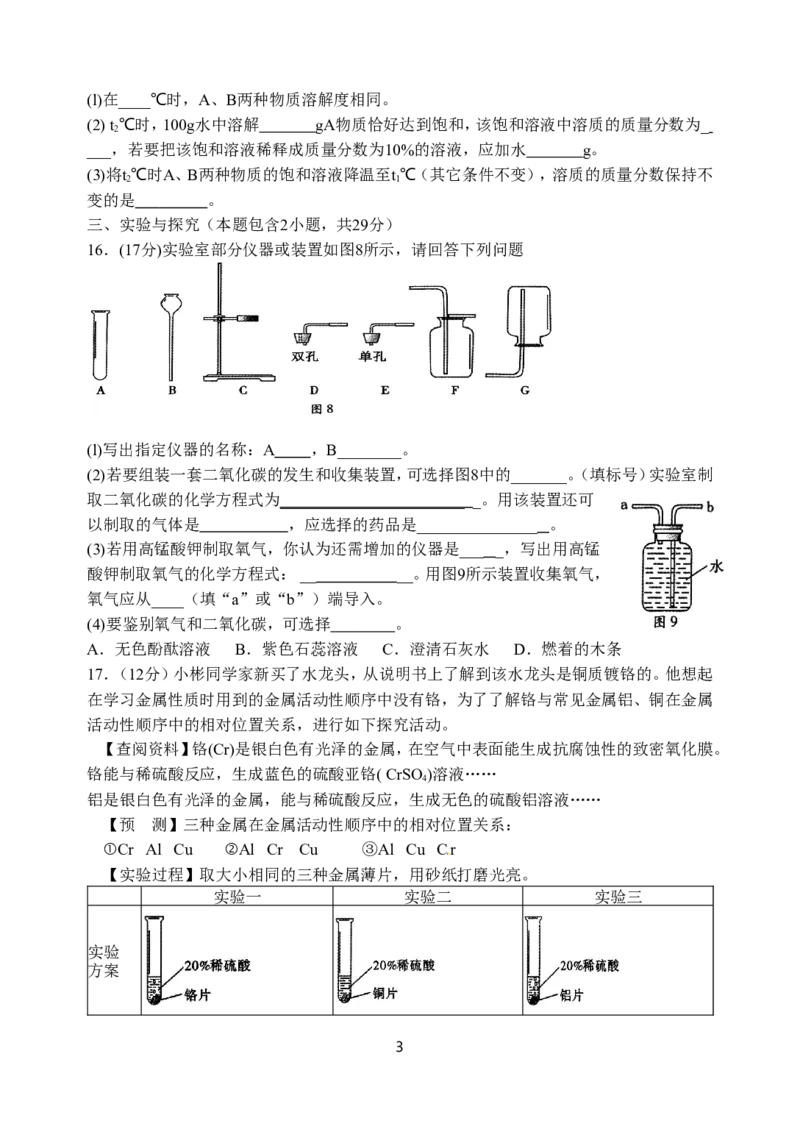
17.(12分)小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起
在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属
活动性顺序中的相对位置关系,进行如下探究活动。
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。
铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO)溶液……
4
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液……
【预 测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
实验一 实验二 实验三
实验
方案
3实验 铬片表面产生气泡缓慢,溶
_______________________ 铝片表面产生气泡较快。
现象 液变蓝色。
铬能和稀硫酸发生反应,反
铜不与稀硫酸反应 _______________________
应速率较慢。 [ 来
结论 [来源:学科网] 源:Z#xx#k.Com]
[来源:Zxxk.Co
三种金属在金属活动性顺序中的相对位置关系是__________________________
【回答问题】(1)用砂纸打磨金属片的目的是_____________________。
(2)实验一所发生反应的化学方程式是____________________________。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺
序中的相对位置关系,小燕认为不可行,理由是__________________。
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相
对位置关系,这三种药品可以是________________。
【归 纳】比较金属活动性强弱的方法有① ② 。
四、分析与计算(本题包含2小题,共13分)
可能用到的相对原子质量:H -l C-12 N-14 O-16 Na -23 Ca -40
18.(3分)维生素B (C H ON)可以用于防治舌炎、口角炎、角膜炎和溢脂性皮炎,其主要
2 17 20 6 4
存在于牛奶、动物内脏、蛋、瘦肉、麦胚、黄豆、花生等食物中。请回答下列问题:
(l)维生素B 由_______种元素组成。 (2)维生素B 中各元素的原子个数比为________。
2 2
(3)维生索B 中碳、氢两种元素的质量比为 。
2
19.(10分)实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质情况,设计了实验,实
验过程如下:实验一:取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢
氧化钠已变质,变质的原因是___________________________(用化学方程式表示)。
实验二:
通过实验二,能进一步推算出氢氧化钠变质的程度。请计算实验二中参加反应的碳酸钠质
量。(化学方程式:NaCO+ CaC1 =CaCO↓+2NaCl)
2 3 2 3
结论:16.0 g干燥的样品中已变质的氢氧化钠的质量是 g。
4二○一○年福州市初中毕业会考、高级中等学校招生考试
化学试卷参考答案
一、选择题(本题包含l0小题。每小题3分,共30分)
题号 l 2 3 4 5 6 7 8 9 10
答案 A C B C D C D B B A
二、填空与简答(本题包含5小题,共28分)
+2
11.(2分)①2N ②Ca2+ ③AlCl ④BaSO(答对两个得2分)
2 3 4
12.(8分)
(1)CO(合理答案均可得分)
2
(2)Ca(OH) +2HCl=CaCl +2H O
2 2 2
NaCO+Ca(OH) =CaCO↓+2NaOH(合理答案均可得分)
2 3 2 3
13.(9分)
(1)合成材料
(2)A B C
点燃
(3)C HO+3O====2CO+3H O
2 6 2 2 2
(4)吸附 物理变化
14.(4分)
高温
HO+C====CO+H
2 2
置换反应
15.(5分)
(1)t (2)25 20% 125 (3)B
1
三、实验与探究(本题包含2小题,共29分)
16.(17分)
(1) 试管 长颈漏斗
(2) A C E F或A B C D F
CaCO+2HCl=CaCl +H O+CO↑
3 2 2 2
氧气(或O) 过氧化氢溶液和二氧化锰 (合理答案均可得分)
2
△
(3)酒精灯 2KMnO====K MnO+MnO+O↑ a
4 2 4 2 2
(4) B C D
17.(12分)
实验现象:无现象
结论:铝能与稀硫酸发生反应,反应速率较快
Al Cr Cu(或“②”)
回答问题:
(1)除去金属表面氧化物(或污物)
(2) Cr+H SO=CrSO+H ↑
2 4 4 2
5(3) 无法比较铬和铝的金属活动性强弱(合理答案均可得分)
(4) A1、CrSO溶液、Cu(合理答案均可得分)
4
归纳:①通过金属与酸反应判断金属活动性强弱
②通过金属与盐溶液反应判断金属活动性强弱 (合理答案均可得分)
四、分析与计算(本题包含2小题,共l3分)
18.(3分)(1)4 (2)碳、氢、氧、氮原子个数比为17:20:6:4 (3)51:5
19.(10分)(1)2NaOH+CO=NaCO+H O
2 2 3 2
(2)解:设参加反应的碳酸钠质量为x
Na CO+CaCl =CaCO↓+2NaCl
2 3 2 3
106 100
x 10.0g
x=10.6g
答:参加反应的碳酸钠质量为10.6g。
结论:8.0
6