文档内容
2014 年四川省德阳市中考化学试卷
一、选择题(本题包括16小题,每小题3分,共48分.每小题只有一个选项符合
题意)
1.(3分)下列变化中,属于化学变化的是( )
A.海水晒盐 B.火柴折断 C.食物腐烂 D.干冰升华
2.(3分)化学与生活、生产密切相关,下列说法正确的是( )
A.普通玻璃是一种纯净物
B.大力开发新能源以替代不可再生的化石燃料
C.人体因碘摄入量不足,容易导致骨质疏松症
D.为了增加草木灰肥料,大力提倡在田间焚烧秸秆
3.(3分)2014年4月兰州发生了自来水苯超标事故,引起人们对水安全的关注。
已知苯的化学式为C H ,下列有关说法正确的是( )
6 6
A.苯中的C、H元素的质量比为12:1
B.苯分子是由6个碳元素和6个氢元素组成
C.苯分子中碳的原子结构示意图为
D.苯中碳、氢元素均位于元素周期表的第二周期
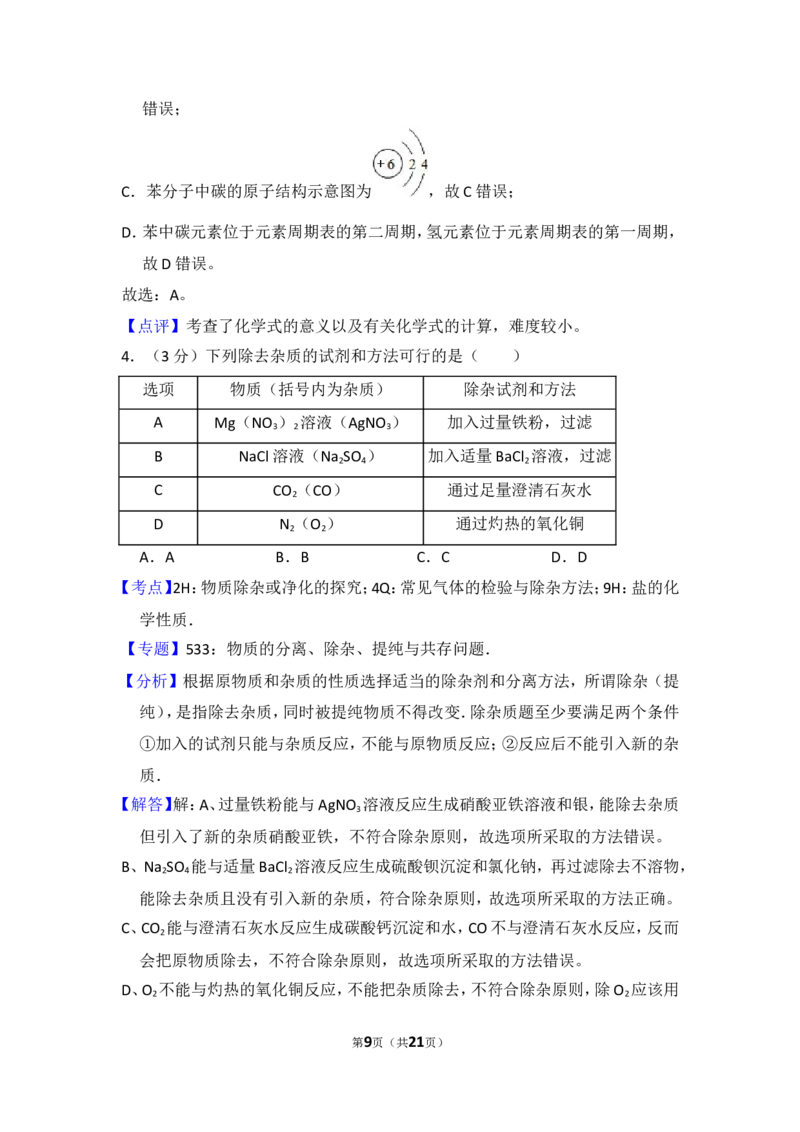
4.(3分)下列除去杂质的试剂和方法可行的是( )
选项 物质(括号内为杂质) 除杂试剂和方法
A Mg(NO ) 溶液(AgNO ) 加入过量铁粉,过滤
3 2 3
B NaCl溶液(Na SO ) 加入适量BaCl 溶液,过滤
2 4 2
C CO (CO) 通过足量澄清石灰水
2
D N (O ) 通过灼热的氧化铜
2 2
A.A B.B C.C D.D
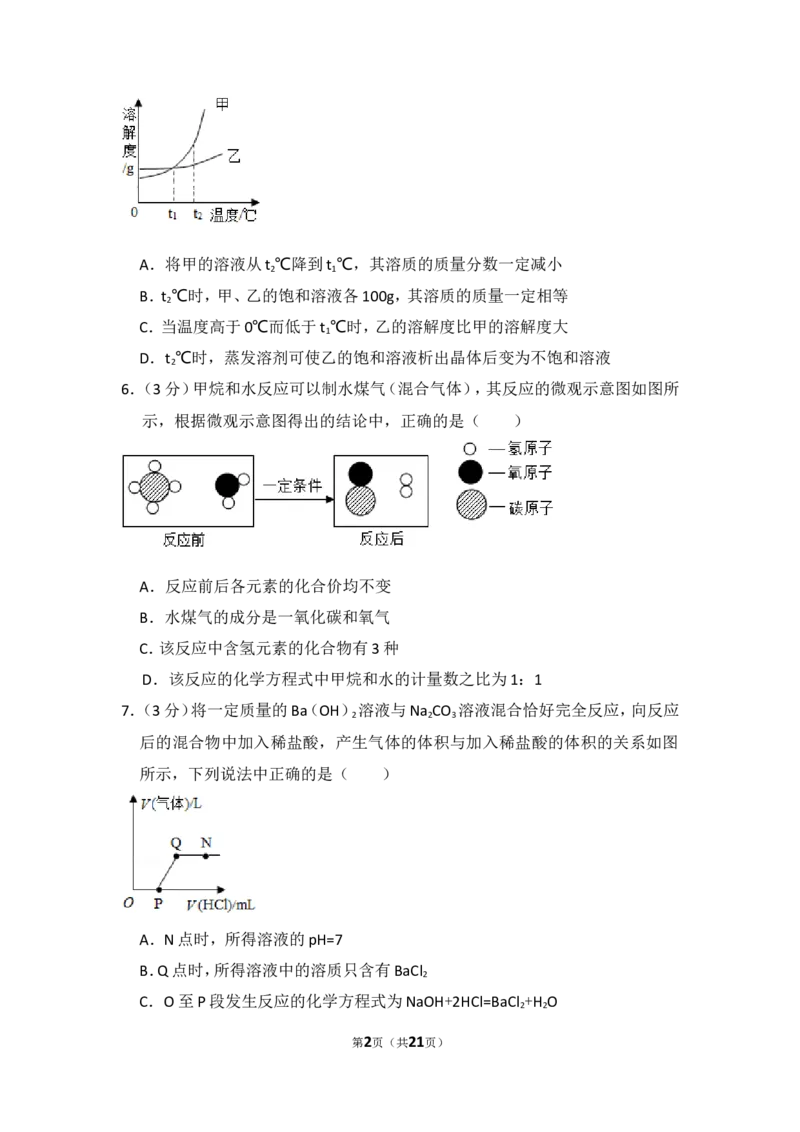
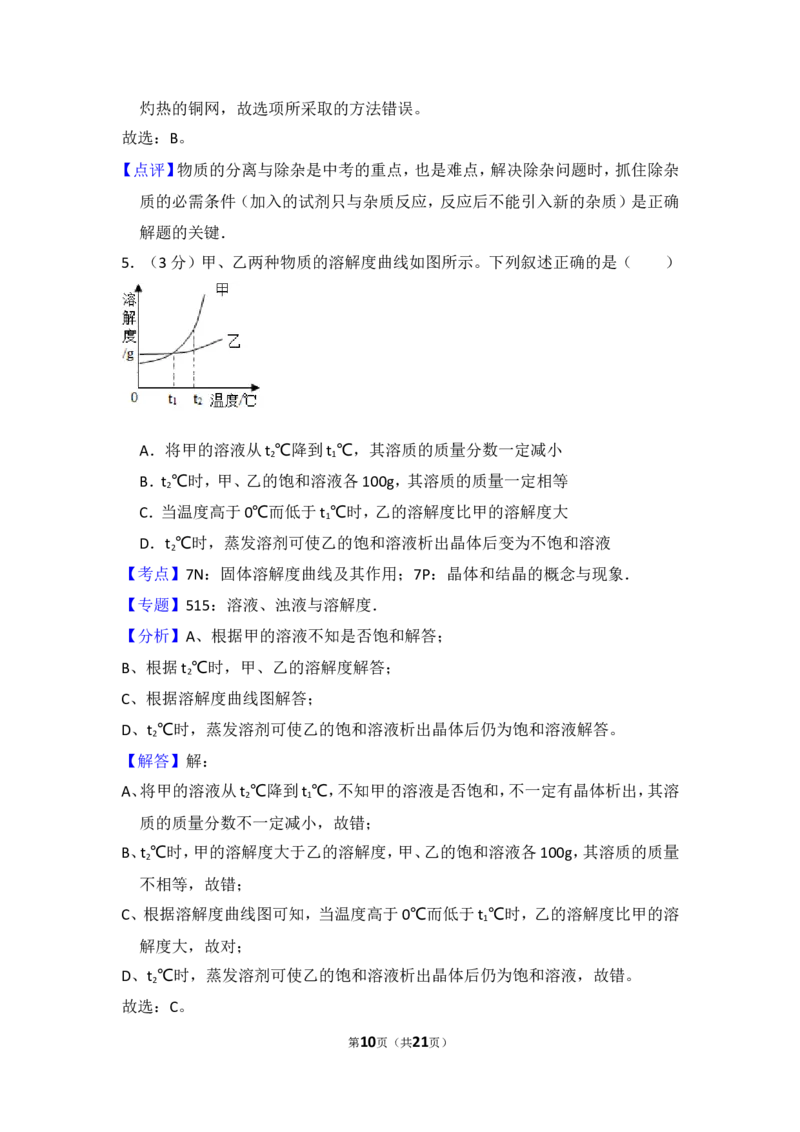
5.(3分)甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
第1页(共21页)A.将甲的溶液从t ℃降到t ℃,其溶质的质量分数一定减小
2 1
B.t ℃时,甲、乙的饱和溶液各100g,其溶质的质量一定相等
2
C.当温度高于0℃而低于t ℃时,乙的溶解度比甲的溶解度大
1
D.t ℃时,蒸发溶剂可使乙的饱和溶液析出晶体后变为不饱和溶液
2
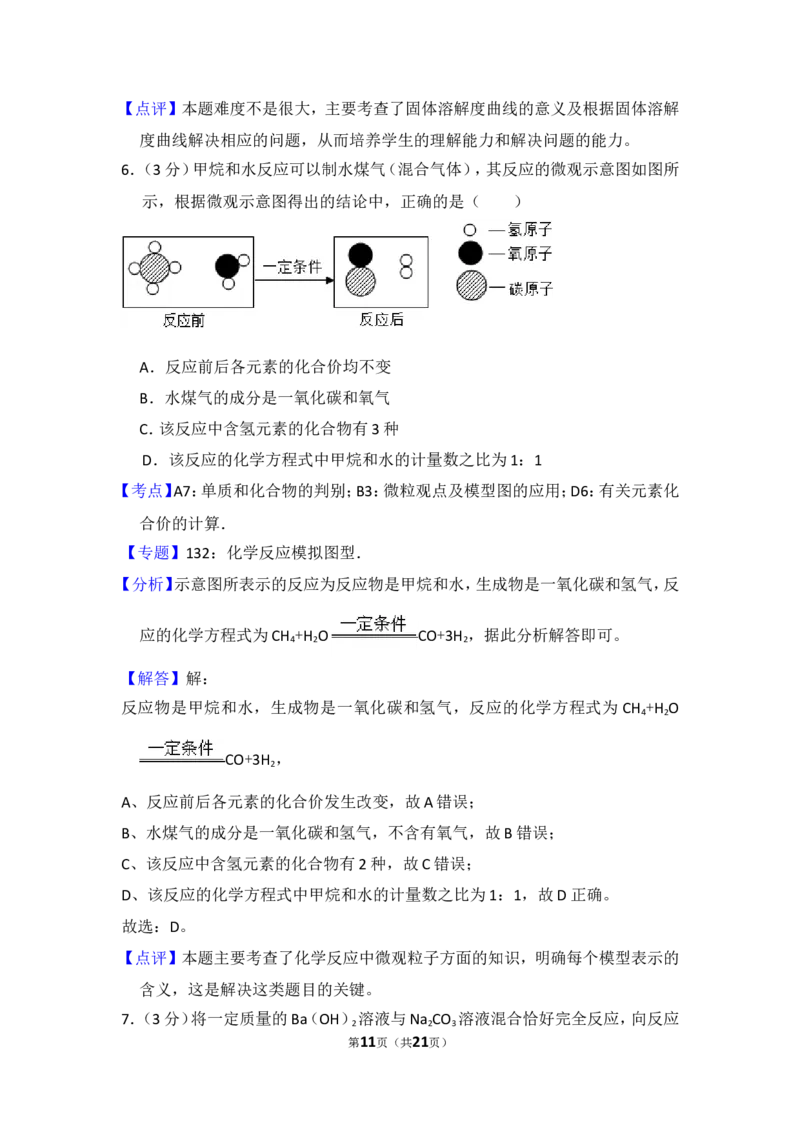
6.(3分)甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所
示,根据微观示意图得出的结论中,正确的是( )
A.反应前后各元素的化合价均不变
B.水煤气的成分是一氧化碳和氧气
C.该反应中含氢元素的化合物有3种
D.该反应的化学方程式中甲烷和水的计量数之比为1:1
7.(3分)将一定质量的Ba(OH)溶液与Na CO 溶液混合恰好完全反应,向反应
2 2 3
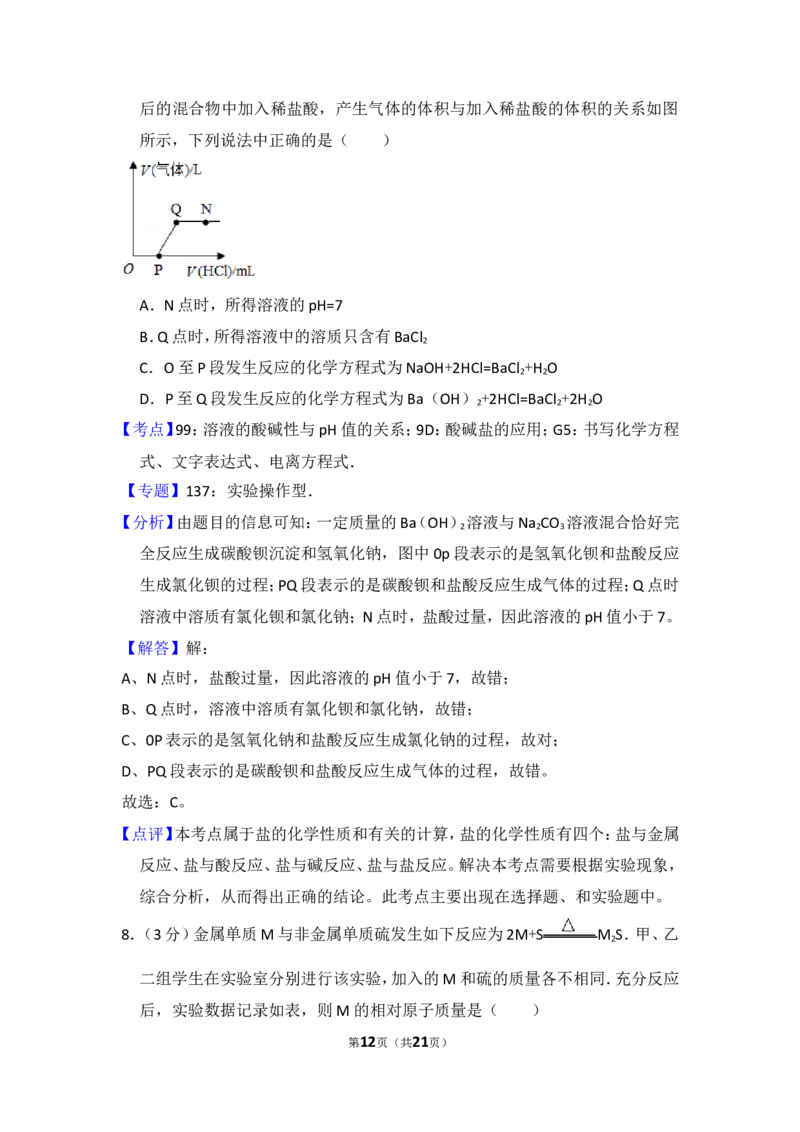
后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图
所示,下列说法中正确的是( )
A.N点时,所得溶液的pH=7
B.Q点时,所得溶液中的溶质只含有BaCl
2
C.O至P段发生反应的化学方程式为NaOH+2HCl=BaCl +H O
2 2
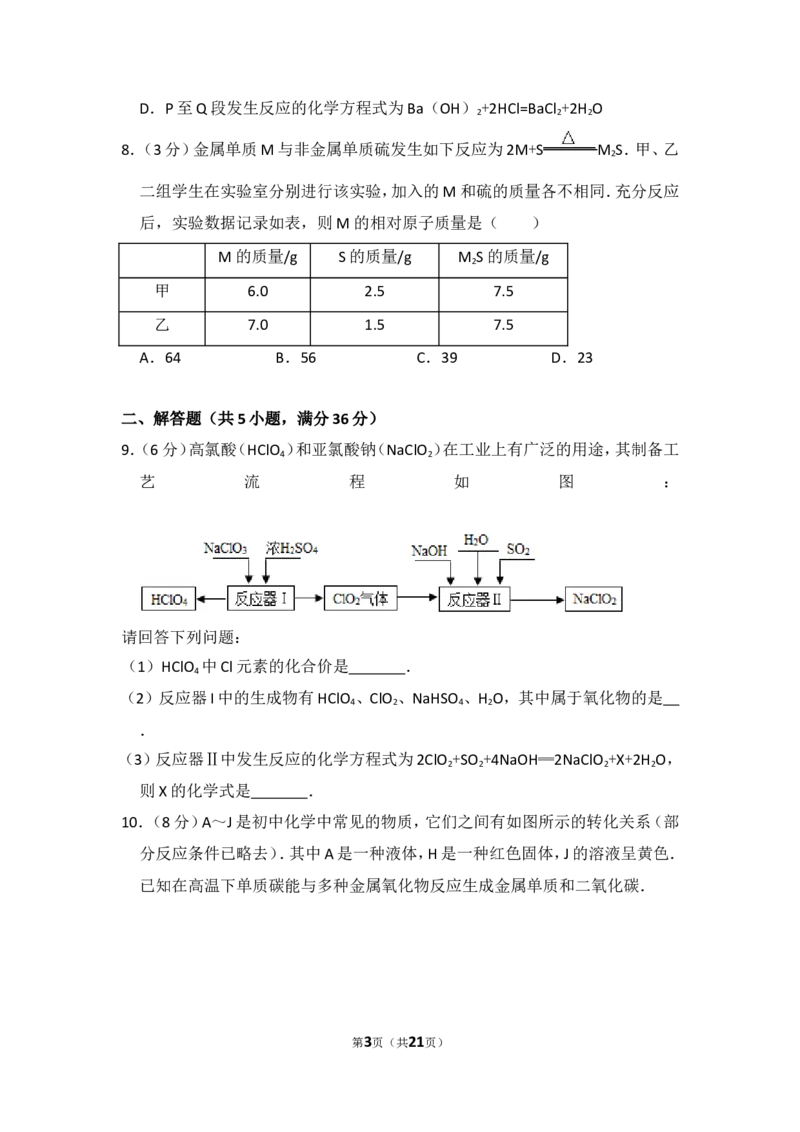
第2页(共21页)D.P至Q段发生反应的化学方程式为Ba(OH) +2HCl=BaCl +2H O
2 2 2
8.(3分)金属单质M与非金属单质硫发生如下反应为2M+S M S.甲、乙
2
二组学生在实验室分别进行该实验,加入的M和硫的质量各不相同.充分反应
后,实验数据记录如表,则M的相对原子质量是( )
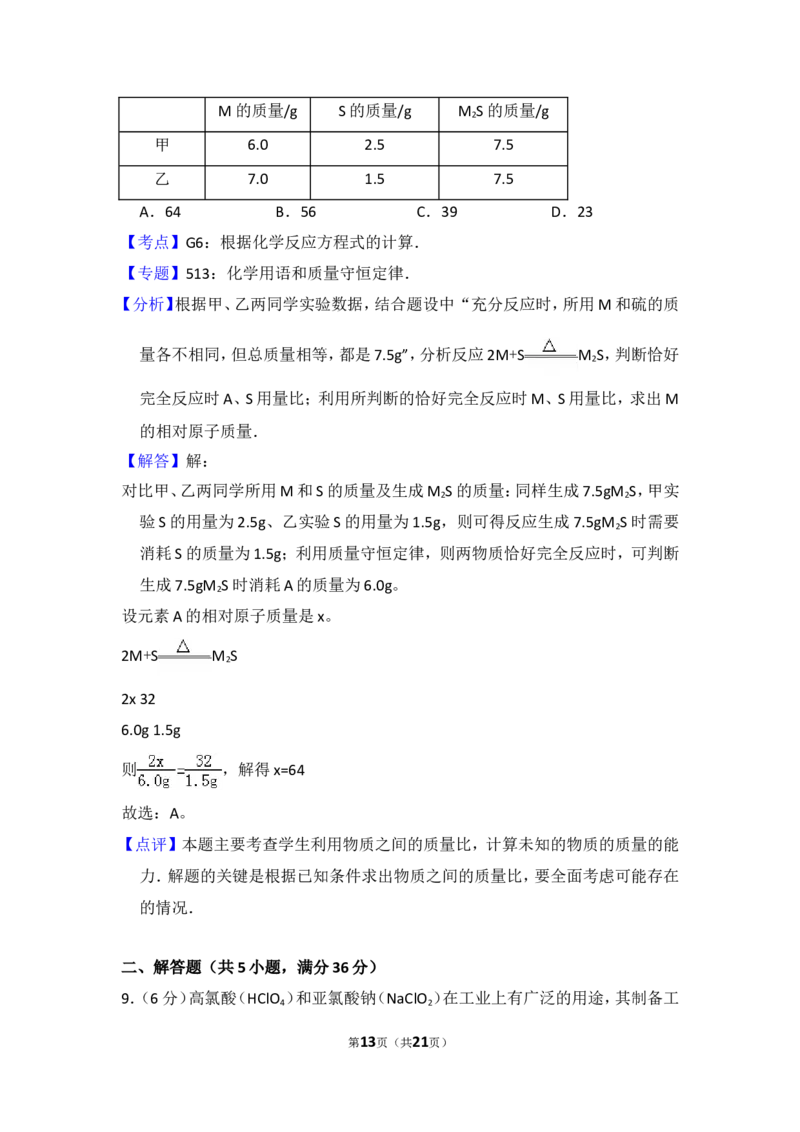
M的质量/g S的质量/g M S的质量/g
2
甲 6.0 2.5 7.5
乙 7.0 1.5 7.5
A.64 B.56 C.39 D.23
二、解答题(共5小题,满分36分)
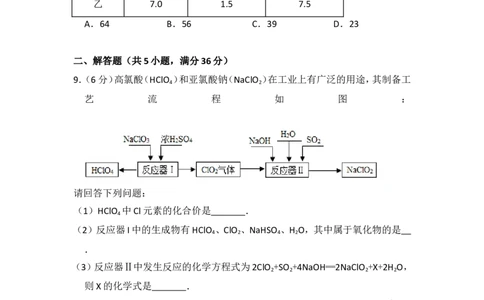
9.(6分)高氯酸(HClO )和亚氯酸钠(NaClO )在工业上有广泛的用途,其制备工
4 2
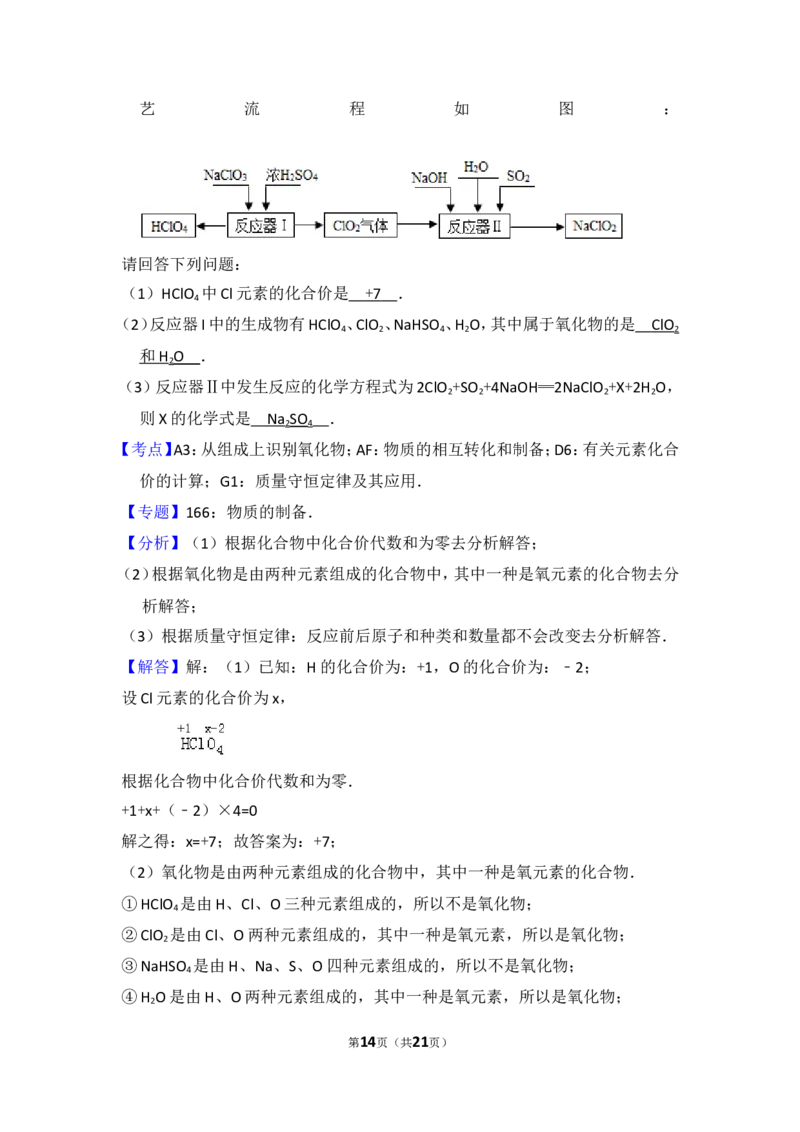
艺 流 程 如 图 :
请回答下列问题:
(1)HClO 中Cl元素的化合价是 .
4
(2)反应器I中的生成物有HClO 、ClO 、NaHSO 、H O,其中属于氧化物的是
4 2 4 2
.
(3)反应器Ⅱ中发生反应的化学方程式为2ClO +SO +4NaOH═2NaClO +X+2H O,
2 2 2 2
则X的化学式是 .
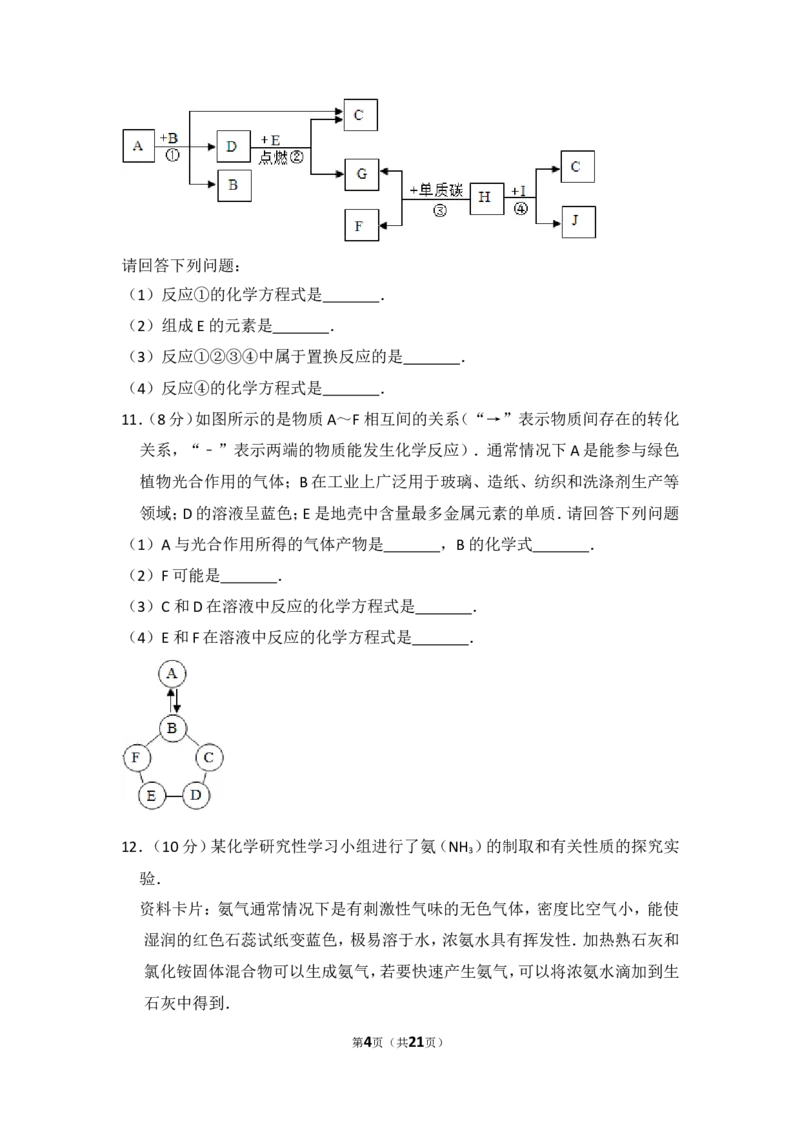
10.(8分)A~J是初中化学中常见的物质,它们之间有如图所示的转化关系(部
分反应条件已略去).其中A是一种液体,H是一种红色固体,J的溶液呈黄色.
已知在高温下单质碳能与多种金属氧化物反应生成金属单质和二氧化碳.
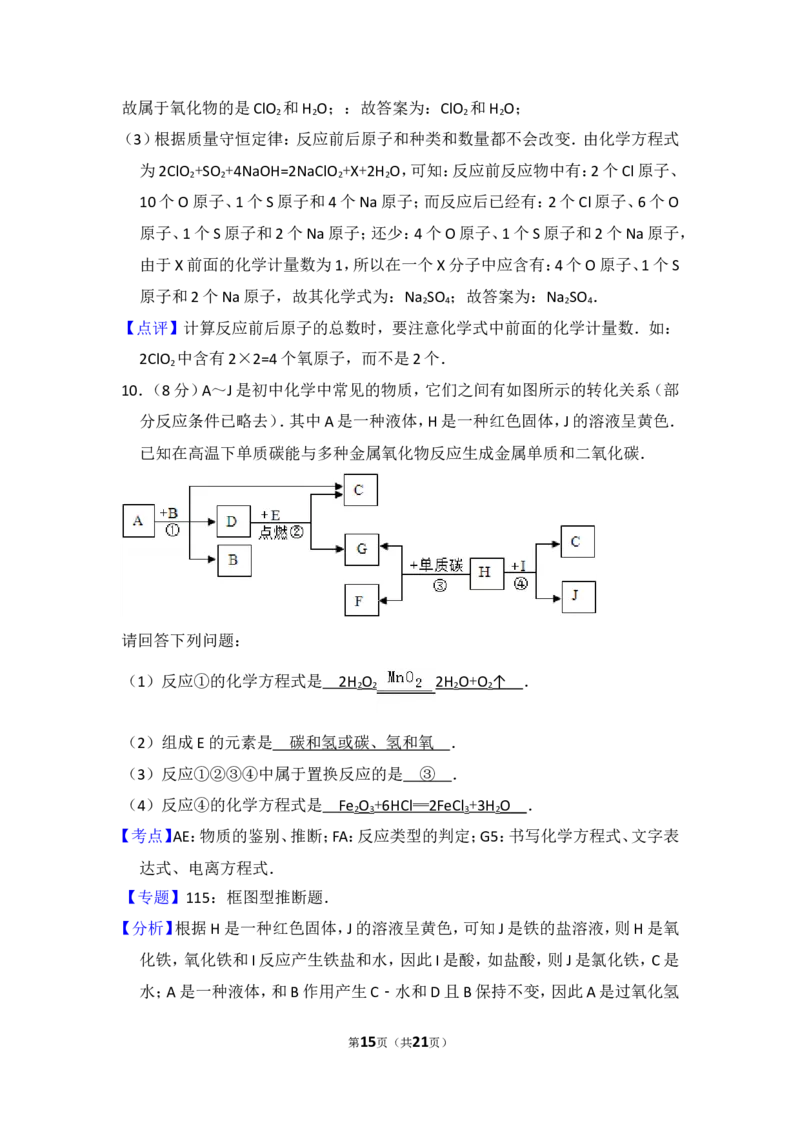
第3页(共21页)请回答下列问题:
(1)反应①的化学方程式是 .
(2)组成E的元素是 .
(3)反应①②③④中属于置换反应的是 .
(4)反应④的化学方程式是 .
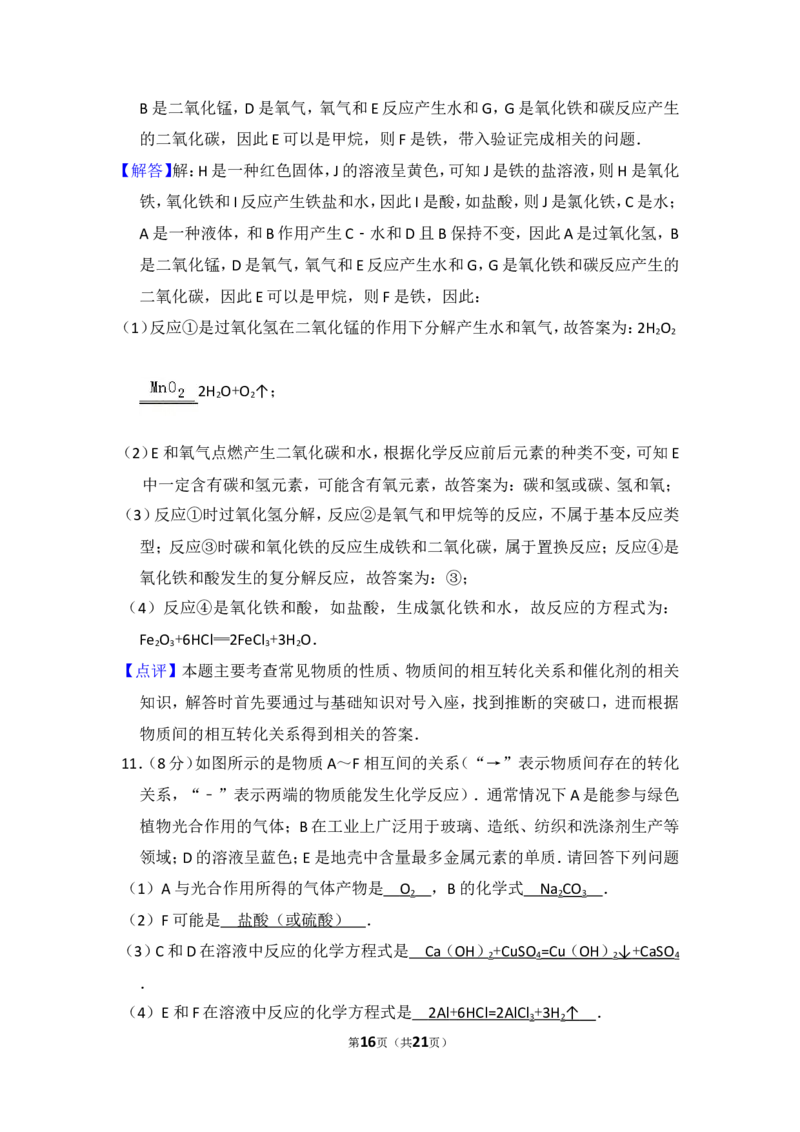
11.(8分)如图所示的是物质A~F相互间的关系(“→”表示物质间存在的转化
关系,“﹣”表示两端的物质能发生化学反应).通常情况下A是能参与绿色
植物光合作用的气体;B在工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等
领域;D的溶液呈蓝色;E是地壳中含量最多金属元素的单质.请回答下列问题
(1)A与光合作用所得的气体产物是 ,B的化学式 .
(2)F可能是 .
(3)C和D在溶液中反应的化学方程式是 .
(4)E和F在溶液中反应的化学方程式是 .
12.(10分)某化学研究性学习小组进行了氨(NH )的制取和有关性质的探究实
3
验.
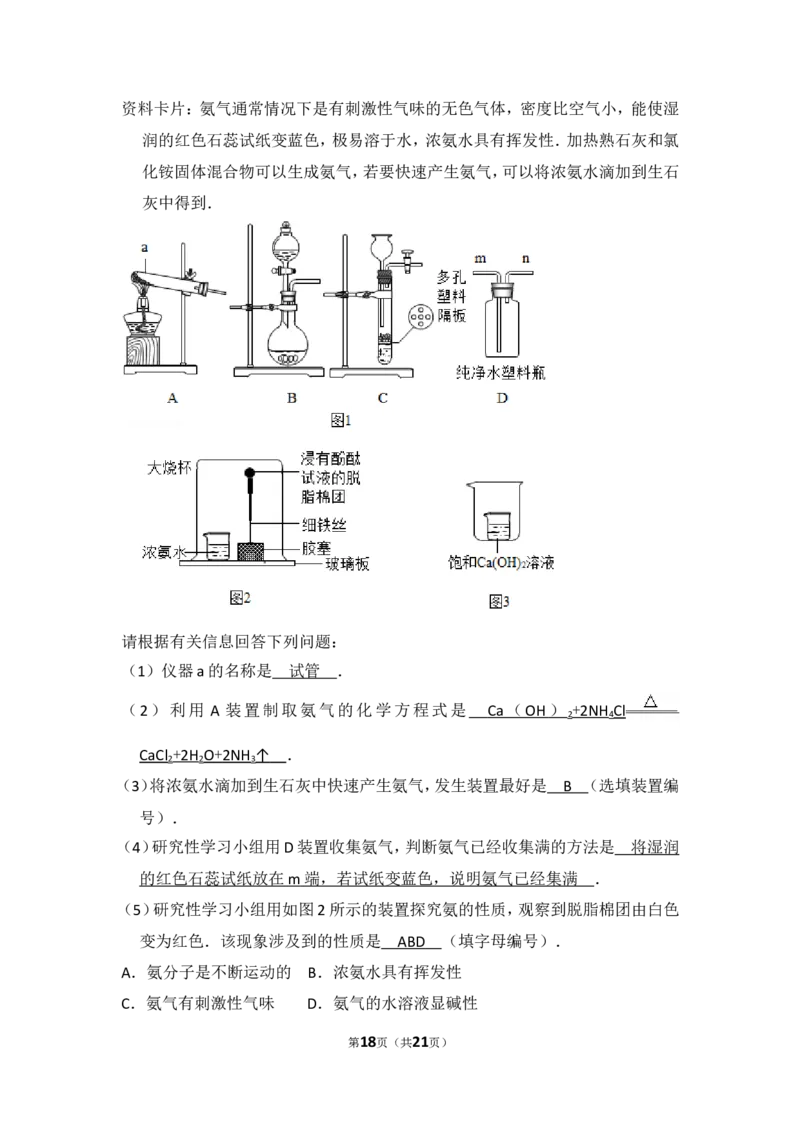
资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,能使
湿润的红色石蕊试纸变蓝色,极易溶于水,浓氨水具有挥发性.加热熟石灰和
氯化铵固体混合物可以生成氨气,若要快速产生氨气,可以将浓氨水滴加到生
石灰中得到.
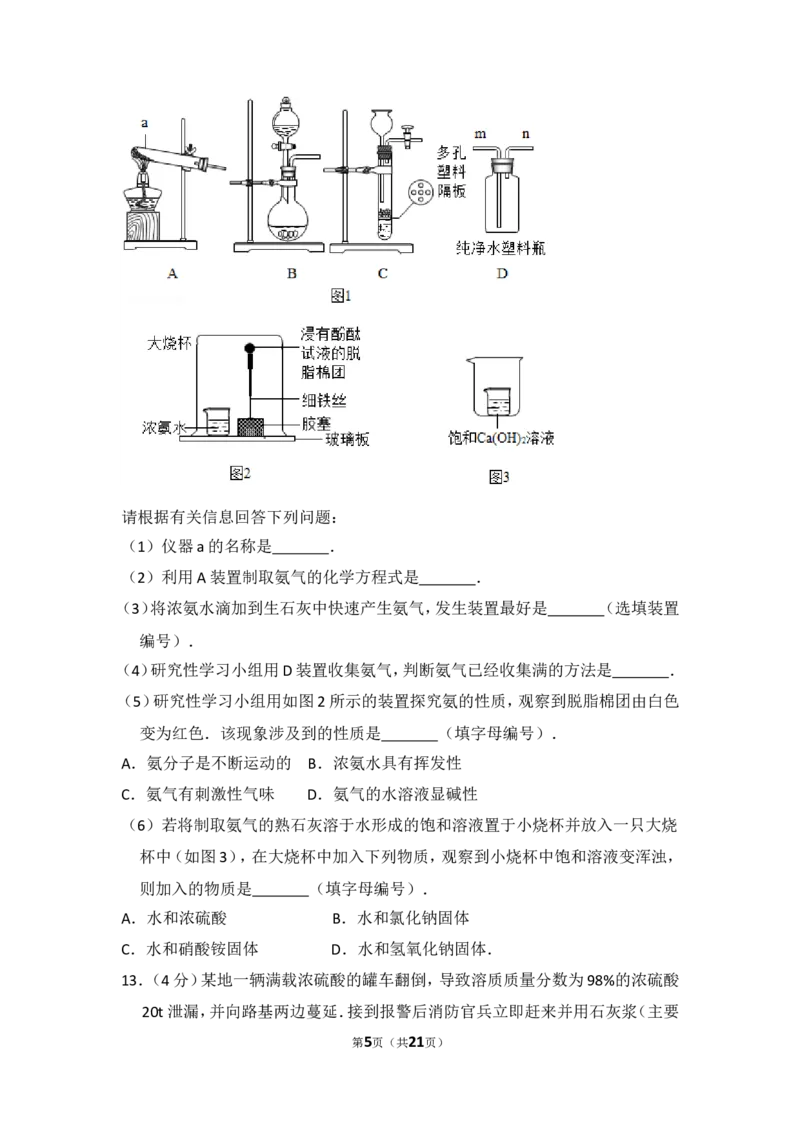
第4页(共21页)请根据有关信息回答下列问题:
(1)仪器a的名称是 .
(2)利用A装置制取氨气的化学方程式是 .
(3)将浓氨水滴加到生石灰中快速产生氨气,发生装置最好是 (选填装置
编号).
(4)研究性学习小组用D装置收集氨气,判断氨气已经收集满的方法是 .
(5)研究性学习小组用如图2所示的装置探究氨的性质,观察到脱脂棉团由白色
变为红色.该现象涉及到的性质是 (填字母编号).
A.氨分子是不断运动的 B.浓氨水具有挥发性
C.氨气有刺激性气味 D.氨气的水溶液显碱性
(6)若将制取氨气的熟石灰溶于水形成的饱和溶液置于小烧杯并放入一只大烧
杯中(如图3),在大烧杯中加入下列物质,观察到小烧杯中饱和溶液变浑浊,
则加入的物质是 (填字母编号).
A.水和浓硫酸 B.水和氯化钠固体
C.水和硝酸铵固体 D.水和氢氧化钠固体.
13.(4分)某地一辆满载浓硫酸的罐车翻倒,导致溶质质量分数为98%的浓硫酸
20t泄漏,并向路基两边蔓延.接到报警后消防官兵立即赶来并用石灰浆(主要
第5页(共21页)成分为氢氧化钙)中和硫酸解除了险情.请回答:
(1)溶质质量分数为98%的浓硫酸20t中含H SO 的质量是 ;
2 4
(2)计算中和泄漏的98%浓硫酸20t,理论上需要氢氧化钙的质量.
第6页(共21页)2014 年四川省德阳市中考化学试卷
参考答案与试题解析
一、选择题(本题包括16小题,每小题3分,共48分.每小题只有一个选项符合
题意)
1.(3分)下列变化中,属于化学变化的是( )
A.海水晒盐 B.火柴折断 C.食物腐烂 D.干冰升华
【考点】E3:化学变化和物理变化的判别.
【专题】512:物质的变化与性质.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、海水晒盐过程中没有新物质生成,属于物理变化。
B、火柴折断过程中只是形状发生改变,没有新物质生成,属于物理变化。
C、食物腐烂过程中有新物质生成,属于化学变化。
D、干冰升华过程中只是状态发生改变,没有新物质生成,属于物理变化。
故选:C。
【点评】本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物
质生成属于物理变化,若有新物质生成属于化学变化.
2.(3分)化学与生活、生产密切相关,下列说法正确的是( )
A.普通玻璃是一种纯净物
B.大力开发新能源以替代不可再生的化石燃料
C.人体因碘摄入量不足,容易导致骨质疏松症
D.为了增加草木灰肥料,大力提倡在田间焚烧秸秆
【考点】9J:常见化肥的种类和作用;A5:纯净物和混合物的判别;HE:资源综合利
用和新能源开发;J1:人体的元素组成与元素对人体健康的重要作用.
【专题】213:化学与能源;516:物质的分类;527:常见的盐 化学肥料;528:化学
与生活.
【分析】A、普通玻璃中含有硅酸钠、硅酸钙、二氧化硅等物质;
第7页(共21页)B、化石燃料属于不可再生能源;
C、人体缺乏钙元素时,易患骨质疏松症或佝偻病,缺乏碘元素时,易患甲状腺肿
大;
D、焚烧秸秆时能够产生大量污染空气的物质.
【解答】解:A、普通玻璃中含有多种物质,属于混合物,故A错误;
B、化石燃料用完之后不能再生,因此应该积极开发利用新能源,以代替化石燃料,
故B正确;
C、人体因碘摄入量不足,容易导致甲状腺肿大,故C错误;
D、焚烧秸秆虽然可以增加草木灰肥料,但是会污染环境,得不偿失,故D错误。
故选:B。
【点评】化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关
的化学知识也是重要的中考热点之一.
3.(3分)2014年4月兰州发生了自来水苯超标事故,引起人们对水安全的关注。
已知苯的化学式为C H ,下列有关说法正确的是( )
6 6
A.苯中的C、H元素的质量比为12:1
B.苯分子是由6个碳元素和6个氢元素组成
C.苯分子中碳的原子结构示意图为
D.苯中碳、氢元素均位于元素周期表的第二周期
【考点】B8:原子结构示意图与离子结构示意图;D1:化学式的书写及意义;D9:元
素质量比的计算.
【专题】513:化学用语和质量守恒定律.
【分析】A.根据化合物中各元素质量比的计算方法来分析;
B.根据物质中元素质量比的计算方法来分析;
C.根据物质的组成来分析;
D.根据物质的结构来分析。
【解答】解:A.由苯的化学式C H 可知,其中C、H元素的质量比为:(12×6):
6 6
(1×6)=12:1,故A正确;
B.苯是由碳元素和氢元素组成的,元素是个宏观概念,只讲种类,不讲个数,故B
第8页(共21页)错误;
C.苯分子中碳的原子结构示意图为 ,故C错误;
D.苯中碳元素位于元素周期表的第二周期,氢元素位于元素周期表的第一周期,
故D错误。
故选:A。
【点评】考查了化学式的意义以及有关化学式的计算,难度较小。
4.(3分)下列除去杂质的试剂和方法可行的是( )
选项 物质(括号内为杂质) 除杂试剂和方法
A Mg(NO ) 溶液(AgNO ) 加入过量铁粉,过滤
3 2 3
B NaCl溶液(Na SO ) 加入适量BaCl 溶液,过滤
2 4 2
C CO (CO) 通过足量澄清石灰水
2
D N (O ) 通过灼热的氧化铜
2 2
A.A B.B C.C D.D
【考点】2H:物质除杂或净化的探究;4Q:常见气体的检验与除杂方法;9H:盐的化
学性质.
【专题】533:物质的分离、除杂、提纯与共存问题.
【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提
纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件
①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂
质.
【解答】解:A、过量铁粉能与AgNO 溶液反应生成硝酸亚铁溶液和银,能除去杂质
3
但引入了新的杂质硝酸亚铁,不符合除杂原则,故选项所采取的方法错误。
B、Na SO 能与适量BaCl 溶液反应生成硫酸钡沉淀和氯化钠,再过滤除去不溶物,
2 4 2
能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
C、CO 能与澄清石灰水反应生成碳酸钙沉淀和水,CO不与澄清石灰水反应,反而
2
会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
D、O 不能与灼热的氧化铜反应,不能把杂质除去,不符合除杂原则,除O 应该用
2 2
第9页(共21页)灼热的铜网,故选项所采取的方法错误。
故选:B。
【点评】物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂
质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确
解题的关键.
5.(3分)甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
A.将甲的溶液从t ℃降到t ℃,其溶质的质量分数一定减小
2 1
B.t ℃时,甲、乙的饱和溶液各100g,其溶质的质量一定相等
2
C.当温度高于0℃而低于t ℃时,乙的溶解度比甲的溶解度大
1
D.t ℃时,蒸发溶剂可使乙的饱和溶液析出晶体后变为不饱和溶液
2
【考点】7N:固体溶解度曲线及其作用;7P:晶体和结晶的概念与现象.
【专题】515:溶液、浊液与溶解度.
【分析】A、根据甲的溶液不知是否饱和解答;
B、根据t ℃时,甲、乙的溶解度解答;
2
C、根据溶解度曲线图解答;
D、t ℃时,蒸发溶剂可使乙的饱和溶液析出晶体后仍为饱和溶液解答。
2
【解答】解:
A、将甲的溶液从t ℃降到t ℃,不知甲的溶液是否饱和,不一定有晶体析出,其溶
2 1
质的质量分数不一定减小,故错;
B、t ℃时,甲的溶解度大于乙的溶解度,甲、乙的饱和溶液各100g,其溶质的质量
2
不相等,故错;
C、根据溶解度曲线图可知,当温度高于0℃而低于t ℃时,乙的溶解度比甲的溶
1
解度大,故对;
D、t ℃时,蒸发溶剂可使乙的饱和溶液析出晶体后仍为饱和溶液,故错。
2
故选:C。
第10页(共21页)【点评】本题难度不是很大,主要考查了固体溶解度曲线的意义及根据固体溶解
度曲线解决相应的问题,从而培养学生的理解能力和解决问题的能力。
6.(3分)甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所
示,根据微观示意图得出的结论中,正确的是( )
A.反应前后各元素的化合价均不变
B.水煤气的成分是一氧化碳和氧气
C.该反应中含氢元素的化合物有3种
D.该反应的化学方程式中甲烷和水的计量数之比为1:1
【考点】A7:单质和化合物的判别;B3:微粒观点及模型图的应用;D6:有关元素化
合价的计算.
【专题】132:化学反应模拟图型.
【分析】示意图所表示的反应为反应物是甲烷和水,生成物是一氧化碳和氢气,反
应的化学方程式为CH +H O CO+3H ,据此分析解答即可。
4 2 2
【解答】解:
反应物是甲烷和水,生成物是一氧化碳和氢气,反应的化学方程式为 CH +H O
4 2
CO+3H ,
2
A、反应前后各元素的化合价发生改变,故A错误;
B、水煤气的成分是一氧化碳和氢气,不含有氧气,故B错误;
C、该反应中含氢元素的化合物有2种,故C错误;
D、该反应的化学方程式中甲烷和水的计量数之比为1:1,故D正确。
故选:D。
【点评】本题主要考查了化学反应中微观粒子方面的知识,明确每个模型表示的
含义,这是解决这类题目的关键。
7.(3分)将一定质量的Ba(OH)溶液与Na CO 溶液混合恰好完全反应,向反应
2 2 3
第11页(共21页)后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图
所示,下列说法中正确的是( )
A.N点时,所得溶液的pH=7
B.Q点时,所得溶液中的溶质只含有BaCl
2
C.O至P段发生反应的化学方程式为NaOH+2HCl=BaCl +H O
2 2
D.P至Q段发生反应的化学方程式为Ba(OH) +2HCl=BaCl +2H O
2 2 2
【考点】99:溶液的酸碱性与pH值的关系;9D:酸碱盐的应用;G5:书写化学方程
式、文字表达式、电离方程式.
【专题】137:实验操作型.
【分析】由题目的信息可知:一定质量的Ba(OH)溶液与Na CO 溶液混合恰好完
2 2 3
全反应生成碳酸钡沉淀和氢氧化钠,图中0p段表示的是氢氧化钡和盐酸反应
生成氯化钡的过程;PQ段表示的是碳酸钡和盐酸反应生成气体的过程;Q点时
溶液中溶质有氯化钡和氯化钠;N点时,盐酸过量,因此溶液的pH值小于7。
【解答】解:
A、N点时,盐酸过量,因此溶液的pH值小于7,故错;
B、Q点时,溶液中溶质有氯化钡和氯化钠,故错;
C、0P表示的是氢氧化钠和盐酸反应生成氯化钠的过程,故对;
D、PQ段表示的是碳酸钡和盐酸反应生成气体的过程,故错。
故选:C。
【点评】本考点属于盐的化学性质和有关的计算,盐的化学性质有四个:盐与金属
反应、盐与酸反应、盐与碱反应、盐与盐反应。解决本考点需要根据实验现象,
综合分析,从而得出正确的结论。此考点主要出现在选择题、和实验题中。
8.(3分)金属单质M与非金属单质硫发生如下反应为2M+S M S.甲、乙
2
二组学生在实验室分别进行该实验,加入的M和硫的质量各不相同.充分反应
后,实验数据记录如表,则M的相对原子质量是( )
第12页(共21页)M的质量/g S的质量/g M S的质量/g
2
甲 6.0 2.5 7.5
乙 7.0 1.5 7.5
A.64 B.56 C.39 D.23
【考点】G6:根据化学反应方程式的计算.
【专题】513:化学用语和质量守恒定律.
【分析】根据甲、乙两同学实验数据,结合题设中“充分反应时,所用M和硫的质
量各不相同,但总质量相等,都是7.5g”,分析反应2M+S M S,判断恰好
2
完全反应时A、S用量比;利用所判断的恰好完全反应时M、S用量比,求出M
的相对原子质量.
【解答】解:
对比甲、乙两同学所用M和S的质量及生成M S的质量:同样生成7.5gM S,甲实
2 2
验S的用量为2.5g、乙实验S的用量为1.5g,则可得反应生成7.5gM S时需要
2
消耗S的质量为1.5g;利用质量守恒定律,则两物质恰好完全反应时,可判断
生成7.5gM S时消耗A的质量为6.0g。
2
设元素A的相对原子质量是x。
2M+S M S
2
2x 32
6.0g 1.5g
则 ,解得x=64
故选:A。
【点评】本题主要考查学生利用物质之间的质量比,计算未知的物质的质量的能
力.解题的关键是根据已知条件求出物质之间的质量比,要全面考虑可能存在
的情况.
二、解答题(共5小题,满分36分)
9.(6分)高氯酸(HClO )和亚氯酸钠(NaClO )在工业上有广泛的用途,其制备工
4 2
第13页(共21页)艺 流 程 如 图 :
请回答下列问题:
(1)HClO 中Cl元素的化合价是 + 7 .
4
(2)反应器I中的生成物有HClO 、ClO 、NaHSO 、H O,其中属于氧化物的是 ClO
4 2 4 2 2
和 H O .
2
(3)反应器Ⅱ中发生反应的化学方程式为2ClO +SO +4NaOH═2NaClO +X+2H O,
2 2 2 2
则X的化学式是 N a SO .
2 4
【考点】A3:从组成上识别氧化物;AF:物质的相互转化和制备;D6:有关元素化合
价的计算;G1:质量守恒定律及其应用.
【专题】166:物质的制备.
【分析】(1)根据化合物中化合价代数和为零去分析解答;
(2)根据氧化物是由两种元素组成的化合物中,其中一种是氧元素的化合物去分
析解答;
(3)根据质量守恒定律:反应前后原子和种类和数量都不会改变去分析解答.
【解答】解:(1)已知:H的化合价为:+1,O的化合价为:﹣2;
设Cl元素的化合价为x,
根据化合物中化合价代数和为零.
+1+x+(﹣2)×4=0
解之得:x=+7;故答案为:+7;
(2)氧化物是由两种元素组成的化合物中,其中一种是氧元素的化合物.
①HClO 是由H、Cl、O三种元素组成的,所以不是氧化物;
4
②ClO 是由Cl、O两种元素组成的,其中一种是氧元素,所以是氧化物;
2
③NaHSO 是由H、Na、S、O四种元素组成的,所以不是氧化物;
4
④H O是由H、O两种元素组成的,其中一种是氧元素,所以是氧化物;
2
第14页(共21页)故属于氧化物的是ClO 和H O;:故答案为:ClO 和H O;
2 2 2 2
(3)根据质量守恒定律:反应前后原子和种类和数量都不会改变.由化学方程式
为2ClO +SO +4NaOH=2NaClO +X+2H O,可知:反应前反应物中有:2个Cl原子、
2 2 2 2
10个O原子、1个S原子和4个Na原子;而反应后已经有:2个Cl原子、6个O
原子、1个S原子和2个Na原子;还少:4个O原子、1个S原子和2个Na原子,
由于X前面的化学计量数为1,所以在一个X分子中应含有:4个O原子、1个S
原子和2个Na原子,故其化学式为:Na SO ;故答案为:Na SO .
2 4 2 4
【点评】计算反应前后原子的总数时,要注意化学式中前面的化学计量数.如:
2ClO 中含有2×2=4个氧原子,而不是2个.
2
10.(8分)A~J是初中化学中常见的物质,它们之间有如图所示的转化关系(部
分反应条件已略去).其中A是一种液体,H是一种红色固体,J的溶液呈黄色.
已知在高温下单质碳能与多种金属氧化物反应生成金属单质和二氧化碳.
请回答下列问题:
(1)反应①的化学方程式是 2H O 2H O + O ↑ .
2 2 2 2
(2)组成E的元素是 碳和氢或碳、氢和氧 .
(3)反应①②③④中属于置换反应的是 ③ .
(4)反应④的化学方程式是 F e O + 6HC l ═ 2FeC l + 3H O .
2 3 3 2
【考点】AE:物质的鉴别、推断;FA:反应类型的判定;G5:书写化学方程式、文字表
达式、电离方程式.
【专题】115:框图型推断题.
【分析】根据H是一种红色固体,J的溶液呈黄色,可知J是铁的盐溶液,则H是氧
化铁,氧化铁和I反应产生铁盐和水,因此I是酸,如盐酸,则J是氯化铁,C是
水;A是一种液体,和B作用产生C﹣水和D 且B保持不变,因此A是过氧化氢
第15页(共21页)B是二氧化锰,D是氧气,氧气和E反应产生水和G,G是氧化铁和碳反应产生
的二氧化碳,因此E可以是甲烷,则F是铁,带入验证完成相关的问题.
【解答】解:H是一种红色固体,J的溶液呈黄色,可知J是铁的盐溶液,则H是氧化
铁,氧化铁和I反应产生铁盐和水,因此I是酸,如盐酸,则J是氯化铁,C是水;
A是一种液体,和B作用产生C﹣水和D 且B保持不变,因此A是过氧化氢,B
是二氧化锰,D是氧气,氧气和E反应产生水和G,G是氧化铁和碳反应产生的
二氧化碳,因此E可以是甲烷,则F是铁,因此:
(1)反应①是过氧化氢在二氧化锰的作用下分解产生水和氧气,故答案为:2H O
2 2
2H O+O ↑;
2 2
(2)E和氧气点燃产生二氧化碳和水,根据化学反应前后元素的种类不变,可知E
中一定含有碳和氢元素,可能含有氧元素,故答案为:碳和氢或碳、氢和氧;
(3)反应①时过氧化氢分解,反应②是氧气和甲烷等的反应,不属于基本反应类
型;反应③时碳和氧化铁的反应生成铁和二氧化碳,属于置换反应;反应④是
氧化铁和酸发生的复分解反应,故答案为:③;
(4)反应④是氧化铁和酸,如盐酸,生成氯化铁和水,故反应的方程式为:
Fe O +6HCl═2FeCl +3H O.
2 3 3 2
【点评】本题主要考查常见物质的性质、物质间的相互转化关系和催化剂的相关
知识,解答时首先要通过与基础知识对号入座,找到推断的突破口,进而根据
物质间的相互转化关系得到相关的答案.
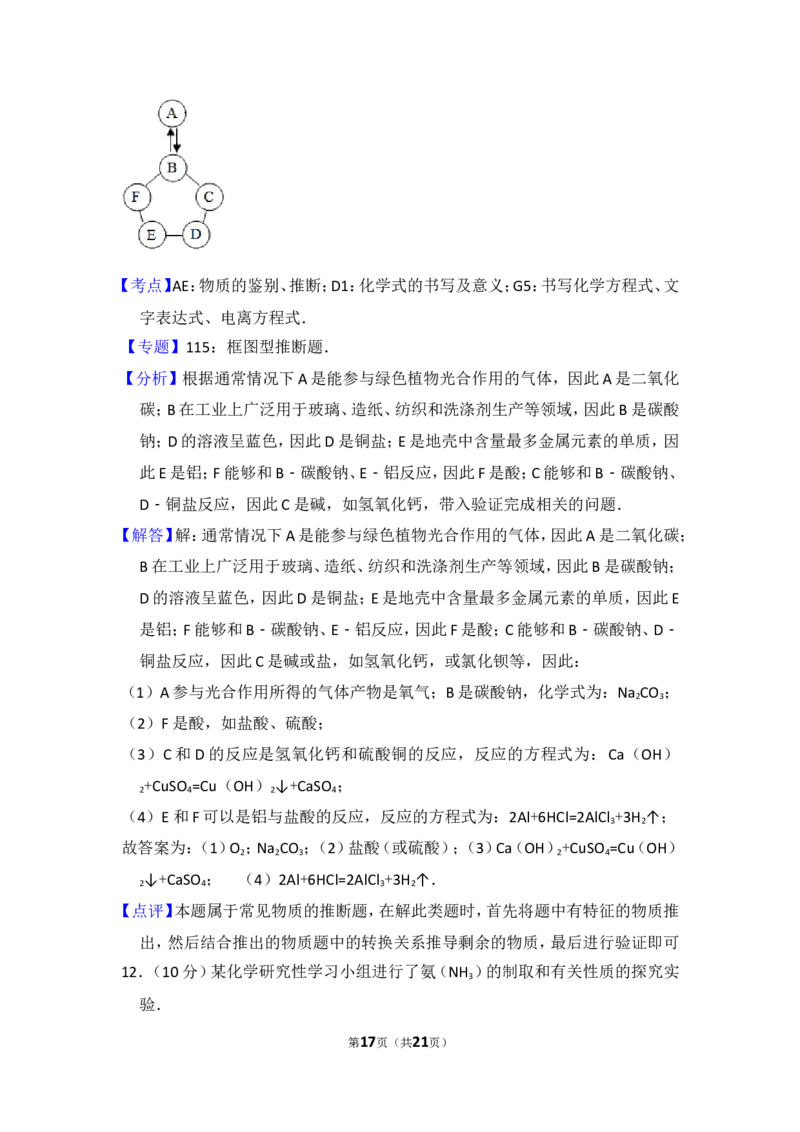
11.(8分)如图所示的是物质A~F相互间的关系(“→”表示物质间存在的转化
关系,“﹣”表示两端的物质能发生化学反应).通常情况下A是能参与绿色
植物光合作用的气体;B在工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等
领域;D的溶液呈蓝色;E是地壳中含量最多金属元素的单质.请回答下列问题
(1)A与光合作用所得的气体产物是 O ,B的化学式 N a CO .
2 2 3
(2)F可能是 盐酸(或硫酸) .
(3)C和D在溶液中反应的化学方程式是 C a( OH ) + CuSO =Cu ( OH ) ↓ + CaSO
2 4 2 4
.
(4)E和F在溶液中反应的化学方程式是 2A l + 6HCl=2AlC l + 3H ↑ .
3 2
第16页(共21页)【考点】AE:物质的鉴别、推断;D1:化学式的书写及意义;G5:书写化学方程式、文
字表达式、电离方程式.
【专题】115:框图型推断题.
【分析】根据通常情况下A是能参与绿色植物光合作用的气体,因此A是二氧化
碳;B在工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等领域,因此B是碳酸
钠;D的溶液呈蓝色,因此D是铜盐;E是地壳中含量最多金属元素的单质,因
此E是铝;F能够和B﹣碳酸钠、E﹣铝反应,因此F是酸;C能够和B﹣碳酸钠、
D﹣铜盐反应,因此C是碱,如氢氧化钙,带入验证完成相关的问题.
【解答】解:通常情况下A是能参与绿色植物光合作用的气体,因此A是二氧化碳;
B在工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等领域,因此B是碳酸钠;
D的溶液呈蓝色,因此D是铜盐;E是地壳中含量最多金属元素的单质,因此E
是铝;F能够和B﹣碳酸钠、E﹣铝反应,因此F是酸;C能够和B﹣碳酸钠、D﹣
铜盐反应,因此C是碱或盐,如氢氧化钙,或氯化钡等,因此:
(1)A参与光合作用所得的气体产物是氧气;B是碳酸钠,化学式为:Na CO ;
2 3
(2)F是酸,如盐酸、硫酸;
(3)C和D的反应是氢氧化钙和硫酸铜的反应,反应的方程式为:Ca(OH)
+CuSO =Cu(OH) ↓+CaSO ;
2 4 2 4
(4)E和F可以是铝与盐酸的反应,反应的方程式为:2Al+6HCl=2AlCl +3H ↑;
3 2
故答案为:(1)O ;Na CO ;(2)盐酸(或硫酸);(3)Ca(OH)+CuSO =Cu(OH)
2 2 3 2 4
↓+CaSO ; (4)2Al+6HCl=2AlCl +3H ↑.
2 4 3 2
【点评】本题属于常见物质的推断题,在解此类题时,首先将题中有特征的物质推
出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可
12.(10分)某化学研究性学习小组进行了氨(NH )的制取和有关性质的探究实
3
验.
第17页(共21页)资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,能使湿
润的红色石蕊试纸变蓝色,极易溶于水,浓氨水具有挥发性.加热熟石灰和氯
化铵固体混合物可以生成氨气,若要快速产生氨气,可以将浓氨水滴加到生石
灰中得到.
请根据有关信息回答下列问题:
(1)仪器a的名称是 试管 .
(2)利用 A 装置制取氨气的化学方程式是 Ca ( OH ) + 2NH Cl
2 4
CaCl + 2H O + 2NH ↑ .
2 2 3
(3)将浓氨水滴加到生石灰中快速产生氨气,发生装置最好是 B (选填装置编
号).
(4)研究性学习小组用D装置收集氨气,判断氨气已经收集满的方法是 将湿润
的红色石蕊试纸放在 m 端,若试纸变蓝色,说明氨气已经集满 .
(5)研究性学习小组用如图2所示的装置探究氨的性质,观察到脱脂棉团由白色
变为红色.该现象涉及到的性质是 ABD (填字母编号).
A.氨分子是不断运动的 B.浓氨水具有挥发性
C.氨气有刺激性气味 D.氨气的水溶液显碱性
第18页(共21页)(6)若将制取氨气的熟石灰溶于水形成的饱和溶液置于小烧杯并放入一只大烧
杯中(如图3),在大烧杯中加入下列物质,观察到小烧杯中饱和溶液变浑浊,
则加入的物质是 AD (填字母编号).
A.水和浓硫酸 B.水和氯化钠固体
C.水和硝酸铵固体 D.水和氢氧化钠固体.
【考点】4O:常用气体的发生装置和收集装置与选取方法;7F:溶解时的吸热或放
热现象;8L:生石灰的性质与用途;BA:分子的定义与分子的特性;G5:书写化
学方程式、文字表达式、电离方程式.
【专题】534:常见气体的实验室制法、检验、干燥与净化.
【分析】(1)要熟悉各种仪器的名称、用途和使用方法;
(2)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程
式;
(3)不同的实验装置,功能不同;
(4)氨气的密度比空气小;
(5)根据实验现象可以判断相关方面的问题;
(6)浓硫酸溶于水放出大量的热,氢氧化钠溶于水放出大量的热,氯化钠溶于水
时温度无明显变化,硝酸铵溶于水时吸收热量;
氢氧化钙的溶解度随着温度的升高而减小,随着温度的降低而增大.
【解答】解:(1)仪器a的名称是试管.
故填:试管.
(2)利用 A 装置制取氨气的化学方程式是:Ca(OH) +2NH Cl
2 4
CaCl +2H O+2NH ↑.
2 2 3
故填:Ca(OH) +2NH Cl CaCl +2H O+2NH ↑.
2 4 2 2 3
(3)将浓氨水滴加到生石灰中快速产生氨气,该反应不需要加热,因此A排除,最
好是B装置,因为分液漏斗能够控制浓氨水的流速,从而可以控制反应速率,
同时分液漏斗还能够防止氨气从分液漏斗逸出.
故填:B.
(4)研究性学习小组用D装置收集氨气,判断氨气已经收集满的方法是将湿润的
红色石蕊试纸放在m端,若试纸变蓝色,说明氨气已经集满.
第19页(共21页)故填:将湿润的红色石蕊试纸放在m端,若试纸变蓝色,说明氨气已经集满.
(5)观察到脱脂棉团由白色变为红色,说明氨分子是不断运动的,浓氨水具有挥
发性,氨气的水溶液显碱性.
故填:ABD.
(6)若将制取氨气的熟石灰溶于水形成的饱和溶液置于小烧杯并放入一只大烧
杯中,若观察到小烧杯中饱和溶液变浑浊,说明加入的物质能使温度升高,加
入水和浓硫酸、水和氢氧化钠固体都能够使温度升高.
故填:AD.
【点评】实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实
验、分析实验,为揭示物质之间相互作用的实质奠定基础.
13.(4分)某地一辆满载浓硫酸的罐车翻倒,导致溶质质量分数为98%的浓硫酸
20t泄漏,并向路基两边蔓延.接到报警后消防官兵立即赶来并用石灰浆(主要
成分为氢氧化钙)中和硫酸解除了险情.请回答:
(1)溶质质量分数为98%的浓硫酸20t中含H SO 的质量是 19.6 t ;
2 4
(2)计算中和泄漏的98%浓硫酸20t,理论上需要氢氧化钙的质量.
【考点】7U:有关溶质质量分数的简单计算;G6:根据化学反应方程式的计算.
【专题】193:有关化学方程式的计算.
【分析】稀释前后的硫酸溶液中,硫酸的质量是不变的,所以,中和掉的硫酸就是
25吨98%的浓硫酸中的硫酸;根据反应的化学方程式,由硫酸的质量计算氢氧
化钙的质量.经过化学方程式的计算得出氢氧化钙.
【解答】解:
(1)20t质量分数为98%的浓硫酸中硫酸的质量=20t×98%=19.6t
(2)解:设理论上需要氢氧化钙的质量为x
H SO +Ca(OH) ═CaSO +2H O
2 4 2 4 2
98 74
19.6t x
x=14.8t
答案:
第20页(共21页)(1)98%的浓硫酸20t中含H SO 的质量为19.6t;
2 4
(2)中和泄漏的硫酸理论上需要氢氧化钙的质量为14.8t.
【点评】考查学生化学方程式与溶液的溶质质量分数的综合计算,计算过程较为
简单,此题能锻炼学生的良好思维及解题能力.
第21页(共21页)