文档内容
2025 年普通高中学业水平选择性考试(模拟)
化 学 参 考 答 案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C B C C A C D A D D C D B A D
16、(1)C (2)打开放空阀,打开活塞,逐滴放出过量水
(3)降低过氧乙酸浓度,提高其稳定性,防止反应时发生爆炸 当油水分离器中
水层不再增加(4)① EHFC ②
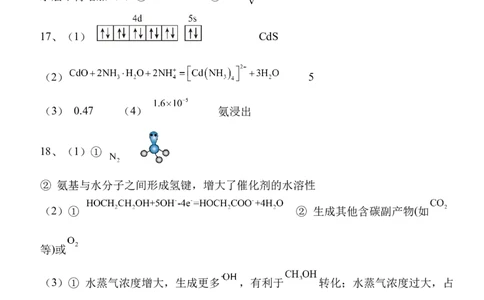
17、(1) CdS
(2) 5
(3) 0.47 (4) 氨浸出
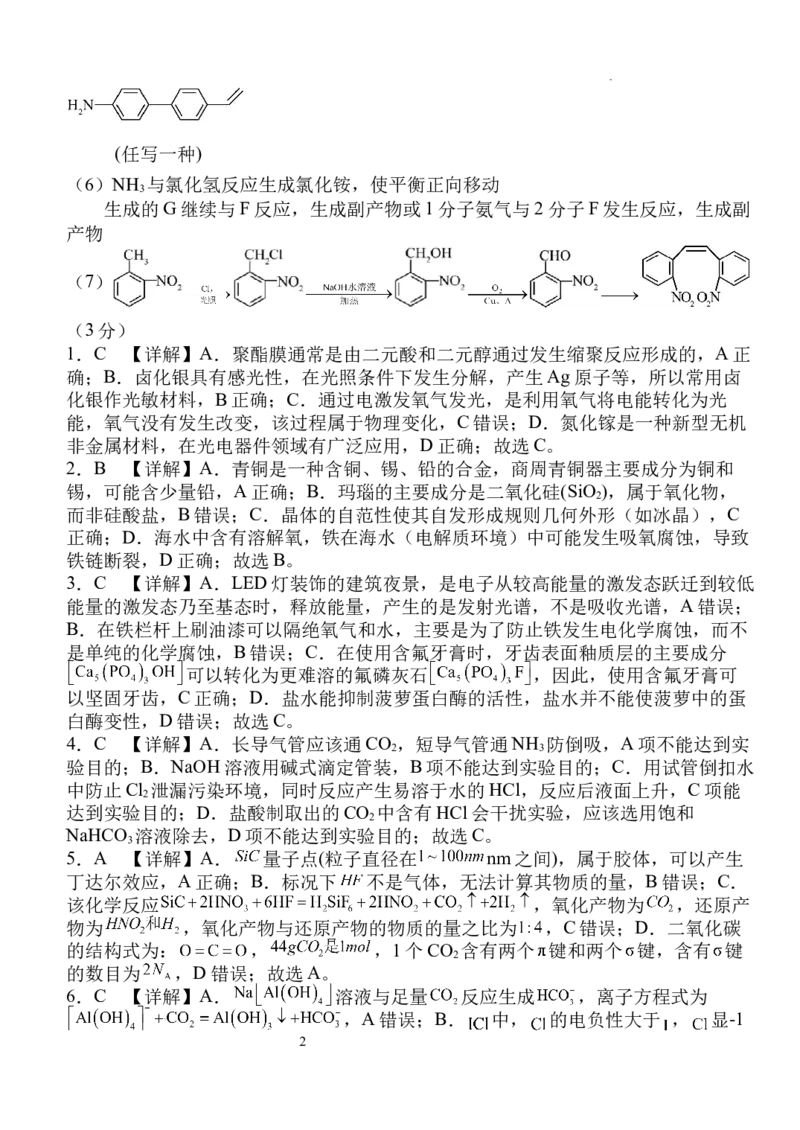
18、(1)①
② 氨基与水分子之间形成氢键,增大了催化剂的水溶性
(2)① ② 生成其他含碳副产物(如
等)或
(3)① 水蒸气浓度增大,生成更多 ,有利于 转化;水蒸气浓度过大,占
据较多氧空位,不利于甲醇吸附 ② CO被 氧化(或 )
19、(1)BD(1分) (2)2(1分)
(3)浓硫酸、浓硝酸、加热(1分) 邻硝基甲苯或2-硝基甲苯(1分) (4)
AB
(5) 、 、
1
学科网(北京)股份有限公司(任写一种)
(6)NH 与氯化氢反应生成氯化铵,使平衡正向移动
3
生成的G继续与F反应,生成副产物或1分子氨气与2分子F发生反应,生成副
产物
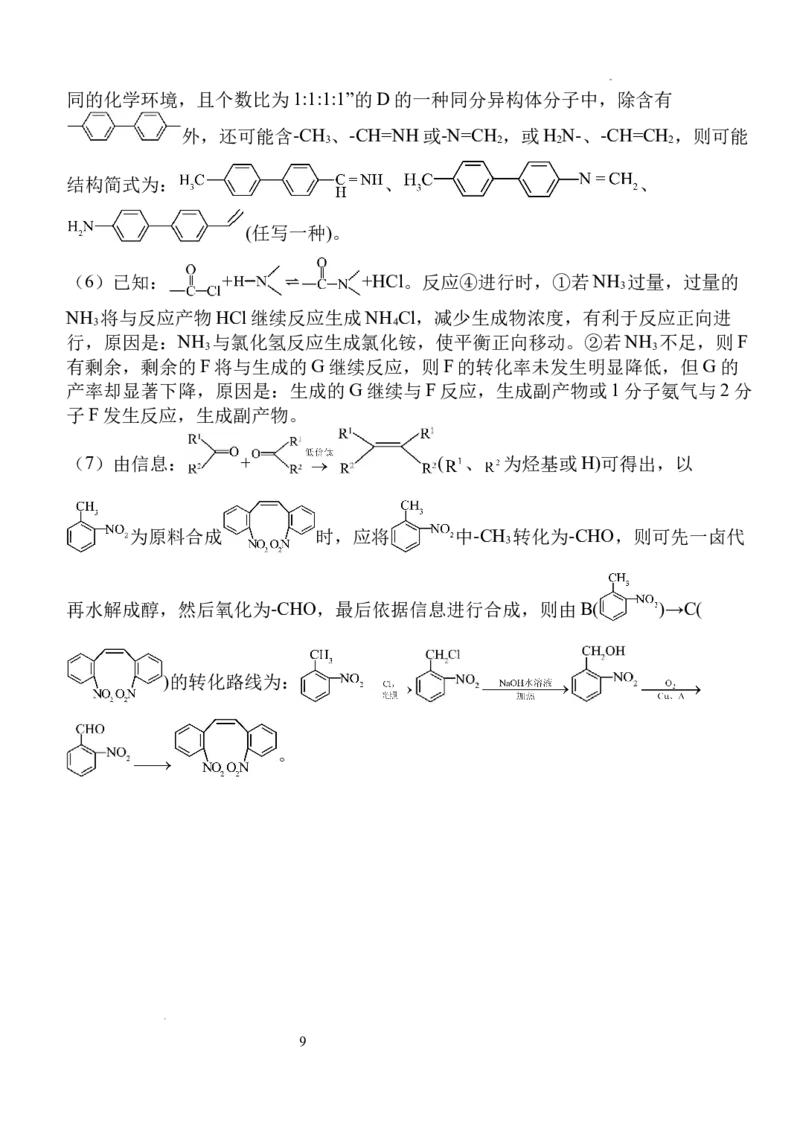
(7)
(3分)
1.C 【详解】A.聚酯膜通常是由二元酸和二元醇通过发生缩聚反应形成的,A正
确;B.卤化银具有感光性,在光照条件下发生分解,产生Ag原子等,所以常用卤
化银作光敏材料,B正确;C.通过电激发氧气发光,是利用氧气将电能转化为光
能,氧气没有发生改变,该过程属于物理变化,C错误;D.氮化镓是一种新型无机
非金属材料,在光电器件领域有广泛应用,D正确;故选C。
2.B 【详解】A.青铜是一种含铜、锡、铅的合金,商周青铜器主要成分为铜和
锡,可能含少量铅,A正确;B.玛瑙的主要成分是二氧化硅(SiO ),属于氧化物,
2
而非硅酸盐,B错误;C.晶体的自范性使其自发形成规则几何外形(如冰晶),C
正确;D.海水中含有溶解氧,铁在海水(电解质环境)中可能发生吸氧腐蚀,导致
铁链断裂,D正确;故选B。
3.C 【详解】A.LED灯装饰的建筑夜景,是电子从较高能量的激发态跃迁到较低
能量的激发态乃至基态时,释放能量,产生的是发射光谱,不是吸收光谱,A错误;
B.在铁栏杆上刷油漆可以隔绝氧气和水,主要是为了防止铁发生电化学腐蚀,而不
是单纯的化学腐蚀,B错误;C.在使用含氟牙膏时,牙齿表面釉质层的主要成分
可以转化为更难溶的氟磷灰石 ,因此,使用含氟牙膏可
以坚固牙齿,C正确;D.盐水能抑制菠萝蛋白酶的活性,盐水并不能使菠萝中的蛋
白酶变性,D错误;故选C。
4.C 【详解】A.长导气管应该通CO ,短导气管通NH 防倒吸,A项不能达到实
2 3
验目的;B.NaOH溶液用碱式滴定管装,B项不能达到实验目的;C.用试管倒扣水
中防止Cl 泄漏污染环境,同时反应产生易溶于水的HCl,反应后液面上升,C项能
2
达到实验目的;D.盐酸制取出的CO 中含有HCl会干扰实验,应该选用饱和
2
NaHCO 溶液除去,D项不能达到实验目的;故选C。
3
5.A 【详解】A. 量子点(粒子直径在 nm之间),属于胶体,可以产生
丁达尔效应,A正确;B.标况下 不是气体,无法计算其物质的量,B错误;C.
该化学反应 ,氧化产物为 ,还原产
物为 ,氧化产物与还原产物的物质的量之比为 ,C错误;D.二氧化碳
的结构式为: , ,1个CO 含有两个 键和两个 键,含有 键
2
的数目为 ,D错误;故选A。
6.C 【详解】A. 溶液与足量 反应生成 ,离子方程式为
,A错误;B. 中, 的电负性大于 , 显-1
2
学科网(北京)股份有限公司价, 显+1价,则离子方程式为 ,B错误;C.用惰性电极
电解 溶液,阳极上 放电生成 ,阴极上 放电生成 和 , 和
反应生成 沉淀,方程式书写正确,C正确;D. 和 会发生氧
化还原反应,D错误;故答案为:C。
7.D 【详解】A.乙醇和二甲醚互为同分异构体,但由于乙醇中存在分子间氢
键,而二甲醚中不存在,导致乙醇(78.3℃)的沸点高于二甲醚(-29.5℃),即与氢键作
用有关,A不合题意;B.AlF 是离子晶体,AlCl 是分子晶体,作用力:离子键>范
3 3
德华力,导致AlF 的熔点远高于AlCl ,则AlF 的熔点远高于AlCl 与晶体类型有
3 3 3 3
关,B不合题意;C.电负性:F>Cl,故PF 中共用电子对离P更远,排斥力更小,
3
键角更小,且原子半径:F<Cl,故PF 的键角小于PCl ,即与F、Cl的电负性差异有
3 3
关,C不合题意; D.热分解温度:HBr为500℃,HI为300℃,稳定性HBr>HI,
是由于非金属性Br>I,导致H-Br的键能比H-I的键能大,与分子间作用力无关,D
符合题意;故答案为:D。
8.A 【详解】A. 分子中的大π键可用符号 表示,其中m表示参与形成大π键
的原子数,n表示参与形成大π键的电子数; 中N原子有一个孤电子和一对孤电
子
对,一个孤电子参与形成大π键,则6个原子(5个C原子和1个N原子)和6个电
子形成大π键,表示为 ,故A正确;B . 按照系统命名法,选择含有碳原子最多的
碳链作为主链,从靠近最简单支链的一端给主链编号,故该有机物的名称为2,2,
4,5-四甲基-3-乙基己烷,故B错误;C. 酚醛树脂是一种人工合成的高分子材料,由
苯酚和甲醛缩聚而成,故C错误;D.生成水的同时又生成CaSO 微溶,故
4
ΔH<2×(-57.3)kJ·mol-1,D错误;故答案为:A。
9.D 【详解】A.纤维素分子中含有多个羟基,链间能形成多个氢键,导致与水
分子间氢键作用减弱,故纤维素难溶于水,A正确;B.纤维素在低温下可溶于氢氧
化钠溶液,是因为碱性体系主要破坏纤维素链之间的氢键,水分子通过扩散进入纤维
素链间隙,引发溶胀,B正确;C.尿素分子可以在纤维素分子链周围形成动态的
“包覆层”,防止纤维素分子链在室温下重新形成氢键,从而保持纤维素的稳定性,
C正确;D.低温时,纤维素分子链间的氢键相互作用力增强,使得纤维素更难被溶
解,D错误;故选D。
10.D 【分析】在催化剂中加入盐酸和过氧化氢混合溶液,将钯转化为 、
,氧化铝转化为可溶性金属氯化物,SiO 不反应,过滤得到滤渣,则滤渣中含
2
有:SiO 和C;滤液中含有 、 ;SiO -18-冠-6超分子具有识别功能,可以
2 2
分离 和 ,得到 ,加入氯化铵和过氧化氢将 转化为(NH ) PdCl
4 2 6
沉淀,将(NH ) PdCl 与 发生氧化还原反应制得钯。
4 2 6
【详解】A.由分析可知,滤渣的主要成分为SiO 、C,A项正确;B.“酸浸”时,
2
主要发生的反应为:Pd+2H++H O +4Cl-= +2H O,B项正确;C.由分析可知,
2 2 2
SiO -18-冠-6超分子具有识别功能,可以分离 和 ,得到 ,C项正
2
3
学科网(北京)股份有限公司确;D.“沉钯”时, 被氧化为 并形成(NH ) PdCl 沉淀,D项错误;故
4 2 6
选:D。
11.C 【详解】A.因鲁米诺在碱性环境中,可被 分解产生的活性氧氧化并释
放蓝色荧光,故实验需要维持溶液碱性环境,A正确;B.探究速率时,需要控制唯
一变量,实验1、2的总体积为150.5mL,故 ,B正确;C.实验1和实验2中,
发光时间越长,说明溶液中 分解速率慢,溶液中发挥催化作用的 浓度越
低,C错误;D.实验2中滴加 ,则发光时间长,荧光强度弱,说明 浓度
越低, 与 配位,故与 配位能力: ,D正确;故选C。
12.D 【分析】短周期中,钠原子半径最大,故Y为钠;由基态X原子价层电子排
布式为 知,价层电子排布式为 ,X为氧;W的最高正化合价和最低负化
合价代数和等于0,W最高正化合价和最低负化合价绝对值相等,W原子序数大于
11,所以W为硅,由“ ”组成可知,化合价代数和等于 为 价,故Z为
铝。
【详解】A.电子层数相同,则核电荷数越多半径越小,故离子半径: ,
A错误;B. 、 的阴、阳离子数目比均为 ,B错误;C. 分子是极性
分子,C错误;D.钠,铝是金属晶体,硅是共价晶体,硅的熔点最高;金属原子的
半径越小,价电子数越多,金属键越强,铝的价电子数多于钠,半径小于钠,故铝的
熔点高于钠,单质熔点: ,D正确;故答案选D。
13.B 【分析】由图可知,甲烷在a极失去电子发生氧化反应生成二氧化碳和氢离
子,a极为阳极,生成的氢离子通过质子交换膜由阳极区进入阴极区,b极为阴极,
酸性条件下氧气在阴极得到电子发生还原反应生成过氧化氢,反应生成的过氧化氢与
Fe2+反应生成羟基自由基,羟基自由基与溶液中的CN-反应生成氮气和二氧化碳。
【详解】A.由分析可知,a极为电解池的阳极,水分子作用下甲烷在阳极失去电子
发生氧化反应生成二氧化碳和氢离子,生成的氢离子通过质子交换膜由阳极区进入阴
极区,故A正确;B.由分析可知,a极为电解池的阳极,a极电极反应为CH -8e-
4
+2H O=CO +8H+,反应中消耗水,若为弱酸条件下,电解过程中a极区pH减小,故
2 2
B错误;C.由分析可知,b极为阴极,酸性条件下氧气在阴极得到电子发生还原反
应生成过氧化氢,电极反应式为 ,反应生成的过氧化氢与Fe2+反
应生成羟基自由基,反应的离子方程式为 ,故C正
确;D.由分析可知,b极为阴极,酸性条件下氧气在阴极得到电子发生还原反应生
成过氧化氢,电极反应式为 ,反应生成的过氧化氢与Fe2+反应生
成羟基自由基,反应的离子方程式为 ,羟基自由基与
溶液中的CN-反应生成氮气和二氧化碳,反应的离子方程式为2CN-
+10·OH+2H+=2CO ↑+N ↑+ 6H O,由方程式可得如下转化关系CN-
2 2 2
~5·OH~5H O ~10e-,则处理1molCN-时,不考虑其他副反应,理论上电路中通过电子
2 2
的物质的量为10mol,故D正确;故选B。
14.A 【详解】A.图3中原子3和原子4的连线为面对角线,长度为 ,故
A错误;B.根据均摊原则,晶胞中钼原子数为 ,金属钼的密度为
4
学科网(北京)股份有限公司,故B正确;C.原子 2在体心,若图1中原子1的
分数坐标为 ,则原子2的分数坐标为 ,故C正确;D.金属钼晶胞为
体心立方堆积,晶胞中钼原子数为2,钼原子半径为体对角线的 ,所以钼原子半径
为 ,钼原子的空间利用率为 ,故D正确;选A。
15.D 【详解】A.从图像可知,当pH过大时,会生成 、 等含铅微
粒,并非pH越大除铅效果越好,因为这些含铅微粒仍存在于溶液中,A错误;B.
已知NH ·H O的Kb=1.74×10-5,当pH=8时,c(OH-)=10-6mol/L,根据K =
3 2 b
可得 = = =17.4,说明溶液中的氨主要以 的
形式存在,B错误;C.由题干图像可知,当pH=7.9时,含铅微粒为Pb(OH) 、
2
Pb2+和Pb(OH)+,则Pb2+的浓度为0.01mol/L×0.42=0.0042mol/L,c(OH-)=10-6.1mol/L,
则 =0.0042mol/L×(10-6.1)2=0.0042×10-12×10-0.2=0.0042×0.63×10-
12=2.6×10-15,C错误;D. 的平衡常数为K=
,由图像可知,当pH=7.9时,c(Pb2+)=c[Pb(OH)+],此时c(OH-)=10-6.1,
故K=10-6.1,D正确;故答案为:D。
16.【分析】本题实验目的是制备过氧化乙酸,其实验原理是CH COOH+H O
3 2 2
CH COOOH+H O,为了增加过氧化氢的利用率,恒压滴液漏斗中盛放双氧
3 2
水,三颈烧瓶中盛放固体酸催化剂、乙酸丁酯、冰醋酸,达到要求后再滴加双氧水,
据此分析;
【详解】(1)A.根据上述分析,液体A为醋酸,醋酸过量,提高H O 的转化率,
2 2
故A错误;B.仪器6中冷凝水应是a进b出,故B错误;C.过氧乙酸见光或受热
易分解,因此为防止分解,利用抽气泵降低装置内的压强,降低共沸物的沸点,减少
过氧化乙酸的分解,故C正确;D.为防止抽气泵的损坏,反应结束后,先打开仪器
5
学科网(北京)股份有限公司7处的放空阀,再关闭抽气泵,故D错误;答案为C;
(2)分离器中水层液面升高到支管口时,防止水流入三颈烧瓶中,降低产品的产
率,需要将水排除,具体操作为打开放空阀,打开活塞,逐滴放出过量水;故答案为
打开放空阀,打开活塞,逐滴放出过量水;
(3)纯品过氧乙酸极为敏感,易发生爆炸性反应,因此乙酸丁酯的作用之一是降低
过氧乙酸浓度,提高其稳定性,防止反应时发生爆炸;当油水分离器中水层不再增
加,说明反应已完成;故答案为降低过氧乙酸浓度,提高其稳定性,防止反应时发生
爆炸;当油水分离器中水层不再增加;
(4)①过氧乙酸的氧化性与高锰酸钾相当,应用移液管或酸式滴定管量取一定体积
的样品,置于锥形瓶中,从淀粉溶液滴瓶中取出并加入指示剂,硫代硫酸钠溶液显碱
性,因此用碱式滴定管盛装,故答案为EHFC;
②滴定1中建立关系式为“-O-O-”~I ~2Na S O ,得出“-O-O-”的物质的量为
2 2 2 3
;滴定2中5H O ~2MnO ,过氧化氢的物质的量为
2 2
;则样品中过氧乙酸中浓度为
= mol/L;故答案为
。
17.【分析】烧结电尘(主要成分为CdO、CdSO ,含CdS、Pb、Zn等杂质)加入
4
硫酸铵和氨水浸出,金属元素与NH 配位形成配合物进入溶液, 浸出得到
3
,则CdO浸出也得到 ,净化工序中除去铅,含Cd微粒未发
生变化,则电解工序中, 在阴极得电子生成粗Cd,沉镉工序中,加入锌
粉置换出镉,精炼后得到精Cd;沉Cd余液中加入H S,生成ZnS,过滤得到沉锌余
2
液,据此分析回答。
【详解】(1)Zn的原子序数为30,基态Zn原子的价电子排布式为 ,Cd与Zn
同族且相邻,
基态Cd原子的价电子排布式为 ,价电子轨道表示式为:
,烧结电尘的主要成分为CdO、 ,含CdS、Pb、Zn等
杂质,结合净化工序得到富铅残渣可知,Pb元素进入净化工序,根据已知信息①可
知,CdS既不溶于水也不溶于氨溶液,则浸出渣的主要成分是CdS;
6
学科网(北京)股份有限公司(2)根据已知信息①可知, 浸出得到 ,则CdO浸出也得到
,离子方程式为 ;由图2可
知,
时,Cd浸出率最大,Zn浸出率相对小,则最佳 ,由图3可知,氨
铵比为 时,Cd浸出率大,Zn浸出率小于Cd,则最佳氨铵比为 ,结合
,可知 ;
(3)沉镉工序中,加入锌粉置换出镉,消耗 锌粉时,置换出
,质量为1.12g,则溶液质量减轻 ;
(4)溶液 , , ,
,
,
, ,
;为实现闭环循环,使元素充分利用,
沉锌余液可返回氨浸出工序。
18.【详解】(1)①肼硼烷水解: ,因为生
成的 可进一步转化为 或 ,若要增大氢气的产率,需提高生成 的选择
性; 中心原子价层电子对数为3+ =4,且含有1个孤电子对, 模
型为四面体形 ;②氨基中含有“N—H”键,它们能与水分子形成氢键,从而增
大了粒子间的亲合性,增大了催化剂的水溶性;
(2)①左侧乙二醇→乙醇酸,被氧化,失电子,为阳极,电极反应为
;
②1个乙二醇转化为1个乙醇酸,根据阳极反应式可知,转移了4个电子,因生成其
他含碳副产物(如 等)或 ,消耗了部分电量,导致生成乙醇酸的电量减少,乙醇
酸的法拉第效率小于100%;
(3)①由反应机理图可知,随着水蒸气浓度的增大, 的转化率先增大后减小
的原因是:水蒸气浓度增大,生成更多 (占据氧空位),有利于 转化,水
蒸气浓度过大,占据较多氧空位,甲醇无法占据氧空位,不利于甲醇吸附( );
7
学科网(北京)股份有限公司②由反应机理图可知,过程中 会分解生成CO,导致催化剂中毒,适当增大水
蒸气的浓度,能降低CO的含量,原因是:活性 具有氧化性,CO被活性 氧化
(或 )。
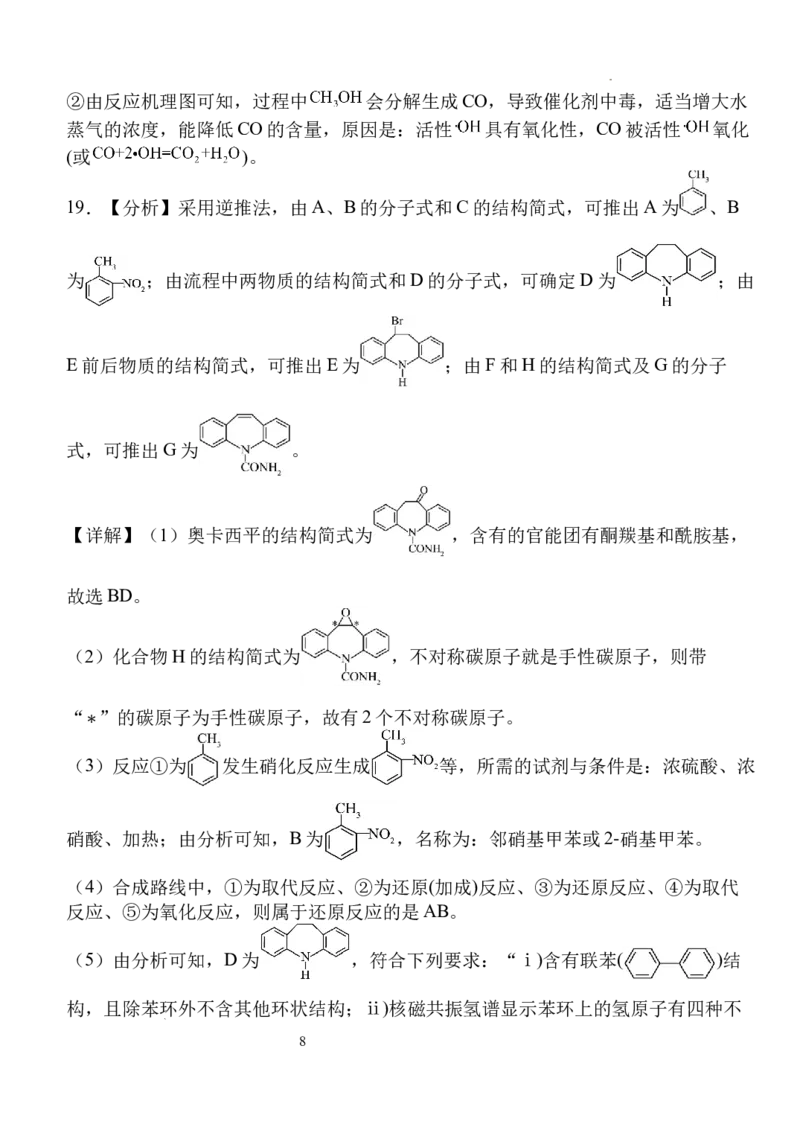
19.【分析】采用逆推法,由A、B的分子式和C的结构简式,可推出A为 、B
为 ;由流程中两物质的结构简式和D的分子式,可确定D为 ;由
E前后物质的结构简式,可推出E为 ;由F和H的结构简式及G的分子
式,可推出G为 。
【详解】(1)奥卡西平的结构简式为 ,含有的官能团有酮羰基和酰胺基,
故选BD。
(2)化合物H的结构简式为 ,不对称碳原子就是手性碳原子,则带
“∗”的碳原子为手性碳原子,故有2个不对称碳原子。
(3)反应①为 发生硝化反应生成 等,所需的试剂与条件是:浓硫酸、浓
硝酸、加热;由分析可知,B为 ,名称为:邻硝基甲苯或2-硝基甲苯。
(4)合成路线中,①为取代反应、②为还原(加成)反应、③为还原反应、④为取代
反应、⑤为氧化反应,则属于还原反应的是AB。
(5)由分析可知,D为 ,符合下列要求:“ⅰ)含有联苯( )结
构,且除苯环外不含其他环状结构;ⅱ)核磁共振氢谱显示苯环上的氢原子有四种不
8
学科网(北京)股份有限公司同的化学环境,且个数比为1:1:1:1”的D的一种同分异构体分子中,除含有
外,还可能含-CH 、-CH=NH或-N=CH ,或H N-、-CH=CH ,则可能
3 2 2 2
结构简式为: 、 、
(任写一种)。
(6)已知: + ⇌ +HCl。反应④进行时,①若NH 3 过量,过量的
NH 将与反应产物HCl继续反应生成NH Cl,减少生成物浓度,有利于反应正向进
3 4
行,原因是:NH 与氯化氢反应生成氯化铵,使平衡正向移动。②若NH 不足,则F
3 3
有剩余,剩余的F将与生成的G继续反应,则F的转化率未发生明显降低,但G的
产率却显著下降,原因是:生成的G继续与F反应,生成副产物或1分子氨气与2分
子F发生反应,生成副产物。
(7)由信息: + ( 、 为烃基或H)可得出,以
为原料合成 时,应将 中-CH 转化为-CHO,则可先一卤代
3
再水解成醇,然后氧化为-CHO,最后依据信息进行合成,则由B( )→C(
)的转化路线为:
。
9
学科网(北京)股份有限公司