文档内容
主 编:麻生明 陈 寅
本册主编:王韻华
编写人员: (以姓氏笔画为序)
王程杰 朱万森 刘瑞婷 李锋云
陆晨刚 陈雪莹
责任编辑:胡恺岩
美术设计:诸梦婷
普通高中教科书 化学 选择性必修2 物质结构与性质
上海市中小学(幼儿园)课程改革委员会组织编写
出
版
上海世纪出版(集团)有限公司 上海科学技术出版社
(上海市钦州南路71 号 邮政编码200235)
发 行 上海新华书店
印 刷 当纳利(上海)信息技术有限公司
版 次 2021 年3 月第1 版
印 次 2021 年3 月第1 次
开 本 890 毫米×1240 毫米 1/16
印 张 6.5
字 数 144 千字
书 号 ISBN 978—7—5478—5300—9/G·1038
定 价 8.40 元
版权所有·未经许可不得采用任何方式擅自复制或使用本产品任何部分·违者必究
如发现印装质量问题或对内容有意见建议,请与本社联系。电话:021—64848025,邮箱:jc@sstp.cn
全国物价举报电话:12315
声明 按照《中华人民共和国著作权法》第二十三条有关规定,我们已尽量寻找原作
者支付报酬。原作者如有关于支付报酬事宜可及时与出版社联系。
1.1
氢原子结构模型 …………………………………………………… 3
1.2
多电子原子核外电子的排布 ……………………………………… 12
1.3
元素周期律 ………………………………………………………… 17
本章复习 ………………………………………………………………… 26
2.1
共价分子的空间结构 ……………………………………………… 31
2.2
分子结构与物质的性质 …………………………………………… 45
2.3
配位化合物和超分子 ……………………………………………… 56
本章复习 ………………………………………………………………… 65
3.1
金属晶体 …………………………………………………………… 71
3.2
离子晶体 ……………………………………………………………80
3.3
共价晶体和分子晶体 ……………………………………………… 85
本章复习 …………………………………………………………………94
目 录
第1 章 原子结构与性质…………………………………………………
1
第2 章 分子结构与性质………………………………………………… 29
第3 章 晶体结构与性质………………………………………………… 69
Ⅰ
化学词汇中英文对照表 ………………………………………………98
Ⅱ
学生必做实验索引 …………………………………………………98
Ⅲ
元素周期表 …………………………………………………………99
附
录
… …………………………………………………………………………… 98
1
第1 章
1
科学家们锲而不舍地努力,揭示了原
子结构的奥秘,知道了原子核外电子的排
布决定元素在周期表中的位置。
原子结构与性质
氢原子结构模型
多电子原子核外电子的排布
元素周期律
1.1
1.2
1.3
2
原
子(atom)”一词是从希腊语转化而来,原意为不可切分
的。直到20 世纪初,科学家们才发现原子其实具有复杂的
内部结构。原子由原子核和绕核运动的电子构成,原子核由带正电
的质子和电中性的中子构成。原子的质子数决定了该原子属于哪一
种元素,而中子数则决定了该原子是此元素的哪一种核素。这一章
将介绍原子核外电子的运动规律、电子的运动与宏观物体运动的区
别,以及科学家是怎样描述原子核外电子运动状态的。
通过学习,我们将更深入地了解原子核外电子的运动特点,认
识原子核外电子的排布与元素性质之间的关系,并从本质上理解元
素的原子半径、电离能、电负性等基本性质的周期性变化规律。
“
氢原子结构模型
3
1.1
身边的有机化合物
第7 章
1.1
氢原子结构模型
科学家是通过研究原子光谱来了解原子核外电子运动
状态的。
光谱就是通过棱镜或光栅的分光作用,将一束复色光分
解成各种波长的单色光,按照波长或频率大小顺序排列起来
形成的图案。得到的图案如果是一条连续的亮带,就是连续
光谱[图1.1(a)];得到的图案如果是不连续的亮线,就是线
光谱。各元素原子的线光谱就叫做原子光谱[图1.1(b)
(c)]。
氢原子光谱和玻尔原子结构模型
原子是肉眼和一般仪器都看不到的微粒,科学家们是
根据可观察、可测量的宏观实验事实,经过分析和推理,建
立原子结构的模型。如果出现新的实验事实无法得到解释,
那么原来提出的原子结构模型就会被修正,甚至被推翻。从
道尔顿原子论到原子结构的葡萄干面包模型,再进一步发展
为原子结构的有核模型,科学家们对原子结构模型的探索,
经历了一个不断深化和逐渐完善的过程。那么,原子中的电
子在核外又是如何运动的呢?科学家从最简单的、只有一个
电子的氢原子着手,来研究原子核外电子的运动规律。
了解有关原子核外电子运动模
型的历史发展过程
知道电子运动的能量状态具有
量子化的特征
知道电子的运动状态可通过原
子轨道和电子云模型来描述
知道原子光谱分析
学习聚焦
知识回放
● 卢瑟福的α 粒子散射实验
● 原子结构有核模型
● 原子核外电子排布
原子光谱是由原子中电子运动状态发生变化时释放或
吸收的能量形成的,与原子中电子的能量状态有最直接的关
系。例如,氢原子光谱在可见光区有4 条明亮的谱线,它们
的波长分别为:410.1 nm、434.1 nm、486.1 nm、656.3 nm
图1.1 可见光区内白光的连续光谱和汞、锶的原子光谱
(a) 白光的连续光谱
(b) 汞的原子光谱
(c) 锶的原子光谱
λ/nm
400
400
400
450
450
450
500
500
500
550
550
550
600
600
600
650
650
650
700
700
700
750 nm
750 nm
750 nm
原子结构与性质
第1 章
4
(图1.2)。氢原子光谱为什么是线光谱?氢原子在可见光
区的这些谱线,与氢原子核外电子运动的能量变化之间
有什么关系?
图1.2 氢原子在可见光区的线光谱
1913 年,丹麦物理学家玻尔(N. Bohr, 1885—1962)
在普朗克量子论、爱因斯坦光子学说和卢瑟福原子结构有核
模型的基础上,对核外电子的运动做了重要假设,建立了玻
尔原子结构模型,并解释了氢原子光谱。玻尔原子结构模型
的主要观点如下:
(1) 原子中的电子只能在某些确定半径的圆周轨道上
绕原子核运动。电子在这些轨道上绕核运动时既不吸收能
量也不辐射能量,这些轨道称为定态轨道。
(2) 在不同定态轨道上运动的电子具有不同的能量
(E),而且能量是量子化的,即轨道能量是“一份一份”地增
加或减少的。轨道能量与n 值有关。n 的取值为正整数1、2、
3、……、∞,n 值越小,电子离核越近,能量就越低;反之
能量就越高。一般把原子能量最低的电子状态称为基态。对
氢原子而言,当核外的一个电子处于n =1 的轨道时能量最低,
这个状态称为氢原子的基态;当这个电子跃迁至n>1 的轨道
上运动时,这些状态称为氢原子的激发态。
(3) 电子在不同能量的两个轨道之间发生跃迁时,才
会辐射或吸收能量。如果电子从高能量的轨道跃迁回到低
能量轨道,就会以光的形式释放出这些能量,光辐射的波
长(λ)与两个轨道的能量差(ΔE)有关。
400
410.1 434.1
486.1
656.3
H
450
500
550
棱镜
氢气放电管
照相底板
狭
缝
600
650
700
750 nm
氢原子结构模型
5
1.1
由于轨道的能量是不连续的,因此不同轨道之间的能
量差是不连续的,导致光辐射的波长也是不连续的。氢原
子光谱在可见光区中的4 条谱线,就是电子分别从n = 3,4,
5,6 的轨道跃迁回到n = 2 的轨道时释放的能量所形成的。
光辐射的波长和电子跃迁时吸收或释放的能量ΔE 有关,
ΔE = E2 — E1 = h· c
λ (h = 6.626 ×10
—34 J·s,为普朗克常数;
c = 2.997 924 58×10
8 m·s
—1,为真空中光速)。请指出氢原
子中电子分别从n = 5 和n = 2 的轨道跃迁到基态时,哪种光
辐射的波长更长。
氢原子光谱和里德伯公式
1885 年,在玻尔原子结构模型提出之前,瑞士科学家巴尔末(J. J. Balmer,
1825—1898)基于数据而非理论,发现了氢原子在可见光区4 条谱线的波长可以
用一个简单的公式来归纳:
λ = B(
n2
n2 — 4 )
上式叫做巴尔末公式,是一个经验公式,式中的n = 3,4,5,6,B = 364.56 nm。
1890 年,瑞典科学家里德伯(J. R. Rydberg,1854—1919)发现了描述碱金
属和氢原子光谱的通用公式,把描述氢原子光谱的巴尔末公式改写为:
= RH(
1
1
2
2
n2)
v = 1
λ
式中v 为波数,是λ 的倒数;n 是大于2 的正整数;RH 为里德伯常数,等于
1.096 776×10
7 m
—1。
随着玻尔原子结构模型的建立,光谱学家推导出了描述氢原子光谱的通用公式:
= RH(
1
1
n2
2
n1
2
)
v = 1
λ
式中的n1 和n2 分别表示核外电子发生跃迁的两个轨道的量子数,其中n1 < n2。
化学史话
想一想
原子结构与性质
第1 章
6
每当夜幕降临,华灯初上,五颜六色的灯光就把城市装扮得五彩缤纷。请联系氢原子
光谱的成因,说明这些美丽的光是怎样产生的。
图1.4 华灯初上的上海陆家嘴夜景
图1.3 列出了氢原子核外电子在不同轨道之间跃迁所产生的部分光谱系列。
图1.3 轨道跃迁与氢原子光谱系列的关系
想一想
红外系列
(n1=3)
紫外系列
(n1=1)
可见系列
(n1=2)
n=1
n=2
n=3
n=4
n=5
n=6
氢原子结构模型
7
1.1
玻尔原子结构模型不仅成功解释了氢原子光谱,也能
够对核外只有一个电子的离子(如He
+、Li
2+ 等)光谱做出
很好的解释,但不能解释多电子原子的光谱。科学家研究
发现,微观粒子既有波动性又有粒子性,它的运动速度和
空间位置无法同时准确测量,描述宏观物体运动的经典力
学方法不适用于描述微观粒子的运动。
自20 世纪20 年代起,科学家用原子轨道和电子云模
型来描述电子在原子核外空间运动的状态。下面我们来介
绍氢原子结构模型中的几个重要概念。
1. 原子轨道
当电子处于不同的运动状态时具有的能量是不同的。
通过有关的理论计算,可以得到氢原子核外电子运动的各
种状态和相对应的能量。人们沿用了玻尔原子结构模型中
“轨道”的概念,把氢原子中电子的一个空间运动状态称
为一个原子轨道。需要注意的是,此处轨道的含义与玻尔
原子结构模型中轨道的含义完全不同,它既不是圆周轨道,
也不是其他经典意义上的固定轨迹。由于描述电子运动状
态用的都是一些复杂的函数,所以常用图像的方式在三维
空间坐标系中表示出来。
电子运动的空间离核的远近是不同的。人们用n 表示
电子层数,n 相同的原子轨道称为一个电子层,n 的取值
为正整数1、2、3、4、5、6、7……。一个电子层也叫做
一个能层,和n = 1,2,3,4,5,6,7,……的电子层
相对应的能层符号分别用K、L、M、N、O、P、Q……
表示。n = 1 时,K 层的电子离核最近,电子运动状态的
能量最低;n 越大,表示电子离核越远,电子运动状态的
能量越高。
n 相同的原子轨道,轨道的图像形状可以不同,人们
分别用s、p、d、f……表示不同形状的原子轨道。例如,s
轨道是呈球形的,p 轨道是呈哑铃形的。不同形状的原子
轨道可能有不同的能量,因此同一能层中的原子轨道,还
可以分成不同的能级,如ns、np、nd、nf 等能级。第一能
层只有1s 一个能级,第二能层有2s、2p 两个能级,第三
能层有3s、3p、3d 三个能级。
氢原子的结构模型
原子结构与性质
第1 章
8
同一能级的原子轨道在三维空间坐标系中还可以有不同
的伸展方向。s 轨道只有一种空间取向,所以ns 只有一个原
子轨道[图1.5(a)]。p 轨道分别沿着x 轴、y 轴、z 轴有三
个不同的伸展方向,所以np 有px、py、pz 三个原子轨道[图
1.5(b)]。d 轨道有五个伸展方向,则nd 有五个原子轨道。
f 轨道有七个伸展方向,则nf 有七个原子轨道。
人们将表示电子层的n 值和表示原子轨道形状的s、p、
d、f 结合起来表示原子轨道,如1s、2s、2p(2px、2py、
2pz)等。
此外,原子核外电子还存在一种被称为“自旋”的运
动状态。处于同一原子轨道的电子有两种不同的自旋状态,
通常用向上箭头“ ”和向下箭头“ ”表示。当然,电子
“自旋”并非真像地球绕轴自旋一样,它只是表示电子两种
不同的自旋状态。
图1.5 原子轨道的空间伸展方向
电子自旋的提出
1921 年,德国物理学家施特恩(O. Stern,1888— 1969)和格拉赫(W. Gerlach,
1889 —1979)发现一束气态银原子束通过狭缝,再通过抽成真空的不均匀磁场后会发
生分裂,一半原子向上偏转,一半原子向下偏转。这个结果说明原子在磁场中不能任
意取向,首次证实了原子在磁场中取向量子化的事实。1925 年,荷兰物理学家乌伦贝
克(G. Uhlenbeck,1900 —1988)和古德斯密特(S. A. Goudsmit,1902 —1978)提出
电子自旋的假设,从而解释了施特恩—格拉赫实验的结果。
化学史话
(a)s 轨道
z
z
z
z
y
y
y
y
x
x
x
x
(b)p 轨道
+
+
+
+
—
—
—
氢原子结构模型
9
1.1
图1.7 氢原子的能级图
图1.6 银原子束在不均匀磁场中的分裂
原子中的能级按能量由低到高、由下往上排
列的示意图叫做原子的能级图,图1.7 是氢原子
的能级图。在只有一个电子的氢原子中,原子轨
道的能量仅与n 值有关,因此n 相同的原子轨道
处于同一个能级。
2. 电子云
由于微观粒子的运动特性,人们不能同时准
确测量电子运动的速度和位置,于是用统计的方
法来了解电子在原子核外空间某处出现的概率大
小。为了便于理解,人们常用小黑点的疏密程度
来表示电子在原子核外单位体积内出现的概率大
小。点密集的地方,表示电子在单位体积内出现
的概率大;点稀疏的地方,表示电子在单位体积
内出现的概率小。这种对电子在原子核外空间单
位体积内出现概率大小的形象化描述称为电子云。
1s、2p 轨道的电子云,如图1.8 所示。处于
1s 轨道上的电子(也称1s 电子)在空间出现的
概率分布呈球形对称,并且电子在原子核附近单
位体积内出现的概率大,离核越远,单位体积内
电子出现的概率越小。处于2p 轨道上的电子在
空间单位体积内出现的概率是沿着一个坐标轴(x
轴、y 轴或z 轴)对称分布的。2px 最大的电子云
① a.u. 是能量的原子单位的缩写,1 a.u. = 27.211 396 eV。
银原子流
银原子束
磁场
S
N
①
0
—0.5
1s
2s
3s
4s
2p
3p
3d
4p
4d
4f
n=∞
E/a.u.
原子结构与性质
第1 章
10
密度沿着x 轴分布,2py 最大的电子云密度沿着y 轴分布,
2pz 最大的电子云密度沿着z 轴分布。
图1.8 1s 和2p 轨道电子云空间分布图
量子化学是应用量子力学的基本原理和方法研究化学问题的一门基础学科。
量子化学研究范围包括:稳定和不稳定分子的结构、性能以及它们的结构与性能
之间的关系;分子与分子之间的相互作用;分子与分子之间的碰撞和相互反应等
问题。量子化学基础研究主要是,寻求量子化学中的自身规律,建立量子化学的
计算方法等。量子化学应用研究主要是,用量子化学方法处理化学问题,用量子
化学的结果解释化学现象。
量子化学在催化与表面化学、原子簇化学、分子动态学、生物与药物大分子
等其他化学分支学科的研究方面将发挥更大的作用。量子化学的研究结果在其他
化学分支学科的直接应用,建立了一些交叉学科,如量子有机化学、量子无机化
学、量子生物化学和量子药物化学等。
量子化学
链接学科
原子光谱分析法主要包括原子发射光谱分析法和原子
吸收光谱分析法。
原子在高温的作用下发射出各种波长的光,复合光经
分光后得到的由一系列不连续亮线组成的光谱,就是该种
元素的原子发射光谱。每一种元素的原子发射光谱都有其
各自确定的特征谱线, 这些谱线给出了原子核外电子在不
同能级的分布、能级之间跃迁的概率等丰富信息。科学家
根据原子发射光谱所提供的大量的、最直接的实验数据,
在研究、分析和阐明原子光谱的过程中建立和发展了原子
原子光谱分析
z
z
z
z
y
y
y
y
x
x
x
x
2pz
2py
2px
1s
氢原子结构模型
11
1.1
学习指南
● 请问n 等于3 的能层中有几个原子轨道?
● n 等于3 时,含有3s、3p 和3d 能级,3s 能级有1 个原子轨道,3p
能级有3 个原子轨道,3d 能级有5 个原子轨道。因此,n 等于3
的能层中一共含有9 个原子轨道。
例题导引
问题:
分析:
练习巩固
1. 下列叙述中,不符合玻尔原子结构模型观点的是( )。
(A) 原子核外电子做圆周运动的轨道分布是不连续的
(B) 电子从一个轨道跃迁至另一个轨道时,将吸收或辐射能量
(C) 电子在定态轨道上绕核运动时,不向外辐射能量
(D) 在不同轨道上运动的电子所具有的能量是连续分布的
2. 下列能级中,有3 个原子轨道的是( )。
(A) 1s
(B) 2p
(C) 3d
(D) 4f
3. 下列关于电子云或原子轨道的叙述中,正确的是( )。
(A) 电子云图中的小黑点越密,表示原子核外单位体积内的电子越多
(B) 原子轨道是电子运动的轨迹
(C) 原子轨道表示电子在空间各处出现的概率
(D) 电子云是用小黑点的疏密程度来表示电子在原子核外单位体积内出
现概率的大小
4. 简要说明不同的原子结构模型中轨道的含义有什么不同。
结构理论。原子发射光谱分析法也是元素定性、定量分析
和发现新元素的重要方法。
如果将一束白光通过受电或热的作用而产生的某种元
素的气态原子,由于气态原子吸收了白光中某些波长的单色
光,因此通过气态原子后的白光经分光后就会出现一系列不
连续的暗线,得到的光谱就是该种元素的原子吸收光谱。科
学家在对太阳光谱的研究中,就是根据原子吸收光的现象,
分析并发现了太阳中的化学元素。在此基础上发展起来的原
子吸收光谱分析法也被广泛应用于元素的定量分析中。
原子结构与性质
第1 章
12
除了氢原子外,其他的原子都是多电子原子。多电子
原子的电子运动状态也是用原子轨道来描述的,但是原子
轨道的能量除了与n 值有关,还与其他因素有关。通过原
子光谱和有关理论计算,人们能够推测基态原子中的电子
都排布在哪些原子轨道上。物质的化学性质与原子的电子
结构密切相关。了解多电子原子核外电子的排布,是学习
物质化学性质及其变化规律的重要基础。
科学研究表明,原子中的电子是按一定的规律排布在
各原子轨道上的,那么电子排布时又遵循了哪些规律呢?
科学家们根据光谱学和磁学研究提供的信息,总结出了基
态原子核外电子排布遵循的三条经验规则。
1. 能量最低原理
能量最低原理是指,原子核外电子在各原子轨道上的
排布方式应使整个原子的能量处于最低的状态。
确定原子核外电子填入原子轨道顺序的一个经验方法
是构造原理:从氢原子开始,按照原子核内增加一个质子,
核外增加一个电子的方式逐个构建原子,那么随着原子序
数的增加,每个新增加的核外电子将按照图1.9 中箭头所
指的先后顺序填入各组原子轨道中。
根据构造原理,基态原子核外电子排布的能级顺序依
次为:1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、5p、
6s……
2. 泡利不相容原理
1925 年,奥地利物理学家泡利(W. Pauli,1900 —1958)
通过总结大量原子光谱实验事实后指出,每个原子轨道中
最多只能容纳2 个自旋状态不同的电子,这条规则称为泡
利不相容原理。泡利不相容原理规定了每个能级可能容纳
的最大电子数。例如,ns 能级只有1 个原子轨道,最多能
容纳2 个电子;np 能级有3 个原子轨道,最多能容纳6 个
电子;nd 能级有5 个原子轨道,最多能容纳10 个电子;nf
能级有7 个原子轨道,最多能容纳14 个电子等。每个原子
轨道中的2 个电子自旋状态是不同的,例如:
身边的有机化合物
1.2
多电子原子核外电子的排布
基态原子核外电子的排布规则
认识原子核外电子排布规则
会书写1 ~36 号元素基态原
子的核外电子排布式和轨道
表示式
知道洪特规则的应用
学习聚焦
知识回放
● 原子轨道和电子云
● 各能级的原子轨道数
● 氢原子的能级图
● 结构示意图和电子式
图1.9 构造原理示意图
1s
2s
2p
3s
3p
4s
4p
5s
5p
6s
6p
6d
5d
4d
4f
5f
3d
7s
7p
13
1.2
多电子原子核外电子的排布
3. 洪特规则
当电子在能量相同的原子轨道上排布时,电子总是优先
按自旋状态相同的方式单独地占据各个原子轨道,然后再配
对,这样体系能量最低,这就是洪特规则。例如,氮原子2p
能级上有3 个电子,它们以自旋状态相同的方式排布如下:
此外,洪特规则还指出,当np、nd、nf 能级上电子处
于半满(p
3、d
5、f
7)或全满(p
6、d
10、f
14)状态时,体系
能量最低。
原子中的电子按照这三条规则在各原子轨道上排布
时,原子能量处于最低状态,这种状态是原子的基态,其
他状态则是原子的激发态。
根据泡利不相容原理完成下表。
书写表达
n 值
1
2
3
4
……
能级
1s
能级最多容纳
电子数
2
能层
K
……
能层最多容纳
电子数
2
s 轨道
p 轨道
d 轨道
原子结构与性质
第1 章
14
原子核外电子的排布该怎样来表示?我们以氮原子为例。
氮原子的原子序数为7,按照电子排布遵循的三条规
则,电子在各原子轨道上的排布为:
1s
22s
22p
3
上式中,写在原子轨道符号右上角的是各能级中的电
子数。这样的表示方法称为电子排布式。
由于在内层原子轨道上的电子能量较低,在外层原子
轨道上的电子能量较高,元素的化学性质主要取决于外层
原子轨道上的电子,这些电子被称为价电子。为方便起见,
通常我们只需要表示出原子价电子的排布,内层电子的排
布可用相应的稀有气体元素符号加方括号来表示。例如,
基态氮原子的电子排布式可以表示为:
[He]2s
22p
3
根据洪特规则,氮原子2p 能级上的3 个电子应以自旋
状态相同的方式排布,但电子排布式无法体现。为了明确
表示电子排布在同一能级各原子轨道时的方式,我们可以
用轨道表示式来表示。例如,基态氮原子的轨道表示式为:
核外电子排布的表示方法
根据前面讨论的原子核外电子排布遵循的三条规则,
就能写出各元素基态原子的电子排布式和轨道表示式。例
如,第2 周期元素基态原子的电子排布式和轨道表示式如
表1.1 所示。
表1.1 第2 周期元素基态原子的电子排布式和轨道表示式
原子序数
元素符号
电子排布式
轨道表示式
3
Li
1s
22s
1 或[He]2s
1
1s
2s
4
Be
1s
22s
2 或[He]2s
2
1s
2s
1s
2s
2p
15
1.2
多电子原子核外电子的排布
原子序数
元素符号
电子排布式
轨道表示式
5
B
1s
22s
22p
1 或[He]2s
22p
1
1s
2s
2p
6
C
1s
22s
22p
2 或[He]2s
22p
2
1s
2s
2p
7
N
1s
22s
22p
3 或[He]2s
22p
3
1s
2s
2p
8
O
1s
22s
22p
4 或[He]2s
22p
4
1s
2s
2p
9
F
1s
22s
22p
5 或[He]2s
22p
5
1s
2s
2p
10
Ne
1s
22s
22p
6 或[He]2s
22p
6
1s
2s
2p
(续表)
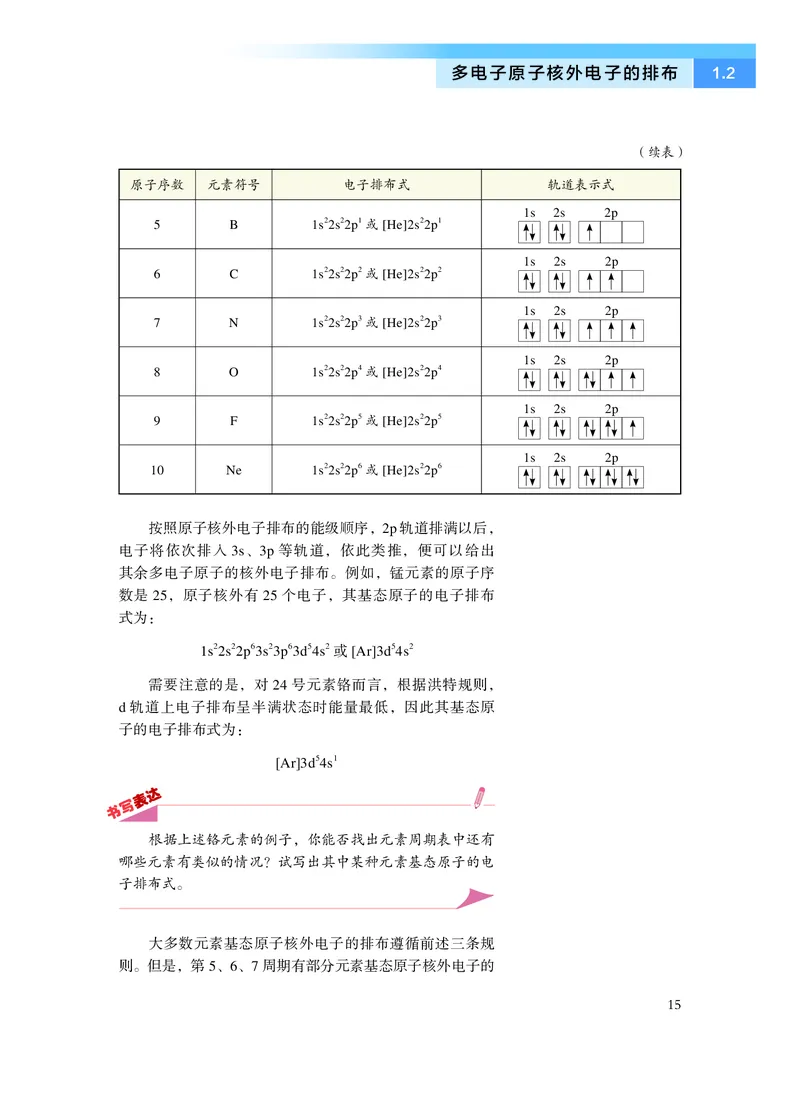
按照原子核外电子排布的能级顺序,2p 轨道排满以后,
电子将依次排入3s、3p 等轨道,依此类推,便可以给出
其余多电子原子的核外电子排布。例如,锰元素的原子序
数是25,原子核外有25 个电子,其基态原子的电子排布
式为:
1s
22s
22p
63s
23p
63d
54s
2 或[Ar]3d
54s
2
需要注意的是,对24 号元素铬而言,根据洪特规则,
d 轨道上电子排布呈半满状态时能量最低,因此其基态原
子的电子排布式为:
[Ar]3d
54s
1
大多数元素基态原子核外电子的排布遵循前述三条规
则。但是,第5、6、7 周期有部分元素基态原子核外电子的
根据上述铬元素的例子,你能否找出元素周期表中还有
哪些元素有类似的情况?试写出其中某种元素基态原子的电
子排布式。
书写表达
原子结构与性质
第1 章
16
练习巩固
1. 原子中n = 2 的能层最多能容纳的电子数是( )。
(A) 2 个
(B) 8 个
(C) 18 个
(D) 32 个
2. 基态Mg
2+的电子排布式正确的是( )。
(A) 1s
22s
22p
63s
1 (B) 1s
22s
22p
63s
2 (C) 1s
22s
22p
5
(D) 1s
22s
22p
6
3. 某元素基态原子的电子排布式为[Ne]3s
23p
3。下列关于它的描述中,正
确的是( )。
(A) 3p能级上的3 个电子能量相等,自旋状态相同
(B) 该原子的核外电子数为5
(C) 3p能级上的3 个电子能量相等,但自旋状态不同
(D) 该元素的原子的价电子数为3
4. 某元素基态原子的电子排布式为[Ar]3d
74s
2,该元素的原子序数是多少?
学习指南
● 根据多电子原子核外电子排布的规则,写出基态F
—的电子排布式。
● F 原子得到一个电子形成F
—,F 原子核外有9 个电子,因此F
—核
外有10 个电子。根据核外电子排布的三条规则,基态F
—的电子排
布式为:1s
22s
22p
6。
例题导引
问题:
分析:
根据基态原子核外电子排布的三条规则,写出11 ~ 18
号元素基态原子的电子排布式和轨道表示式。通过书写
练习,你能否总结出19 ~ 36 号元素的电子排布有怎样的
规律?
书写表达
排布并不完全符合这些规则。因此,原子核外电子的排布要
以实验测定结果为准。
17
1.3
元素周期律
身边的有机化合物
第7 章
1.3
元素周期律
1939 年美国化学家鲍林(L. Pauling,1901— 1994)
根据大量光谱实验结果和理论计算,总结出多电子原子
外层原子轨道能级高低顺序的一般规律,根据这一规律
画出的原子轨道能级图,称为鲍林近似能级图(图1.10)。
图中的每个小圆圈代表一个原子轨道,能量相同的原子
轨道并列为一个能级,能量相近的能级都纳入一个方框
内,同一方框内的能级称为一个能级组,共划分出7 个
能级组。除第一能级组只有1 个1s 能级,其余能级组均
由2 个及以上能级组成,且以ns 开始,以np 结束。能级
组间能量差较大,而能级组内各能级间能量差较小。多
电子原子核外电子排布的构造原理图就是以鲍林近似能
级图为基础绘制的。
核外电子排布与区、周期、族的划分
认识元素周期表中区、周期和
族的划分与原子核外电子排布
的关系
认识元素的原子半径、第一电
离能、电负性等性质的周期性
变化规律
能利用电负性判断元素的金属
性与非金属性的强弱,判断化
学键的类型
能举例说明元素周期律(表)
的应用,了解元素周期律
(表)的应用价值
学习聚焦
知识回放
● 基态原子核外电子的排布规则
● 电子排布式和轨道表示式
● 元素周期表的结构
图1.10 鲍林近似能级图
从1 ~36 号元素基态原子核外电子的排布中可以看到,
随着原子序数的增加,核外电子排布发生了周期性的变化。
考察元素周期表可以发现,区、周期、族的划分与原子核
外电子排布的周期性变化有内在联系。物质结构决定物质
的性质,原子核外电子排布的周期性变化也决定了元素性
质随着原子序数的递增呈现周期性递变规律。
能量
7p
6p
5p
4p
4p
5p
5d
6p
7s
5f
6d
7p
3d
4d
5d
6d
4f
5f
3d
4d
4f
3p
3p
2p
2p
7s
6s
5s
4s
4s
5s
6s
3s
3s
2s
2s
1s
1s
原子结构与性质
第1 章
18
鲍林近似能级图中的7 个能级组分别对应了元素周期
表中的7 个周期,每个周期所包含的元素种类数等于所对
应的能级组中所有原子轨道最多能容纳的电子数。
根据1 ~36 号元素在元素周期表中的位置,联系每一
族元素原子的价电子排布,尝试从中找出原子核外电子排布
与族划分之间的内在关系。
族的划分与元素原子价电子排布密切相关。一般来说,
同族元素的价电子数相同,对主族元素而言,其价电子数
与主族序数相同。主族元素原子的价电子全部排布在最外
层的ns 或nsnp 轨道上。对于主族元素原子而言,价电子
就是最外层电子。例如,碱金属元素原子的价电子排布为
ns
1,只有1 个价电子,为ⅠA 族。再如,卤族元素原子的
价电子排布为ns
2np
5,有7 个价电子,为ⅦA 族。稀有气
体元素原子的最外层电子排布都是ns
2np
6(He 是1s
2)。对
于过渡元素原子,价电子不仅仅是最外层电子,还包括次
第4 周期对应第4 能级组(4s、3d、4p),最多能容纳
18 个电子,因此第4 周期共包含18 种元素,其中第3 ~12
族元素(也称过渡元素)的原子新增的电子排布在3d 轨道
上。第4 周期元素价电子排布呈现从4s
1 经过4s
1 ~23d
1 ~10
过渡到4s
24p
6 的变化。以此类推,第5 周期也可以容纳18
种元素,而第6、7 周期分别可以容纳32 种元素。
周期
能级组
能级组包含的
原子轨道
能级组最多
容纳的电子数
周期包含的
元素种类数
价电子排布的
递变规律
1
2
3
根据鲍林近似能级图完成下表。
书写表达
想一想
19
1.3
元素周期律
外层电子,甚至倒数第三层电子,同一族内,价电子排布
基本相同。
根据元素原子的价电子排布特征,还可以将元素周期
表分为s 区、p 区、d 区和f 区,如图1.11 所示,区的名称
一般来自最后填入电子的能级的符号(除He 以外)。
s 区包含氢元素、第1 族的碱金属元素和第2 族的碱
土金属元素,共两个纵列,除氢元素以外,其余都是较活
泼的金属元素。s 区元素原子的最后一个电子填充在s 轨道
上,价电子排布为ns
1 ~2。
p 区包含第13 ~18 族元素,共6 个纵列,除氢元素
外,所有非金属元素(包括稀有气体元素)都在p 区。p
区元素原子的价电子排布为ns
2np
1 ~6(He 是1s
2)。
d 区包含除镧系和锕系元素以外的第3 ~12 族元素,
共10 个纵列。一般来说,d 区元素原子的价电子排布为
(n —1)d
1 ~10ns
1 ~2。d 区元素原子核外电子排布的差别主要在
(n —1)d 轨道上。
图1.11 元素周期表分区的简图
科学研究表明,随着原子序数的递增,原子核外电
子排布呈周期性变化,使元素的原子半径、第一电离能以
及电负性等性质也呈现周期性变化。它们都有哪些变化规
律?与核外的电子排布又有什么关系?
元素性质的周期性变化规律
s 区
d 区
f 区
p 区
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
原子结构与性质
第1 章
20
1. 原子半径
元素的原子半径是一个重要的参数,对元素及其化合
物的性质有较大影响。由于核外电子在原子核附近到离核
很远的地方都有可能出现,所以原子并没有明确的边界,
原子半径是根据一定规则,结合实验测定得到的。原子半
径的大小取决于两个因素:一个是电子层数,另一个是核
电荷数。显然,电子层数越多,电子之间的排斥作用将使
原子的半径增大;核电荷数越大,核对电子的吸引力也越
大,将使原子半径缩小。这两个因素的共同作用,使得原
子半径发生周期性变化。主族元素的原子半径如图1.12 所
示:同一周期中,从左至右,元素的原子半径逐渐减小;
同一主族中,从上至下,元素的原子半径逐渐增大。
图1.12 主族元素的原子半径示意图
拓展视野
同一种元素原子依据不同规则得到的原子半径差别可能很大,所以比较不同
原子的相对大小时,取用的数据来源必须一致。常见的原子半径有金属半径、共
价半径和范德华半径等。
金属半径:金属晶体中,相邻两原子核间距的一半称为金属半径。例如,钠
原子的金属半径为186 pm[图1.13(a)]。
三种原子半径
H
Li
Na
K
Rb
Cs
Ba
Sr
Ca
Mg
Be
Tl
In
Ga
Al
B
Pb
Sn
Ge
Si
C
Bi
Sb
As
P
N
Po
Te
Se
S
O
At
I
Br
Cl
F
21
1.3
元素周期律
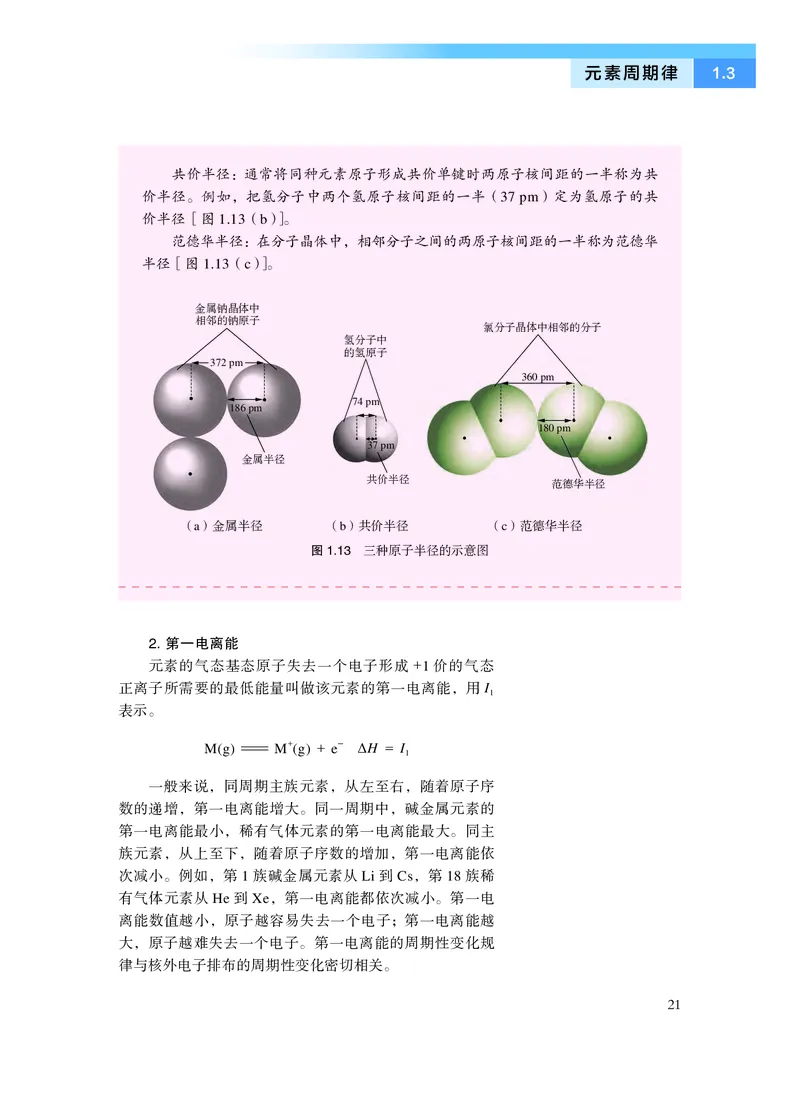
共价半径:通常将同种元素原子形成共价单键时两原子核间距的一半称为共
价半径。例如,把氢分子中两个氢原子核间距的一半(37 pm)定为氢原子的共
价半径[图1.13(b)]。
范德华半径:在分子晶体中,相邻分子之间的两原子核间距的一半称为范德华
半径[图1.13(c)]。
图1.13 三种原子半径的示意图
2. 第一电离能
元素的气态基态原子失去一个电子形成+1 价的气态
正离子所需要的最低能量叫做该元素的第一电离能,用I1
表示。
一般来说,同周期主族元素,从左至右,随着原子序
数的递增,第一电离能增大。同一周期中,碱金属元素的
第一电离能最小,稀有气体元素的第一电离能最大。同主
族元素,从上至下,随着原子序数的增加,第一电离能依
次减小。例如,第1 族碱金属元素从Li 到Cs,第18 族稀
有气体元素从He 到Xe,第一电离能都依次减小。第一电
离能数值越小,原子越容易失去一个电子;第一电离能越
大,原子越难失去一个电子。第一电离能的周期性变化规
律与核外电子排布的周期性变化密切相关。
M(g)
M
+(g) + e
— ΔH = I1
金属钠晶体中
相邻的钠原子
氢分子中
的氢原子
氯分子晶体中相邻的分子
范德华半径
共价半径
金属半径
186 pm
74 pm
37 pm
180 pm
360 pm
372 pm
(a)金属半径
(b)共价半径
(c)范德华半径
原子结构与性质
第1 章
22
1. 已知Na 的第一电离能为496 kJ·mol
—1,Mg 的第一
电离能为738 kJ·mol
—1。请你根据这些数据,解释Na 和Mg
的金属性差异。
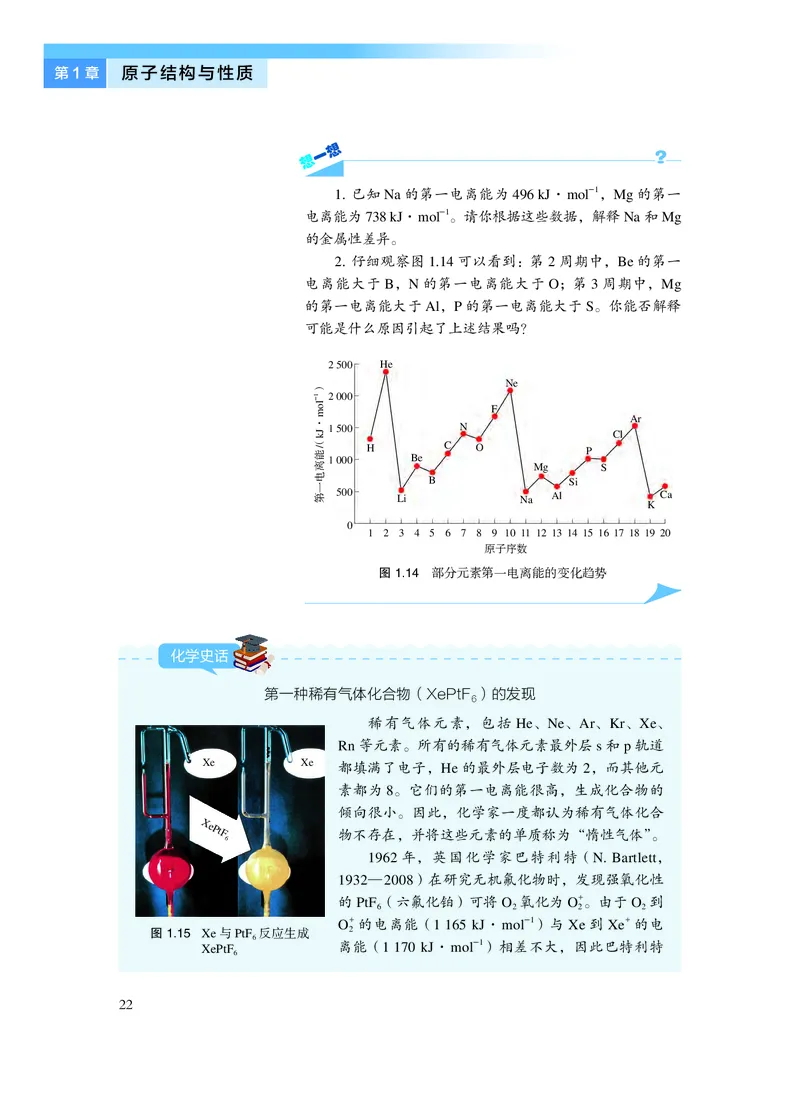
2. 仔细观察图1.14 可以看到:第2 周期中,Be 的第一
电离能大于B,N 的第一电离能大于O;第3 周期中,Mg
的第一电离能大于Al,P 的第一电离能大于S。你能否解释
可能是什么原因引起了上述结果吗?
图1.14 部分元素第一电离能的变化趋势
第一种稀有气体化合物(XePtF6)的发现
稀有气体元素,包括He、Ne、Ar、Kr、Xe、
Rn 等元素。所有的稀有气体元素最外层s 和p 轨道
都填满了电子,He 的最外层电子数为2,而其他元
素都为8。它们的第一电离能很高,生成化合物的
倾向很小。因此,化学家一度都认为稀有气体化合
物不存在,并将这些元素的单质称为“惰性气体”。
1962 年,英国化学家巴特利特(N. Bartlett,
1932—2008)在研究无机氟化物时,发现强氧化性
的PtF6(六氟化铂)可将O2 氧化为O2
+。由于O2 到
O2
+ 的电离能(1 165 kJ·mol
—1)与Xe 到Xe
+ 的电
离能(1 170 kJ·mol
—1)相差不大,因此巴特利特
化学史话
图1.15 Xe 与PtF6 反应生成
XePtF6
Xe
XePtF6
Xe
想一想
原子序数
第一电离能 / (kJ·mol
—1)
2 500
2 000
1 500
1 000
500
0
1
2
3
4
5
6
7
8
9 10 11 12 13 14 15 16 17 18 19 20
Ca
K
S
Cl
Ar
P
Si
Al
Na
Mg
Ne
F
N
O
C
B
Be
Li
H
He
23
1.3
元素周期律
3. 电负性
电负性概念是由美国化学家鲍林在1932 年提出的,用
来表示元素的原子在化合物中吸引电子能力的相对大小。
元素的电负性越大,表示原子在化合物中吸引电子的能力
越强。鲍林根据实验数据进行了理论计算,以氟的电负性
4.0 作为相对标准,在此基础上得出了其他元素的电负性。
图1.16 列出了部分主族元素电负性的周期性变化。
从图1.16 可以看到,金属元素的电负性较小,非金属
元素的电负性相对较大。一般来说,同周期主族元素,从
左至右,电负性逐渐变大(稀有气体元素除外);同主族元
素,从上至下,电负性逐渐变小。
电负性的大小也可用于判断元素的金属性和非金属性
的强弱。一般来说,金属元素的电负性小于1.8,数值越
小,金属性越强;非金属元素的电负性大于1.8,数值越大,
非金属性越强。位于金属元素和非金属元素交界处的元素
图1.16 部分主族元素电负性的周期性变化
尝试用PtF6 氧化Xe。巴特利特将PtF6 和Xe 适量混合后,反应得到了橙黄色的固体,
他认为该固体是XePtF6(六氟合铂酸氙)。XePtF6 是第一种制得的稀有气体化合物,
这在化学界引起了很大震动。后期的实验证明该化合物的化学式并非如此简单,而
是包括XeF
+PtF6
—和XeF
+Pt2F11
—。XePtF6 的成功合成不仅意味着稀有气体元素有可能
形成化合物,而且极大地推动了对稀有气体化合物的系统研究。众多稀有气体化合
物也是在此不久之后被发现,“惰性气体”也因此更名为“稀有气体”。
电负性增大
电
负
性
增
大
1
2
H
2.1
Li
1.0
Na
0.9
K
0.8
Rb
0.8
Cs
0.7
Be
1.5
B
2.0
Al
1.5
Ga
1.6
In
1.7
Tl
1.8
C
2.5
Si
1.8
Ge
1.8
Sn
1.8
Pb
1.9
N
3.0
P
2.1
As
2.0
Sb
1.9
Bi
1.9
O
3.5
S
2.5
Se
2.4
Te
2.1
Po
2.0
F
4.0
Cl
3.0
Br
2.8
I
2.5
At
2.2
Mg
1.2
Ca
1.0
Sr
1.0
Ba
0.9
13
14
15
16
17
原子结构与性质
第1 章
24
● A 元素原子的负一价离子与基态氩原子核外电子的排布相同。请写出
A 元素基态原子的电子排布式,指出该元素位于元素周期表的第几周
期、第几族,写出元素符号和最高价氧化物对应水化物的化学式。
● 氩原子的原子序数是18,A 元素原子的负一价离子与基态氩原子
核外电子的排布相同,所以A 元素的原子序数是17,基态原子的
电子排布式为:[Ne]3s
23p
5,位于元素周期表的第3 周期、第17 族。
元素符号为Cl,最高价氧化物对应水化物的化学式为HClO4。
学习指南
例题导引
问题:
分析:
(如锗元素、锑元素等)电负性则在1.8 左右,这些元素
既具有金属性,又有非金属性。通常,还可以利用两种元
素电负性的差值判断化学键的类型。当成键的两个原子相
应的元素电负性差值大于1.7 时,所形成的一般为离子键;
当差值小于1.7 时,一般为共价键。
根据前面学习的同周期和同主族元素电负性的变化趋
势,分别完成11 ~17 号元素、碱金属元素和卤族元素的电
负性变化折线图,并解释碱金属元素的金属性和卤族元素的
非金属性的递变规律。
书写表达
图1.17 电负性变化折线图
电负性
Na
11 ~ 17 号元素
碱金属元素
卤族元素
Mg Al Si P
S Cl
Li Na K Rb Cs
F Cl Br I At
电负性
电负性
4
3.5
3
2.5
2
1.5
1
0.5
0
4
3.5
3
2.5
2
1.5
1
0.5
0
4
3.5
3
2.5
2
1.5
1
0.5
0
25
1.3
元素周期律
练习巩固
1. 下列各组元素中,按照原子半径依次减小顺序排列的是( )。
(A) Be、Mg、Ca
(B) F、Cl、Br
(C) C、N、O
(D) B、Be、Li
2. 下列关于元素第一电离能的比较中,正确的是( )。
(A) I1(B) < I1(C) < I1(N)
(B) I1(Li) < I1(Be) < I1(B)
(C) I1(Na) < I1(Mg) < I1(Al)
(D) I1(Li) < I1(Na) < I1(K)
3. 分别写出第3 周期中电负性最大和最小元素的名称、符号。
4. 怎样理解元素第一电离能、电负性可以衡量元素金属性和非金属性的强弱?
原子结构与性质
第1 章
26
素养提升
■ 能分别从宏观和微观视角认识宏观物体运动特点和微观粒子的运动状态,并能说明
两者的差异。认识建构模型在人类认识原子结构过程中的重要作用,理解科学家如
何依据实验证据建立原子结构模型、依据新的实验事实和科学理论改进模型的发展
过程。通过原子结构理论的发展历史,体会科学研究的基本方法和过程,崇尚科学
真理,逐步养成严谨求实的科学态度。
■ 能理解、描述和表示原子结构模型。能从原子核外电子在空间出现的概率分布和能
量两个方面,理解原子核外电子空间运动的状态,指出原子轨道和电子云等基本概
念的具体含义。能知道多电子原子核外电子是分层排布的,知道电子排布遵循的基
本规则和电子排布的表示方法。
■ 认识运用原子等微观粒子的结构模型,对解释和推测物质结构、性质和变化的重要
意义。能说出主族元素的原子半径、第一电离能、电负性等性质的周期性变化规律,
并能从核外电子排布的周期性变化规律进行解释。能从原子价电子数目和价电子排
布的角度解释元素周期表的分区、周期和族的划分,并列举元素周期律(表)的应
用,从宏观与微观结合的视角认识元素周期律的内因和本质。
本章复习
26
核心框图
原子结构与性质
多电子原子核
外电子的排布
元素周期表
和元素周期律
氢原子结构
玻尔原子
结构模型
原子
轨道
电子
云
能层
能级
周期
族
原子
半径
第一
电离
能
电负
性
s、p、d、
f 区
氢原子的
结构模型
能量
最低
原理
洪特
规则
元素
周期
表
元素
周期
律
泡利
不相容
原理
27
1.4
原子光谱分析
27
27
27
练习巩固
1. 下列原子轨道不存在的是( )。
(A) 2s
(B) 3p
(C) 2d
(D) 3d
2. 判断下列说法是否正确,正确的在 内画“√”,错误的画“×”。
(1) p 轨道的空间伸展方向是哑铃形的
(2) n = 4 的能层中有4 个原子轨道4s、4p、4d、4f
(3) 基态O
2—的核外电子排布式是1s
22s
22p
4
(4) 元素的基态和激发态原子核外电子排布都要遵守电子排布的三条规则
(5) Cr 的基态原子核外电子排布式是1s
22s
22p
63s
23p
63d
44s
2
3. 某元素基态原子共有4个价电子,其中2个价电子位于第三能层d轨道,请完成:
(1) 写出该元素基态原子的电子排布式。
(2) 指出该元素的原子序数、在元素周期表中的周期数和族数以及最高正化合价。
4. 某元素基态原子的电子排布式为1s
22s
22p
63s
23p
4,写出它的元素符号。该元素最
高价氧化物对应的水化物的酸性与碳酸相比,哪个更强?
5. 当原子、分子或离子内有单电子存在时,能被外磁场所吸引,表现出顺磁性。请
问24 号元素的基态原子是否具有顺磁性?该元素位于元素周期表的第几周期?该周期中
共有几种元素?
6. 具有下列价电子排布的基态原子中,第一电离能最低的是( )。
(A) ns
2np
3
(B) ns
2np
4
(C) ns
2np
5
(D) ns
2np
6
7. 元素周期表可以分为哪几个区?每个区包括哪几个族?各区元素原子的价电子排
布各有什么特征?
8. A、B、C 是元素周期表中相邻的三种短周期元素。A和B同周期,B 和C 同主族,
三种元素原子的最外层电子数之和是11,核内质子数之和是25,则A、B、C分别是哪
三种元素?
体验 · 分享
在下列选题中,开展文献、调查、实验等研究,并将成果和体会制成海报、演示文稿,
进行分享和交流。
讨论玻尔原子结构模型的成功与不足之处。查阅相关资料,了解玻尔原子结构
模型的建立与当时的哪些科学发展成果有关,并谈谈从中受到的启迪。
查阅历史上物理学家对光的本质的争论和人们接受光的波粒二象性的过程。回
顾并简述人们对原子结构的认识逐渐深入的过程,交流你对建构模型在认识原
子结构过程中的重要作用的认识。
原子结构与性质
第1 章
28
28
在元素周期表中,某些主族元素与其右下方的主族元素的有些性质是相似的,
如Li 与Mg,Be 与Al,B与Si,这种相似性被称为“对角线规则”。请查阅有关
元素电负性等数据,解释元素的“对角线规则”,并列举如氢氧化物的酸碱性、
最高价含氧酸的酸性强弱等实例,予以说明。
电负性在1.8左右的元素兼有金属性和非金属性,是制造半导体材料的重要元
素。请收集相关资料,了解这些元素在现代科技中的某些重要作用。
观看关于光谱的纪录片,深入了解光谱的发现和应用,用小论文形式完成观后感。
查阅第一电离能数据,利用电子表格软件,参考图1.18 绘制短周期元素第一电
离能的三维柱状图。
徐光宪院士是2008年度“国家最高科学技术奖”获得者,长期从事物理化学和
无机化学的教学和研究,涉及量子化学、化学键理论、配位化学、萃取化学、
核燃料化学和稀土科学等领域。请查阅相关资料,了解徐光宪院士在物质结构
理论方面取得的研究成果。
图1.18 前四周期主族元素电负性的周期性变化
电负性
第1 周期
第2 周期
第3 周期
第4 周期
0
0.5
1.0
1.5
2.0
2.5
3.0
3.5
4.0
2.1
0.8
0.9
1.0
1.0
1.2
1.61.5
1.8
1.8
2.0
2.1
2.4
2.5
2.8
3.0
3.0
2.5
3.5
4.0
2.0
1.5
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
分子结构与性质
第2 章
29
具有规整孔道结构的硅铝酸盐结
晶,其孔径大小与普通分子相当,因
而能在分子水平上筛分分子。
共价分子的空间结构
分子结构与物质的性质
配位化合物和超分子
2.1
2.2
2.3
30
在
化学必修课程的学习中,我们已经了解自然界形形色色的物
质仅由近百种元素的原子构建而成。分子是由原子通过一定
的作用力以一定的次序和排列方式构成的。有的分子是由几个原子
构成的简单分子,有的则是由许许多多原子构成的复杂分子。有的
分子是直线形,而有的分子是正四面体形。分子的空间结构对于物
质的性质有什么影响?分子之间是否存在相互作用呢?如果存在,
又将对物质的性质产生怎样的影响?
通过学习共价键和分子间作用力的相关理论,我们能知道怎样
解释和预测分子的空间结构,并进一步深入理解分子结构与物质性
质之间的关系。
31
2.1
共价分子的空间结构
身边的有机化合物
2.1
共价分子的空间结构
1. 共价键的本质
让我们以氢分子的形成过程为例,来认识共价键的本
质。理论计算表明,若两个氢原子1s 轨道上的单电子呈不
同的自旋状态,当两个氢原子从无限远处逐渐相互接近时,
它们的1s 轨道会发生重叠,其结果是使这对电子在两个原
子核之间出现的概率增大,两个原子核与电子对之间的吸引
也逐渐增大,从而使体系能量逐渐降低。能量随核间距的变
化如图2.1 所示。当两个氢原子的核间距为74 pm 时,体系
能量降到最低;若两个氢原子进一步接近,由于两个原子核
之间的排斥作用逐渐增强,体系能量又开始上升。这就表明
两个氢原子的核间距为74 pm 时体系处于最稳定状态,形成
了氢分子。我们把原子之间通过共用一对自旋状态不同的电
子所形成的化学键称为共价键,而共价键的本质就是两个原
子核与共用电子对的电性相互作用。
共价键的形成与性质
在学习化学的过程中,我们先后认识了很多共价分
子,即原子之间通过共价键而形成的分子,如H2、N2、Cl2、
H2O、NH3 等。同种原子或电负性相近的原子之间通过共用
一对或几对电子形成共价键。那么,为什么原子之间通过共
用电子对就能形成稳定的分子?共价键的本质究竟是什么?
共价键的哪些性质决定了分子的构成与空间结构?
认识共价键的形成和本质
知道共价键的类型和性质
了解共价分子具有一定的空间
结构
运用相关理论和模型解释和预
测分子的空间结构
学习聚焦
知识回放
● 元素的电负性
● 共价键
● 原子轨道
● 多电子原子核外电子的排布
图2.1 氢分子形成过程中的体系能量变化
(太近)
(太远)
核间距 /pm
0
74
H H
H
HH
H
—436
O
能量 / (kJ·mol
—1)
分子结构与性质
第2 章
32
2. 共价键的饱和性与方向性
每个原子能提供的未成对电子数是一定的,在形成共价
键时,通常该原子的若干个未成对电子分别与其他原子相同
数目的单电子,以自旋状态不同的方式配对成键,即每个原
子可以形成共价键的数目是一定的,因此共价键具有饱和性。
例如,氯原子的价层中只有一个未成对电子,只能形成一个
共价键,如氯化氢分子中的H—Cl键、氯分子中的Cl—Cl键。
氮原子有三个未成对电子,能形成三个共价键,如氨分子中
的三个N—H 键、氮分子中的N
N 键等。第2 周期元素的
原子最多形成四个共价键就是共价键具有饱和性的典型例证。
共价键是否稳定,与原子轨道的重叠程度有关。只有
当它们沿着原子轨道电子云密度最大的方向才能达到最大
程度的有效重叠,形成稳定的共价键。原子中的s 轨道呈球
形对称分布,两个s 轨道上的电子相互成键时轨道可沿任意
方向发生最大程度的有效重叠,而p、d、f 等轨道均有一定
的空间伸展方向,这些轨道上的电子相互成键或与s 轨道上
的电子成键时,必须沿着合适的方向以达到最大程度的有
效重叠,才可形成稳定的共价键,所以共价键具有方向性。
3. 共价键的类型
我们知道氮气的化学性质很不活泼,通常条件下不易发
生化学反应,这与氮分子中两个氮原子的原子轨道重叠形成
的共价键有关。氮原子的价电子排布式为2s
22p
3。根据洪特规
则可知,2p 轨道上的三个电子分别排布在2px、2py 和2pz 轨道
上,所以氮原子有三个未成对电子。若两个氮原子沿x 轴相
互接近时,它们各自的px 轨道沿x 轴方向以“头碰头”的方
式相互重叠,那么两个氮原子的py 和pz 轨道只能分别在垂直
于x 轴方向上以相互平行的“肩并肩”方式发生重叠(图2.2)。
图2.2 氮分子中原子轨道的重叠方式
原子轨道沿键轴(成键原子核间连线)方向以“头碰头”
方式重叠而形成的共价键称为σ 键。原子轨道沿键轴两侧以
“肩并肩”的方式重叠而形成的共价键称为π 键。一般而言,
x
x
y
z
x
+
+
+
+
+
—
—
—
—
—
—
+
33
2.1
共价分子的空间结构
图2.3 氮分子中的共价键
你能说出过氧根离子(O2
2—)中有哪些共价键吗?请参照
图2.3 用示意图描述过氧根离子中的共价键。
书写表达
4. 共价键的极性
在氢分子、氯分子等双原子分子中,由于两个原子吸
引电子的能力相同,共用电子对不偏向其中任何一个原子,
这样的共价键叫做非极性共价键,简称非极性键。不同元
素的原子以共价键相结合时,由于两个原子吸引电子的能
力不同,共用电子对偏向吸引电子能力强的原子一方,这
样的共价键叫做极性共价键,简称极性键,如H—Cl 键、
H—O 键等。一般而言,我们可用成键原子的电负性差值
粗略地判断键的极性强弱,成键原子的电负性差值越大,
共价键的极性越强。键的极性是一向量,其方向由正电荷
指向负电荷,常以符号“
”表示,如图2.4 所示。
图2.4 氯化氢分子中的极性
共价键(键的极性方
向以箭头指向表示)
价键理论的发展
为解释共价分子的结构,美国科学家路易斯(G. N. Lewis,1875— 1946)于
1916 年提出了共价键理论。他认为分子中的原子之间可以通过共用电子对形成稳
定的稀有气体元素原子的电子结构,即八隅体规则。他把原子之间通过共用电子
对形成的化学键称为共价键。
化学史话
对于确定的两个原子,成键时优先形成σ 键。这是因为形成
π 键时原子轨道的重叠程度较小,不如形成σ 键稳定。氮
分子中含有一个σ 键和两个π 键(图2.3),这三个共价键
使得两个氮原子结合紧密,因此氮气的化学性质很稳定。
z
z
y
y
π 键
π 键
σ 键
x
带部分
正电荷(δ+)
H
Cl
带部分
负电荷(δ
—)
分子结构与性质
第2 章
34
路易斯的经典共价键理论初步解释了同种元素的原子或电负性相近的元素原
子如何形成稳定分子,并说明了共价键与离子键的区别。但是,该经典共价键理
论有其局限性:其一是它未能阐明共价键的本质和特性;其二是它不能解释很多化
合物的中心原子的外围电子数超过8 个却仍然稳定的事实,如PCl5、SF6 分子的中
心原子外围电子数分别是10 个、12 个。
为解决这些问题,德国科学家海特勒(W. H. Heitler,1904 —1981)和伦敦
(F. W. London,1900 —1954)于1927 年首次将量子力学理论应用到化学键与分
子结构中,后经鲍林等人的发展,建立了现代价键理论,简称为VB 法。1932 年,
美国科学家马利肯(R. S. Mulliken,1896 —1986)和德国科学家洪特(F. Hund,
1896 —1997)提出了分子轨道理论,成功地解释了分子的磁性等问题。
5. 共价键的稳定性
我们知道化学反应中的能量变化与化学键的断裂和生
成密切相关。相同条件下,不同化学反应的反应热不同,
说明不同化学键的强度不同。人们常用键能来定量描述共
价键的强度,把在100 kPa、298.15 K 条件下,1 mol 气态
AB 分子分解成气态A 原子和气态B 原子所需要的能量称
为A—B 键的键能,用EA— B 来表示。
一般而言,键能越大,断键时所需要的能量越大,键
越牢固,由该键构成的分子越稳定。因为N
N 键的键能
大于H — H 键的键能,所以氮气比氢气稳定,不易发生化
学反应。部分共价键的键能如表2.1 所示。
H2(g)
2H(g) EH— H = 436 kJ·mol
—1
N2(g)
2N(g) EN
N = 946 kJ·mol
—1
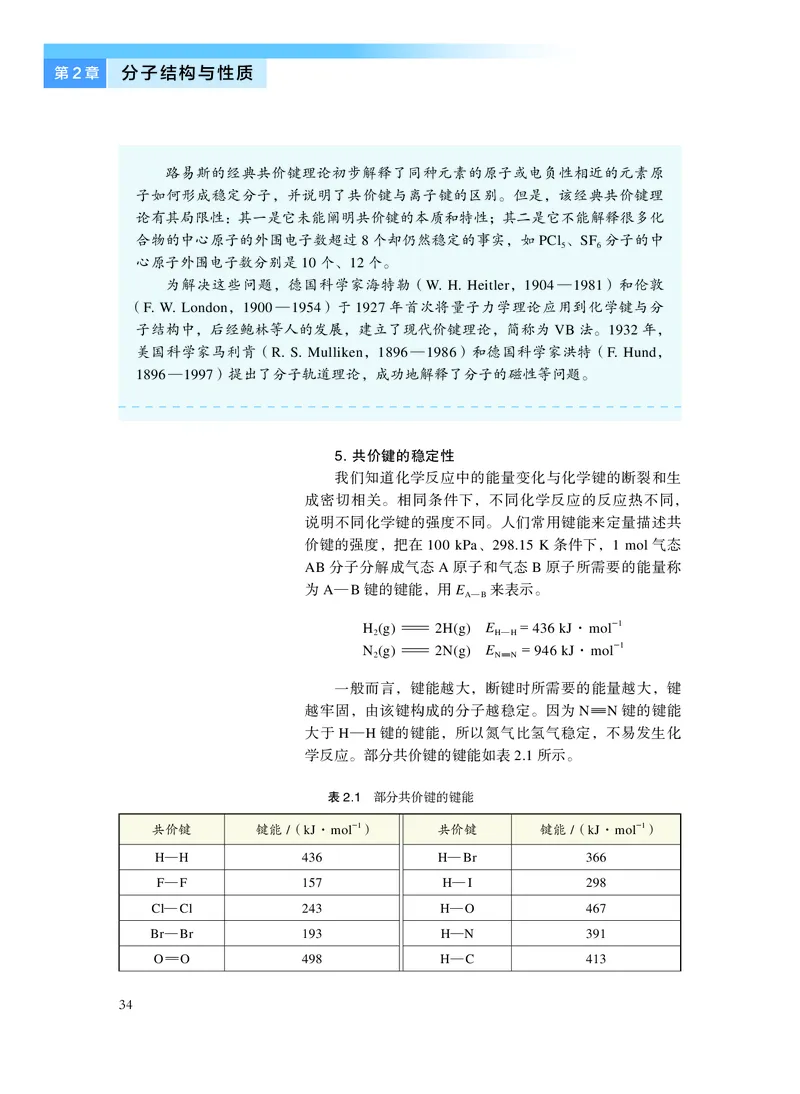
表2.1 部分共价键的键能
共价键
键能/(kJ·mol
—1)
共价键
键能/(kJ·mol
—1)
H —H
436
H—Br
366
F—F
157
H—I
298
Cl—Cl
243
H—O
467
Br—Br
193
H—N
391
O
O
498
H—C
413
35
2.1
共价分子的空间结构
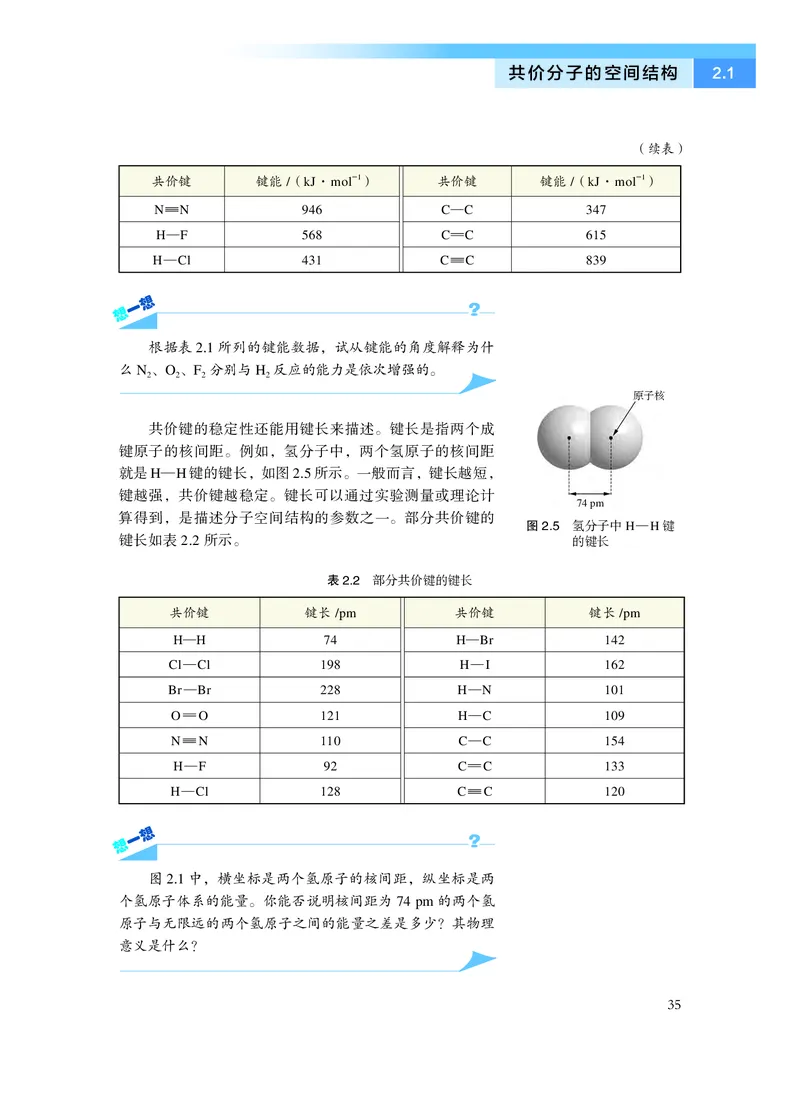
表2.2 部分共价键的键长
共价键
键长/pm
共价键
键长/pm
H—H
74
H —Br
142
Cl —Cl
198
H — I
162
Br —Br
228
H —N
101
O
O
121
H —C
109
N
N
110
C —C
154
H —F
92
C
C
133
H —Cl
128
C
C
120
共价键
键能/(kJ·mol
—1)
共价键
键能/(kJ·mol
—1)
N
N
946
C—C
347
H—F
568
C
C
615
H —Cl
431
C
C
839
(续表)
图2.1 中,横坐标是两个氢原子的核间距,纵坐标是两
个氢原子体系的能量。你能否说明核间距为74 pm 的两个氢
原子与无限远的两个氢原子之间的能量之差是多少?其物理
意义是什么?
根据表2.1 所列的键能数据,试从键能的角度解释为什
么N2、O2、F2 分别与H2 反应的能力是依次增强的。
共价键的稳定性还能用键长来描述。键长是指两个成
键原子的核间距。例如,氢分子中,两个氢原子的核间距
就是H—H 键的键长,如图2.5 所示。一般而言,键长越短,
键越强,共价键越稳定。键长可以通过实验测量或理论计
算得到,是描述分子空间结构的参数之一。部分共价键的
键长如表2.2 所示。
图2.5 氢分子中H—H 键
的键长
想一想
想一想
原子核
74 pm
分子结构与性质
第2 章
36
自然界中形形色色的多原子分子都具有一定的空间结
构,这是因为多原子分子中原子间所形成的共价键有一定
的空间指向。我们把多原子分子中两个共价键之间的夹角
称为键角。键角是描述分子空间结构的重要参数。如图2.6
所示:二氧化碳分子中两个C
O 键的夹角为180°,说
明它是一个直线形分子;水分子中两个H —O 键的夹角为
104.5°,说明它是一个角形(V 形)分子;氨分子中任意两
个N —H 键的夹角均为107°18′,说明它是一个三角锥形分
子;甲烷分子中任意两个C —H 键的夹角均为109°28′,说
明它是一个正四面体形分子。
分子的空间结构
图2.6 二氧化碳、水、氨、甲烷分子中的键角与分子的空间结构
1931 年,美国化学家鲍林在价键理论的基础上提出了
杂化轨道理论,较好地解释了甲烷等分子的空间结构。
我们先来了解一下杂化轨道理论的基本要点。
碳原子的价电子排布式为2s
22p
2,根据洪特规则可知
价层中只有2 个未成对电子,但为什么碳原子能与4 个氢
原子形成甲烷分子?又为什么甲烷分子具有正四面体形的
空间结构?
想一想
(a)CO2
(c)NH3
(b)H2O
(d)CH4
180°
104.5°
109°28′
107°18′
H
H
H
H
H
H
H
O
O
O
C
H
H
C
N
37
2.1
共价分子的空间结构
杂化轨道理论指出,原子形成分子时,中心原子中类
型不同、能量相近的几个原子轨道(如ns 和np 轨道)可
以进行组合,重新形成数目相同、能量相等或相近的新原
子轨道。原子轨道进行组合时,轨道中原来已经成对的电
子可以被激发到空轨道上成为单电子。这个重新组合的过
程叫做原子轨道的杂化,组合以后形成的新原子轨道称为
杂化轨道。杂化轨道的能量和空间伸展方向都发生了变化,
使相应的电子云分布更集中,成键时轨道的重叠程度更大,
所以成键能力更强。例如,一个ns 轨道和一个np 轨道进
行杂化,杂化前后轨道空间分布方向和分布情况的变化如
图2.7 所示。
图2.7 杂化前后轨道空间分布方向和分布情况
杂化前
杂化后
鲍林
美国化学家鲍林一生曾两次获得诺贝尔奖,
分别是因在化学键方面的工作获1954 年化学奖和
因推动禁止核试验获1962 年和平奖。
鲍林对化学最大的贡献是关于化学键本质的
研究及其在物质结构方面的应用。他把量子力学
应用于分子结构,把价键理论扩展到金属和金属
间化合物,并发展了原子核结构和核裂变过程本
质的理论。他的研究领域还涉及生物化学和医学,
如研究了蛋白质的结构、麻醉作用的分子基础等。
鲍林在研究量子化学和其他化学理论时,创造性地提出了许多新的概念,如
共价半径、金属半径、电负性标度等,这些概念的应用对现代化学、凝聚态物理
的发展都有重大意义。
化学史话
图2.8 鲍林
x
x
x
x
y
y
y
y
z
z
z
z
+
+
+
+
—
—
—
分子结构与性质
第2 章
38
我们可以运用杂化轨道理论来解释甲烷分子的正四面
体结构。
在形成甲烷分子的过程中,碳原子2s 轨道上的一个电
子受激发进入2p 空轨道上,然后能量相近的一个2s 轨道
和三个2p 轨道进行杂化,形成了四个能量相等的新轨道,
称为sp
3 杂化轨道。
四个sp
3 杂化轨道在空间的伸展方向正好指向正四面
体的四个顶点。四个sp
3 杂化轨道上各占有一个未成对电
子,它们分别与四个氢原子的1s 轨道发生“头碰头”的重
叠,形成四个完全相同的σ 键,如图2.9 所示。四个C— H
键相互间的夹角均为109°28′[见图2.6(d)],所以甲烷
分子为正四面体形。
激发
杂化
sp
3 杂化
图2.9 甲烷分子的成键情况
ns 轨道与np 轨道的杂化有多种情况。它们除了能形
成sp
3 杂化轨道外,还可以是一个ns 轨道和一个np 轨道进
行杂化,形成两个sp 杂化轨道;又或者是一个ns 轨道和
两个np 轨道进行杂化,形成三个sp
2 杂化轨道。与sp
3 杂
化轨道不同的是,sp 杂化轨道、sp
2 杂化轨道的空间分布分
别呈直线形和平面三角形,如图2.10 所示。
已知三氯甲烷分子(CHCl3)呈四面体形,参考甲烷分
子的成键情况示意图,画出该分子的成键情况示意图。
书写表达
H
H
H
H
H
H
H
H
C
C
39
2.1
共价分子的空间结构
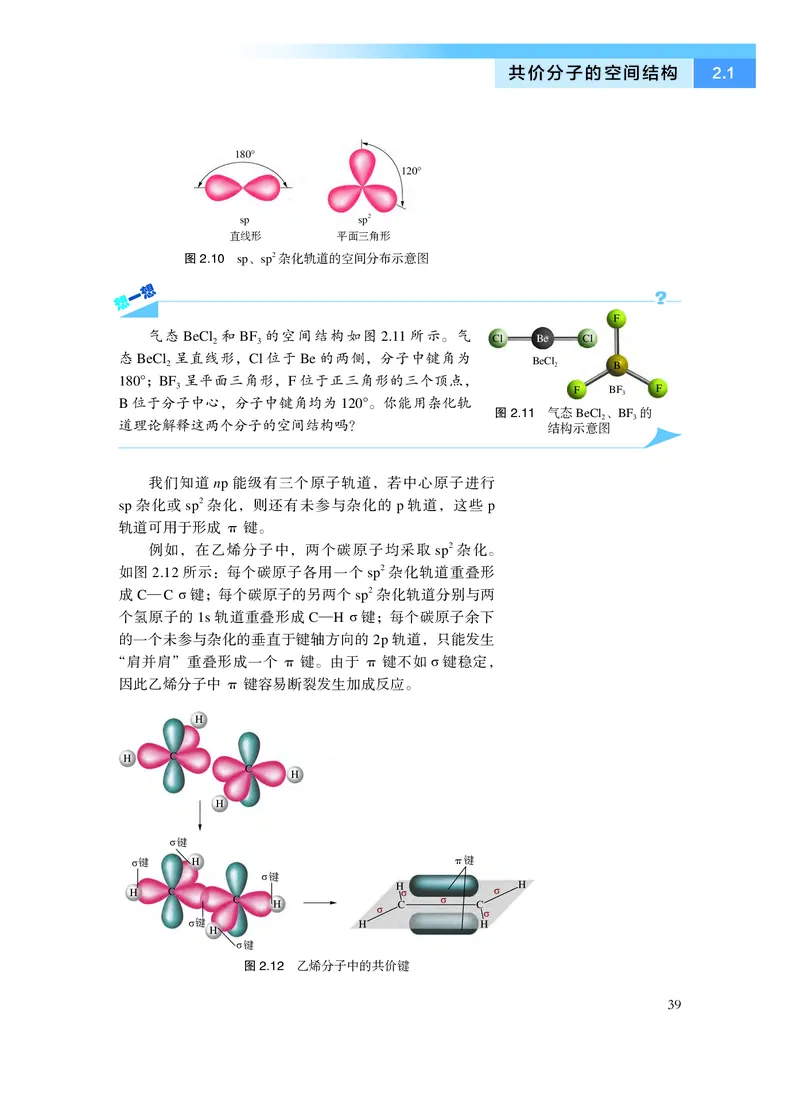
图2.10 sp、sp
2 杂化轨道的空间分布示意图
气态BeCl2 和BF3 的空间结构如图2.11 所示。气
态BeCl2 呈直线形,Cl 位于Be 的两侧,分子中键角为
180°;BF3 呈平面三角形,F 位于正三角形的三个顶点,
B 位于分子中心,分子中键角均为120°。你能用杂化轨
道理论解释这两个分子的空间结构吗?
我们知道np 能级有三个原子轨道,若中心原子进行
sp 杂化或sp
2 杂化,则还有未参与杂化的p 轨道,这些p
轨道可用于形成π 键。
例如,在乙烯分子中,两个碳原子均采取sp
2 杂化。
如图2.12 所示:每个碳原子各用一个sp
2 杂化轨道重叠形
成C—C σ 键;每个碳原子的另两个sp
2 杂化轨道分别与两
个氢原子的1s 轨道重叠形成C—H σ 键;每个碳原子余下
的一个未参与杂化的垂直于键轴方向的2p 轨道,只能发生
“肩并肩”重叠形成一个π 键。由于π 键不如σ 键稳定,
因此乙烯分子中π 键容易断裂发生加成反应。
图2.12 乙烯分子中的共价键
图2.11 气态BeCl2、BF3 的
结构示意图
想一想
直线形
平面三角形
180°
sp
sp
2
120°
BF3
BeCl2
Cl
Cl
F
B
F
F
Be
H
H
H
H
H
H
H
C
π 键
C
C
C
H
H
H
H
H
C
C
σ 键
σ 键
σ 键
σ 键
σ 键
σ
σ
σ
σ
σ
分子结构与性质
第2 章
40
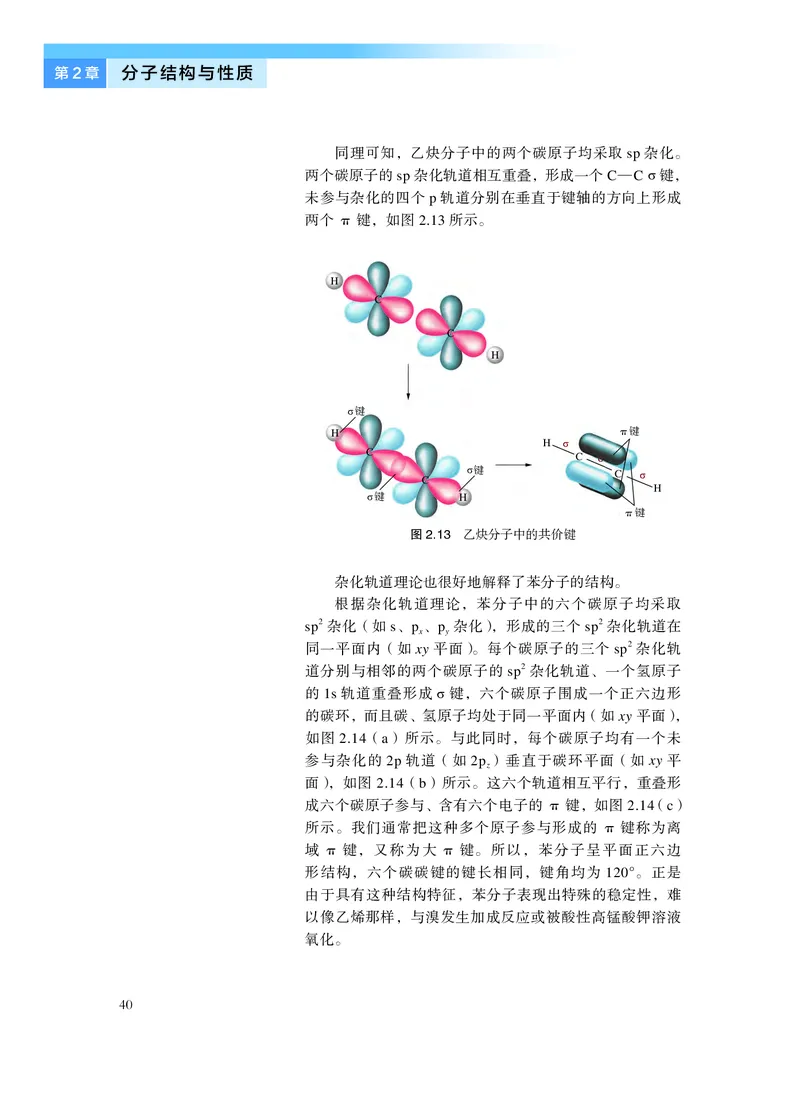
同理可知,乙炔分子中的两个碳原子均采取sp 杂化。
两个碳原子的sp 杂化轨道相互重叠,形成一个C—C σ 键,
未参与杂化的四个p 轨道分别在垂直于键轴的方向上形成
两个π 键,如图2.13 所示。
杂化轨道理论也很好地解释了苯分子的结构。
根据杂化轨道理论,苯分子中的六个碳原子均采取
sp
2 杂化(如s、px、py 杂化),形成的三个sp
2 杂化轨道在
同一平面内(如xy 平面)。每个碳原子的三个sp
2 杂化轨
道分别与相邻的两个碳原子的sp
2 杂化轨道、一个氢原子
的1s 轨道重叠形成σ 键,六个碳原子围成一个正六边形
的碳环,而且碳、氢原子均处于同一平面内(如xy 平面),
如图2.14(a)所示。与此同时,每个碳原子均有一个未
参与杂化的2p 轨道(如2pz)垂直于碳环平面(如xy 平
面),如图2.14(b)所示。这六个轨道相互平行,重叠形
成六个碳原子参与、含有六个电子的π 键,如图2.14(c)
所示。我们通常把这种多个原子参与形成的π 键称为离
域π 键,又称为大π 键。所以,苯分子呈平面正六边
形结构,六个碳碳键的键长相同,键角均为120°。正是
由于具有这种结构特征,苯分子表现出特殊的稳定性,难
以像乙烯那样,与溴发生加成反应或被酸性高锰酸钾溶液
氧化。
图2.13 乙炔分子中的共价键
π 键
π 键
σ 键
σ 键
σ 键
σ
σ
σ
H
H
H
H
H
H
C
C
C
C
C
C
41
2.1
共价分子的空间结构
杂化轨道理论虽然能解释很多已知分子的空间结构,
但是无法预测分子的空间结构。那么如何来预测分子的空
间结构呢?我们可以借助价层电子对互斥理论来进行判断。
1940 年,英国化学家西奇威克(N. V. Sidgwick,
1873 —1952)和鲍威尔(H. M. Powell,1906 —1991)在
总结大量已知分子结构的基础上,提出价层电子对互斥理
论,简称VSEPR 理论。该理论的基本观点是:分子的中心
原子价层中的电子对(包括成键电子对
①和孤电子对),由
于相互间静电排斥作用,而趋向于尽可能彼此远离,分子
以此形成稳定的空间结构。
由于价层电子对之间要尽可能彼此远离,当价层电子
对数分别为2、3、4 时,价层电子对分别排列成直线形、
平面三角形和正四面体形,如图2.15 所示。
那么中心原子的价层电子对数如何来计算呢?我们以
ABn 型分子(其中A 为中心原子)为例来讨论。该分子中
A 的价层电子对数可通过下式确定:
共价分子空间结构的预测
图2.14 苯分子中的共价键
图2.15 不同数目价层电子
对的空间结构
ABn 中A 的价层电子对数=
成键电子对数(σ 键电子对数)
n
2
A 的价电子数 — n 个B 的单电子总数
孤电子对数
① 分子中共价键的空间指向是由σ 键决定的,因此此处成键电子对仅指σ 键电子对。
+
(b) 碳原子的2p 轨道
(c)π 键
平面三角形
3对
直线形
2 对
180°
120°
109°28′
正四面体形
4 对
(a)σ 键
H
H
H
H
H
H
C
C
C
C
C
C
分子结构与性质
第2 章
42
根据中心原子的价层电子对数,可以很方便地确定
价层电子对的空间结构,进而确定ABn 的空间结构。
若ABn 的中心原子的价层电子对全部是成键电子对,
那么,分子的空间结构与价层电子对的空间结构一致。
以CH4 为例,其中心原子是C,价层中有4 个电子,
而每个H 各提供1 个成键电子,则:
4 对价层电子对的空间结构是正四面体形,由于它们
都是成键电子对,所以CH4 的空间结构是正四面体形。
若ABn 的中心原子的价层电子对中有孤电子对,那么,
分子的空间结构与价层电子对的空间结构不一致。
以NH3 为例,其中心原子是N,价层有5 个电子,而
每个H 各提供1 个成键电子,则:
CH4 中C 的价层电子对数 = 4 +
2
4—4×1 = 4
NH3 中N 的价层电子对数 = 3 +
2
5—3×1 = 4
4 对价层电子对的空间结构是四面体形,但其中有1
对孤电子对,由于分子形状只与1 个N 和3 个H 有关,因
此NH3 呈三角锥形。
由于孤电子对相比成键电子对更靠近中心原子的原子
核,故价层电子对之间的静电排斥作用强弱顺序为:孤电
子对—孤电子对> 孤电子对—成键电子对> 成键电子对—成
键电子对。NH3 中有1 对孤电子对,它对成键电子对的排
斥作用更大一些,所以NH3 中N—H 键之间的键角只有
107°18′,如图2.16 所示。
图2.16 NH3 中价层电子对的空间结构和分子的空间结构
孤电子对
价层电子对的空间结构
(四面体形)
分子的空间结构
(三角锥形)
N
H
H
H
H
H
H
N
107°18′
43
2.1
共价分子的空间结构
请你根据VSEPR 理论,画出H2O 的空间结构示意图,
比较CH4、NH3 和H2O 键角的大小并说明原因。
书写表达
拓展视野
1919年,美国化学家朗缪尔(I. Langmuir,1881—1957)提出等电子体原理,
该原理认为化学通式相同(如AXm)且价电子总数相等的分子或离子具有相同的
结构特征,这里的“结构特征”主要指化学键类型和空间结构。
利用等电子体原理可以判断一些简单分子或离子的空间结构。例如,CCl4、
SO4
2—、PO4
3—等具有AX4 通式,价电子总数都为32,它们互为等电子体,中心原
子均采取sp
3 杂化,都呈正四面体形。
等电子体原理在帮助人们寻找特殊用途的新材料方面,起到了推动作用。
等电子体原理
● 请用所学的知识预测SO2 的空间结构。
● 我们可以根据价层电子对互斥理论进行预测。中心原子S 的价层
中有6 个电子。O 的最外层电子数为6,根据洪特规则,O 的单
电子数为2。SO2 的中心原子S 的价层电子对数列式计算如下:
2
6 —2×2 = 3
2 +
中心原子S 的价层电子对数 =
所以,中心原子S 的价层电子对数为3,其中有1 对孤电子对。
故SO2 中价层电子对的空间结构为平面三角形,但分子形状只与
1 个S 和2 个O 有关,因此SO2 为角形分子。
学习指南
例题导引
问题:
分析:
分子结构与性质
第2 章
44
练习巩固
1. 下列说法中,正确的是( )。
(A) 两个氢原子的核间距越小,就越容易形成共价键
(B) 任意两个p 轨道都可以发生相互重叠形成共价键
(C) 对于双原子分子而言,所含共价键的键能越大,分子越稳定
(D) 键长越长,共价键越稳定
2. 下列分子中,同时含有σ键和π键的是( )。
(A) C2H6
(B) NH3
(C) H2S
(D) N2
3. 为什么两个F 能结合成F2,而在元素周期表与其相邻的Ne 的两个原子却
不能形成Ne2 ?
4. 运用价层电子对互斥理论预测三氯化磷分子的空间结构,并说明其中心
原子杂化轨道的类型。
45
2.1
共价分子的空间结构
通常,分子都具有一定的空间结构,这是由构成分子
的共价键性质所决定。分子的空间结构又决定了分子的极
性、对称性等很多性质,而且也会影响物质的化学性质。
物质中存在着分子之间的相互作用,它们的性质、强弱与
物质的各种物理性质密切相关。
分子的极性
2.2
分子结构与物质的性质
知道极性分子和非极性分子
理解分子的极性与分子中键的
极性、分子的空间结构的关系
学会判断简单共价分子的极
性,了解分子的极性对物质物
理性质的影响
了解分子结构对物质化学性质
的影响
知道范德华力和氢键
理解范德华力对物质熔、沸点
的影响
了解分子间氢键和分子内氢
键,理解它们对物质熔、沸点
的影响
学习聚焦
知识回放
● 极性键与非极性键
● 价层电子对互斥理论的基本要点
● 元素的电负性
● 共价键的键长
● 羧酸的酸性
● 分子的同分异构现象
我们知道,分子是电中性的,但分子都有一个正电荷
重心和一个负电荷重心。如果分子的正、负电荷重心重合,
分子内就不显正、负极,这种分子称为非极性分子;如果
1. 取一支50 mL 滴
定管,向管中注入20 mL
蒸馏水,用滴定管夹固
定。滴定管下方放置一
小烧杯,如图2.17 所
示。打开滴定管活塞,
让水流成细线状慢慢流
下,将经毛皮摩擦过的
橡胶棒靠近水流并缓缓
向外移动。观察水流方
向的变化。
2. 用正己烷(或环己烷)替换蒸馏水后进行
相同的操作,观察液体流动方向。
分子的极性
实验探究
图2.17 分子极性实验装置
编号
现象记录
实验结论
1
2
分子结构与性质
第2 章
46
分子的正、负电荷重心不重合,分子内就存在正、负极,
这种分子称为极性分子。通过实验,我们已经看到,用毛
皮摩擦过的橡胶棒靠近水流时,它能使水滴流动的方向发
生偏转。又因为毛皮摩擦过的橡胶棒带负电,这就说明它
和水流之间存在电性相互作用。由此可知,水分子内存在
正、负极,是极性分子;正己烷分子内没有正、负极,是
非极性分子。
双原子分子的极性与成键原子间的共价键极性是一致
的。以极性键结合的异核双原子分子是极性分子,如氯化
氢分子、一氧化碳分子、一氧化氮分子等。以非极性键结
合的同核双原子分子是非极性分子,如氯分子、氮分子、
氢分子等。
多原子分子的极性不仅与共价键的极性有关,还与分
子的空间结构有关。如果形成分子的共价键都是非极性键,
那么分子的正、负电荷重心是重合的,所以该分子是非极
性分子。如果形成分子的共价键是极性键,那么分子是否
有极性还与分子的空间结构有关。共价键的极性是有方向
的,如果分子中所有共价键的极性能相互抵消,从而使分
子的正、负电荷重心重合,那么该分子是非极性分子。例
如,二氧化碳分子呈直线形,两个C
O 键的极性正好相
互抵消,所以它是非极性分子。如果分子中所有共价键的
极性不能相互抵消,分子就会出现正、负极,那么该分子
是极性分子。例如,水分子呈角形,两个H—O 键的极性
不能相互抵消,所以它是极性分子。
通常,分子的极性是通过分子中各共价键极性的向量
和是否为零来判断的。
例如,通过分子空间结构的预测得知:四氯化碳分
子呈正四面体形,四个C—Cl 键的极性的向量和为零
[图2.18(a)],所以四氯化碳分子是非极性分子;氨分子
呈三角锥形,三个N—H 键的极性的向量和显然不为零[图
2.18(b)],所以氨分子是极性分子。
图2.18 四氯化碳分子和氨
分子极性的判断
根据相关理论判断CS2、H2S、NF3、SiF4 等分子的空间
结构,并指出哪些是极性分子,哪些是非极性分子。
想一想
Cl
Cl
Cl
Cl
H
H
H
N
C
(a)四氯化碳分子—非极性分子
(b)氨分子—极性分子
47
2.2
分子结构与物质的性质
分子的极性与偶极矩
分子极性的强弱,可用
偶极矩来量度。偶极矩(μ)
是电荷量(Q)与正、负电
荷重心间的距离(r)的乘积,
单位为库·米(C·m)。由
于偶极矩数值通常较小,所
以更常用的单位是德拜(D),
1D = 3.336×10
—30 C·m。偶
极矩是一个向量,习惯上规
定偶极矩的方向是由正电荷
重心指向负电荷重心。
资料库
分子的极性对物质的熔、沸点和溶解性等物理性质有
显著的影响。一般而言,由极性分子构成的物质易溶于极
性溶剂中,由非极性分子构成的物质易溶于非极性溶剂中,
这就是“相似相溶”经验规则。例如,氯化氢、氨等极性
物质极易溶于极性溶剂水,而碘、溴等非极性物质易溶于
非极性溶剂四氯化碳。
图2.19 互为对映异构体的分子
当四个不同的原子或基团连接在碳原子上时,该碳原
子称为不对称碳原子。对于大多数有机分子而言,分子的
手性主要是由分子中的不对称碳原子引起的。
手性分子在生命科学和生产手性药物方面有广泛的应用。
在20 世纪60 年代,镇静药沙利度胺(又名“反应停”)是以
一对对映体的混合物来缓解妊娠反应的药物。后来发现,在
欧洲服用过此药的孕妇中有不少产下畸形儿,成为震惊国际
医药界的悲惨事件。随后的研究表明,沙利度胺的一对对映
体中只有一个具有缓解妊娠反应的作用,而另一个则有强致
畸作用。人们从该事件中吸取了教训,不仅研究出了用于分
离对映体的多种方法,而且开始关注药物的不对称合成。
手性
日常生活中我们经常会遇见物体具有一定的对称性,
在分子微观结构的学习中我们观察到许多分子的空间结构
也有一定的对称性。分子的对称性不仅会影响分子的极性,
甚至还会影响分子的化学性质。
手性与分子的对称性密切相关。如图2.19 所示的两个分
子如同人的左、右手一样互为实物与镜像关系,彼此不能重
合。人们将一种物质不能与其镜像重合的特征称为手性。具
有手性的分子称为手性分子。这种互为实物与镜像,又不能
重合的分子互称为对映异构体,简称对映体。
分子结构与性质
第2 章
48
在日常生活中,许多气体分子在降温、加压时会凝聚成相
应的液体或固体,这表明分子之间存在着相互作用力,人们
将这种作用力称为分子间作用力。分子间作用力本质上是一种
静电相互作用,但强度比化学键弱得多,是一种较弱的相互作
用。范德华力和氢键是两种最常见的分子间作用力。
1. 范德华力
范德华力普遍存在于固体、液体和气体分子之间,由
于相互作用的成因不同,范德华力包括多种类型的相互作
用力。范德华力本质上也是电性相互作用,没有饱和性和
方向性,但这种作用力随分子间距离增加而快速减弱,只
有在分子相当接近时才起作用。范德华力很弱,通常比化
学键的键能小1 ~ 2 个数量级,因此克服分子间范德华力
所需的能量要比断裂分子内化学键所需的能量少很多。例
如,干冰吸收能量升华时,仅仅是CO2 间的范德华力改变
了,其分子内的C
O 键没有变化,所以需要的能量较少。
分子间作用力
分子结构对化学性质的影响
分子的空间结构会对物质的化学性质产生重要影响。
组成相同、空间结构不同的分子,常常表现出不
同的化学性质。例如,乙醇(CH3CH2OH)和二甲醚
(CH3OCH3)的分子式都为C2H6O,互为同分异构体。乙
醇分子中含有羟基(— OH),能与活泼金属和羧酸等
发生反应,但二甲醚不具有这些化学性质。2— 氯丁酸
(CH3CH2CHClCOOH)和3—氯丁酸(CH3CHClCH2COOH)
也互为同分异构体,它们在水溶液中都可以电离产生氢离
子而显酸性,但前者的酸性强于后者。这是因为氯原子吸
引电子的能力较强,会影响羧基中O—H 键的极性,而且
氯原子离羧基越近,这种影响越大,从而导致2—氯丁酸羧
基中的O—H 键更容易断裂。在一定条件下,有些互为对
映体的手性分子也会有明显不同的化学性质。例如,某种
手性分子具有很强的杀菌作用,而它的对映体却完全没有
这种效果。通常,人们会利用互为对映体的手性分子在特
定条件下的化学性质差异,将两者进行分离。
表2.3 两种羧酸的电离
平衡常数(25℃)
羧酸
电离平衡常数
2—氯丁酸
1.38×10
—3
3—氯丁酸
8.91×10
—5
资料库
49
2.2
分子结构与物质的性质
拓展视野
范德华力本质上是电性相互作用,但由于形成的偶极不同,所以范德华力包
括取向力、诱导力和色散力等三种类型。
1. 取向力
极性分子的正、负电荷重心不重合,始终存在着一个
正极和一个负极,这种固有的偶极称为永久偶极。当两个
极性分子靠近时,同极相斥,异极相吸,产生相对转动,
极性分子按一定方向排列,这种极性分子间由于永久偶极
的作用而产生的力称为取向力,如图2.20 所示。取向力只
存在于极性分子之间。
2. 诱导力
当极性分子接近非极性分子时,极性分子的偶极电场使非极性分子发生极
化,从而产生正、负电荷重心不重合,这种由于外电场作用而产生的偶极叫做
诱导偶极。分子间由于诱导偶极的作用而产生的力称为诱导力,如图2.21 所示。
诱导力存在于极性分子与极性分子、极性分子与非极性分子之间。
三种不同类型的范德华力
3. 色散力
由于每个分子中电子的不断运动和原子核的不断振动,某一瞬间正、负电荷
重心不重合而产生的偶极称为瞬时偶极。分子间由于瞬时偶极的作用而产生的力
称为色散力,如图2.22 所示。色散力不仅存在于非极性分子之间,也存在于极
性分子之间、极性分子与非极性分子之间。
实验表明,在绝大多数分子之间存在的范德华力都是以色散力为主的。只有极
少数极性特别强的共价分子间才可能以取向力为主。例如,H2O、NH3 等少数分子间
的取向力超过色散力,其他像HCl、HBr、CO 等分子间的作用力都是以色散力为主。
图2.21 诱导力
图2.22 色散力
偶极—偶极力
氯化氢分子
δ
—
δ
— δ +
δ +
图2.20 取向力
δ
—
δ
—
δ
—
δ +
δ +
δ +
δ +
δ +
极性的水分子使非极性
的氧分子产生诱导偶极
O2
O2
O
O
H
H
H
H
偶极—诱导偶极力
δ
—
δ
—
δ
—
δ
—
δ
—
δ
—
δ
—
δ
—
δ
—
δ +
δ +
δ +
δ +
δ +
δ +
δ +
δ +
δ +
瞬时偶极
分子结构与性质
第2 章
50
拓展视野
壁虎能在光滑的墙壁上行走自如,还能倒挂在天花板上爬行,你对此感到惊
讶吗?答案就在于范德华力。壁虎的脚底部长着数百万根极细的刚毛,而每根刚
毛末端又有很多根更细的分支。这种精细结构使得刚毛与物体表面分子间的距离
非常近,从而产生范德华力。壁虎的每根刚毛和墙壁表面之间的范德华力之和足
够强大,能够支撑最高约120 kg 的重量。
科学家从壁虎身上得到启发,发明了可重复使用胶带。
范德华力和壁虎的脚
图2.23 壁虎脚上数百万根极细的刚毛
影响范德华力强弱的因素很多。由表2.4 可看出,对
于组成和结构相似的物质,随着相对分子质量的增大,范
德华力逐渐增强,它们的熔、沸点依次升高。
表2.4 卤素单质的熔、沸点
卤素单质
熔点/℃
沸点/℃
F2
—219.6
—188.1
Cl2
—101.5
—34.0
Br2
—7.2
58.8
I2
113.6
185.2
范德华力的大小主要影响物质的熔、沸点等物理性质。
范德华力越强,物质的熔、沸点越高。表2.4 列出了卤素单
质的熔、沸点数据,你能总结出它们熔、沸点的变化有什么
规律吗?又如何解释这一规律呢?
51
2.2
分子结构与物质的性质
2. 氢键
通常,物质从液态变为固态时,体积是变小的,但水结
成冰后体积却变大,这是为什么呢?
H2O、H2S 同属于氧族元素的氢化物,从相对分子质量对
范德华力和物质熔、沸点的影响的角度分析,应该是H2O 的
沸点低于H2S。然而,事实却相反,H2O 的沸点高于H2S,常
温、常压下,H2O 是液体,H2S 却是气体,这又是为什么呢?
这些问题的存在促使人们思考,除了范德华力外,水分
子之间是否还存在其他作用力,从而使水分子之间的相互作
用变得更强。研究证实,水分子之间确实存在其他作用力,
该作用力就是氢键。
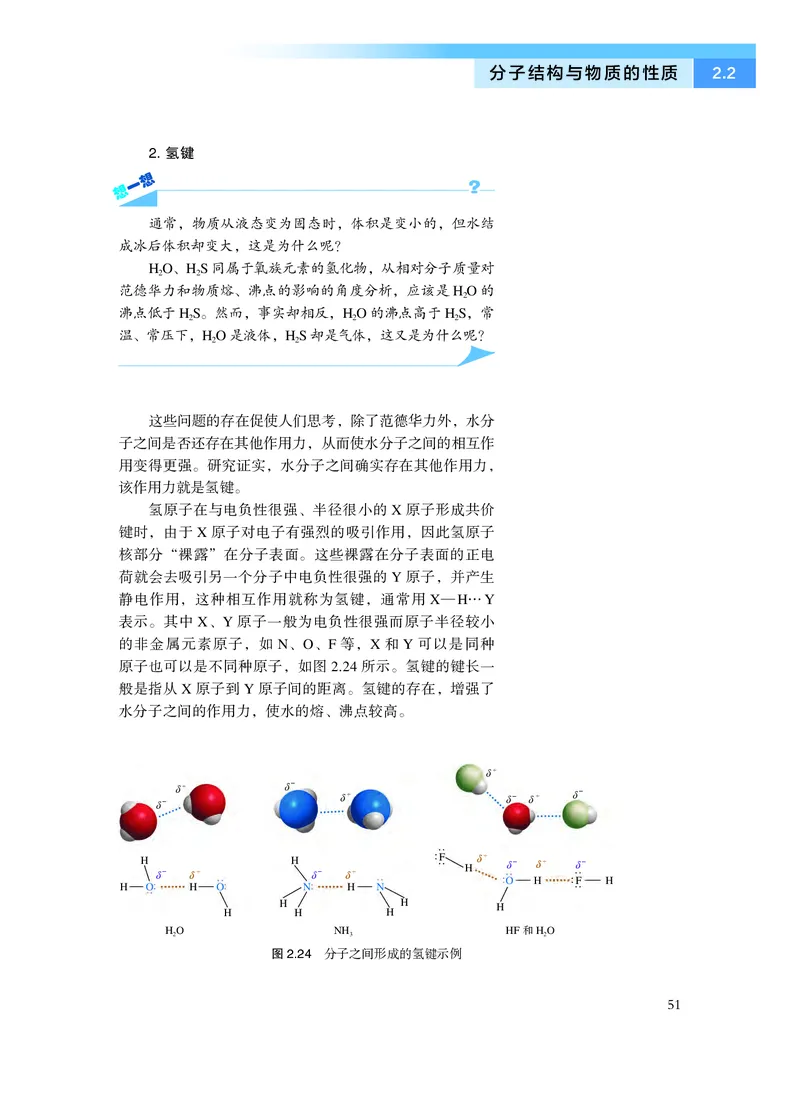
氢原子在与电负性很强、半径很小的X 原子形成共价
键时,由于X 原子对电子有强烈的吸引作用,因此氢原子
核部分“裸露”在分子表面。这些裸露在分子表面的正电
荷就会去吸引另一个分子中电负性很强的Y 原子,并产生
静电作用,这种相互作用就称为氢键,通常用X—H…Y
表示。其中X、Y 原子一般为电负性很强而原子半径较小
的非金属元素原子,如N、O、F 等,X 和Y 可以是同种
原子也可以是不同种原子,如图2.24 所示。氢键的键长一
般是指从X 原子到Y 原子间的距离。氢键的存在,增强了
水分子之间的作用力,使水的熔、沸点较高。
想一想
图2.24 分子之间形成的氢键示例
HF 和H2O
H2O
NH3
δ
—
δ
—
δ
—
δ
—
δ
—
δ
—
δ
—
δ
—
δ +
δ +
δ +
δ +
δ +
δ +
δ +
δ +
H
H
H
O
O
O
N
N
H
H
H
H
H
H
H
H
H
H
F
F
H
分子结构与性质
第2 章
52
拓展视野
在水面下,每个水分子在各个方向上都被相邻的分子
所吸引。然而,表面上的每一个水分子都只受到表面及以
下各个方向上相邻分子的吸引,如图2.26 所示。该作用
的净效应是将分子从表面拉入水中。这种倾向导致水面被
拉紧,像一张弹性薄膜。这种由分子间作用力产生的液体
性质称为表面张力。
由具有较强分子间作用力的分子构成的液体具有很
大的表面张力。水分子之间有广泛的氢键,因此水具有
很大的表面张力。这也解释了许多日常现象,如图2.27
所示,回形针可以浮在水面上,叶子上的水珠呈现椭圆
或近似球体,水虫可以在水面滑行。
水的表面张力与氢键
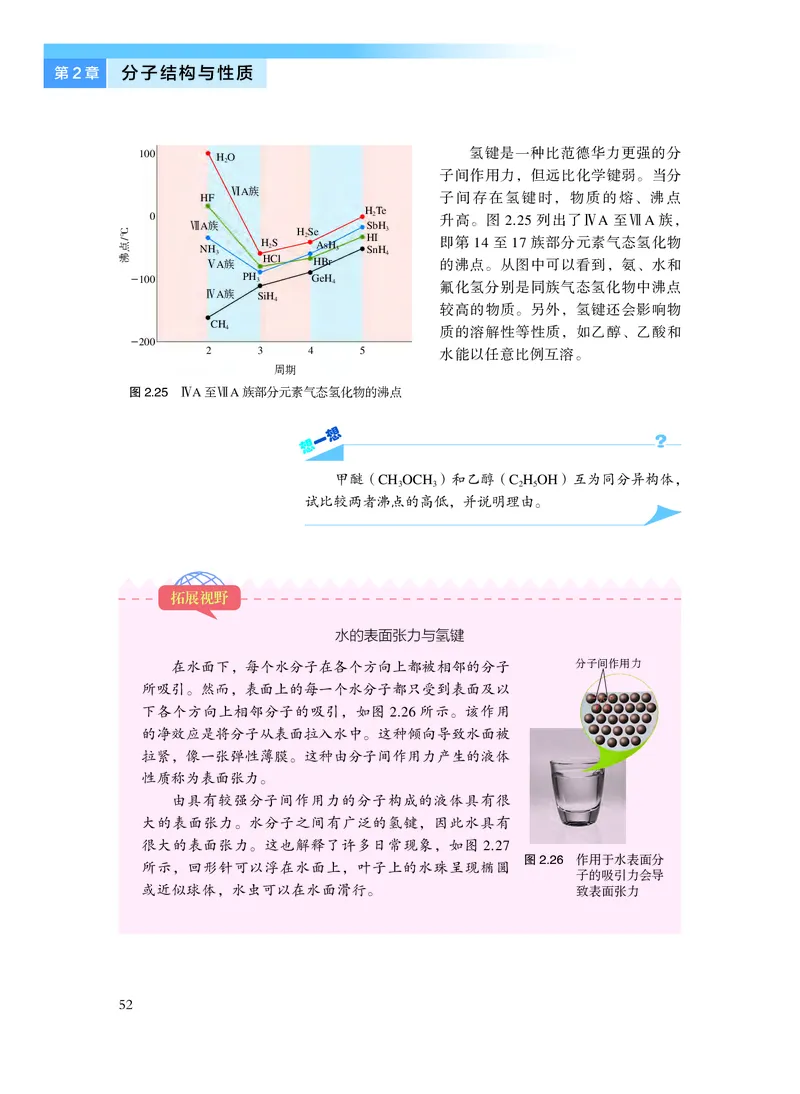
氢键是一种比范德华力更强的分
子间作用力,但远比化学键弱。当分
子间存在氢键时,物质的熔、沸点
升高。图2.25 列出了ⅣA 至ⅦA 族,
即第14 至17 族部分元素气态氢化物
的沸点。从图中可以看到,氨、水和
氟化氢分别是同族气态氢化物中沸点
较高的物质。另外,氢键还会影响物
质的溶解性等性质,如乙醇、乙酸和
水能以任意比例互溶。
图2.25 ⅣA 至ⅦA 族部分元素气态氢化物的沸点
甲醚(CH3OCH3)和乙醇(C2H5OH)互为同分异构体,
试比较两者沸点的高低,并说明理由。
想一想
图2.26 作用于水表面分
子的吸引力会导
致表面张力
分子间作用力
周期
100
0
—100
—200
2
CH4
SiH4
PH3
NH3
HF
GeH4
HBr
SnH4
HI
SbH3
H2Te
H2Se
AsH3
H2S
HCl
H2O
ⅥA族
ⅦA族
ⅤA族
ⅣA族
3
4
5
沸点 /℃
53
2.2
分子结构与物质的性质
邻羟基苯甲醛和对羟基苯甲醛是同分异构体,但邻
羟基苯甲醛的熔、沸点比对羟基苯甲醛的低,这是为什
么呢?
实验证实,氢键不仅存在于分子之间,也可以存在于
分子内。邻羟基苯甲醛分子的羟基与醛基之间存在分子内
氢键(图2.28),而对羟基苯甲醛存在分子间氢键,增强了
分子间的相互作用,所以,对羟基苯甲醛的熔、沸点分别
高于邻羟基苯甲醛的熔、沸点。
图2.28 邻羟基苯甲醛分子
内的氢键
图2.27 与水的表面张力相关的日常现象
氢键会对物质的物理性质产生显著影响。表2.5 列出了两种物质的部分物理性质。请
根据表中数据,试判断哪一种物质能形成分子内氢键。
表2.5 对硝基苯酚、邻硝基苯酚部分物理性质
物质
结构简式
溶解度(25℃)/[g· (100 g H2O)
—1]
熔点/℃
沸点/℃
对硝基苯酚
OH
NO2
1.7
114
279
邻硝基苯酚
OH
NO2
0.2
45
214
想一想
分子内氢键
H
C
O
O
H
分子结构与性质
第2 章
54
学习指南
● Ge(锗)是典型的半导体元素,在电子、材料等领域应用广泛。
回答下列有关锗卤化物的问题。
(1) 判断GeCl4 的空间结构和分子的极性。
(2) 比较下列锗卤化物的熔、沸点,分析其变化规律及原因。
例题导引
问题:
物质
GeCl4
GeBr4
GeI4
熔点/℃
—49.5
26
146
沸点/℃
83.1
186
约400
拓展视野
生命体中许多大分子
内也存在氢键。氢键对维持
生物大分子的空间结构和
生理活性具有重要意义。例
如,蛋白质的α—螺旋是因
分子内氢键而形成的,如图
2.29 所示。
DNA 分子有两条长链,
链内原子间以共价键结合,
其双螺旋结构则是由两条长
链上的碱基通过氢键配对形
成,这构成了遗传机制的化
学基础。DNA 双螺旋结构的
发现,开启了分子生物学时
代,使遗传学研究深入到了
分子层次,生命的奥秘在分
子层次得到了清晰的阐明。
生物大分子中的氢键
图2.29 蛋白质α—螺旋中的分子内氢键
氮原子
氧原子
碳原子
氢原子
支链
氢键
氢键
C
O
H
N
H
N
H
N
H
N
H
N
H
N
H
N
C
O
C
O
C
O
C
O
C
O
C
O
55
2.2
分子结构与物质的性质
● (1) GeCl4 中Ge 的4 个价电子全部用于形成共价键,根据价层
电子对互斥理论可判断出它的空间结构是正四面体形。四个
Ge—Cl 键的极性的向量和为零,故GeCl4 是非极性分子。
(2) 锗卤化物的结构相似,都是正四面体形的非极性分子。从表
中数据不难看出GeCl4、GeBr4、GeI4 的熔、沸点依次升高。
这是因为对于组成和结构相似的物质来说,相对分子质量越
大,分子间作用力越大,熔、沸点越高。
分析:
练习巩固
1. 下列说法中,正确的是( )。
(A) 双原子分子都是非极性分子
(B) 键长越长,分子的极性越强
(C) 非极性分子中一定含有非极性键
(D) 含有极性键的分子不一定是极性分子
2. 下列分子中,含有极性键且为极性分子的是( )。
(A) CCl4
(B) NO
(C) CO2
(D) C2H4
3. 下列物质中,存在分子间氢键的是( )。
(A) HBr
(B) H2S
(C) C2H5OC2H5
(D) H2O2
4. 按要求填写下表。
气态分子
分子的空间结构
分子有无极性
BeCl2
Cl2O
SO3
PH3
分子结构与性质
第2 章
56
身边的有机化合物
第7 章
2.3
配位化合物和超分子
配位键和配位化合物
我们知道NH3 与HCl 反应可以得到白色的NH4Cl。
NH4Cl 溶解在水中电离成NH4
+ 和Cl
—,其中NH4
+ 是由NH3
与H
+ 反应得到的:NH3 + H
+
NH4
+。那么,它们之间的
化学键是怎么形成的?又有什么特点?
NH3 的中心原子是N,它与三个H 形成共价单键后,价
层中还留有一对孤电子对。H 失去电子成H
+ 后,1s 轨道是
空的。NH3 与H
+ 形成NH
+
4 时,NH3 给出了N 上的孤电子对,
H
+ 的空轨道接受了这对电子,于是两个原子共用一对电子
形成了共价键,以这种方式形成的共价键称为配位键。
知道配位键及其特点
认识简单配位化合物的组成
知道简单配位化合物的空间
结构
了解配位化合物的应用
了解超分子化学的特点
知道分子光谱分析
学习聚焦
知识回放
● 共价键的形成和本质
● 分子的空间结构
● 预测分子的空间结构的方法
● 杂化轨道理论
● 分子间作用力
1. 取2 支试管,分别加入1 mL 0.1 mol·L
—1 CuSO4 溶液,然后向溶液中
滴加2 mL 0.1 mol·L
—1 NaOH 溶液,生成Cu(OH)2 沉淀。向一支试管中再滴加
2 mL 0.1 mol·L
—1 NaOH 溶液,观察试管内沉淀是否发生变化。向另一支试管
中滴加2 mL 6 mol·L
—1 氨水,观察试管内沉淀是否发生变化。记录实验现象。
2. 取1 支试管,加入1 mL 0.1 mol·L
—1 AgNO3 溶液,然后向溶液中滴加
1 mL 0.1 mol·L
—1 NaCl 溶液,生成白色的AgCl 沉淀。再向试管中滴加2 mL
6 mol·L
—1 氨水,观察试管内沉淀是否发生变化。记录实验现象。
简单配位化合物的生成
实验探究
实验过程
现象记录
现象分析
Cu(OH)2 沉淀中滴加过量NaOH 稀溶液
Cu(OH)2 沉淀中滴加氨水
AgCl 沉淀中滴加氨水
常见的NH3、H2O、HCl、NaCl、AgCl 等都是由共价
键或离子键结合而成的化合物。这些简单化合物之间还可
以通过进一步的相互作用,形成更为复杂的分子间化合物,
如配位化合物和超分子等。这些复杂的分子间化合物在生物
科技、纳米技术等前沿科学领域有举足轻重的作用。
配位化合物和超分子
57
2.3
从实验中可以看到,向Cu(OH)2 沉淀中加入过量的
NaOH 稀溶液,沉淀无明显变化。但是,Cu(OH)2 沉淀却
可以被过量的氨水溶解,得到澄清的深蓝色溶液。这是因
为Cu
2+ 与氨水发生了化学反应,生成了一种深蓝色的离子。
该离子称为四氨合铜( Ⅱ ) 离子,其化学式是[Cu(NH3)4]
2+。
这个反应可以用离子方程式来表示:
Cu
2+ + 4 NH3
[Cu(NH3)4]
2+
[Cu(NH3)4]
2+ 和SO4
2—再以离子键结合生成[Cu(NH3)4]SO4。
实验中还可以看到,向AgCl 沉淀中加入过量的氨水,
可以使沉淀溶解,得到无色的溶液。这是因为Ag
+ 和氨水
之间发生了化学反应,生成了一种无色的离子。该离子称
为二氨合银( Ⅰ ) 离子,其化学式是[Ag(NH3)2]
+。这个反应
可以用离子方程式来表示:
Ag
+ + 2NH3
[Ag(NH3)2]
+
[Ag(NH3)2]
+ 和Cl
—再以离子键结合生成[Ag(NH3)2]Cl。
这类化合物很多,它们是由金属离子或金属原子(主
要是过渡金属元素)和一些小分子或离子通过配位键结
合而形成的,称为配位化合物,简称配合物。配合物中
的配位键通常是由金属离子或原子提供空轨道[价层中
的(n—1)d、ns 或np 轨道,也有可能是nd 轨道]、小分子
或离子(如H2O、NH3、Cl
—、F
—等)提供孤电子对而形
成的。例如,[Cu(NH3)4]
2+ 中,四个NH3 中的N 各提供
一对孤电子对给Cu
2+,Cu
2+ 的空轨道接受了NH3 提供的
四对电子对,从而形成四个配位键。如图2.30 所示,在
[Cu(NH3)4] SO4 中,SO4
2—称为配合物的外界,Cu
2+ 与NH3
以配位键结合而成的[Cu(NH3)4]
2+ 称为配合物的内界,其
中的Cu
2+ 称为中心离子,NH3 称为配位体,简称配体。
目前已知的配合物超过百万种,是一个庞大的化合
物家族。大多数过渡金属元素的离子对多种配体都具有很
强的结合力,常作为中心离子,因而过渡金属配合物比主
族金属配合物多得多。H2O、NH3、CO、F
—、Cl
—、CN
—、
SCN
—等含有孤电子对的分子或离子常作为配体。配位键的
强度有强有弱,因而有的配合物很稳定,有的则很不稳定。
配合物的中心离子或原子、配体种类和数目不同,配
合物的空间结构会不同。例如,[Ag(NH3)2]
+ 是直线形,
[Zn(NH3)4]
2+是正四面体形,[Co(NH3)6]
3+是正八面体形(图2.31)。
图2.30 [Cu(NH3)4]SO4 配合
物的组成示意图
NH3
NH3
NH3
SO4
2—
2+
Cu
H3N
中心
离子
配位体
内界
外界
分子结构与性质
第2 章
58
图2.31 几种配合物离子的空间结构
如果MA2B2 型的配合物是四面体形的,那么该配合物
有顺反异构体吗?
含有两种或两种以上配体的配合物,若配体在空间的
排列方式不同,还能形成不同的几何结构的配合物。例如,
平面正方形的MA2B2 配合物(M 表示中心离子或原子,A
和B 表示不同的配体)就有图2.32 所示的两种异构体,两
个相同配体在同侧的为顺式异构体,两个相同配体在异侧
的为反式异构体。
配合物在生产、生活中有非常广泛的应用。在工业生
产和许多尖端研究领域,如高新材料、抗癌药物、催化剂
研制等,配合物都发挥着越来越重要的作用。
1. 工业生产中的配合物
工业生产中人们常用形成配合物的方法来检验、分离
金属离子等。例如,从金矿石提炼黄金可以采用氰化法提
取,该方法利用CN
—与Au
+ 生成稳定的配合物离子—
[Au(CN)2]
—,使得不活泼的金属Au 从金矿石进入溶液中
而与其他杂质进行分离,然后再用金属Zn 把溶液中的
[Au(CN)2]
—置换成金属Au。
人们也常利用很多金属羰基配合物的热分解来提纯金属,
如蒙德法提纯金属Ni。该方法利用金属Ni 能与CO 在相对
温和的条件下(50 ~60 ℃)快速地形成易挥发的[Ni(CO)4]
(四羰基合镍)液体,与其他不能形成相应羰基化合物的杂质
生产、生活中的配位化合物
图2.33 从金矿石提炼黄金
图2.32 MA2B2 的顺反
异构体
顺式
反式
想一想
M
M
A
A
B
B
B
A
A
B
[Ag(NH3)2]
+
Ag
+
H3N:
H3N:
H3N:
:NH3
:NH3
:NH3
[Zn(NH3)4]
2+
Zn
2+
[Co(NH3)6]
3+
Co
3+
H3N
NH3
NH3
NH3
NH3
H3N
配位化合物和超分子
59
2.3
元素进行分离。生成的[Ni(CO)4] 不稳定,在220 ~250 ℃下
又会迅速分解成金属Ni 和CO,从而得到高纯度的金属Ni。
2. 生命科学中的配合物
生命体中有很多具有重要生物功能的分子都是金属配
合物。例如,动物血红蛋白的血红素是一种铁的配合物,
植物光合作用所需要的叶绿素是一种镁的配合物,维生素
B12 是一种钴的配合物。血红蛋白的输氧过程、叶绿素等的
生物学功能都离不开配合物的反应机理。
图2.34 血红素、叶绿素的结构
环境污染、过量服用含金属元素的药物,或误食重金属
盐等,都可能导致人体金属中毒。这是因为进入体内的金属
元素作为中心离子(或原子)、蛋白质作为配体,两者之间
形成了配合物,使得蛋白质丧失正常的生物学功能,人体机
能发生异常。医学上常选用一些配位能力更强的化合物作为
药物,进入体内与这些金属元素结合生成更稳定、水溶性大
的配合物,从而将金属元素排出体外,达到解毒的目的。
3. 药物科学中的配合物
1969 年,美国化学家罗森伯格(B. Rosenberg, 1926—
2009)等人发现了第一种具有抗癌活性的金属配合物—顺
铂,即顺式的[PtCl2(NH3)2],如图2.35 所示。顺铂是一种有
效的广谱抗癌药物,可以抑制癌细胞的DNA 复制过程,对
人体的泌尿系统、生殖系统的恶性肿瘤和甲状腺癌、食道癌
等均有一定的治疗效果,但它对肾脏产生的明显伤害和动物
实验表明的毒副作用使它难以推广。迄今为止,各国科学家
已合成并检验了数千种与铂相关的金属配合物,从中筛选并研
制出了对肾功能伤害较小的新型抗癌铂配合物,已用于临床。
血红蛋白的输氧功能
血液中O2 的输送是由
血红蛋白(Hb)来完成的。
人体呼吸时,肺部的O2 通
过配位键与血红蛋白中血红
素上的Fe
2+ 结合,生成氧合
血红蛋白(HbO2)。血液中
的氧合血红蛋白把O2 输送
到人体的各个部位,以维持
正常的生理功能。
资料库
卟啉环
卟啉环
Fe
2+
Mg
2+
O2
分子结构与性质
第2 章
60
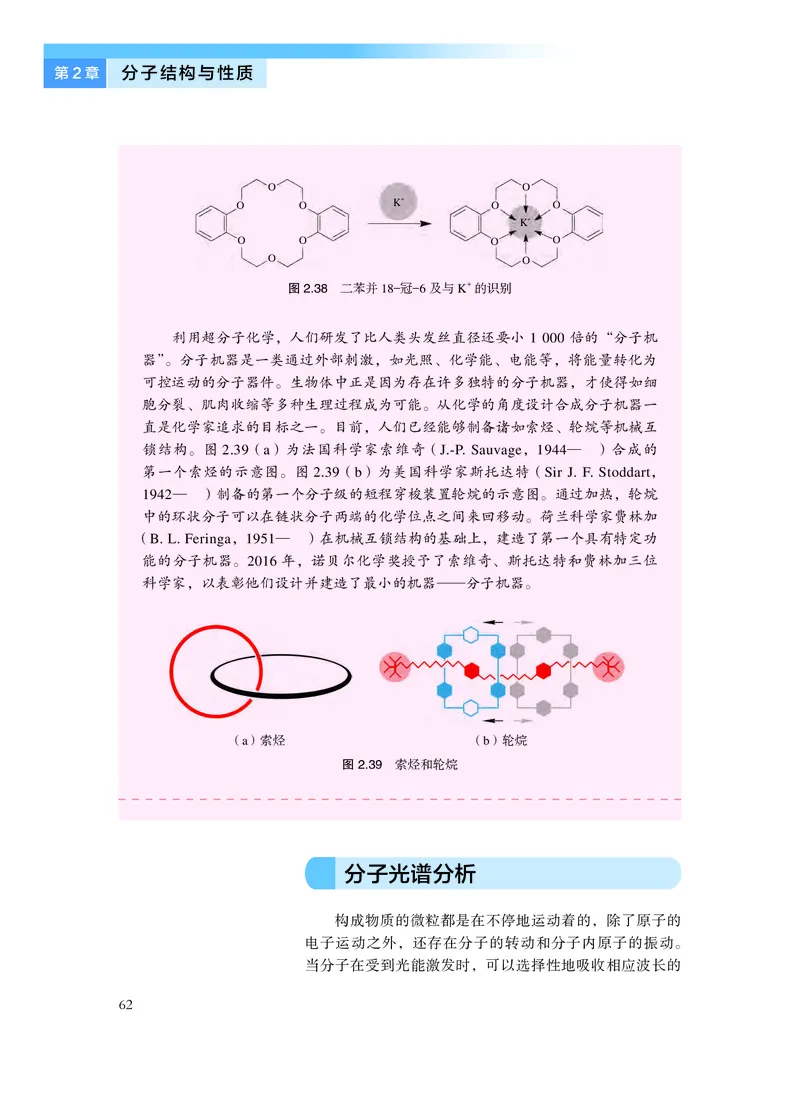
图2.35 [PtCl2(NH3)2] 的顺反异构体
(a) 顺式的[PtCl2(NH3)2] —
有抗癌活性
(b) 反式的[PtCl2(NH3)2] —
无抗癌活性
由两种或两种以上的化学物质,通过分子间非共价键相
互作用所形成的复杂有序且具有特定功能的分子集合体系,
称为超分子。超分子具有明确的微观结构和宏观特性,其框
架结构可通过光谱和晶体X 射线衍射等方法进行分析测定。
范德华力、疏水作用、氢键等非共价键的弱相互作用
是构筑超分子体系的基本作用力。超分子是以分子间的相互
作用力作为工具,把具有特定结构和功能的分子或建筑模块
按照一定的方式组装成新的化合物。这些新的化合物能表现
出单个分子所不具备的特有性质。生物体中执行生物功能的
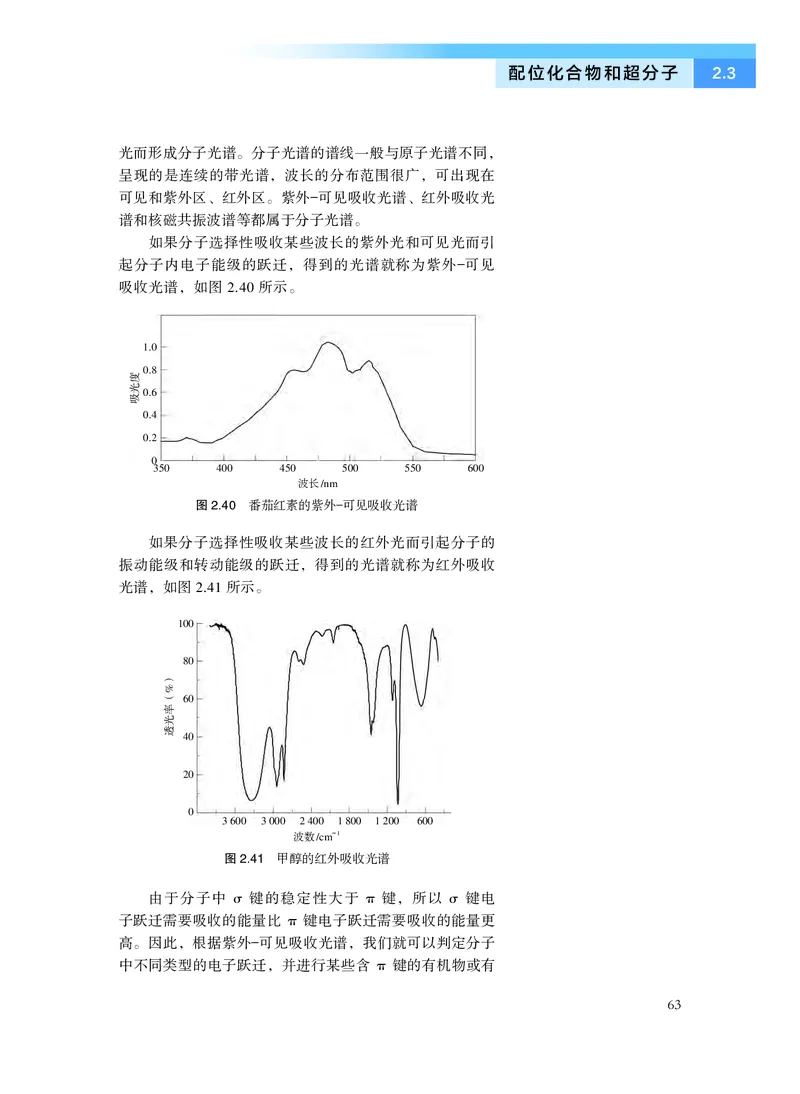
就是无数个这样的超分子体系。例如,生物体中DNA 的双
螺旋结构是在氢键作用的基础上组装而成的超分子体系(图
2.36)。虽然分子间非共价键的弱相互作用力普遍存在于普
通的分子之间,但因这种作用力较小,而且相互作用时无选
择性,所以分子间简单的结合通常不会产生特殊的功能。
超分子和超分子化学
图2.36 通过氢键作用而形成的DNA 双螺旋结构
含氮碱基
腺嘌呤
胸腺嘧啶
鸟嘌呤
胞嘧啶
碱基对
糖—磷酸骨架
3′
5′
A
C
T
G
A
T
C
A
T
G
A
C
T
A
G
T
5′ O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
O
N
N
N
N
N
N
N
C
A
T
G
A
T
G
C
N
N
N
N
N
N
N
N
N
N
N
N
N
NH2
NH2
HN
H2N
H2N
H2N
NH
NH
NH2
OH
HN
OH
O
O
O
O
O
O
O
P
5′
5′
5′
5′
5′
5′
5′
5′
4′
4′
4′
4′
4′
4′
4′
4′
3′
3′
3′
3′
3′
3′
3′
3′
2′
2′
2′
2′
2′
2′
2′
2′
1′
1′
1′
1′
1′
1′
1′
1′
P
P
P
P
P
P
P
5′
3′
3′
3′
5′
配位化合物和超分子
61
2.3
我们所熟知的化学主要是以原子间形成的化学键为
基础,以分子为研究对象。超分子化学则是分子以上层
次的化学,是以多种分子间弱相互作用为基础,研究超分
子—分子组装体的化学分支学科。目前,超分子化学的研
究主要包括分子识别、分子自组装、超分子催化和超分子
器件等。其中,分子识别是超分子化学研究中的核心课题
之一。分子识别,就是一个分子选择性结合另一个分子并
产生某种功能的过程,是组装高级结构必要的途径。图
2.37 展示了如何从分子层次发展到超分子层次。
图2.37 从分子层次到超分子层次
分子层次
分子以上层次
原子
超分子
分子①
分子②
合成
分子间相互作用
(非共价键)
(共价键)
超分子化学的研究成果已经在药物化学、光化学、电
化学传感器、有机半导体、导体和超导体、催化及模拟酶
等研究中得到应用。具有特定结构和功能的超分子体系的
发现,为21 世纪化学、材料科学和生命科学的发展开拓了
一条崭新的研究道路和发展方向。目前,超分子化学的理
论和方法正发挥着越来越重要的作用。
拓展视野
目前,超分子化学的研究热点有两大类:① 环状配体组成的主客体体系;
② 用超分子化合物组装分子机器。
冠醚、穴醚、环糊精等大环化合物具有穴状结构和特殊的配位能力,能与金
属离子或中性分子形成超分子,在物质的提纯分离、功能材料的研制及超分子催
化方面表现出广阔的应用前景。例如,二苯并18—冠—6,由于其空腔大小与K
+ 直
径(266 pm)相匹配,可以识别K
+,如图2.38 所示。
超分子化学
分子结构与性质
第2 章
62
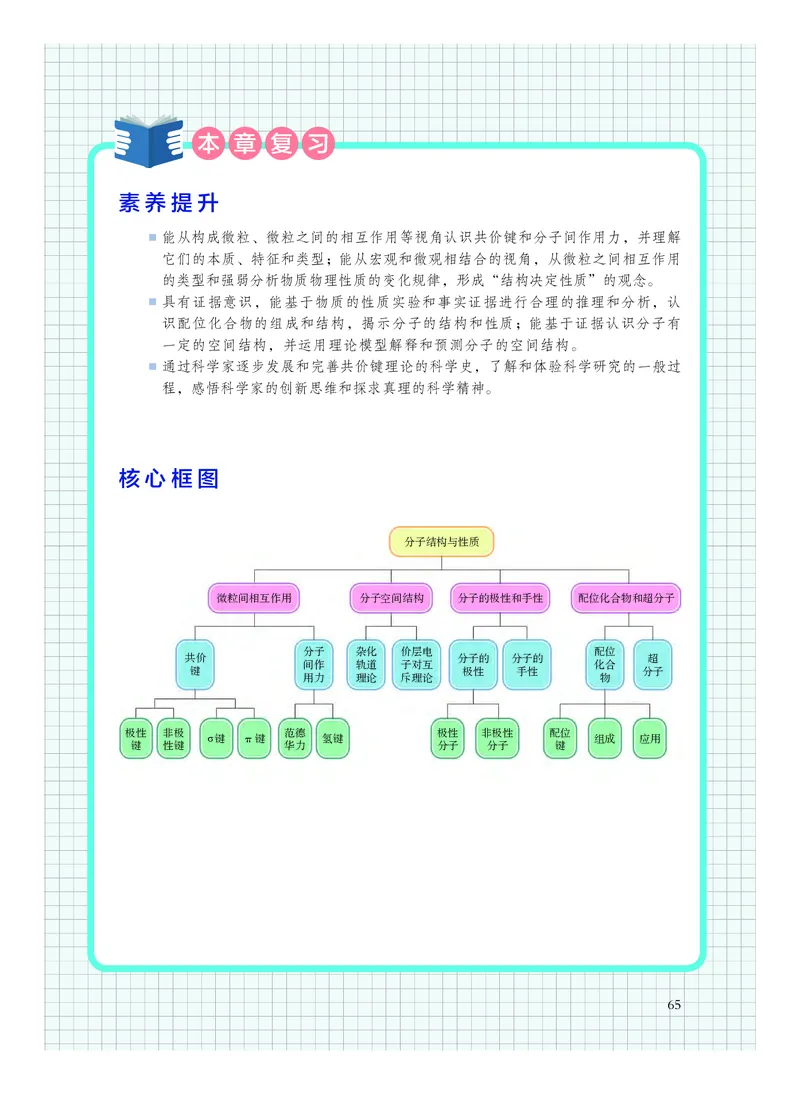
利用超分子化学,人们研发了比人类头发丝直径还要小 1 000 倍的“分子机
器”。分子机器是一类通过外部刺激,如光照、化学能、电能等,将能量转化为
可控运动的分子器件。生物体中正是因为存在许多独特的分子机器,才使得如细
胞分裂、肌肉收缩等多种生理过程成为可能。从化学的角度设计合成分子机器一
直是化学家追求的目标之一。目前,人们已经能够制备诸如索烃、轮烷等机械互
锁结构。图2.39(a)为法国科学家索维奇(J.-P. Sauvage,1944— )合成的
第一个索烃的示意图。图2.39(b)为美国科学家斯托达特(Sir J. F. Stoddart,
1942— )制备的第一个分子级的短程穿梭装置轮烷的示意图。通过加热,轮烷
中的环状分子可以在链状分子两端的化学位点之间来回移动。荷兰科学家费林加
(B. L. Feringa,1951— )在机械互锁结构的基础上,建造了第一个具有特定功
能的分子机器。2016 年,诺贝尔化学奖授予了索维奇、斯托达特和费林加三位
科学家,以表彰他们设计并建造了最小的机器—分子机器。
图2.38 二苯并18—冠—6 及与K
+ 的识别
图2.39 索烃和轮烷
(b) 轮烷
(a) 索烃
构成物质的微粒都是在不停地运动着的,除了原子的
电子运动之外,还存在分子的转动和分子内原子的振动。
当分子在受到光能激发时,可以选择性地吸收相应波长的
分子光谱分析
K
+
K
+
O
O
O
O
O
O
O
O
O
O
O
O
配位化合物和超分子
63
2.3
图2.41 甲醇的红外吸收光谱
如果分子选择性吸收某些波长的红外光而引起分子的
振动能级和转动能级的跃迁,得到的光谱就称为红外吸收
光谱,如图2.41 所示。
光而形成分子光谱。分子光谱的谱线一般与原子光谱不同,
呈现的是连续的带光谱,波长的分布范围很广,可出现在
可见和紫外区、红外区。紫外—可见吸收光谱、红外吸收光
谱和核磁共振波谱等都属于分子光谱。
如果分子选择性吸收某些波长的紫外光和可见光而引
起分子内电子能级的跃迁,得到的光谱就称为紫外—可见
吸收光谱,如图2.40 所示。
图2.40 番茄红素的紫外—可见吸收光谱
由于分子中σ 键的稳定性大于π 键,所以σ 键电
子跃迁需要吸收的能量比π 键电子跃迁需要吸收的能量更
高。因此,根据紫外—可见吸收光谱,我们就可以判定分子
中不同类型的电子跃迁,并进行某些含π 键的有机物或有
波长 /nm
吸光度
350
0
0.2
0.4
0.6
0.8
1.0
400
450
500
550
600
波数 /cm
—1
透光率(%)
0
3 600
3 000
2 400
1 800
1 200
600
20
40
60
80
100
分子结构与性质
第2 章
64
色配合物的定性分析和定量分析。
根据红外吸收光谱,我们可以通过红外特征吸收确定
分子内化学键的键长和键的强度等信息,从而推测分子的
结构。我们还可以依据各种化学键的特征吸收峰判断分子
中可能存在的基团,以鉴别不同类型的有机物。
学习指南
● 一种配合物由Pt、NH3、Cl 组成,实验显示Pt、NH3、Cl 的物质的
量之比为1 ∶ 2 ∶ 4。该配合物的水溶液不导电,加入AgNO3 溶液不
产生沉淀,加入强碱处理不释放NH3。根据上述实验结果,确定该
配合物的化学式、中心离子和配体。
● 该配合物水溶液不导电,说明其不是离子化合物。加入AgNO3 溶
液不产生沉淀,加入强碱不释放NH3,说明Cl
—和NH3 均与Pt
4+ 之
间生成了配位键。所以,该化合物的化学式为[PtCl4(NH3)2],中心
离子是Pt
4+,配体是Cl
—和NH3。
例题导引
问题:
分析:
练习巩固
1. 下列物质中,不属于配合物的是( )。
(A) [Cu(NH3)4]SO4
(B) [PtCl2(NH3)2]
(C) Na3[FeF6]
(D) NH4Cl
2. 下列各组微粒中,都能作为简单配合物中心离子的是( )。
(A) Fe
3+、Ag
+
(B) Al
3+、Na
+
(C) Zn
2+、Li
+
(D) Cu
2+、F
—
3. 下列各组微粒中,都不能作为配体的是( )。
(A) H2O、CO
(B) NH3、F
—
(C) SCN
—、CN
—
(D) Ag
+、NH4
+
4. 下列作用力中,不属于构筑超分子体系的基本作用力的是( )。
(A) 氢键
(B) 范德华力
(C) 共价键
(D) 疏水作用
5. 指出下列配合物离子的中心离子和配体。
① [Au(CN)2]
—
② [AlF6]
3—
③ [Ag(NH3)2]
+
配位化合物和超分子
65
2.3
素养提升
■ 能从构成微粒、微粒之间的相互作用等视角认识共价键和分子间作用力,并理解
它们的本质、特征和类型;能从宏观和微观相结合的视角,从微粒之间相互作用
的类型和强弱分析物质物理性质的变化规律,形成“结构决定性质”的观念。
■ 具有证据意识,能基于物质的性质实验和事实证据进行合理的推理和分析,认
识配位化合物的组成和结构,揭示分子的结构和性质;能基于证据认识分子有
一定的空间结构,并运用理论模型解释和预测分子的空间结构。
■ 通过科学家逐步发展和完善共价键理论的科学史,了解和体验科学研究的一般过
程,感悟科学家的创新思维和探求真理的科学精神。
本章复习
核心框图
65
分子结构与性质
分子空间结构
分子的极性和手性
配位化合物和超分子
微粒间相互作用
共价
键
极性
键
非极
性键
范德
华力
极性
分子
非极性
分子
配位
键
组成
应用
氢键
σ 键
π 键
分子
间作
用力
杂化
轨道
理论
价层电
子对互
斥理论
配位
化合
物
分子的
极性
分子的
手性
超
分子
分子结构与性质
第2 章
66
练习巩固
1. 下列关于共价键和分子极性的叙述中,正确的是( )。
(A) 金属原子和非金属原子之间不可能形成共价键
(B) 极性共价键中的电子对,通常靠近电负性较大的原子
(C) 直线形的分子不可能具有极性
(D) 分子的极性只取决于共价键的极性
2. 碘晶体升华时,下列所述内容发生变化的是( )。
(A) 共价键的键能
(B) 共价键的键长
(C) 碘的化学性质
(D) 分子间作用力的强弱
3. 将乙烷、乙烯、乙炔按照分子中碳碳键键长由短至长的顺序排序,正确的是( )。
(A) 乙烷、乙烯、乙炔
(B) 乙炔、乙烷、乙烯
(C) 乙炔、乙烯、乙烷
(D) 乙烯、乙烷、乙炔
4. 下列变化过程中,共价键被破坏的是( )。
(A) 液溴受热变为气体
(B) 干冰受热变为气体
(C) 钠与水反应
(D) 酒精溶解在水中
5. 下列分子中,所有原子都满足最外层为8电子结构的是( )。
(A) CH4
(B) XeF2
(C) BF3
(D) NF3
6. 下列微粒中,不含有配位键的是( )。
(A) [Fe(SCN)6]
3—
(B) NH3
(C) [Ag(NH3)2]
+
(D) H3O
+
7. 下列分子中,含有不对称碳原子的是( )。
(A) CHCl3
(B) CH3CH2OH
(C)CH3—CH—COOH
—
OH
(D) (CH3)2CHCHO
8. 试计算NCl3和CCl4的中心原子周围各有多少成键电子对和多少孤电子对。分别
66
分子光谱分析
67
2.4
67
体验· 分享
在下列选题中,开展文献、调查、实验等研究,并将成果和体会制作成海报、演示文稿,
进行分享和交流。
ABn型分子的空间结构与中心原子的价层电子对密切相关。那么,它们与中心
原子的杂化轨道类型又有怎样的关系呢?请查询相关资料,并以表格的形式展
示研究成果。参考样表格式如下。
分子的极性对物质的物理性质有显著的影响。请查询资料,设计不同的实验方
案用于检测分子是否有极性,并通过实验比较各种方案的优劣。
含有不对称碳原子的分子是否一定就是手性分子?请查询资料举例说明。
配合物在材料化学、医药科学、催化反应和生命科学等领域有广泛应用,近些
年来的发展尤其迅速。请查询相关资料,撰写一份有关配合物应用的报告。
中心原子价
层电子对数
中心原子的杂
化轨道类型
成键电
子对数
孤电子
对数
价层电子对
的空间结构
分子的空
间结构
实例
2
2
0
3
3
0
2
1
4
4
0
3
1
2
2
1
3
画出这两个分子的空间结构示意图。
9. NiSO4溶于氨水形成蓝色的[Ni(NH3)6]SO4溶液。试回答下列问题。
(1)在[Ni(NH3)6]
2+中,Ni
2+与NH3之间形成了哪种类型的共价键?形成该共价键
时,是哪个成键原子提供了孤电子对?
(2)从[Ni(NH3)6]SO4的组成来看,Ni
2+、NH3和SO4
2—分别称为什么?
10. 苯甲酸(相对分子质量为122)的结构如图所示,但以三氯甲烷为
溶剂时,测得苯甲酸相对分子质量通常介于122 ~244 之间,试对此现象
做出合理解释。
11. 元素As 与N 同族。试预测As 的氢化物分子的空间结构。As 的氢
化物沸点比NH3高还是低?试做出合理解释。
(第10 题)
OH
O
C
分子结构与性质
第2 章
68
参观高等院校或科研院所的红外光谱分析实验室,了解不同状态及不同性质的
有机物测试样的制备方法、红外光谱仪的主要工作原理,并尝试一种简单有机
物的测试和谱图解析。
科学仪器对揭示分子结构的奥秘起着重要作用。请查询资料,列举出有哪些科
学仪器可用于探究分子结构,并说明它们各自的特点。通过这些信息,请思考
和阐述科学仪器对科学研究的意义。
68
晶体结构与性质
第3 章
69
自然界中的晶体千姿百态,美丽
的外形令人赏心悦目。晶体有规则的
外形是原子、分子或离子等微粒有序、
重复排列的宏观表现。
金属晶体
离子晶体
共价晶体和分子晶体
3.1
3.2
3.3
70
早
在史前时期,美丽晶莹的晶体就引起了人们的注意。它们表面光洁而又棱角
分明,千姿百态而又对称有致,充分展示了大自然的鬼斧神工。随着现代科
学技术的发展,有特殊物理性质的人工合成晶体广泛应用于能源、环境、材料、生
命科学等领域。为什么同样是由碳原子构成的晶体,钻石和石墨的硬度却相差很
大?为什么化学式相似的干冰(CO2)和水晶(SiO2)的熔点截然不同?晶体物质
的性质,与晶体中分子、离子、原子等微粒的空间排列和相互作用又有什么关系?
通过对晶体物质的深入了解和学习,我们将进一步掌握晶体物质中微粒有序排
列的一般规律,了解晶体物质中微粒间相互作用的特征和实质,理解晶体的结构与
晶体特殊物理性质之间的关系,认识晶体结构测定是确定分子空间结构的重要方法
和途径之一。
71
3.1
金属晶体
身边的有机化合物
第7 章
3.1
金属晶体
许多天然矿石,如绿柱石、重晶石、水晶等,不仅有
绚丽的色彩,还有光滑平整的表面和规则的几何外形。人类
很早就开始利用晶体,并关注到晶体的几何外形特征。在我
国周口店的中国猿人遗址中就有用水晶等晶体制造而成的工
具;在西汉时期,《韩诗外传》中有对雪花六角形的描述“凡
草木花多五出,雪花独六出”的记载。
晶体的特性
构成物质的分子、原子和离子等微粒可以通过各种相
互作用凝聚成固体,地球上就有许多物质是固体。固体种
类繁多,性质也千变万化,有些固体在电学、磁学或光学
等某一方面具有特殊的性质。固体通常有晶体和非晶体之
分。自然界常见的固体物质中,如食盐、冰、水晶、金属
和许多矿石等,都是晶体,而玻璃、玛瑙、橡胶之类的物
质则属于非晶体。那么,晶体有哪些明显不同于非晶体的
特性呢?
知道晶体与非晶体的区别
知道晶体中微粒的空间排布存
在周期性
知道金属键与金属性质的关系
知道金属晶体的结构
学习聚焦
知识回放
● 共价键
● 物质的聚集状态
图3.1 自然界中各种各样的晶体
雪花
绿柱石
重晶石
水晶
晶体的最基本特性是它们内部结构的有序性以及外形
的对称性。在适宜的条件下,晶体能够自发地呈现封闭的、
规则的几何多面体外形,这称为晶体的自范性。本质上,
晶体的自范性是晶体中原子、分子和离子等微粒在三维空
间里呈现周期性有序排列的宏观表现。相反,非晶体中微
粒的排列则相对无序,因而无自范性。例如,自然界中存
晶体结构与性质
第3 章
72
在的各种石英晶体(晶体SiO2),它们几乎都具有对称的六
角形棱柱状的外形,而玻璃、玛瑙(非晶体SiO2)等就没
有天然的、有规则的外形,如图3.2 所示。根据晶体内部
微粒的种类(原子、离子或分子)和微粒间的相互作用不
同,可以将晶体分为金属晶体、离子晶体、共价晶体和分
子晶体等。
晶体内部微粒的排列呈现周期性,而不同方向上的微粒
排列情况是不同的。因此,在晶体中,不同的方向上具有不
同的物理性质,如导电性、导热性、硬度、解理性
①等,这
称为晶体的各向异性。例如,石墨晶体的导电性表现出各向
异性,在与层平行的方向上的电导率数值约为与在层垂直的
方向上的电导率数值的1 万倍。又如,云母晶体各个方向解
理性不同,若沿两层平面的平行方向施加外力就容易剥离,
若沿着垂直于平面的方向剥离就困难得多。非晶体在各个方
向上的物理性质都一致,显各向同性。例如,玻璃的折光
率、热膨胀系数等,一般不随测定的方向而改变。
图3.2 石英(晶体SiO2)和玛瑙(非晶体SiO2)及其微粒
排列投影图
石英
玛瑙
① 解理性是晶体在外力作用下沿特定的方向裂开成较光滑断面的性质。
73
3.1
金属晶体
取一张云母薄片,用酒精棉擦拭
后晾干,在其表面均匀地涂上一薄层石
蜡,然后放置在铁圈上。将一锥尖固定
在电烙铁的发热头上,电烙铁用铁夹固
定,调节高度,使锥尖刚好与云母薄片
接触,如图3.3 所示。接通电源,观察
云母薄片上石蜡熔化后扩张的形状。再
取一玻璃薄片进行相同的实验,观察玻
璃薄片上石蜡熔化后扩张的形状。
晶体的各向异性
实验探究
图3.3 晶体的各向异性实验装置图
实验物质
现象记录
实验结论
云母薄片
玻璃薄片
拓展视野
中国、以色列、美国和法国等国家的学者于1984 年
前后几乎同时在急冷的合金中发现了一种新的固体,即准
晶体。我们已经知道,物质的构成由其微粒排列特点而
定,构成物质的微粒呈周期性排列的固体物质叫做晶体,
呈无序排列的叫做非晶体。准晶体则介于两者之间,其结
构是长程有序,但又不具有晶体结构内部微粒排列的周期
性,如图3.4 所示。准晶体的发现,是20 世纪80 年代晶
体学研究中的一次突破。
准晶体被发现的几十年来,科学家们在实验室中发
现或创造了各个类型的数百种准晶体。直到2009 年,
科学家们才在俄罗斯采集的矿物样本中首次发现了天然
形成的准晶体,从而为准晶体学说提供了有力的矿物学支撑。
随着研究的不断深入,准晶体越来越多地应用于日常生活和工业生产中。例
如,作为热和电的不良导体,准晶体可用于制作温差电材料,能把热能转化为电能;
因为具有表面不粘、高硬度、耐磨损等特性,准晶体可用于制作煎锅表面的涂层。
图3.4 Al—Mn 准晶体的
微观结构
准晶体
晶体结构与性质
第3 章
74
晶体外形的对称性,是晶体内部结构微粒有序排列的
反映。从内部结构看,晶体中的微粒呈现可重复的周期性
排列,因此,研究晶体结构时只需要找出其中的基本重复
单元加以分析,就能了解整个晶体的结构。晶体结构中基
本的重复单元称为晶胞。如图3.5 所示的就是在由无数金原
子构成的金属晶体中找到的一个基本重复单元。
金属晶体的结构
图3.5 金属金的晶体结构和晶胞
晶胞一般都是平行六面体。晶体可以看作由数量巨大
的晶胞在三维空间无隙并置而成。因此,知道了晶胞的大
小和形状以及晶胞中微粒的种类、数目和微粒所处的空间
位置,就可以了解整个晶体的空间结构。
以金属金的一个晶胞为例(图3.6)。表面上看,在8 个
顶角有8 个原子,6 个面上有6 个原子,一共有14 个原子。
但是,在这个晶胞的上、下、前、后、左、右还重复地排列
着其他晶胞,所以处于顶角和面心的金原子并不为一个晶胞
所独有。其中,处于晶胞顶角的金原子被8 个晶胞所共有,
每一个晶胞占有1
8 个金原子。处于晶胞面心的金原子被2 个
晶胞所共有,每一个晶胞占有 1
2 个金原子。因此,实际在
这个金的晶胞中的金原子数为1
8 ×8 + 1
2 ×6 = 4。
图3.6 金属金的晶胞及其切割示意图
75
3.1
金属晶体
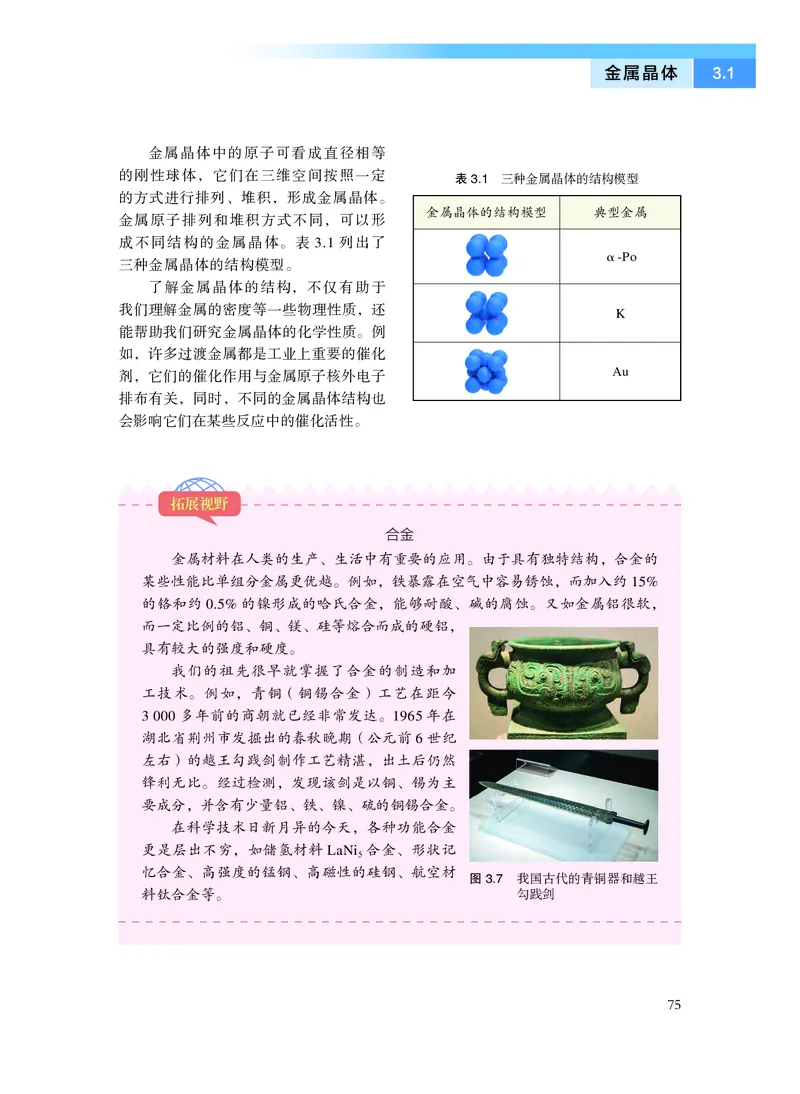
金属晶体中的原子可看成直径相等
的刚性球体,它们在三维空间按照一定
的方式进行排列、堆积,形成金属晶体。
金属原子排列和堆积方式不同,可以形
成不同结构的金属晶体。表3.1 列出了
三种金属晶体的结构模型。
了解金属晶体的结构,不仅有助于
我们理解金属的密度等一些物理性质,还
能帮助我们研究金属晶体的化学性质。例
如,许多过渡金属都是工业上重要的催化
剂,它们的催化作用与金属原子核外电子
排布有关,同时,不同的金属晶体结构也
会影响它们在某些反应中的催化活性。
表3.1 三种金属晶体的结构模型
金属晶体的结构模型
典型金属
α-Po
K
Au
拓展视野
金属材料在人类的生产、生活中有重要的应用。由于具有独特结构,合金的
某些性能比单组分金属更优越。例如,铁暴露在空气中容易锈蚀,而加入约15%
的铬和约0.5% 的镍形成的哈氏合金,能够耐酸、碱的腐蚀。又如金属铝很软,
而一定比例的铝、铜、镁、硅等熔合而成的硬铝,
具有较大的强度和硬度。
我们的祖先很早就掌握了合金的制造和加
工技术。例如,青铜(铜锡合金)工艺在距今
3 000 多年前的商朝就已经非常发达。1965 年在
湖北省荆州市发掘出的春秋晚期(公元前6 世纪
左右)的越王勾践剑制作工艺精湛,出土后仍然
锋利无比。经过检测,发现该剑是以铜、锡为主
要成分,并含有少量铝、铁、镍、硫的铜锡合金。
在科学技术日新月异的今天,各种功能合金
更是层出不穷,如储氢材料LaNi5 合金、形状记
忆合金、高强度的锰钢、高磁性的硅钢、航空材
料钛合金等。
合金
图3.7
我国古代的青铜器和越王
勾践剑
晶体结构与性质
第3 章
76
在金属晶体中,由于金属元素的电离能较小,金属原
子的原子核对其价电子的吸引力较弱,价电子容易脱离原
子核的束缚成为自由电子。这些自由电子不再属于某一金
属原子,可以在整个金属晶体中自由移动。金属正离子可
看作是“浸泡”在自由电子的“海洋”中。因此,金属晶
体的基本结构微粒是金属正离子和自由电子。金属晶体中
金属正离子与自由电子之间的强烈相互作用,称为金属键。
金属键本质上也是一种静电作用,没有方向性和饱和性。
由于金属晶体的结构特点,所以金属有一些特殊的物
理性质,例如,金属不透明,但具有金属光泽及良好的延
展性、导电性和导热性等。因为金属晶体中有自由电子,
所以当可见光照射到金属晶体表面时,晶体中的自由电子
可以吸收光能而呈现能量较高的状态。但是,这种状态
不稳定,电子跃迁回到低能量状态时,会将吸收的各种波
长的光辐射出来,使得金属不透明并具有金属光泽。金属
键没有方向性,当金属受到外力作用时,金属原子之间发
生相对滑动(图3.8),各层金属原子之间仍然保持金属键
的作用。因此,在一定强度的外力作用下,金属可以发生
形变,表现出良好的延展性。需要指出的是,不同的金属
晶体中金属键的强弱差异非常显著,因此金属的熔点、硬
度相差很大。例如,Hg 的熔点是—39℃,而W 的熔点是
3 410℃;Na 的莫氏硬度为0.4,而Cr 的莫氏硬度为9。
金属键与金属的性质
莫氏硬度
硬度是指物质抵抗某些
外部机械作用,特别是刻划
作用的能力。德国矿物学家
莫斯(F. Mohs,1773—1839)
于1822年首先提出莫氏硬度。
莫氏硬度表示物质的相对硬
度,是衡量硬度的一种标准。
资料库
图3.8 金属延展性示意图
请用金属键理论解释为什么金属具有良好的导电性和
导热性。
想一想
金属离子
错位
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
金属原子
自由电子
77
3.1
金属晶体
拓展视野
我们已经知道,当宏观物质处于气、液、固态时,微粒之间的运动方式、
内部结构特点和相互作用不同,使得处于不同聚集状态的物质表现出不同的性
质。当物质处于其他一些聚集状态时,如等离子体、液晶、准晶体等,也表现
出了各自的特殊性质,甚至聚集态物质的颗粒大小、形状或形态等也会影响物
质的性质。
金属纳米晶体指的是具有晶体结构的金属纳米颗粒。纳米是一个长度单位,
1 nm 为1 m 的十亿分之一,100 nm 约为一根头发丝直径的一千分之一。当金属
晶体的粒径减小到纳米级别(通常为1 ~ 100 nm)时,这些尺寸很小的金属晶体
就会表现出与一般金属晶体不同的物理和化学性质。
金属纳米晶体有一个与尺寸相关的有趣特性。我们常见的金属金晶体是“金
色”的,但是实验表明,如果金纳米晶体的尺寸减小至几十到几个纳米时,不同
尺寸的金纳米晶体形成的胶体可以呈现出不同的颜色。此外,不同形状的金纳米
晶体,如球形和棒状金纳米晶体形成的胶体颜色也各不相同。
近年来,金属纳米晶体已经受到基础研究和工业应用的广泛关注。诸如四面
体、立方体、八面体等形状的贵金属纳米晶体,已经能够通过简便的方法制备得
到,它们在催化、光学、电子学、生物医学等领域都有着重要的应用。
金属纳米晶体
图3.9 金纳米晶体形成的不同颜色胶体
晶体结构与性质
第3 章
78
学习指南
● 数一数金属钠、镍、钋的晶胞中分别含有的原子个数。
● (1) 观察金属钠的晶胞可以发现:有8 个钠原子位于晶胞顶角位置,
由于晶胞之间是无隙并置地排列的,所以处于顶角的钠原子被
8 个晶胞所共有,每一个晶胞占有1
8 个钠原子;另有1 个钠原
子处于晶胞内部(体心),并没有被其他晶胞共有,每个晶胞
单独占有这个钠原子。因此,金属钠的晶胞中含有的钠原子数
目为:1
8
×8 + 1 = 2。
(2) 观察金属镍的晶胞可以发现:立方体的8 个顶角均有1
8 个镍原
子,同时6 个面的面心都有1
2 个镍原子。因此,金属镍的晶胞
中含有的镍原子个数为:1
8
×8 + 1
2 ×6 = 4。
(3) 显而易见,金属钋的晶胞中,8 个钋原子位于立方体的顶角。
因此,金属钋的晶胞中含有的钋原子个数为:1
8 ×8 = 1。
例题导引
问题:
分析:
图3.10 金属钠、镍、钋的晶胞
练习巩固
1. 下列物质中,属于晶体的是( )。
(A) 橡胶
(B) 玛瑙
(C) 水晶
(D) 玻璃
2. 下列关于晶体的说法中,正确的是( )。
(A) 固体就是晶体
(B) 凡有规则外形的固体一定是晶体
(C) 晶胞是晶体结构中的基本重复单元
(D) 晶体中不同方向上的物理性质都相同
钋
镍
钠
79
3.1
金属晶体
( 第4 题)
3. 下列说法中,正确的是( )。
(A) 金属在常温下都是固体
(B) 晶体中有正离子就一定有负离子
(C) 金属镁中1 个Mg
2+只与最外层的2个电子存在强烈的相互作用
(D) 金属晶体发生形变时其内部金属离子与“自由电子”之间的相互作
用仍然存在
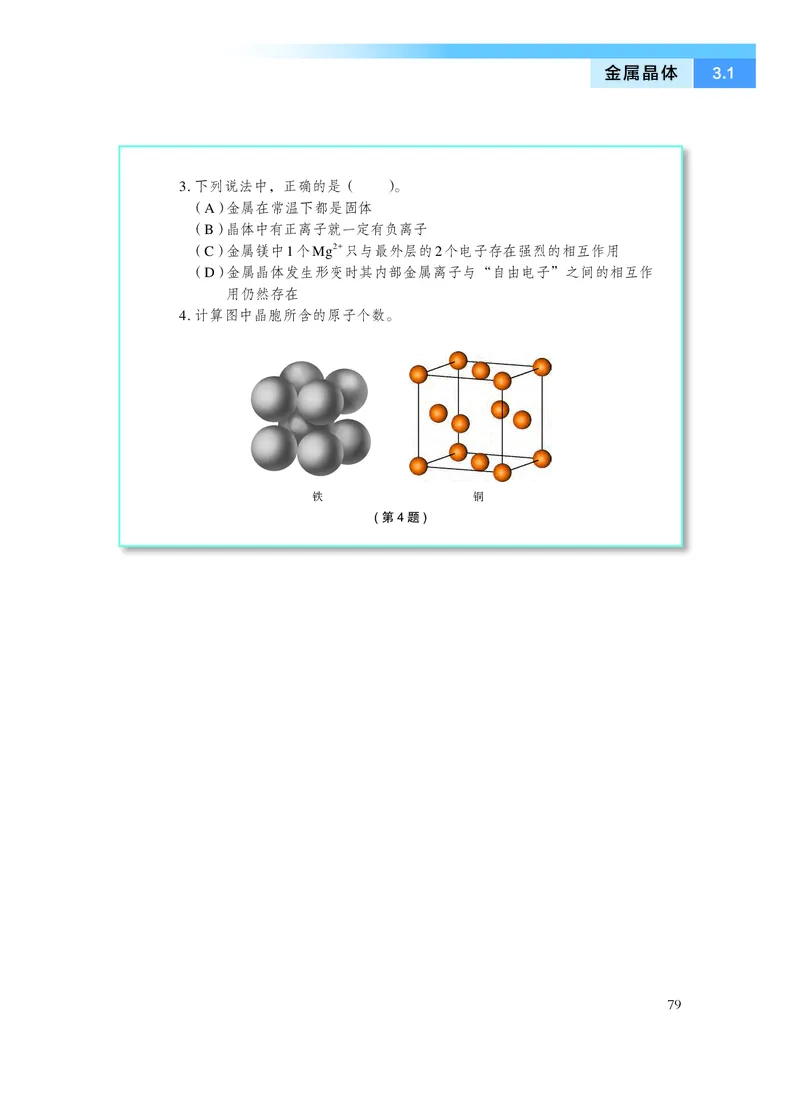
4. 计算图中晶胞所含的原子个数。
铜
铁
晶体结构与性质
第3 章
80
身边的有机化合物
第7 章
3.2
在离子化合物中,由正、负离子之间通过静电相互作
用所形成的化学键叫做离子键。由于离子键的本质是静电
作用,所以离子键的特点是既没有方向性也没有饱和性。
例如,我们把NaCl 晶体中的正、负离子看成是均匀带电
的小球,这些小球在空间各个方向上吸引带相反电荷离子
的能力是相同的,所以形成的离子键没有一定的方向。正、
负离子周围接触的带相反电荷的离子数,主要取决于正、
负离子的相对大小,与它们所带的电荷数无关,只要空间
条件允许,一个离子将尽可能多地吸引带相反电荷的离子
排列在其周围,所以离子键没有饱和性。
离子键和离子晶体
我们周围广泛存在着离子化合物。通常情况下,如
NaCl、MgO、CsCl 等一些常见的离子化合物都是以晶体形
态存在的。在这些离子化合物形成的晶体中,正、负离子
的排列具有怎样的规律?离子晶体中的微粒之间存在哪些
相互作用?这些离子晶体又有哪些性质呢?
认识典型离子晶体的结构特点
能运用离子键解释离子晶体的
某些典型性质
学习聚焦
知识回放
● 晶胞中结构微粒个数的计算
● 金属晶体的结构
离子晶体
分析表3.2 中所列物质的一些物理性质及其递变规律,
讨论结构相似的离子晶体中离子键的强弱可能与哪些因素
有关。
表3.2 几种离子晶体的一些物理性质
离子晶体
核间距/pm
熔点/℃
莫氏硬度
NaCl
276
801
2.5
NaBr
290
750
<2.5
NaI
311
662
<2.5
MgO
205
2 852
6.5
想一想
81
3.2
离子晶体
图3.11 NaCl 晶体的晶胞
图3.12 CsCl 晶体的晶胞
离子半径和离子所带的电荷会影响离子键的强弱。一般
来说,离子半径越小,离子所带的电荷数越大,离子键就越
强。例如,随着卤素离子半径的增大,从NaCl 到NaI,晶
体的熔点降低、莫氏硬度减小。与NaCl 晶体相比,MgO 晶
体的熔点高得多,莫氏硬度也大得多,原因不仅在于Mg
2+
和O
2—的半径都较小,更主要的是Mg
2+ 和O
2—均为二价离子,
而Na
+ 和Cl
—均为一价离子。
离子晶体的基本结构微粒是正、负离子,这些正、负
离子以各种方式在空间呈现一定的、有规则的排列。我们
以NaCl 和CsCl 晶体为例,来了解离子晶体的结构特点。
如图3.11 所示为NaCl 晶体的晶胞,其中,Na
+ 填充在由
6 个Cl
—构成的八面体空隙中,每个Na
+ 与6 个Cl
—相接触,
每个Cl
—与6 个Na
+ 相接触。由于Na
+ 和Cl
—的静电作用,
NaCl 晶体中的Na
+ 和Cl
—尽可能地紧密接触,并通过这种
方式无限延伸,形成NaCl 晶体。
在NaCl 晶体的晶胞中,12 个Na
+ 处于棱心(每个Na
+
被4 个晶胞所共有),1 个Na
+ 处于体心,晶胞中含有的
Na
+ 个数为:12× 1
4 + 1 = 4;8 个Cl
—处于顶角和6 个Cl
—处于
面心,晶胞中含有的Cl
—个数为:8× 1
8 + 6× 1
2 = 4。因此,
晶胞中的Na
+ 和Cl
—个数均为4 个,两者的比值为1 ∶ 1。
如图3.12 所示为CsCl 晶体的晶胞。该晶胞中的Cs
+
填充在由8 个Cl
—构成的立方体空隙中,每个Cs
+ 与8 个
Cl
—相接触,同时每个Cl
—与邻近的8 个Cs
+ 相接触,并通
过这种方式无限延伸,形成CsCl 晶体。
Na
+
Cl
—
Cs
+
Cl
—
晶体结构与性质
第3 章
82
从NaCl、CsCl 晶体的晶胞可以发现,这些由正、负
离子通过离子键交替排列而成的晶体物质,无法从中划分
出一个个独立的NaCl 或CsCl 分子,因此,“NaCl” “CsCl”
等只是表示离子晶体中正、负离子最简个数比的化学式,
而不是分子式。
我们熟悉的NaCl、CsCl、MgO 等离子晶体,是由
正、负离子通过离子键结合而形成的。由于晶体中正、负
离子间排列紧密,静电作用较强,因此这些晶体的熔点都
比较高,硬度也比较大。可以看出,上述列举的这类离子
晶体中的正、负离子都是单原子离子,而实际上大量离子
晶体中的正、负离子是多原子离子,如NH4
+、SO4
2—、NO3
—、
C2H5NH3
+(乙基铵根离子,为一种有机离子)等,有些晶
体中还存在着电中性的小分子。
随着科学研究技术的发展,近几十年来,科学家对
离子晶体的结构和性质有了更深入的了解。通过晶体结
构的测定可以发现,有些离子晶体中还存在氢键、范德
华力或配位键等相互作用。因为构成晶体的微粒之间的
相互作用不同,所以离子晶体的物理性质差异较大。例
如,某些铵盐晶体的熔点并不是很高,如醋酸铵晶体的熔
点仅为112℃。某些由有机正离子或负离子构成的离子化
合物在室温或临近室温的条件下表现为液态,因此又被称
为“离子液体”,如由C2H5NH3
+ 和NO3
—构成的硝酸乙基铵
[(C2H5NH3)NO3] 的熔点只有12℃。
离子晶体的性质
拓展视野
离子液体是指全部由离子构成、在室温或近于室温下呈现液态的物质,也被
称为室温离子液体、室温熔融盐、有机离子液体等。科学家对离子液体的结构进
离子液体
CsCl 晶体的晶胞中Cs
+ 和Cl
—的数目分别是多少?怎样
理解氯化钠和氯化铯的化学式?
想一想
83
3.2
离子晶体
结晶学,又称晶体学,是研究晶体的生成、外部形态、内部化学结构及物理
性质的一门科学。在早期,结晶学的主要研究对象是自然界中的矿物晶体,而结
晶学也在对矿物晶体的研究中得到了发展。19 世纪,随着科学家在物质微观尺
度上认识的加深,结晶学研究范围逐步扩大到矿物以外的各种晶体,并以研究晶
体在原子尺度下的微观结构作为其重要学科领域,已成为研究蛋白质和核酸(如
DNA、RNA)构象的主要方法。 如今,研究人员已建立起了蛋白质数据库,还
利用蛋白质结构分析软件,实现了数据的可视化。
结晶学研究还涉及结晶动力学、结晶技术(材料的结晶行为)以及结晶设备
等。结晶学已有很多分支,如表面晶体学、晶体工程、蛋白晶体学等。结晶学已
成为地质科学家、生命科学家、材料科学家经常使用的主要研究工具。
结晶学
链接学科
行了一系列的研究后指出,由于离子液体一般由离子半径较大的正离子(或负离
子)构成,其结构不对称,较难在空间紧密堆积,正、负离子之间的静电作用较
小,因此其熔点很低。
离子液体具有独特的物理和化学性质,如导电率高,几乎不挥发、不可燃、
热稳定性好,并对有机物和无机物均有良好的溶解性能,可使反应在均相条件下
进行,并显示出反应速率快、转化率高、选择性高、催化体系可重复使用等优点。
因具有良好的化学稳定性,离子液体不仅可以作为溶剂,还可以被循环利用,可
避免引起传统有机溶剂所造成的环境污染和设备腐蚀等问题。离子液体还可以作
为催化剂,可改变反应机理,提高反应的转化率和选择性。
近年来,离子液体作为反应介质、催化剂或促进剂在有机合成、电化学、催
化和萃取分离中,特别是在表面催化、燃料电池中的电解质和导电复合材料方面
都得到了广泛的应用。
晶体结构与性质
第3 章
84
学习指南
● 解释下表中三种离子晶体熔点之间的高低顺序。
● 离子键的强弱可以影响离子晶体的熔点,一般离子键越强,离子
晶体熔点越高。离子键的强度与离子半径和离子所带的电荷有关。
K
+ 和Na
+ 均只携带一个正电荷,而Mg
2+ 携带两个正电荷;同时
K
+、Na
+、Mg
2+ 的半径又逐渐减小。因此,离子键逐渐增强,所以
熔点逐渐升高。
例题导引
问题:
分析:
离子晶体
熔点/℃
KF
858
NaF
993
MgO
2 852
练习巩固
1. 下列数值是元素的原子序数,在它们所对应的原子中,能以离子键结合
成稳定化合物的是( )。
(A) 1 与6
(B) 2 与8
(C) 9 与11
(D) 8 与14
2. 下列关于金属晶体和离子晶体的说法中,正确的是( )。
(A) 构成晶体微粒间的作用力类型不同
(B) 晶体中都含有正、负离子
(C) 晶体都具有很高的熔点
(D) 常温常压下都能导电
3. 离子晶体中的微粒之间可能存在哪些相互作用?试举例说明。
4. 氯化钙在2 700 ℃时熔化,而氯化钠在801 ℃时熔化,两者的离子核间
距相近、晶体结构类似,试解释它们的熔点为何会有如此大的差距。
85
3.2
离子晶体
身边的有机化合物
第7 章
3.3
共价晶体和分子晶体
共价晶体是相邻原子之间通过共价键而形成的三维空
间网状结构的晶体,共价晶体的基本结构微粒是原子。由
于共价键有方向性,晶体中原子的空间排列主要取决于共
价键的空间指向,所以共价晶体中没有球密堆积的特征。
金刚石晶体就是一种常见的共价晶体。
在金刚石晶体中,每个碳原子都采用sp
3 杂化,与紧
邻的四个碳原子以共价键结合,无数碳原子以这种方式相
互连接形成三维空间网状结构(图3.13)。每个C—C 键的
键长为154 pm,键能为347 kJ·mol
—1,相邻两个C—C 键
之间的键角为109°28′。正是这种特殊的排列方式,造就了
金刚石晶体的独特性质。要想破坏或熔化金刚石,必须破
坏其中的共价键,这需要非常大的能量,因此金刚石是一
种熔点很高、硬度很大、性质稳定的物质。
共价晶体
自然界中有许多天然矿石都是晶体。例如,金刚石是
被人们称为宝石的天然晶体,它不仅有绚丽的色彩和光滑
平整的多面体几何外形,还具有诸多优良性质,如熔点高
达3 350 ℃、不导电、莫氏硬度极高。这些性质显然是由
金刚石的晶体结构决定的。那么,在金刚石晶体中,碳原
子又是怎样排列的呢?
认识常见共价晶体、分子晶体
的结构特点及其性质
知道混合型晶体和过渡型晶体
知道晶体X 射线衍射分析
学习聚焦
知识回放
● 共价键
● 范德华力与氢键
图3.13 金刚石晶体及其晶体结构
图3.14 金刚石的晶胞
在金刚石的晶胞(图3.14)中,由于共价键的饱和性与
方向性,每个碳原子都只与周围的四个呈正四面体排列的碳
原子形成碳碳单键。由此可见,金刚石中碳原子的排列方式
与金属晶体和离子晶体中紧密堆积的排列方式有明显的不同。
109°28′
154 pm
晶体结构与性质
第3 章
86
除了金刚石外,常见的共价晶体还有纯净的晶体硅
(Si)、水晶(SiO2)和金刚砂(SiC)等。它们被广泛应用
于光学研究、地质勘探、石油钻井等。
如果将金刚石晶体结构中的碳原子替换为硅原子,可
得到晶体硅的结构。若再向晶体硅结构中的每个Si— Si
键中“插入”一个氧原子,如图3.15 所示,硅原子和氧
原子以共价键结合,每一个硅原子周围有四个氧原子排
列成以硅原子为中心的硅氧四面体,再由许多个这样的
硅氧四面体通过氧原子互相连接,从而形成二氧化硅的
晶体结构。在二氧化硅晶体中,每一个硅原子与周围四
个氧原子形成共价键,每一个氧原子与周围两个硅原子
形成共价键,因此,在二氧化硅晶体中硅原子和氧原子
的个数比为1 ∶ 2。由此可见,由原子通过共价键形成的
共价晶体中也不存在单个分子,因此也有人认为,可以
把整个共价晶体看成是由“无限”数目的原子构成的一
个“巨型分子”。
碳化硅(SiC)是1891 年人工合成的无机非金属材料。
它的晶体结构可以看作是金刚石晶胞内部的四个碳原子替换
成硅原子,从而形成C—Si 交替排列的空间骨架。由图3.16
中的碳化硅晶胞可以看出,晶胞中各有四个碳原子和四个硅
原子,因此在整个碳化硅晶体中碳原子和硅原子的个数比为
1 ∶ 1。
碳化硅晶体硬度大、耐磨性好、耐高温,可用于制作
耐磨的高级工程陶瓷,还可用于制造火箭喷管、燃气轮机
叶片等。此外,碳化硅还广泛应用于半导体、光伏发电、
航空航天等领域。
图3.15 二氧化硅(方石英)的晶体结构
图3.16 碳化硅的晶胞
O
Si
C
Si
87
3.3
共价晶体和分子晶体
从表3.3 中的数据可以看出,共价晶体大多具有较高的熔点和硬度,这是为什么?讨
论表中所给出的结构相似的共价晶体的熔点差别较大的可能原因。
表3.3 部分共价晶体的键长、键能、熔点和莫氏硬度
共价晶体
键长/pm
键能/(kJ·mol
—1)
熔点/℃
莫氏硬度
金刚石
154(C—C)
347(C—C)
3 350
10
碳化硅
184(C—Si)
301(C—Si)
2 600
9
晶体硅
234(Si—Si)
226(Si—Si)
1 415
7
共价晶体熔点的高低与其内部结构密切相关。在共价
晶体中,所有原子均以共价键相结合,只要共价键不被破
坏,原子就不能自由移动。对结构相似的共价晶体来说,
原子半径越小,键长越短,键能越大,晶体的熔点就越高,
硬度也越大。应当指出,硬度大的物质不一定经得起锤击,
例如,金刚石是硬度最大的物质,却很容易在锤击时破碎。
这是因为共价晶体中的共价键具有方向性,当受到大的外
力作用时会发生原子错位而断裂。
拓展视野
金刚石因具有极高的反射率,所以很有观赏性,大颗粒的金刚石(钻石)可
用于珠宝的制作。除此之外,由于金刚石是硬度最大的物质,因此可以用于精密
螺纹的细加工、制作超精密仪器,如精密光学仪器的反射镜等。
早在18 世纪中期,人们通过对金刚石的燃烧产物进行化学分析,发现金刚石和石
墨一样,几乎全部由碳元素组成。但是,什么原因导致了两者的性质存在如此巨大的
差异呢?随着结构化学的发展,人们开始了解金刚石的晶体结构。
现在对天然金刚石的形成过程的普遍认识是,天然金刚石是在地下深处的高
温、高压条件下形成的。知道了天然金刚石的形成条件,于是人们开始研究金刚
石的人工合成,比较常见的方法有高温高压法、化学气相沉积法等。目前,工业
用途的金刚石薄膜大部分是人工合成的产物,人工合成的金刚石作为工程材料广
泛应用在工业生产中。
金刚石人工合成的探索
想一想
晶体结构与性质
第3 章
88
在我们的日常生活中,存在许多由分子聚集而成的物
质,如冰、干冰、酒精等。气体分子可以通过分子间作用力
结合形成晶体。那么,你知道这些晶体的结构是怎样的吗?
它们又具有哪些特殊的性质呢?
我们把分子之间以分子间作用力结合而成的晶体称为
分子晶体。分子晶体的基本结构微粒是分子(或稀有气体元
素原子)。多数由非金属单质、非金属的氢化物、稀有气体
等形成的晶体,属于分子晶体。
二氧化碳在常温下是气态,若将二氧化碳气体加压到约
6.06×10
6 Pa 时,就会凝结成固态二氧化碳。固态二氧化碳
易升华,转变为气态时会吸收大量的热,可使周围温度降低
到—78 ℃左右且不产生液体,所以固态二氧化碳又被称为“干
冰”,常用于人工降雨、低温实验等。图3.17 为干冰及其晶
胞。干冰是一种典型的分子晶体,其基本结构微粒是二氧化
碳分子,相邻的二氧化碳分子之间依靠范德华力相互结合。
分子晶体
表3.4 列出了一些分子晶体的熔点。请根据表中所列数
据讨论:一般情况下,分子晶体的熔点为什么比典型的离子
晶体和共价晶体的熔点低?
表3.4 一些分子晶体的熔点
分子晶体
熔点/℃
CF4
—183.6
CCl4
—22.9
CBr4
90
由于分子晶体是通过分子间作用力构成的,分子晶体
在熔化时,破坏的只是分子间作用力,只需要外界提供较
少的能量,因此分子晶体的熔点通常较低,硬度也较小,
有较强的挥发性。
通常,组成和结构相似的分子晶体,随着相对分子质
量的增大,范德华力增强,熔点升高。
图3.17 干冰及其晶胞
C
O
想一想
89
3.3
共价晶体和分子晶体
图3.18 冰的结构
然而,还有一些是依靠分子间的氢键形成的分子晶体,
如冰。水分子在形成固体时,分子之间除了范德华力相互
作用外,还有氢键相互作用。由于氢键具有一定的方向性,
中间的水分子与周围位于正四面体顶角的四个水分子结合,
这四个顶角的水分子也按照相同的规律再与周围其他的水
分子结合。这样,每个水分子中的氧原子周围都有四个氢
原子,氧原子与其中的两个氢原子通过共价键结合,而与
另外两个水分子的氢原子以氢键结合在一起(图3.18)。在
冰晶体中,水分子之间的距离较大,不如液态水中分子排
列得紧密。因此当水结成冰时,体积变大,密度减小。
同时,因为氢键的作用力比范德华力要大,破坏分子
间的氢键需要消耗较多的能量,所以存在分子间氢键的分
子晶体则具有更高的熔点。
拓展视野
1888 年,奥地利植物学家莱尼茨尔(F. Reinitzer,1857— 1927)在研究苯
甲酸胆固醇酯时发现,该化合物在145.5 ℃以下时呈固态,在145.5 ~ 178.5 ℃时
呈浑浊黏稠状态,在178.5 ℃以上时是透明的液体。科学家研究发现,在这个浑
浊黏稠状态时,苯甲酸胆固醇酯既具有液体的流动性和连续性,又具有固态晶体
的某些光学特性,于是人们把这种特殊的状态称为液晶态(简称液晶)。
液晶
H
O
晶体结构与性质
第3 章
90
石墨的熔点高达3 850 ℃,甚至比金刚石的熔点还要高;
但石墨的层状结构中,层与层之间容易在外力作用下发生
相对滑动;另外,石墨的导电能力比一般非金属单质强一百
倍,导热性能在常温下甚至超过钢铁、铅等金属材料。根据
以上事实依据类比已经学过的晶体类型,想一想石墨的这些
性质分别和哪些晶体类似。推测石墨晶体中可能存在哪些微
粒间的作用力。
液晶分子之间的排列具有方向性,但不整齐,它既不像晶体那样有固定的形
状和排列整齐,也不像液体时那样杂乱无序、可以流动而没有固定的形状,而是
介于固体和液体之间的一种过渡态,如图3.19 所示。
图3.19 液晶材料固体受热形成液晶态及液态的分子排列示意图
从成分和出现液晶的物理条件来看,液晶可以分为热致液晶和溶致液晶两大类。
热致液晶是指由于温度改变出现的液晶。溶致液晶是指由于有机物溶液浓度发生变
化而出现的液晶,溶致液晶广泛存在于自然界、生物体中,与生命息息相关。
20 世纪60 年代后,人们对液晶材料的应用研究逐步发展起来。例如,用热致
液晶材料制作的显示屏具有功耗低、可靠性高、便于携带等优点。因此,热致液
晶材料被广泛应用于计算机显示屏、电子表、手机等各类电子产品的生产。在化
学化工领域,溶致液晶材料可用于纳米材料和多相催化剂的制备等。在医学领域,
溶致液晶材料可作为靶向药物的囊壁材料等。随着液晶材料的不断发展,更多功
能的液晶材料将在不同领域推动人类社会的发展,使我们的生活变得更加美好。
混合型晶体和过渡型晶体
想一想
晶体
液晶
液体
温度
91
3.3
共价晶体和分子晶体
图3.20 石墨的晶体结构
某些晶体的内部同时存在多种不同的微粒间作用
力,所以会具有不同晶体类型的特性,这类晶体称为
混合型晶体。石墨晶体就是一种典型的混合型晶体。
石墨晶体具有层状结构,层与层之间存在范德华力相
互作用,所以石墨质地很软,各层之间容易受力而发
生滑动断裂成鳞状薄片。层内碳原子通过sp
2 杂化轨
道以共价键形成平面六边形结构,每个碳原子还有一
个与碳环平面垂直的未参与杂化的2p 轨道,并含有
一个未成对电子,能够形成遍及整个平面的离域π
键。这些离域π 键中的电子可以在层内自由运动,
在外加电场的作用下定向运动形成电流,这就是石墨
沿层平面方向导电能力强的原因。因为这些独特的性
质,石墨晶体可以用作惰性电极或电刷、机械工业中
的润滑剂、铸造工艺中的高温冶金材料等。
在学习过程中,我们把晶体分成了金属晶体、离
子晶体、共价晶体和分子晶体等类型,但往往有些晶
体结构微粒之间的相互作用和性质,是介于不同种类
的晶型之间,有很多实际晶体属于这种过渡型晶体。
例如,像TiCl4 这类高价态的金属氯化物往往倾向于形
成以共价键为主的过渡型晶体,其熔点仅为—25℃,与
分子晶体性质类似;像TiO2 这类高价态的金属氧化物
也倾向于形成以共价键为主的过渡型晶体,但其性质
偏向于共价晶体,熔点可以高达1 830℃。
宝玉石鉴定需要描述宝玉石的重量、颜色和透明度等物理特征,划分宝玉
石的等级,更重要的是通过荧光光谱、红外光谱等化学分析手段确定宝玉石的
元素组成、结构特征,鉴别宝玉石的种属、真伪。涉及的专业课程有:结晶矿
物学、晶体光学、宝石学概论、宝石鉴定仪器等。宝玉石鉴定师是指经过国家
特殊专业的培训并取得相应职业资格,能出具鉴定证书的高层次专业人才。
宝玉石鉴定
链接职业
142 pm
340 pm
晶体结构与性质
第3 章
92
晶体X 射线衍射分析,就是利用X 射线在晶体中的衍
射效应进行结构分析的技术,是测定晶体结构和分子空间
结构的重要手段。每种晶体都具有特定的晶体结构,因此
在一定波长的X 射线照射下,每种晶体物质都会显示出特
有的衍射图像。
晶体X 射线衍射分析
根据晶体衍射线的方向,可以确定晶胞的大小和形状;
根据衍射线的强度,可以确定晶胞中原子的种类及其在晶胞
中的位置排列,从而知道分子的空间结构。应用晶体X 射线
衍射技术测定得到的纯物质晶体结构的信息中,包括分子中化
学键的键长、键角和分子在晶胞中的实际排列状况等,所以晶
体X 射线衍射分析是测定分子空间结构的重要方法和途径。实
际上,许多化学小分子的空间结构是通过晶体结构测定得到的,
图3.22 就是122 K 时用X 射线衍射分析测得的甲醇晶体结构图。
图3.22 甲醇晶体和甲醇晶胞
X 射线衍射分析,具有不损伤样品、测量精度高、信息量
大等优点,使其在冶金化工、生命科学、材料科学等领域得到
极其广泛的应用。特别是在生命科学研究中,晶体X 射线衍
射分析已发展成为测定蛋白质等生物大分子结构的重要方法。
甲醇晶胞
甲醇晶体
O
H
C
图3.21 X 射线衍射仪和单晶衍射图
X 射线衍射仪
单晶衍射图
93
3.3
共价晶体和分子晶体
练习巩固
1. 金刚石是典型的共价晶体。下列关于金刚石的说法中,正确的是( )。
(A) 晶体中不存在独立的单个分子
(B) 碳原子采用sp
2杂化,相互之间以共价键相结合
(C) 碳原子通过共价键结合形成平面网状结构
(D) 化学性质稳定,即使在高温下也不会与氧气发生反应
2. 下列物质熔化时,不破坏化学键的是( )。
(A) 氯化钠 (B) 固态乙醇 (C) 金刚石 (D) 石英
3. 几种卤化氢(HX)晶体的熔点如下:HF(—83.57 ℃)、HCl(—114.18 ℃)、
HBr(—86.81 ℃)。在HX晶体中,HF的熔点比HCl的熔点高,应如何解释?
4. 干冰是分子晶体,但是科学家已经在一定条件下制得了二氧化碳共价
晶体。试比较二氧化碳共价晶体和二氧化硅共价晶体,哪一种硬度更大?说
明理由。
5. 完成下表。
晶体类型
金属晶体
共价晶体
分子晶体
结构
基本结构微粒
微粒间相互作用
性质
熔点
硬度
实例
学习指南
● 怎样理解二氧化碳和二氧化硅晶体熔点的差异与它们晶体结构之间
的关系?
● 二氧化碳晶体属于分子晶体,是二氧化碳分子之间通过范德华力构
成的;二氧化硅晶体属于共价晶体,硅原子和氧原子是以共价键结
合的。这两种晶体在熔化时,分子晶体破坏的是范德华力,共价晶
体破坏的是共价键。由于二氧化硅晶体中Si—O 键的作用力比二
氧化碳中的范德华力强得多,所以,二氧化硅共价晶体的熔点比二
氧化碳分子晶体的熔点高。
例题导引
问题:
分析:
晶体结构与性质
第3 章
94
素养提升
■ 能结合实验现象说出晶体与非晶体的区别。能从晶体的微观结构说明同类晶体的共
性和不同类晶体性质差异的原因,描述晶体结构中微粒排列的周期性规律。
■ 能联系物质的组成和结构解释各类晶体结构中微粒间作用(金属键、离子键、共价
键和分子间作用力等)的特征和实质,并运用各类晶体模型预测晶体的物理性质,
形成“结构决定性质”的观念。
■ 能举例说明人类对晶体结构的认识是不断发展的,并简单说明促进这些发展的原
因。知道晶体X 射线衍射分析在测定物质结构和分子空间结构中的作用,感受物质
结构的研究及其理论发展对化学学科发展的贡献。
本章复习
核心框图
94
晶体结构与性质
晶体中微粒的
相互作用
晶体结构
测定
晶体的特征
金属晶体
结构
特征
结构
特征
结构
特征
结构
特征
性质
特点
性质
特点
性质
特点
性质
特点
离子晶体
共价晶体
分子晶体
95
3.4
晶体X 射线衍射分析
95
练习巩固
1. 下列关于晶体与非晶体的说法中,正确的是( )。
(A) 晶体的熔化温度一定比非晶体高
(B) 晶体有自范性但晶体中微粒的排列无序
(C) 非晶体无自范性而且非晶体中微粒的排列无序
(D) 晶体和非晶体都有解理性
2. 科学家发现了一种新能源—可燃冰,它的主要成分是甲烷与水分子的结晶水合
物(CH4 · nH2O)。这种可燃冰的晶体类型是( )。
(A) 离子晶体
(B) 分子晶体
(C) 共价晶体
(D) 金属晶体
3. 下列晶体中,化学键种类相同,晶体类型也相同的是( )。
(A) SO2与SiO2
(B) CO2与H2O
(C) NaCl与HCl
(D) CCl4与KCl
4. 下列关于晶体的说法中,正确的是( )。
(A) 只要含有金属正离子的晶体就一定是离子晶体
(B) 离子晶体中一定含金属正离子
(C) 不含共价键的物质形成的晶体只能是金属晶体或离子晶体
(D) 分子晶体的熔点不一定比金属晶体熔点低
5. 下列关于离子晶体的叙述中,正确的是( )。
(A) 1 mol氯化钠中有NA个氯化钠分子
(B) 氯化钠晶体的晶胞中,每个Na
+周围距离最近的Cl
—有6个
(C) 氯化铯晶体的晶胞中,每个Cs
+周围紧邻4个Cl
—
(D) 离子晶体中,结构微粒之间存在的相互作用都是离子键
6. 下列说法中,正确的是( )。
(A) 冰熔化时,分子中H—O键发生断裂
(B) 结构相似的共价晶体中,共价键键长越短的晶体通常熔点越高
(C) 分子晶体中,共价键键能越大的晶体熔点越高
(D) 分子晶体中,分子间作用力越大,分子越稳定
7. Cu2O是一种半导体材料,氧原子位于立方晶胞的顶角和体心,则该晶胞中含有的
铜原子个数为( )。
(A)2
(B)4
(C)6
(D)8
8. 下列关于金属及金属键的说法中,正确的是( )。
(A) 金属键具有方向性与饱和性
(B) 金属键是金属正离子与自由电子间的相互作用
(C) 金属导电是因为在外加电场作用下产生自由电子
(D) 金属具有光泽是因为金属正离子吸收并放出可见光
晶体结构与性质
第3 章
96
选项
(A)
(B)
(C)
(D)
晶体名称
碘化钾
干冰
氖
二氧化硅
基本结构微粒名称
正、负离子
分子
原子
分子
晶体内存在的结合力
离子键
氢键
共价键
范德华力
9. 晶体氢氧化钠、二氧化硅、四氯化碳熔化时,需要克服的微粒间的相互作用依次
是( )。
(A) 离子键、共价键、共价键
(B) 金属键、共价键、范德华力
(C) 离子键、范德华力、范德华力
(D) 离子键、共价键、范德华力
10. 下表列出了有关晶体的说明,其中正确的是( )。
体验 · 分享
在下列选题中,开展文献、调查、实验等研究,并将成果和体会制成海报、演示文稿,
进行分享和交流。
我国古代劳动人民是世界上最早对晶体进行观察、总结和应用的先驱者。陶弘
景(456—536)在《名医别录》中称白石英:
“六面为削,白澈有光”。汉字“晶”
字解为“精光也,从三日”,对晶体表征得入木三分。17 世纪,物理学家惠更斯(C.
Huygens,1629 —1695)提出晶体的规则几何外形起因于构成晶体的微粒有序
排列的猜想。X 射线被发现后,科学家利用晶体做X射线的光栅获得了清晰的
X 射线衍射图,从而可以推测晶体内部的微观结构。请你查阅、搜集有关资料,
用时间轴的方式,总结人类对晶体结构认识的发展过程,以及你从中得到的收
获和体会。
在理想晶体中, 微粒按一定的规则有序排列。 但在实际的晶体中,由于晶体形成
条件、原子的热运动及其他外界条件的影响,微粒的排列往往存在偏离理想晶体
结构的现象。人们将这种现象称为晶体缺陷。晶体缺陷对于晶体的利用既存在不
利的一面,也存在有利的一面。请你查阅相关资料,了解晶体缺陷对于晶体性质
的影响以及人们是如何有目的、有计划地利用晶体缺陷来改变材料性质的。
中国是世界上最早研究和生产合金的国家之一,在商朝(距今3 000 多年前)
青铜(铜锡合金)工艺就已非常发达;春秋晚期(公元前6 世纪左右)已锻
打出锋利的剑(钢制品),越王勾践的青铜剑就是采用硫化技术处理的合金宝
剑,出土后依然锋利无比。随着科技的发展,新型合金的种类日益增多,在
96
97
3.4
晶体X 射线衍射分析
97
不同领域发挥着重要的作用。请搜集不同合金材料以及它们在不同领域中的
应用。
借助放大镜或显微镜,仔细观察食盐颗粒的形状,并与氯化钠的晶胞形状作对
比,你有什么发现?尝试用重结晶方法,通过控制结晶的条件,制取较大颗粒
的胆矾晶体。
应用虚拟仿真技术(X 射线衍射仪仿真软件),学习在计算机上进行仿真操作实
验:
“X 射线衍射测试氯化钠样品”。
选用身边常见的合适材料,搭建金属金晶体晶胞和氯化钠晶体晶胞模型,讨论
两者在微观结构上的差异。
草酸H2C2O4,又名乙二酸(含有羧基—COOH),是一种无色透明结晶或粉末。
它是生物体的一种代谢产物,广泛分布于植物、动物和真菌体中,在人体中容
易与钙离子形成草酸钙而导致肾结石。人体肾结石中,草酸钙肾结石是最为常
见的一种,约占肾结石的80% 以上。如医生在患者体内发现肾结石,需要检测
肾结石的化学成分(草酸钙结晶)。请你根据学过的知识,设计不同的方法,分
析它的化学成分和晶体结构,并比较说明各方法的原理及其优缺点。
晶体结构与性质
第3 章
98
Ⅰ 化学词汇中英文对照表
中文
英文
中文
英文
σ 键
σ bond
极性键
polar bond
π 键
π bond
键长
bond length
电负性
electronegativity
键角
bond angle
电离能
ionization energy
键能
bond energy
电子层
electron shell
金刚石
diamond
电子排布
electron configuration
金属键
metallic bond
电子云
electron cloud
金属晶体
metallic crystal
范德华力
van der Waals force
晶胞
unit cell
非极性分子
nonpolar molecule
晶体
crystal
非极性键
nonpolar bond
离子键
ionic bond
非晶体
noncrystal
离子晶体
ionic crystal
分子光谱
molecular spectroscopy
能级
energy level
分子间作用力
intermolecular force
能量
energy
分子晶体
molecular crystal
泡利不相容原理
Pauli exclusion principle
概率
probability
配合物
coordination compound
共价晶体
covalent crystal
氢键
hydrogen bond
共用电子对
shared electron pair
石墨
graphite
构造原理
Aufbau principle
手性
chirality
光谱
spectrum
原子轨道
atomic orbital
洪特规则
Hund’s rule
原子结构
atomic structure
极性分子
polar molecule
杂化轨道
hybrid orbital
学生必做实验
实验名称
页码
简单配合物的制备
简单配位化合物的生成
56
Ⅱ 学生必做实验索引
附 录
99
3.4
晶体X 射线衍射分析
Ⅲ 元素周期表
晶体结构与性质
第3 章
100
本册教材图片提供信息:
本册教材中的图片由视觉中国、IC photo 等提供。
后 记
本册教材根据教育部颁布的《普通高中化学课程标准(2017 年版)》编写并经国家
教材委员会专家委员会审核通过。
编写过程中,上海市中小学(幼儿园)课程改革委员会专家工作委员会,上海市教
育委员会教学研究室,上海市课程方案教育教学研究基地、上海市心理教育教学研究基
地、上海市基础教育教材建设研究基地及基地所在单位华东师范大学,上海市化学教育
教学研究基地(上海高校“立德树人”人文社会科学重点研究基地)及基地所在单位复
旦大学给予了大力支持。复旦大学化学实验教学示范中心为本册教材中化学实验的验证
和拍摄提供支持。许多专家和社会各界朋友十分关心并提出很多意见和建议。在此一并
表示诚挚的敬意!
本册教材出版之前,我们就教材中使用的照片、图片等选用作品,通过多种途径与
作者进行了联系,得到了他们的大力支持,在此表示衷心的感谢!对于未联系到的作者,
我们也希望作者能及时联系出版社,以便出版社支付相应的稿酬。
欢迎广大师生来电来函指出教材的差错和不足,提出宝贵意见,我们将不断修订,
使教材趋于完善。
2020 年5 月