文档内容
黄冈市 年春季高二年级期末质量监测
2025
化 学
本试卷共 页, 题.全卷满分 分.考试用时 分钟.
8 19 100 75
祝考试顺利
★ ★
注意事项:
答题前 先将自己的姓名 准考证号 考场号 座位号填写在试卷和答题卡上 并
1. , 、 、 、 ,
将准考证号条形码粘贴在答题卡上的指定位置
.
选择题的作答 每小题选出答案后 用 铅笔把答题卡上对应题目的答案标号
2. : , 2B
涂黑 写在试卷 草稿纸和答题卡上的非答题区域均无效
. 、 .
非选择题的作答 用黑色签字笔直接答在答题卡上对应的答题区域内 写在试
3. : .
卷 草稿纸和答题卡上的非答题区域均无效
、 .
考试结束后 请将答题卡上交
4. , .
可能用到的相对原子质量
:H-1 C-12 O-16 Pd-106 Pt-195
一、选择题:本题共 小题,每小题 分,共 分.在每小题给出的四个选项中,只有
15 3 45
一项是符合题目要求的.
化学与生活密切相关 下列说法错误的是
1. .
聚乙炔中存在共轭大 键 可用于制备导电高分子材料
A. π ,
液态氯乙烷汽化吸热 具有冷冻麻醉作用 可用于身体局部快速镇痛
B. , ,
甲醛具有强氧化性 其水溶液具有杀菌 防腐性能 可用于消毒和制作生物标本
C. , 、 ,
聚乳酸具有良好的生物相容性和生物可吸收性 可用于手术缝合线
D. ,
下列方法不能用来测定分子结构的是
2.
色谱法 红外光谱 核磁共振氢谱 射线衍射
A. B. C. D.X
关于物质的分离 提纯 下列说法错误的是
3. 、 ,
用水除去乙烯中混有的乙醇蒸汽
A.
用硫酸铜溶液除去乙炔中混有的硫化氢气体
B.
用浓溴水除去苯中混有的苯酚
C.
用饱和碳酸钠溶液除去乙酸乙酯中混有的乙酸和乙醇
D.
高二化学试卷 第 页 共 页
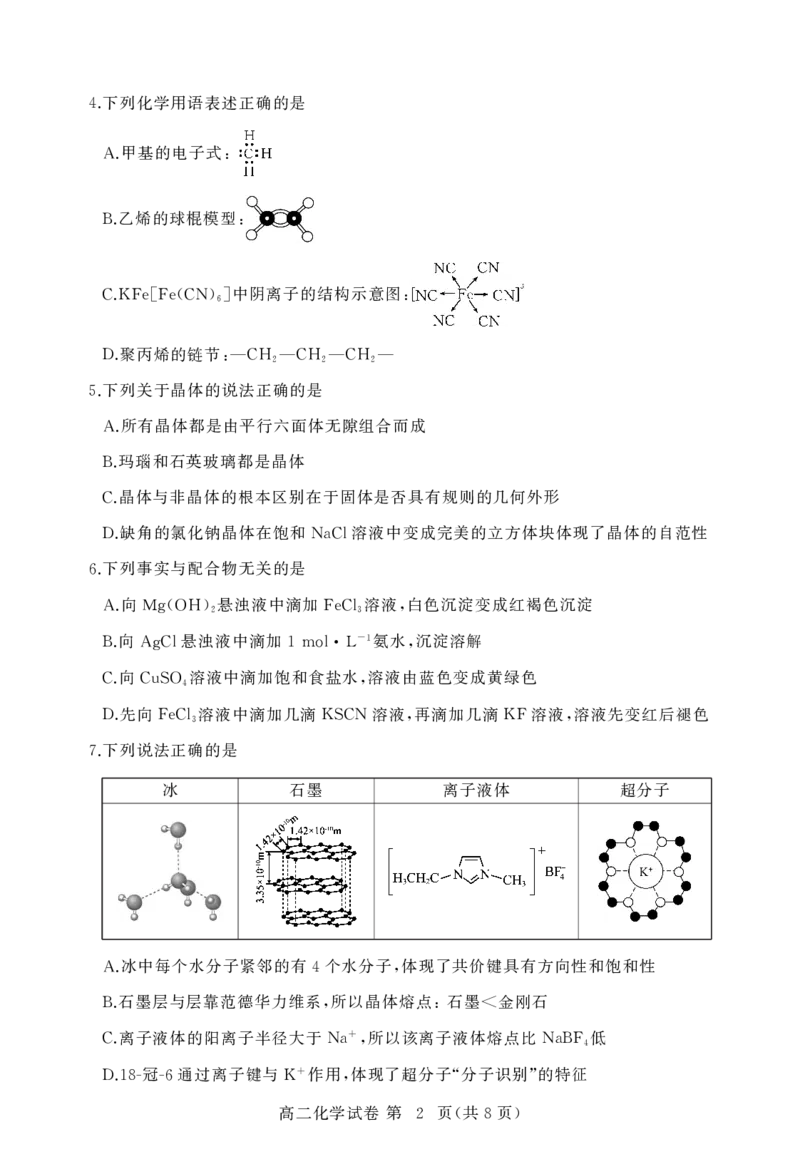
1 ( 8 )下列化学用语表述正确的是
4.
甲基的电子式
A. :
乙烯的球棍模型
B. :
中阴离子的结构示意图
C.KFe[Fe(CN)6] :
聚丙烯的链节
D. :—CH2—CH2—CH2—
下列关于晶体的说法正确的是
5.
所有晶体都是由平行六面体无隙组合而成
A.
玛瑙和石英玻璃都是晶体
B.
晶体与非晶体的根本区别在于固体是否具有规则的几何外形
C.
缺角的氯化钠晶体在饱和 溶液中变成完美的立方体块体现了晶体的自范性
D. NaCl
下列事实与配合物无关的是
6.
向 悬浊液中滴加 溶液 白色沉淀变成红褐色沉淀
A. Mg(OH)2 FeCl3 ,
向 悬浊液中滴加 氨水 沉淀溶解
-1
B. AgCl 1molL ,
向 溶液中滴加饱和食盐水 溶液由蓝色变成黄绿色
C. CuSO4 ,
先向 溶液中滴加几滴 溶液 再滴加几滴 溶液 溶液先变红后褪色
D. FeCl3 KSCN , KF ,
下列说法正确的是
7.
冰 石墨 离子液体 超分子
冰中每个水分子紧邻的有 个水分子 体现了共价键具有方向性和饱和性
A. 4 ,
石墨层与层靠范德华力维系 所以晶体熔点 石墨 金刚石
B. , : <
离子液体的阳离子半径大于 所以该离子液体熔点比 低
+
C. Na , NaBF4
冠 通过离子键与 作用 体现了超分子 分子识别 的特征
+
D.18G G6 K , “ ”
高二化学试卷 第 页 共 页
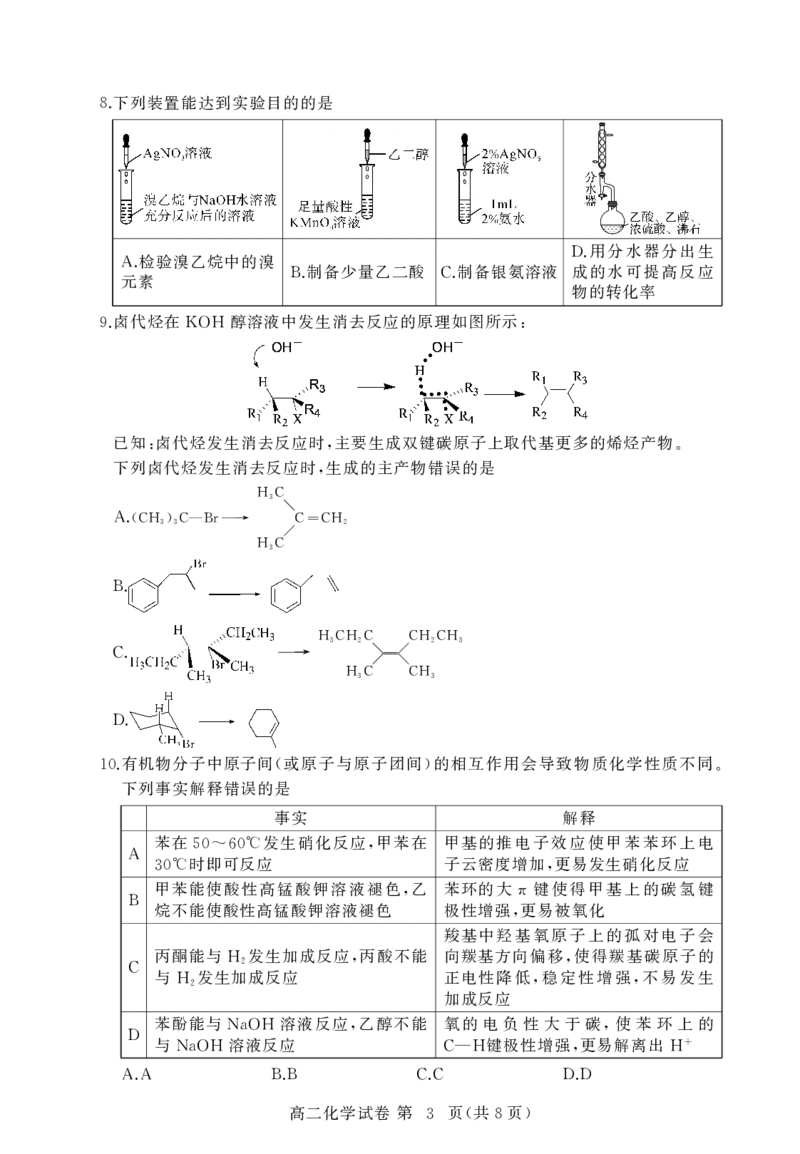
2 ( 8 )下列装置能达到实验目的的是
8.
用分水器分出生
检验溴乙烷中的溴 D.
A. 制备少量乙二酸 制备银氨溶液 成的水可提高反应
元素 B. C.
物的转化率
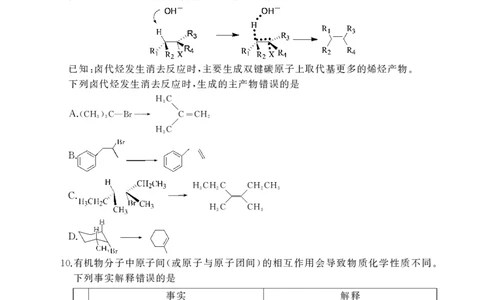
卤代烃在 醇溶液中发生消去反应的原理如图所示
9. KOH :
已知 卤代烃发生消去反应时 主要生成双键碳原子上取代基更多的烯烃产物
: , .
下列卤代烃发生消去反应时 生成的主产物错误的是
,
H3C
A.(CH3)3C—Br → C=CH2
H3C
B.
H3CH2C CH2CH3
C. →
H3C CH3
D.
有机物分子中原子间 或原子与原子团间 的相互作用会导致物质化学性质不同
10. ( ) .
下列事实解释错误的是
事实 解释
苯在 发生硝化反应 甲苯在 甲基的推电子效应使甲苯苯环上电
50~60℃ ,
A 时即可反应 子云密度增加 更易发生硝化反应
30℃ ,
甲苯能使酸性高锰酸钾溶液褪色 乙 苯环的大 键使得甲基上的碳氢键
, π
B 烷不能使酸性高锰酸钾溶液褪色 极性增强 更易被氧化
,
羧基中羟基氧原子上的孤对电子会
丙酮能与 发生加成反应 丙酸不能 向羰基方向偏移 使得羰基碳原子的
H2 , ,
C 与 发生加成反应 正电性降低 稳定性增强 不易发生
H2 , ,
加成反应
苯酚能与 溶液反应 乙醇不能 氧的 电 负 性 大 于 碳 使 苯 环 上 的
NaOH , ,
D 与 溶液反应 键极性增强 更易解离出 +
NaOH C—H , H
A.A B.B C.C D.D
高二化学试卷 第 页 共 页
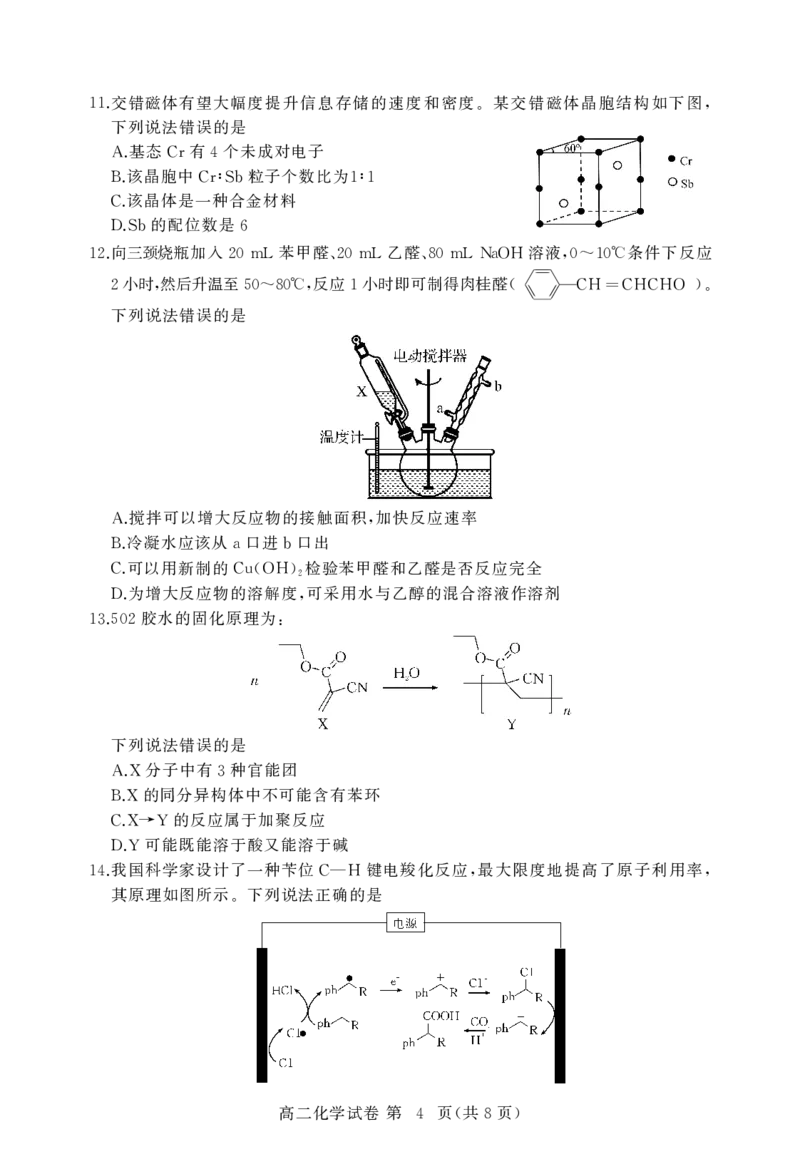
3 ( 8 )交错磁体有望大幅度提升信息存储的速度和密度 某交错磁体晶胞结构如下图
11. . ,
下列说法错误的是
基态 有 个未成对电子
A. Cr 4
该晶胞中 粒子个数比为
B. Cr∶Sb 1∶1
该晶体是一种合金材料
C.
的配位数是
D.Sb 6
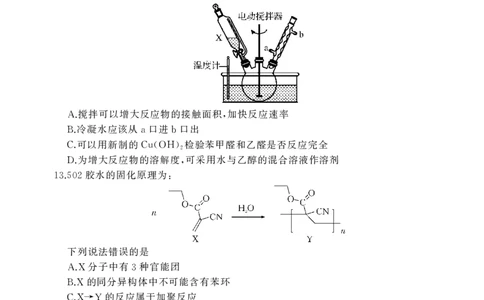
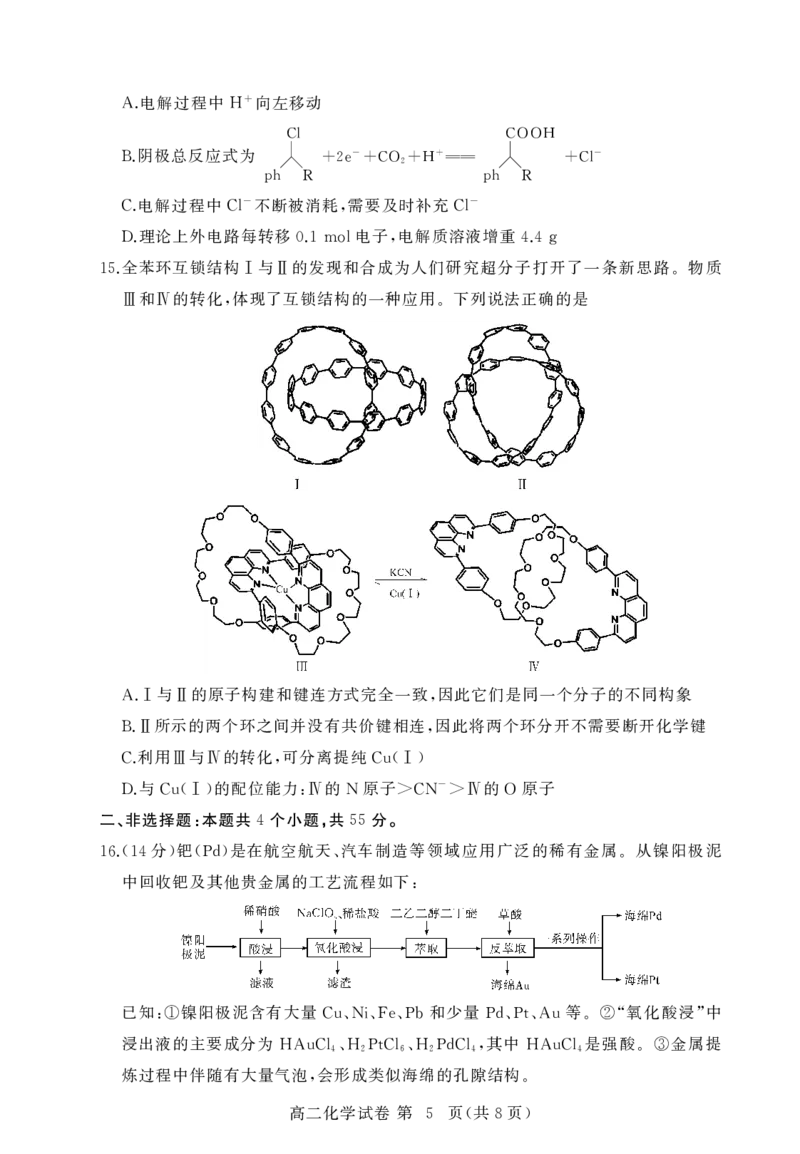
向三颈烧瓶加入 苯甲醛 乙醛 溶液 条件下反应
12. 20mL 、20mL 、80mLNaOH ,0~10℃
小时 然后升温至 反应 小时即可制得肉桂醛
2 , 50~80℃, 1 ( CH=CHCHO ).
下列说法错误的是
搅拌可以增大反应物的接触面积 加快反应速率
A. ,
冷凝水应该从 口进 口出
B. a b
可以用新制的 检验苯甲醛和乙醛是否反应完全
C. Cu(OH)2
为增大反应物的溶解度 可采用水与乙醇的混合溶液作溶剂
D. ,
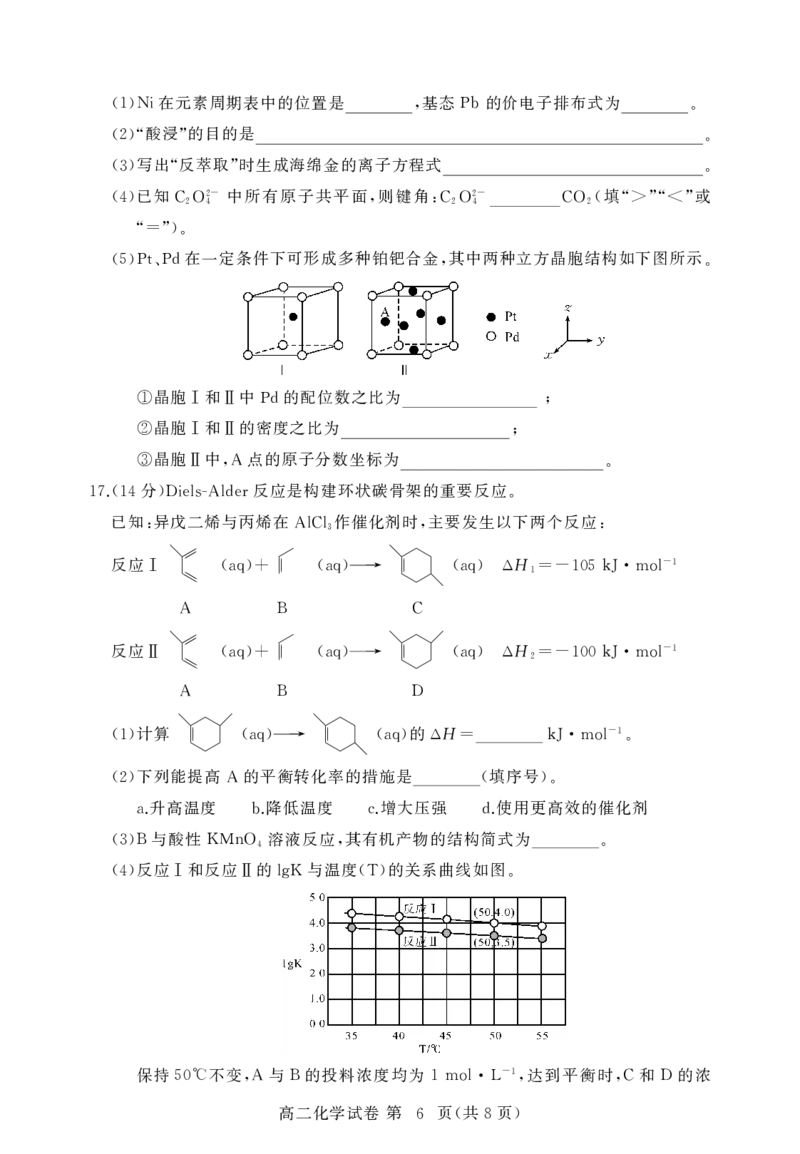
胶水的固化原理为
13.502 :
下列说法错误的是
分子中有 种官能团
A.X 3
的同分异构体中不可能含有苯环
B.X
的反应属于加聚反应
C.X→Y
可能既能溶于酸又能溶于碱
D.Y
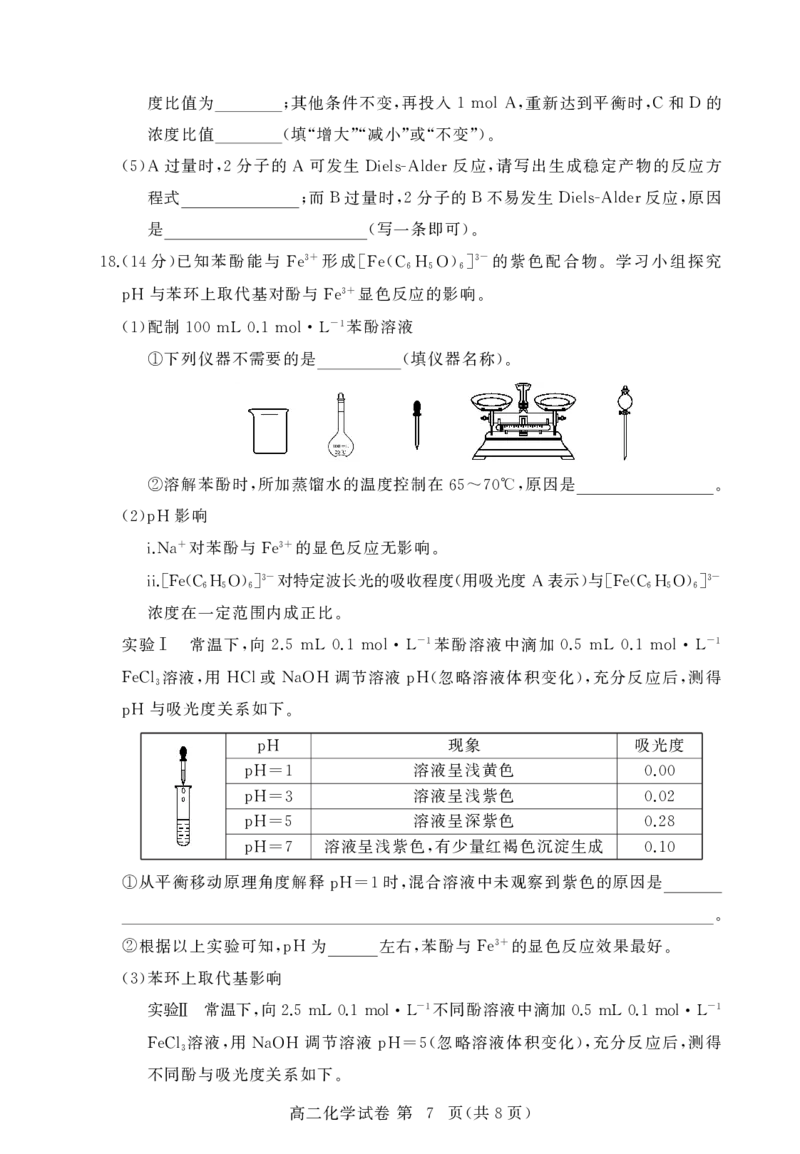
我国科学家设计了一种苄位 键电羧化反应 最大限度地提高了原子利用率
14. C—H , ,
其原理如图所示 下列说法正确的是
.
高二化学试卷 第 页 共 页
4 ( 8 )电解过程中 向左移动
+
A. H
Cl COOH
阴极总反应式为
- + -
B. +2e +CO2+H +Cl
ph R ph R
电解过程中 不断被消耗 需要及时补充
- -
C. Cl , Cl
理论上外电路每转移 电子 电解质溶液增重
D. 0.1mol , 4.4g
全苯环互锁结构 与 的发现和合成为人们研究超分子打开了一条新思路 物质
15. Ⅰ Ⅱ .
和 的转化 体现了互锁结构的一种应用 下列说法正确的是
Ⅲ Ⅳ , .
与 的原子构建和键连方式完全一致 因此它们是同一个分子的不同构象
A.Ⅰ Ⅱ ,
所示的两个环之间并没有共价键相连 因此将两个环分开不需要断开化学键
B.Ⅱ ,
利用 与 的转化 可分离提纯
C. Ⅲ Ⅳ , Cu(Ⅰ)
与 的配位能力 的 原子 的 原子
-
D. Cu(Ⅰ) :Ⅳ N >CN >Ⅳ O
二、非选择题:本题共 个小题,共 分.
4 55
分 钯 是在航空航天 汽车制造等领域应用广泛的稀有金属 从镍阳极泥
16.(14 ) (Pd) 、 .
中回收钯及其他贵金属的工艺流程如下
:
已知 镍阳极泥含有大量 和少量 等 氧化酸浸 中
:① Cu、Ni、Fe、Pb Pd、Pt、Au .②“ ”
浸出液的主要成分为 其中 是强酸 金属提
HAuCl4、H2PtCl6、H2PdCl4, HAuCl4 .③
炼过程中伴随有大量气泡 会形成类似海绵的孔隙结构
, .
高二化学试卷 第 页 共 页
5 ( 8 )在元素周期表中的位置是 基态 的价电子排布式为
(1)Ni , Pb .
酸浸 的目的是
(2)“ ” .
写出 反萃取 时生成海绵金的离子方程式
(3) “ ” .
已知 中所有原子共平面 则键角 填 或
2- 2-
(4) C2O4 , :C2O4 CO2( “>”“<”
“=”).
在一定条件下可形成多种铂钯合金 其中两种立方晶胞结构如下图所示
(5)Pt、Pd , .
晶胞 和 中 的配位数之比为
① Ⅰ Ⅱ Pd ;
晶胞 和 的密度之比为
② Ⅰ Ⅱ ;
晶胞 中 点的原子分数坐标为
③ Ⅱ ,A .
分 反应是构建环状碳骨架的重要反应
17.(14 )DielsGAlder .
已知 异戊二烯与丙烯在 作催化剂时 主要发生以下两个反应
: AlCl3 , :
反应
Ⅰ (aq)+
高二化学试卷 第 页 共 页
6 ( 8 )
(aq) →
H -1
(aq) Δ 1=-105kJmol
A B C
反应
Ⅱ (aq)+
(aq) →
H -1
(aq) Δ 2=-100kJmol
A B D
计算
(1)
(aq) →
的 H -1
(aq) Δ = kJmol .
下列能提高 的平衡转化率的措施是 填序号
(2) A ( ).
升高温度 降低温度 增大压强 使用更高效的催化剂
a. b. c. d.
与酸性 溶液反应 其有机产物的结构简式为
(3)B KMnO4 , .
反应 和反应 的 与温度 的关系曲线如图
(4) Ⅰ Ⅱ lgK (T) .
保持 不变 与 的投料浓度均为 达到平衡时 和 的浓
-1
50℃ ,A B 1molL , ,C D度比值为 其他条件不变 再投入 重新达到平衡时 和 的
; , 1molA, ,C D
浓度比值 填 增大 减小 或 不变
( “ ”“ ” “ ”).
过量时 分子的 可发生 反应 请写出生成稳定产物的反应方
(5)A ,2 A DielsGAlder ,
程式 而 过量时 分子的 不易发生 反应 原因
; B ,2 B DielsGAlder ,
是 写一条即可
( ).
分 已知苯酚能与 形成 的紫色配合物 学习小组探究
3+ 3-
18.(14 ) Fe [Fe(C6H5O)6] .
与苯环上取代基对酚与 显色反应的影响
3+
pH Fe .
配制 苯酚溶液
-1
(1) 100mL0.1molL
下列仪器不需要的是 填仪器名称
① ( ).
溶解苯酚时 所加蒸馏水的温度控制在 原因是
② , 65~70℃, .
影响
(2)pH
对苯酚与 的显色反应无影响
+ 3+
i.Na Fe .
对特定波长光的吸收程度 用吸光度 表示 与
3- 3-
ii.[Fe(C6H5O)6] ( A ) [Fe(C6H5O)6]
浓度在一定范围内成正比
.
实验 常温下 向 苯酚溶液中滴加
-1 -1
Ⅰ , 2.5mL0.1molL 0.5mL0.1molL
溶液 用 或 调节溶液 忽略溶液体积变化 充分反应后 测得
FeCl3 , HCl NaOH pH( ), ,
与吸光度关系如下
pH .
现象 吸光度
pH
溶液呈浅黄色
pH=1 0.00
溶液呈浅紫色
pH=3 0.02
溶液呈深紫色
pH=5 0.28
溶液呈浅紫色 有少量红褐色沉淀生成
pH=7 , 0.10
从平衡移动原理角度解释 时 混合溶液中未观察到紫色的原因是
① pH=1 ,
.
根据以上实验可知 为 左右 苯酚与 的显色反应效果最好
3+
② ,pH , Fe .
苯环上取代基影响
(3)
实验 常温下 向 不同酚溶液中滴加
-1 -1
Ⅱ , 2.5mL0.1molL 0.5mL0.1molL
溶液 用 调节溶液 忽略溶液体积变化 充分反应后 测得
FeCl3 , NaOH pH=5( ), ,
不同酚与吸光度关系如下
.
高二化学试卷 第 页 共 页
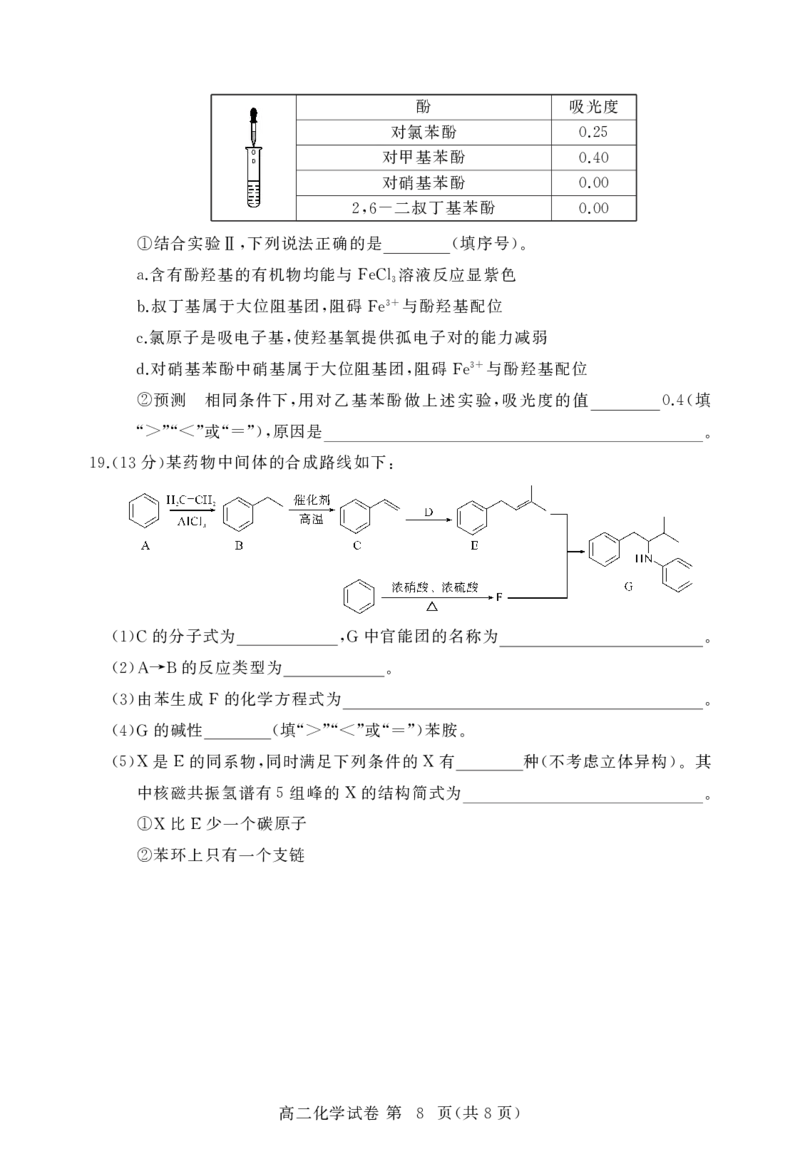
7 ( 8 )酚 吸光度
对氯苯酚
0.25
对甲基苯酚
0.40
对硝基苯酚
0.00
二叔丁基苯酚
2,6- 0.00
结合实验 下列说法正确的是 填序号
① Ⅱ, ( ).
含有酚羟基的有机物均能与 溶液反应显紫色
a. FeCl3
叔丁基属于大位阻基团 阻碍 与酚羟基配位
3+
b. , Fe
氯原子是吸电子基 使羟基氧提供孤电子对的能力减弱
c. ,
对硝基苯酚中硝基属于大位阻基团 阻碍 与酚羟基配位
3+
d. , Fe
预测 相同条件下 用对乙基苯酚做上述实验 吸光度的值 填
② , , 0.4(
或 原因是
“>”“<” “=”), .
分 某药物中间体的合成路线如下
19.(13 ) :
的分子式为 中官能团的名称为
(1)C ,G .
的反应类型为
(2)A→B .
由苯生成 的化学方程式为
(3) F .
的碱性 填 或 苯胺
(4)G ( “>”“<” “=”) .
是 的同系物 同时满足下列条件的 有 种 不考虑立体异构 其
(5)X E , X ( ).
中核磁共振氢谱有 组峰的 的结构简式为
5 X .
比 少一个碳原子
①X E
苯环上只有一个支链
②
高二化学试卷 第 页 共 页
8 ( 8 )