文档内容
2 0 2 5 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 张世雄
粉笔教师教育 粉笔教师目
录
content
1 原子结构与性质
2 分子结构与性质
3 晶体结构与性质原子结构与性质P89
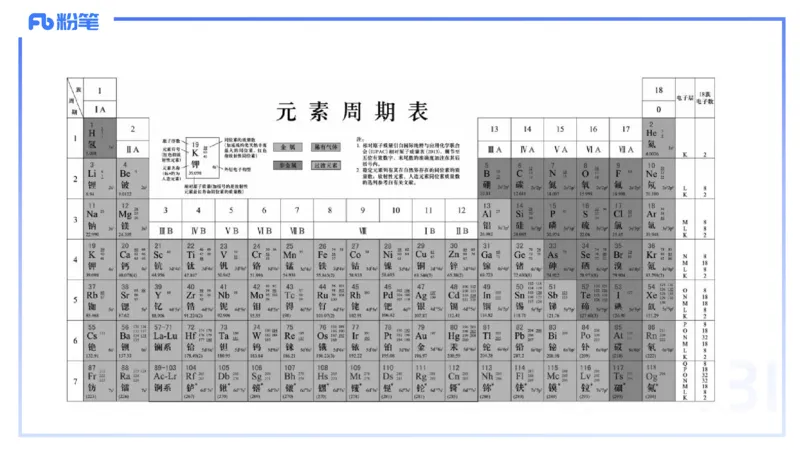
二、元素周期表与元素周期律
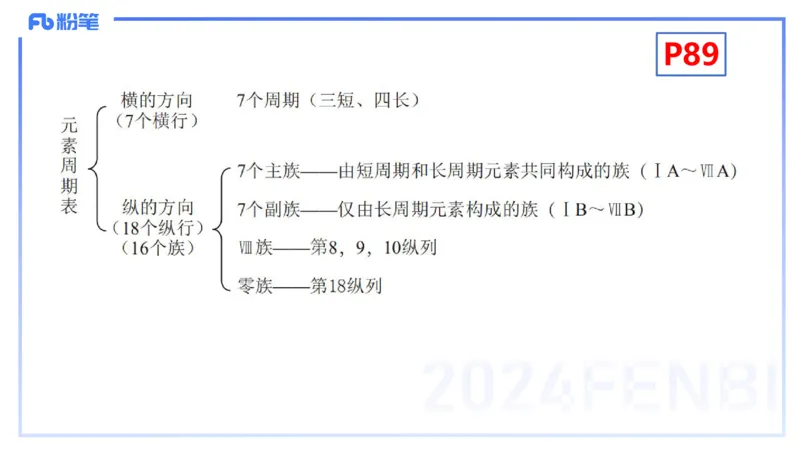
(一)元素周期表的结构
电子层数相同的元素按原子序数递增的顺序从左到右排成横行,
最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行而
得到的表叫元素周期表。
元素周期表是元素周期律的具体表现形式,反映了元素之间相互
联系的规律。P89
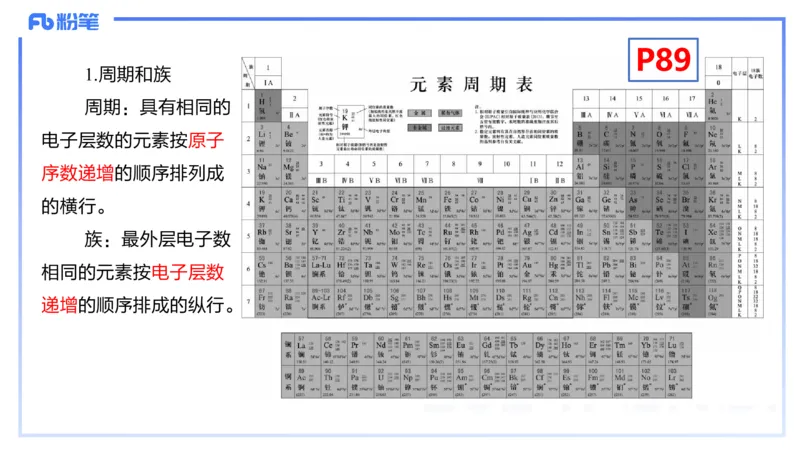
1.周期和族
周期:具有相同的
电子层数的元素按原子
序数递增的顺序排列成
的横行。
族:最外层电子数
相同的元素按电子层数
递增的顺序排成的纵行。P89P90
2.元素、核素、同位素
元素:具有相同核电荷数(质子数)的一类原子的总称。 例如,12C、
13C、14C同属于碳元素。
核素:具有一定数目质子和一定数目中子的一种原子。每一种原子为一
种核素,如12C、13C、14C各为一种核素。
同位素:具有相同质子数、不同中子数的同一元素的不同核素互为同位
素。同位,指核素的质子数相同,在元素周期表中占有相同的位置。
例如:12C、13C、14C,
16O、17O、18O,
35Cl、37Cl,
1H、2H、3H 分别互为同位素。P90
同位素的化学性质相似,物理性质不同。
同位素之间的转化不属于化学变化。原子的裂变、聚变中虽有新
物质形成,但它们不属于中学化学变化研究的范畴。P90
3.价电子层
周期表上元素的“外围电子排布”简称“价电子层”,这是由于这些
能级上的电子数可在化学反应中发生变化。
价电子层中的电子称为价电子。P90
(二)元素周期律
元素的性质随原子序数(核电荷数)的递增而呈周期性的递变,
称为元素周期律。
元素周期律是元素原子的核外电子排布呈周期性变化的必然结果。P90
1.粒子半径大小的比较
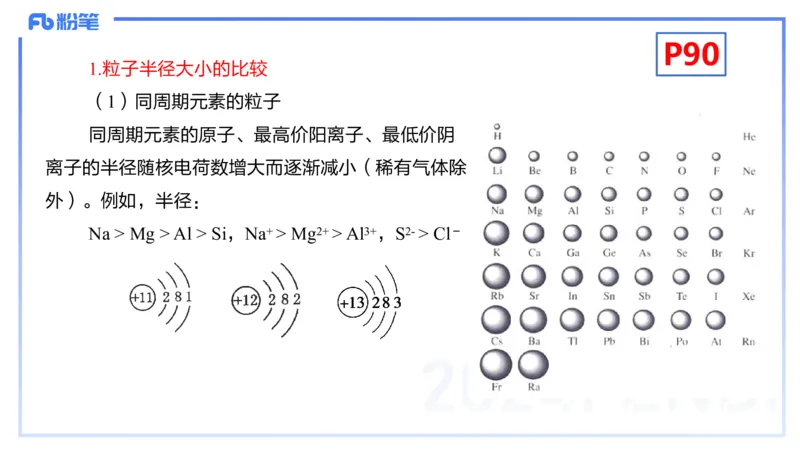
(1)同周期元素的粒子
同周期元素的原子、最高价阳离子、最低价阴
离子的半径随核电荷数增大而逐渐减小(稀有气体除
外)。例如,半径:
Na > Mg > Al > Si,Na+ > Mg2+ > Al3+,S2- > Cl-P90
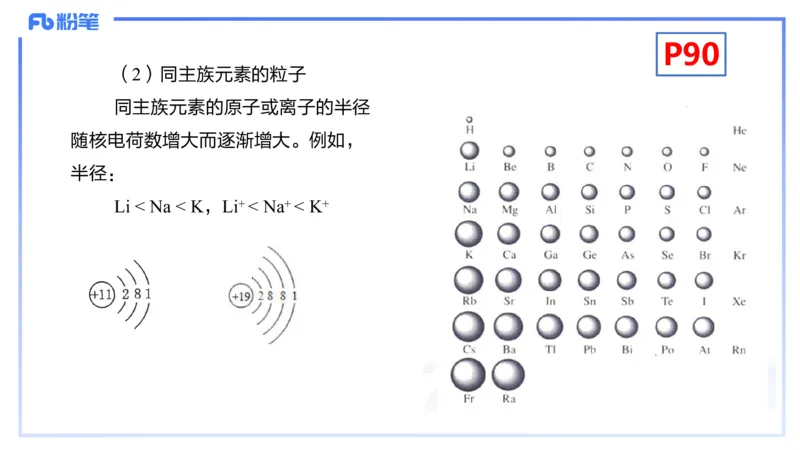
(2)同主族元素的粒子
同主族元素的原子或离子的半径
随核电荷数增大而逐渐增大。例如,
半径:
Li < Na < K,Li+ < Na+ < K+P91
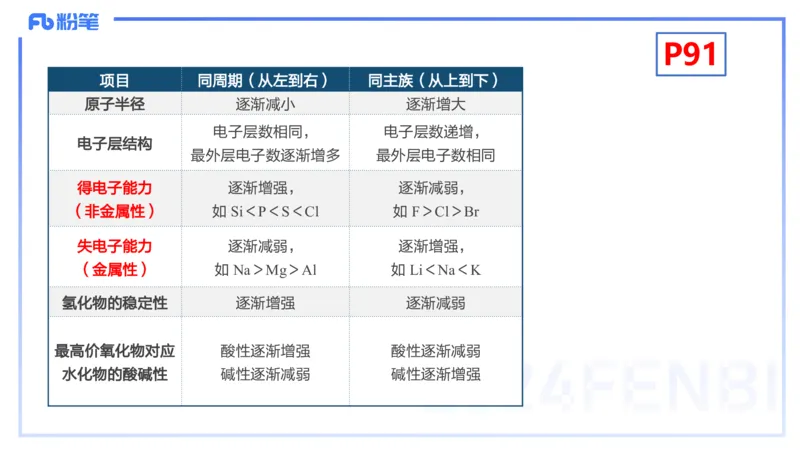
2.金属性与非金属性P91
项目 同周期(从左到右) 同主族(从上到下)
原子半径 逐渐减小 逐渐增大
电子层数相同, 电子层数递增,
电子层结构
最外层电子数逐渐增多 最外层电子数相同
得电子能力 逐渐增强, 逐渐减弱,
(非金属性) 如 Si<P<S<Cl 如 F>Cl>Br
失电子能力 逐渐减弱, 逐渐增强,
(金属性) 如 Na>Mg>Al 如 Li<Na<K
氢化物的稳定性 逐渐增强 逐渐减弱
最高价氧化物对应 酸性逐渐增强 酸性逐渐减弱
水化物的酸碱性 碱性逐渐减弱 碱性逐渐增强P91
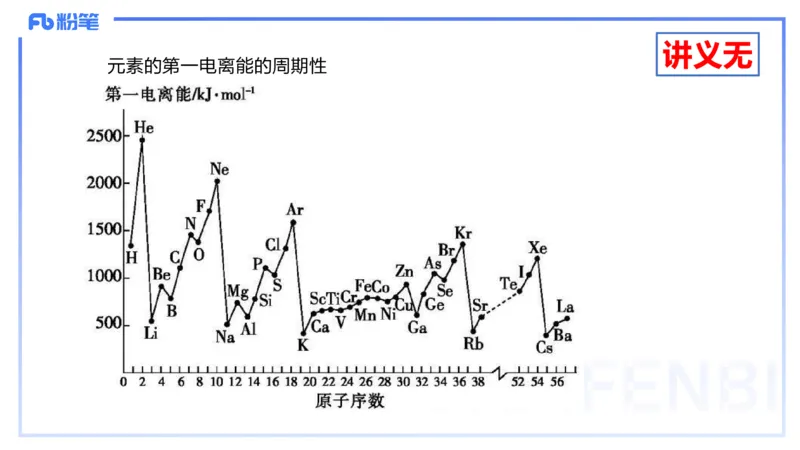
3.第一电离能
(1)概念
气态电中性基态原子失去一个电子转化为气态基态正离子所需要
的最低能量叫作第一电离能。
(2)意义
可以衡量元素的原子失去一个电子的难易程度。一般来说,第一
电离能数值越小,原子越容易失去一个电子;第一电离能数值越大,
原子越难失去一个电子。讲义无
元素的第一电离能的周期性P91
(3)第一电离能的变化规律
第一电离能的大小与原子的核电荷数、半径及电子构型等因素有关。
对于主族元素:
①同一周期原子的电子层数相同,从左至右,随着原子核电荷数增加,原
子核对外层电子的吸引力也增强,原子半径减小,失电子能力减弱,第一电离
能随之增大,元素的金属性逐渐减弱,非金属性逐渐增强。
反常现象:根据洪特规则,当外围电子在能量相等的轨道上形成全空(p0,
d0,f0)、半满(p3,d5,f7)和全满(p6,d10,f14)结构时,原子的能量较低,
元素的第一电离能较大。
同一周期元素的第一电离能:ⅡA>ⅢA,ⅤA>ⅥA 。P92
②同一主族的原子最外层电子数相同,从上到下,电子层数增加,
原子核对外层电子吸引力减小,原子半径随之增大, 第一电离能逐
渐减小,元素的金属性逐渐增强,非金属性逐渐减弱。P92
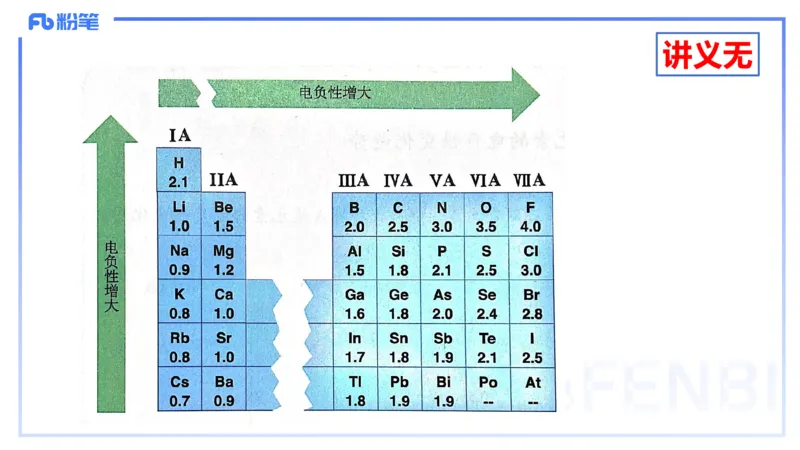
4.电负性
电负性是不同元素的原子对键合电子吸收力的大小的标度。
电负性数值越大,表明原子对键合电子的吸引力越大;电负性数
值越小,表明原子对键合电子的吸引力越小。
元素的电负性较全面地反映了元素的金属性和非金属性的强弱。
主族元素的电负性具有较明显的周期性变化规律,同一周期从左到右,
元素的电负性逐渐增大,同一主族从上到下,元素的电负性逐渐减小。讲义无P92
1. W、X、Y 和 Z 为原子序数依次增大的四种短周期元素。W 与 X 可
生成一种红棕色有刺激性气味的气体,Y 的周期数是族序数的 3 倍,Z 原
子最外层的电子数与 W 的电子总数相同。
下列叙述正确的是( )。
A. W 的氧化物对应的水化物均为强酸
B. 四种元素的简单离子具有相同的电子层结构
C. Y 与其他三种元素分别形成的化合物中只含有离子键
D. X 与其他三种元素均可形成两种或两种以上的二元化合物P92
2. 主族元素 W、X、Y、Z 的原子序数依次增加,且均不大于 20。W、
X、Z 的最外层电子数之和为 10,W 与 Y 同族,W 与 Z 形成的化合物可
与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是( )。
A. 常温常压下,X 的单质为气态
B. Z 的氢化物为离子化合物
C. Y 和 Z 形成的化合物的水溶液呈碱性
D. W 与 Y 具有相同的最高化合价P92
3. 已知 X、Y、Z、W、M 均为短周期元素,且 X、Y、Z、W、M 的
原子半径依次增大,25°C 时其最高价氧化物对应的水化物浓度均为
0.01mol·L–1,溶液的 pH 如下图所示,下列说法不正确的是( )。
A. X、M 简单离子半径大小顺序:X > M
B. X、Y、Z、W、M 五种元素中只有一种是金属元素
C. Z 的最高价氧化物的化学式为 ZO
3
D. X、Z 的最简单气态氧化物反应有白烟形成分子结构与性质P93
一、化学键
1.概念
通常除稀有气体外,大多数物质是依靠原子(或离子)间的某种
强的作用力而将多个原子(或离子)结合成分子或晶体的,分子或晶
体中原子(或离子)之间的这种强作用力称为化学键。P93
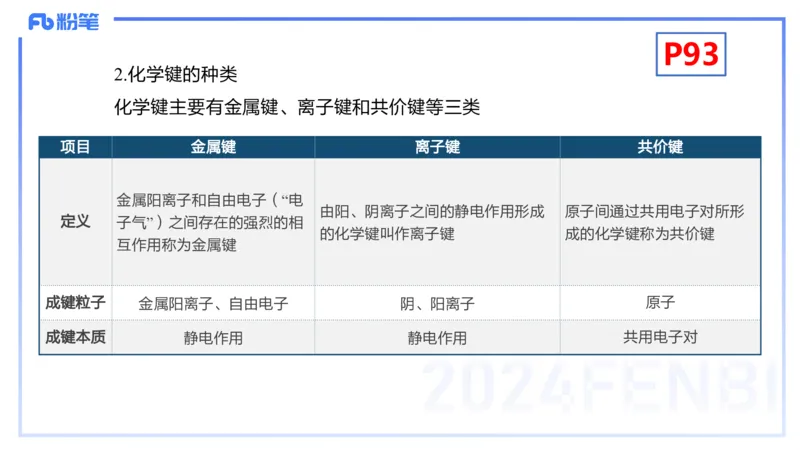
2.化学键的种类
化学键主要有金属键、离子键和共价键等三类
项目 金属键 离子键 共价键
金属阳离子和自由电子(“电
由阳、阴离子之间的静电作用形成 原子间通过共用电子对所形
定义 子气”)之间存在的强烈的相
的化学键叫作离子键 成的化学键称为共价键
互作用称为金属键
成键粒子 金属阳离子、自由电子 阴、阳离子 原子
成键本质 静电作用 静电作用 共用电子对P94
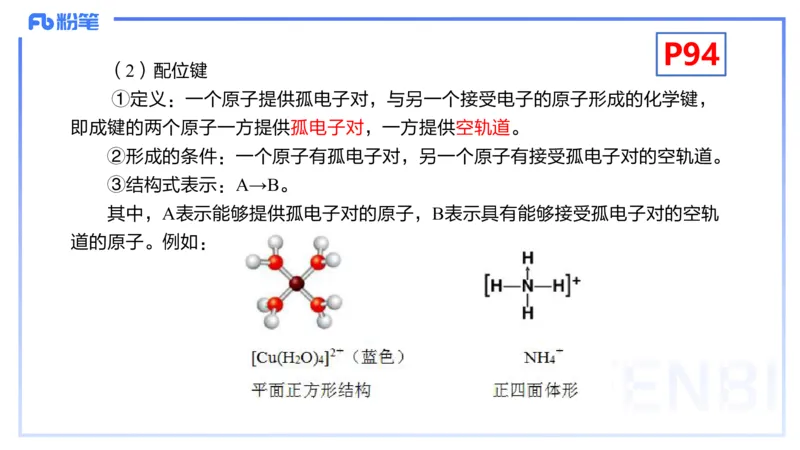
(2)配位键
①定义:一个原子提供孤电子对,与另一个接受电子的原子形成的化学键,
即成键的两个原子一方提供孤电子对,一方提供空轨道。
②形成的条件:一个原子有孤电子对,另一个原子有接受孤电子对的空轨道。
③结构式表示:A→B。
其中,A表示能够提供孤电子对的原子,B表示具有能够接受孤电子对的空轨
道的原子。例如:P94
3.离子键和共价键的比较
共价键
项目 离子键
非极性键 极性键
使阴、阳离子结合成化合
概念 原子之间通过共用电子对所形成的相互作用(电子云重叠)
物的静电作用
共用电子对偏向吸引电子能
特点 阴、阳离子间的相互作用 共用电子对不偏移
力强的一方
成键粒子 阴、阳离子 原子
成键条件 活泼金属和活泼非金属 同种元素的原子 不同种元素的原子
非金属单质(稀有气体除外)、 共价化合物、某些离子化合
存在 离子化合物
某些化合物 物P108
1. 下列各组化合物中,所含化学键类型完全相同的是( )。
A. CO 和 CaO
2
B. CaCl 和 Na S
2 2
C. NaCl 和 NH Cl
4
D. HCl 和 NaOHP94
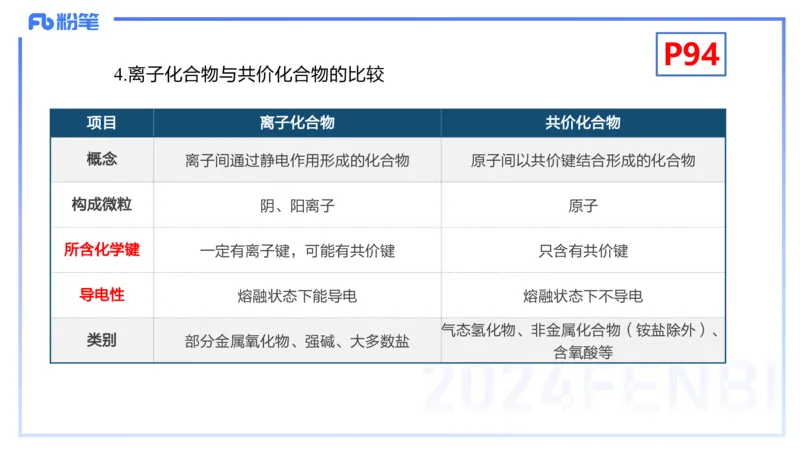
4.离子化合物与共价化合物的比较
项目 离子化合物 共价化合物
概念 离子间通过静电作用形成的化合物 原子间以共价键结合形成的化合物
构成微粒 阴、阳离子 原子
所含化学键 一定有离子键,可能有共价键 只含有共价键
导电性 熔融状态下能导电 熔融状态下不导电
气态氢化物、非金属化合物(铵盐除外)、
类别 部分金属氧化物、强碱、大多数盐
含氧酸等P95
【粉笔提示】
1.离子化合物中可能含有极性和非极性共价键,如 NaOH、Na O 。
2 2
2.离子化合物中不一定含有金属元素,如铵盐都为离子化合物。
3.只含有共价键的物质不一定是共价化合物,还可能是单质。
4.稀有气体单质中没有化学键。P95
二、分子的性质
(一)键的极性与分子的极性
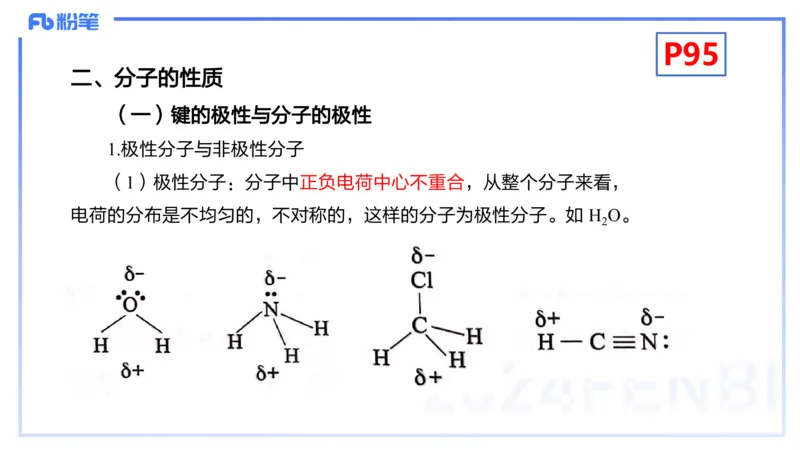
1.极性分子与非极性分子
(1)极性分子:分子中正负电荷中心不重合,从整个分子来看,
电荷的分布是不均匀的,不对称的,这样的分子为极性分子。如 H O。
2P95
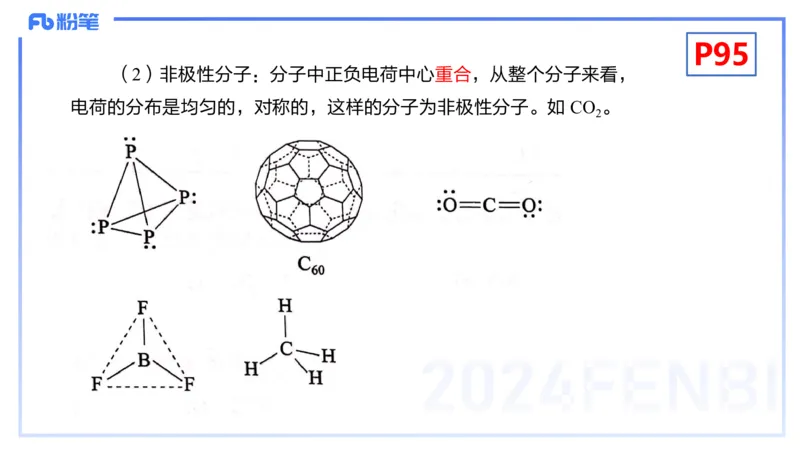
(2)非极性分子:分子中正负电荷中心重合,从整个分子来看,
电荷的分布是均匀的,对称的,这样的分子为非极性分子。如 CO 。
2P109
5. 下列分子中偶极矩为零的是( )。
A. NaCl B. BF
3
C. NH D. H O
3 2P95
2.键的极性与分子的极性
项目 键的极性 分子的极性
分类 极性键和非极性键 极性分子和非极性分子
是否由同种元素的原子形成
决定因素 正负电荷中心是否重合
(共用电子对是否偏移)
(1)以非极性键结合的双原子分子必为非极性分子;
联系 (2)以极性键结合的双原子分子一定是极性分子;
(3)以极性键结合的多原子分子,是否为极性分子,由该分子的空间构型决定
说明 键有极性,分子不一定有极性P96
(二)范德华力及其对物质性质的影响
1.定义
物质的分子间存在的将分子聚集在一起的作用力称为分子间作用
力,也称范德华力。
范德华力很弱,约比化学键的键能小 1~2 个数量级。
2.影响
范德华力影响物质的熔点、沸点、溶解度等物理性质。
(1)相对分子质量越大,范德华力越大。
例如:卤素单质从 F 到 I ,熔、沸点越来越高。
2 2
(2)相对分子质量相同时,分子的极性越大,范德华力越大。P96
(三)氢键及其对物质性质的影响
1.定义
氢原子与电负性大的 X 原子以共价键结合,若与电负性大、半径
小的原子 Y(O、N、F等)接近,在 X 与 Y 之间以 H 为媒介,生成
X-H···Y 形式的一种特殊的分子间或分子内的相互作用,称为氢键。
形成氢键的分子可以是同一种分子,如水分子之间的氢键;也可
以是不同种分子,如一水合氨分子(NH ·H O)之间的氢键。
3 2
氢键不属于化学键,强度介于化学键与范德华力之间。
作用力强弱比较:化学键>氢键>分子间作用力P96
2.影响
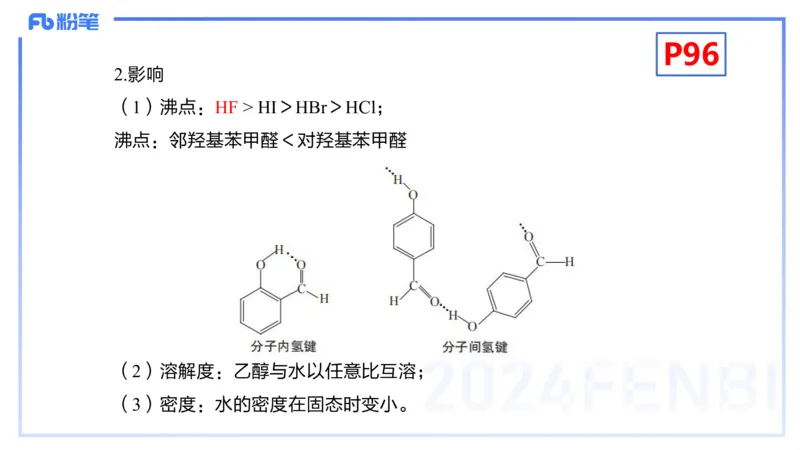
(1)沸点:HF > HI>HBr>HCl;
沸点:邻羟基苯甲醛<对羟基苯甲醛
(2)溶解度:乙醇与水以任意比互溶;
(3)密度:水的密度在固态时变小。P97
3.氢键和范德华力对比
项目 氢键 范德华力
某些物质的分子间(或分子内) 物质的分子间存在的
定义
氢核与非金属原子的静电吸引作用 将分子聚集在一起的作用力
范围 分子间或分子内 分子间
作用力强弱 化学键>氢键>分子间作用力
主要影响物质的物理性质 主要影响物质的物理性质
性质、影响
(如熔点、沸点、密度等) (如熔点、沸点等)P109
4. 可燃冰是一种新型能源,下列表述错误的是( )。
A. 可燃冰是一种化石能源
B. 可燃冰是一种高能清洁能源
C. 可燃冰是甲烷分子与水分子以氢键结合成的晶体
D. 如果开采不当可导致气体泄漏,会引发环境问题P97
(四)溶解性:相似相溶
相似相溶包括两种情况,一种是物质极性的相似,一种是物质结构的相似。
1.分子极性对溶解性的影响
极性溶质一般易溶解于极性溶剂中;非极性溶质一般易溶于非极性溶剂中。
溶质分子与溶剂分子间的范德华力大,则溶质分子的溶解度大。
例如,HCl 易溶于水,而 CH 不易溶于水;Br 和 I 易溶于苯,而水难溶于苯。
4 2 2P98
2.氢键对溶解性的影响
如果存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越
好,反之,不能形成氢键的溶质在有氢键的水中的溶解度就比较小。P98
此外,“相似相溶”还适用于分子结构的相似性。
例如,乙醇的化学式为 CH CH OH,其中的 —OH 与水分子的
3 2
OH- 相近,因而乙醇能与水互溶;
而戊醇 (CH CH CH CH CH OH) 中的烃基较大,其中的 —
3 2 2 2 2
OH 与水分子的 OH- 相似因素小得多,因而它在水中的溶解度就小得
多。P98
(五)手性和手性分子
1.手性碳原子
连有四个不同原子或基团的碳原子称为手性碳原子,常用*C表示。
如 ,R 、R 、R 、R 是互不相同的原子或基团。
1 2 3 4P98
2.手性分子
具有完全相同的组成和原子排列、互为镜像而不能重叠的一对分
子互称手性异构体。有手性异构体的分子叫作手性分子。
互为镜像的两个分子
【粉笔提示】
判断一种有机物是否具有手性异构体,就看其含有的碳原子是否
连有四个不同的原子或基团。(分子中只有一个手性碳原子)P98
3.手性合成
手性异构体药物分子中,往往是一种有毒副作用,而另一种能治
病,没有毒副作用,因此生产手性药物必须把手性异构体分离开。
按照获得2001年诺贝尔化学奖的三位科学家的合成方法,可以只
得到一种手性分子,不得到或者基本不得到它的手性异构分子,这种
独特的合成方法就称为手性合成。手性催化剂只催化或者主要催化一
种手性分子的合成。P99
(六)无机含氧酸分子的酸性
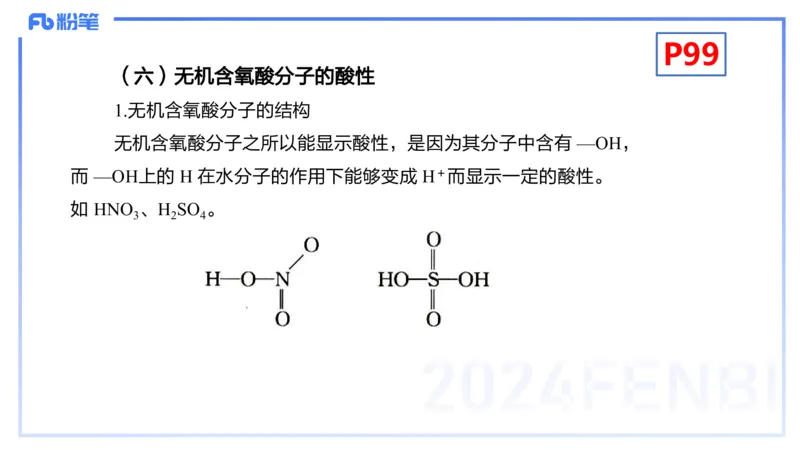
1.无机含氧酸分子的结构
无机含氧酸分子之所以能显示酸性,是因为其分子中含有 —OH,
而 —OH上的 H 在水分子的作用下能够变成 H+而显示一定的酸性。
如 HNO 、H SO 。
3 2 4P99
2.无机含氧酸分子酸性强弱的比较
(1)对于同一种元素的含氧酸,该元素的化合价越高,其含氧酸的酸性越强。
例如 Cl:HClO >HClO >HClO >HClO 。
4 3 2
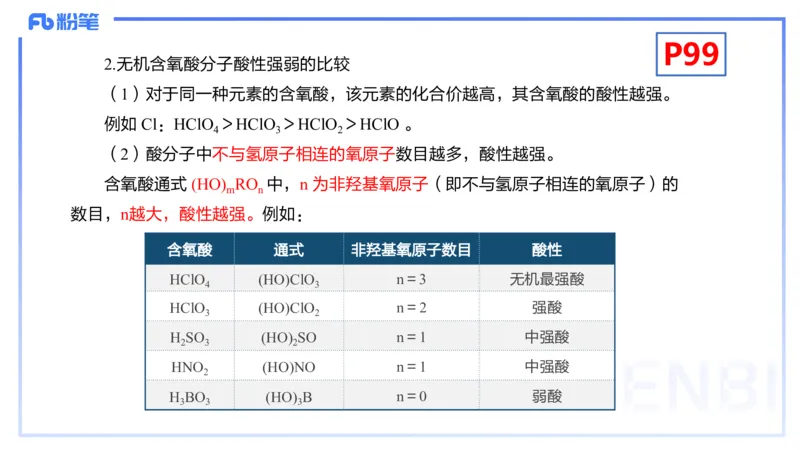
(2)酸分子中不与氢原子相连的氧原子数目越多,酸性越强。
含氧酸通式 (HO) RO 中,n 为非羟基氧原子(即不与氢原子相连的氧原子)的
m n
数目,n越大,酸性越强。例如:
含氧酸 通式 非羟基氧原子数目 酸性
HClO (HO)ClO n=3 无机最强酸
4 3
HClO (HO)ClO n=2 强酸
3 2
H SO (HO) SO n=1 中强酸
2 3 2
HNO (HO)NO n=1 中强酸
2
H BO (HO) B n=0 弱酸
3 3 3P99
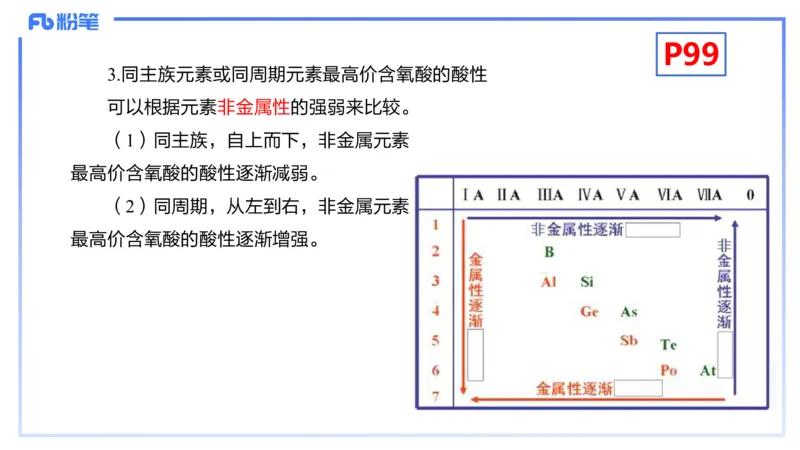
3.同主族元素或同周期元素最高价含氧酸的酸性
可以根据元素非金属性的强弱来比较。
(1)同主族,自上而下,非金属元素
最高价含氧酸的酸性逐渐减弱。
(2)同周期,从左到右,非金属元素
最高价含氧酸的酸性逐渐增强。粉笔教师教育 粉笔教师