文档内容
长沙市 2024 年新高考适应性考试
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号
涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写
在答题卡上,写在本试卷上无效。
3.考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:H~1;O~16;F~19;Na~23;Ni~59;Bi~209
一、选择题:本题共 14 小题,每小题 3 分,共42 分。在每小题给出的四个选项中,只
有一项是符合题目要求。
1.化学与生活、生产及科技密切相关。下列说法错误的是( )
A.2023年杭州亚运会使用聚乳酸塑料代替聚乙烯塑料,可有效减少白色污染
B.湖南岳州窑青瓷以黏土为主要原料,在烧制过程中发生了复杂的化学变化
C.长沙马王堆出土的“素纱襌衣”由蚕丝织成,其主要成分是蛋白质
D.纳米铝粉主要通过物理吸附作用除去污水中的Cu2+、Ag+、Hg2+
2.化学语言是表达化学思想不可缺少的重要工具。下列说法正确的是( )
A B C D
HCl在水中电离 激发态硼原子 盐酸与碳酸氢钠 苯分子中大π键
的示意图 的电子排布图 反应的焓变图 的示意图
3.下列有关化学实验的必备知识,说法正确的是( )
A.中学实验室中未用完的钠、钾、白磷等不宜放回原试剂瓶
B.蒸馏操作中,使用球形冷凝管可以有效提高馏分的冷凝效果
C.碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%的H BO
3 3
D.滴定实验中,可用量筒量取25.00mLNa CO 标准溶液于锥形瓶中
2 3
化学试题第1页(共8页)
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}4.下列有关物质的组成、结构、性质与转化,说法错误的是( )
A.核苷酸可以看作磷酸、戊糖和碱基通过一定方式结合而成的生物大分子
B.烷基是推电子基团,烷基使羧基中羟基的极性减小,羧酸的酸性减弱
C.抗坏血酸(即维生素C)能被氧化为脱氢抗坏血酸而发挥抗氧化作用
D.工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅
5.短周期主族元素 X、Y、Z、W、R 的原子序数依次增大,X 的价层电子数为 5,X
和Y的最简单气态氢化物的质子总数相等,Z的核外没有未成对电子,W与Y属于
同一主族。下列说法错误的是( )
A.离子键的百分数:ZY>ZW
B.含W、R元素的化合物常用作生产农药
C.碱性溶液中:WY2-、XY-、RY-能大量共存
3 3
D.共价化合物RXY的电子式为
6.下列离子方程式书写正确的是( )
A.氢碘酸溶解氢氧化铁:Fe(OH)+3H+===Fe3++3H O
3 2
B.CuSO 溶液中滴入足量氨水:Cu2++2NH H O=Cu(OH)↓+2NH
4 3 2 2 4
C.苯酚钠溶液中通入少量CO :C H O-+H O+CO =C H OH+HCO-
2 6 5 2 2 6 5 3
D.银作电极,电解硝酸银溶液:4Ag++2H O= 电 = 解 =4Ag+4H++O↑
2 2
7.我国古代中药学著作《新修本草》中对“青矾”的描
述为:本来绿色,新出窟未见风者,正如琉璃……,
烧之赤色……。“青矾”的主要成分为FeSO 7H O(结
4 2
构示意图如右图)。下列说法错误的是( )
A.基态气态Fe2+再失去一个电子比基态气态Mn2+
更难
B.FeSO 7H O中存在离子键、极性键、配位键
4 2
C.H O中H-O-H键角小于SO2中O-S-O键角
2 4
D.FeSO 7H O加热脱水时,需克服氢键的作用
4 2
8.下列实验方案能达到实验目的的是( )
甲 乙 丙 丁
化学试题第2页(共8页)
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}A.方案甲可制取无水MgCl
2
B.方案乙可除去CCl 溶液中部分的I
4 2
C.方案丙可验证非金属性:Cl>C>Si
D.方案丁可判断溶度积:K (ZnS)<K (CuS)
sp sp
9.《自然·天文学》发表的一篇研究论文称在金星大气中探测到一个只属于磷化氢(PH )
3
的特征光谱。磷化氢是一种无色、剧毒、易燃的强还原性气体,制备的流程如图所示:
下列说法正确的是( )
A.通过晶体的X射线衍射实验获得P 分子中∠P-P-P键角为10928
4
B.1molP 与足量浓NaOH溶液反应,氧化剂和还原剂的物质的量之比为1:3
4
C.次磷酸的分子式为H PO ,属于三元弱酸
3 2
D.含Ca P 等杂质的电石制得的乙炔中混有PH ,可用高锰酸钾除去乙炔中的PH
3 2 3 3
10.氧化铋(Bi O )作为镍/铋电池的负极材料,因其理论容
2 3
量高、易制备而受到广泛关注。右图为该电池的示意图,
下列说法正确的是( )
A.放电时,OH-从电极a移向电极b
B.充电时,电子从电源负极→电极 a→电极 b→电源
正极
C.放电时,总反应为Bi O +3H O+6NiO===6NiOOH+2Bi
2 3 2
D.充电时,电路转移9.031024个电子,阳极质量增加255g
11.聚席夫碱(结构片段如下图所示)是一种优良的功能高分子材料。碘掺杂的聚席夫
碱表现出优异的电化学性能,在储能方面有良好的应用前景。下列有关说法错误的
是( )
已知:R -NH +R -CHO 一定条件 R N=CH-R +H O
1 2 2 1 2 2
A.该聚合物的链节为
B.制备该聚合物的其中一种单体能与盐酸发生反应
C.核磁共振氢谱能区分制备该聚合物的二种单体
D.该聚合物的共轭大π键体系为电荷传递提供了通路
化学试题第3页(共8页)
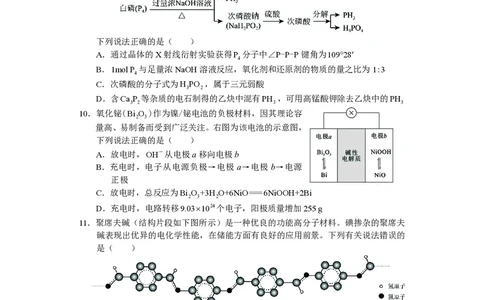
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}12.苯基甲基乙炔(Ph-CC-CH )可用作医药中间体,制备帕瑞昔布钠。一定条件
3
下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
已知:ΔH <ΔH<0,下列说法正确的是( )
2 1
A.Ph-CC-CH 中最多4个碳原子共线
3
B.ΔH +ΔH +ΔH =0
1 2 3
C.产物Ⅱ比产物I稳定,两者互为立体异构体
D.反应I的活化能大于反应Ⅱ
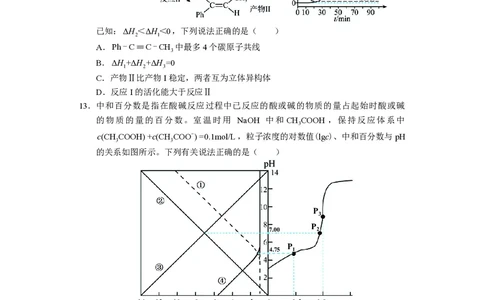
13.中和百分数是指在酸碱反应过程中已反应的酸或碱的物质的量占起始时酸或碱
的物质的量的百分数。室温时用 NaOH 中和 CH COOH ,保持反应体系中
3
c(CH COOH) +c(CH COO-) =0.1mol/L,粒子浓度的对数值(lgc)、中和百分数与pH
3 3
的关系如图所示。下列有关说法正确的是( )
P
3
P
7.00 2
P
4.75 1
A.曲线②表示OH-浓度的对数值随pH的变化关系
B.室温时,CH COO-的水解平衡常数的数量级为109
3
C.水的电离程度:P>P>P
1 2 3
D.中和百分数从0.5到1.0的变化过程中:c(Na+) +c(H+) >c(OH-) +c(CH COOH)
3
化学试题第4页(共8页)
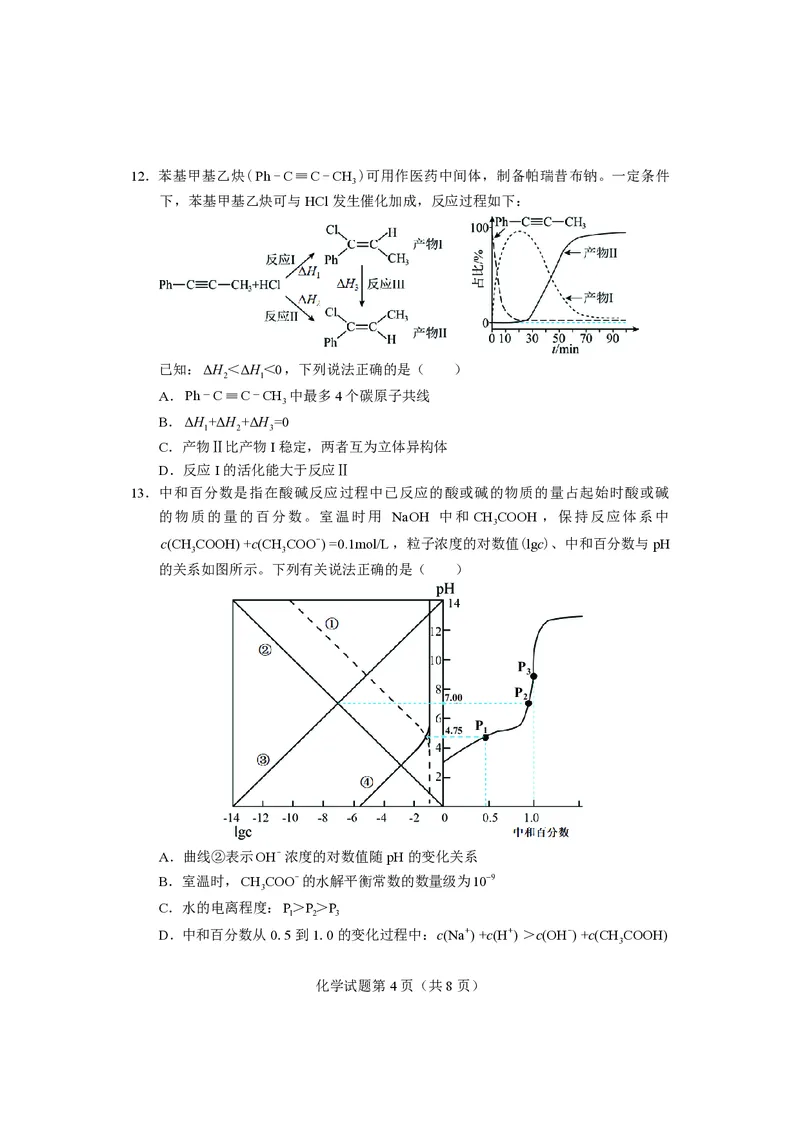
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}14.二氧化碳的捕集、转化有利于实现“碳中和”的战略目标。H 和CO 在一定的温度
2 2
下催化合成甲醇的反应机理如图所示。下列说法正确的是( )
A.催化反应过程(Ⅱ)中,碳元素的化合价未发生改变
B.整个催化反应过程中,有σ键和π键的断裂与形成
C.适当增大H 的浓度,有利于提高产物CO的选择性
2
D.适当减小反应体系的压强,有利于提高CO 的平衡转化率
2
二、非选择题:本题共4大题,共58分。
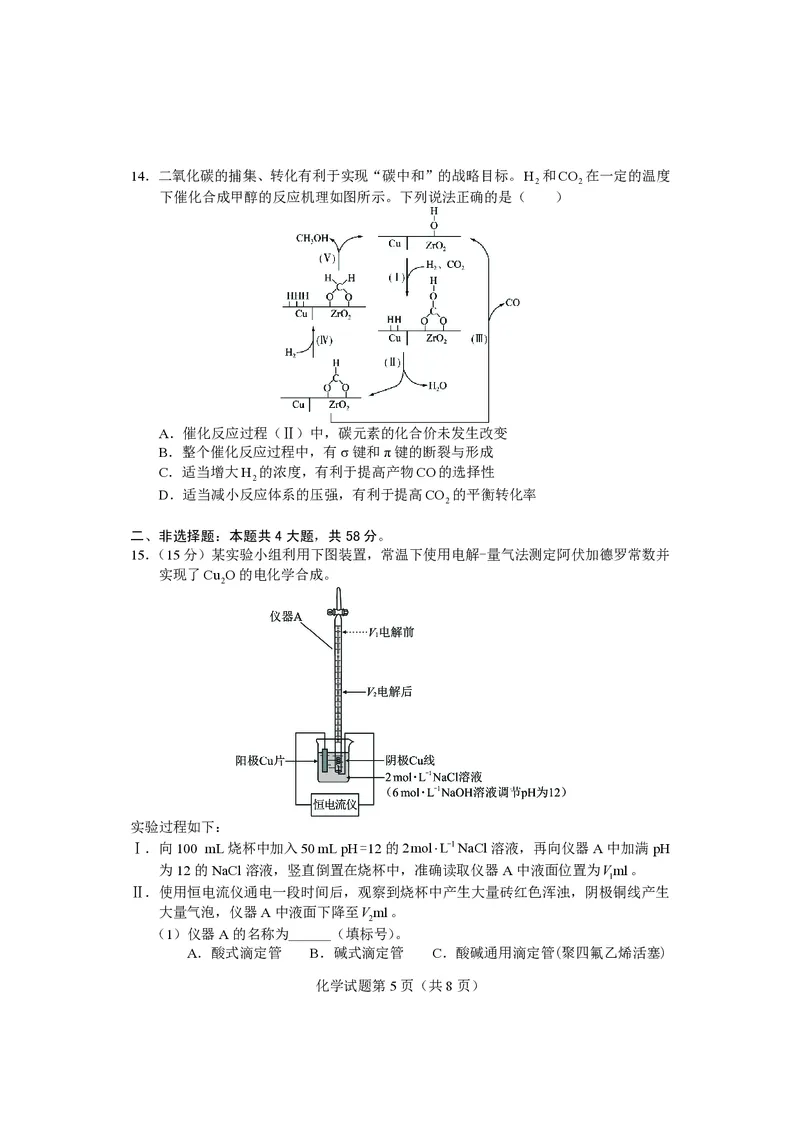
15.(15分)某实验小组利用下图装置,常温下使用电解-量气法测定阿伏加德罗常数并
实现了Cu O的电化学合成。
2
实验过程如下:
Ⅰ.向100 mL烧杯中加入50mLpH=12的2molL-1NaCl溶液,再向仪器A中加满pH
为12的NaCl溶液,竖直倒置在烧杯中,准确读取仪器A中液面位置为Vml。
1
Ⅱ.使用恒电流仪通电一段时间后,观察到烧杯中产生大量砖红色浑浊,阴极铜线产生
大量气泡,仪器A中液面下降至Vml。
2
(1)仪器A的名称为______(填标号)。
A.酸式滴定管 B.碱式滴定管 C.酸碱通用滴定管(聚四氟乙烯活塞)
化学试题第5页(共8页)
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}(2)阳极铜片发生电极反应:Cu-e-+Cl-=CuCl↓,经检测烧杯中产生大量砖红色的
Cu O。写出烧杯中产生Cu O的化学方程式______。
2 2 .....
(3)阴极铜线产生的大量气体B为______(填名称)。以I 安培的电流强度通电t 秒
..
后,仪器A中气体B的体积为V ml(已折算成标准状况下的体积)。已知:一
个电子的电量为e 库仑,则N =______mol-1。(用题中字母符号表示)
A
(4)将上述电化学合成的Cu O离心分离,并用适量纯水洗涤干净。简述如何检验
2
Cu O已经洗涤干净?______。
2
(5)将洗净后的Cu O均分成2等份,分别放入离心管甲、乙中,再分别加入15滴
2
6 mol/L盐酸、15滴 c mol/L H SO 溶液,静置。随着时间的推移,甲中先产
2 4
生白色沉淀CuCl,然后白色沉淀消失,溶液仍为无色,一段时间后得到黄色溶
液;乙中最终得到黑色沉淀(经检测为一种单质)和蓝色溶液。(已知:[CuCl ]-
2
为无色,[CuCl ]2-为黄色)
4
① c =______。
② 甲中溶液由无色最终变成黄色的原因是______。
③ 写出乙中发生反应的离子方程式______。
.....
实验结论:在相同酸性条件下,酸根阴离子不同,与Cu O反应的产物不同。
2
16.(14 分)锡(Sn)是“五金”之一,粗锡电解精炼后的锡阳极泥中金属元素二次回
收利用的部分工艺流程如下:
浓盐酸 空气 足量试剂M (NH)S 海绵锑粉 HO
42 2
滤液 滤液
锡阳极泥 浸出 沉锡 沉铜 沉锑
浸渣 (NH)SnCl Cu S和CuS Sb OCl
42 6 2 4 5 2
已知:① 锡阳极泥中主要成分的质量分数如下表所示
成分 SnO Cu Sb
质量分数 44.81% 12.38% 8.13%
② 常温下,锑(Sb)不溶于浓盐酸
③ 浸出液中主要存在的阳离子有Cu2+和Sb3+
(1)锡有多种同素异形体,其中灰锡的晶体结构与金刚石类似,灰锡属于______晶体。
(2)锡阳极泥在“浸出”前,进行球磨、筛分有利于______。
(3)“浸出”工序中,吹入适量空气的目的是______。
(4)“沉锡”时需在强酸性环境中进行,最适宜加入的试剂M为______。(填标号)
A.NH H O B.NH Cl C.NH HCO
3 2 4 4 3
化学试题第6页(共8页)
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}(5)“沉铜”工序中,加入海绵锑粉的作用是______。
(6)“沉锑”工序中,生成Sb O Cl 的离子方程式为
4 5 2 .....
______。
(7)回收得到的NH SnCl 和Sb O Cl 可合成纳米
4 2 6 4 5 2
锑掺杂二氧化锡(ATO)。二氧化锡的晶胞如图所示,其
中位于晶胞体心的原子是______(填元素符号);位于
晶胞顶角的原子的配位数是______。
17.(14分) 氟化学在现代无机化学中占有相当重要的地位。
(1)1670年,德国人斯瓦恩哈德无意中将萤石(CaF )与浓硫酸1∶1混合在一起,
2
产生了一种刺激性气体,这种气体能腐蚀玻璃。该气体腐蚀玻璃的化学反应方
.....
程式为______。
..
(2)单质氟的制备是化学史上一段悲壮的历史,直到 1886 年法国化学家莫瓦桑电
解熔融的氟化氢钾(KHF )才制得单质氟。电解过程中,两极均有气体产生,
2
阴极的电极反应式为______。
(3)氟单质的反应性非常强,可与稀有气体氙发生反应。已知:
标准平衡常数Kθ
反应方程式
523K 673K
Xe(g) +2F(g) XeF(g) 1.0108 2.0103
2 4
Xe(g) +3F(g) XeF(g) 1.0108 36.0
2 6
分压=总压×该组分物质的量分数,对于反应dD(g)eE(g) gG(g)hH(g)
g h
p p
G H
K
p
p
,其中 p100kPa,p 、p 、p 、p 为各组分的平衡分压)。
G H D E
d e
p p
D E
p
pθ
下图是以0.125 mol/L Xe和1.225 mol/L F 为起始量,得到的生成物在平衡体系
2
中的分压与反应温度的关系。
① 制备XeF 的适宜温度约为______K。
4
② 523K 时,以 Xe 和F 制取XeF 。反应达到平衡
2 6
时,欲使产物中 p(XeF) /p(XeF) >10, p(F) 至
6 4 2
少应保持在______kPa。
③ 反应 XeF(g) +F(g) XeF(g) 的 ΔH______0,
4 2 6
(填“大于”“等于”或“小于”),简述理由为
______。
化学试题第7页(共8页)
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}(4)法国科学家盖·吕萨克也曾试图制备氢氟酸。1809年,他把氟化钙与硼酸混和
加热,却意外地制成了一种所谓的“氟酸气”(BF )。已知:BF+2ClF→ [A]+ [C]-,
3 3
其中[A]+为含多个卤素原子的阳离子,[C]-为一个正四面体结构的阴离子,则
[A]+的VSEPR模型名称为______。
(5)已知:K (CaF)=1.510-10,若向 1 L 0.1 mol/L 的CaCl 溶液中加入 NaF 固
sp 2 2
体,充分反应后,测得溶液中Ca2+浓度为1.510-6mol/L,则加入的NaF固体的
质量为______g。(忽略加入固体后溶液体积的变化,计算结果保留2位小数)
..........
18.(15 分)2022 年度诺贝尔化学奖授与了点击反应。K.B.Sharpless 教授发现,在亚
铜的催化下,末端炔烃可以高区域选择性地与叠氮化合物发生高效的点击反应,这
一反应目前已经应用于生物化学等交叉领域。点击反应代表性示例如下:
(Ph-:苯基)
科学家以环己醇为原料,经过多步转化和点击反应合成化合物 G,请按要求回答下
面的问题。
(1)有机物A转化为有机物B的反应类型为______;浓硫酸也可用作该转化的催化
剂,此处转化不使用浓硫酸作催化剂,其原因有______。
(2)有机物C经水解反应开环后得到有机物D,有机物D的结构简式为______。
(3)有机物E为双环化合物,其所含官能团的名称为______。
(4)叠氮酸根(N-)的结构可表示为 ,其中心原子 N 的杂化类型为
3
______。
(5)有机物F转化为有机物G的反应方程式为______。
(6)满足下列条件的有机物A的同分异构体有______种(不考虑立体异构)。
条件1:含一个五元环;
条件2:含有两个手性碳原子。
(7)根据点击反应信息和相关知识,设计以苯乙烯和CH N 为原料合成 的
3 3
路线。(无机试剂任选)______。
化学试题第8页(共8页)
{#{QQABKQSAgggIQBAAAQhCQwXoCgMQkAAACKoGRAAEsAIAiQFABAA=}#}