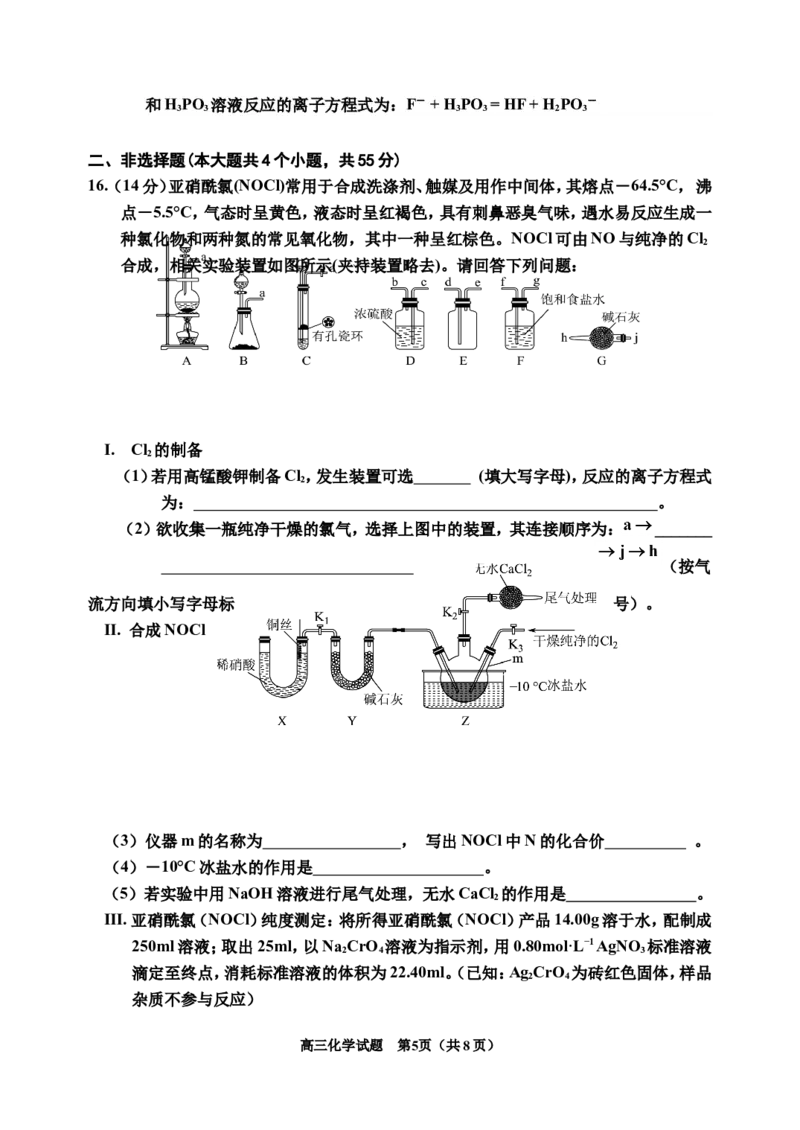文档内容
★ 保密·启用前
★
吉林地区普通高中2023-2024学年度高三年级第二次模拟考试
化 学 试 题
说明:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。答非选择题时,将答案写
在答题卡上。写在试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 O 16 Na 23 P 31 Fe 56
一、选择题: 本题共15小题,每题3分,共45分,在每小题给出的四个选项中,只有一项是
符合题目要求的。
1.拥有中国血统的“雅万高铁”在东南亚刮起了一股中国速度风,成为擦亮中国高铁
的“金名片”,下列说法正确的是
A.高铁列车使用的大丝束碳纤维被称为“新材料之王”,属于新型无机非金属材料
B.高铁列车依托5G技术实现超高清信号长时间稳定传输,5G芯片主要材质是SiO
2
C.高铁列车车厢连接部位使用的聚四氟乙烯材料含有σ键和π键,能使溴水褪色
D.高铁列车马桶的下水口是纳米硅胶材料,保证了卫生间毫无异味,硅胶还常用作
食品抗氧化剂
2.下列有关化学用语的说法正确的是
A.碳酸氢钠在水溶液中的电离方程式为:NaHCO Na++HCO -
3 3
B.基态氮原子的轨道表示式:
C.顺-2-丁烯的球棍模型:
D.HClO的结构式为H-O-Cl
3.氧化物在生产、生活中有广泛应用。下列氧化物的性质描述正确且与用途具有对应关
系的是
A.因为SO 具有氧化性,所以可用于葡萄酒保存
2
B.因为CaO能与水反应,所以可用作食品干燥剂
C.因为Al O 是两性氧化物,所以可用于工业制备金属铝
2 3
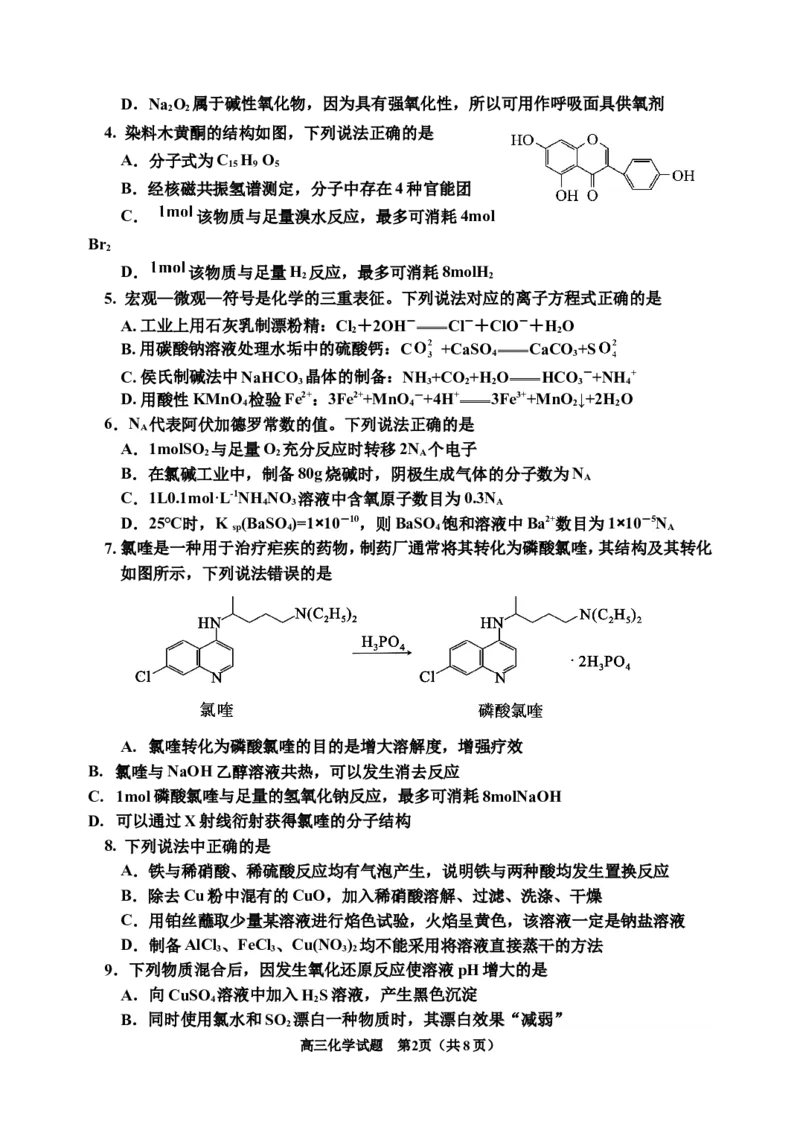
高三化学试题 第1页(共8页)D.Na O 属于碱性氧化物,因为具有强氧化性,所以可用作呼吸面具供氧剂
2 2
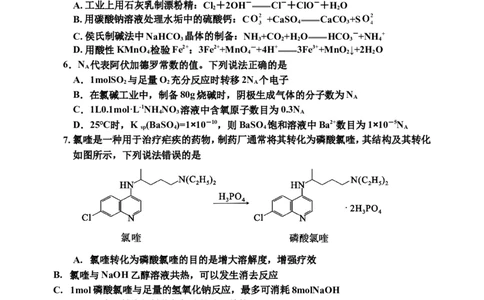
4. 染料木黄酮的结构如图,下列说法正确的是
A.分子式为C H O
15 9 5
B.经核磁共振氢谱测定,分子中存在4种官能团
C. 该物质与足量溴水反应,最多可消耗4mol
Br
2
D. 该物质与足量H 反应,最多可消耗8molH
2 2
5. 宏观—微观—符号是化学的三重表征。下列说法对应的离子方程式正确的是
A. 工业上用石灰乳制漂粉精:Cl +2OH- Cl-+ClO-+HO
2 2
B. 用碳酸钠溶液处理水垢中的硫酸钙:C +CaSO CaCO +S
4 3
C. 侯氏制碱法中NaHCO 晶体的制备:NH +CO+H O HCO -+NH+
3 3 2 2 3 4
D. 用酸性KMnO 检验Fe2+:3Fe2++MnO -+4H+ 3Fe3++MnO ↓+2H O
4 4 2 2
6.N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.1molSO 与足量O 充分反应时转移2N 个电子
2 2 A
B.在氯碱工业中,制备80g烧碱时,阴极生成气体的分子数为N
A
C.1L0.1mol·L-1NH NO 溶液中含氧原子数目为0.3N
4 3 A
D.25℃时,K (BaSO )=1×10-10,则BaSO 饱和溶液中Ba2+数目为1×10-5N
sp 4 4 A
7. 氯喹是一种用于治疗疟疾的药物,制药厂通常将其转化为磷酸氯喹,其结构及其转化
如图所示,下列说法错误的是
A. 氯喹转化为磷酸氯喹的目的是增大溶解度,增强疗效
B. 氯喹与NaOH乙醇溶液共热,可以发生消去反应
C. 1mol磷酸氯喹与足量的氢氧化钠反应,最多可消耗8molNaOH
D. 可以通过X射线衍射获得氯喹的分子结构
8. 下列说法中正确的是
A.铁与稀硝酸、稀硫酸反应均有气泡产生,说明铁与两种酸均发生置换反应
B.除去Cu粉中混有的CuO,加入稀硝酸溶解、过滤、洗涤、干燥
C.用铂丝蘸取少量某溶液进行焰色试验,火焰呈黄色,该溶液一定是钠盐溶液
D.制备AlCl 、FeCl、Cu(NO ) 均不能采用将溶液直接蒸干的方法
3 3 3 2
9.下列物质混合后,因发生氧化还原反应使溶液pH增大的是
A.向CuSO 溶液中加入HS溶液,产生黑色沉淀
4 2
B.同时使用氯水和SO 漂白一种物质时,其漂白效果“减弱”
2
高三化学试题 第2页(共8页)C.向 NaHSO 溶液中加入足量BaCl 溶液,生成白色沉淀
4 2
D.将“84消毒液”与酸性洁厕剂混用,产生黄绿色气体
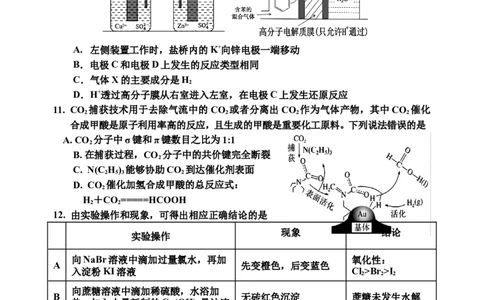
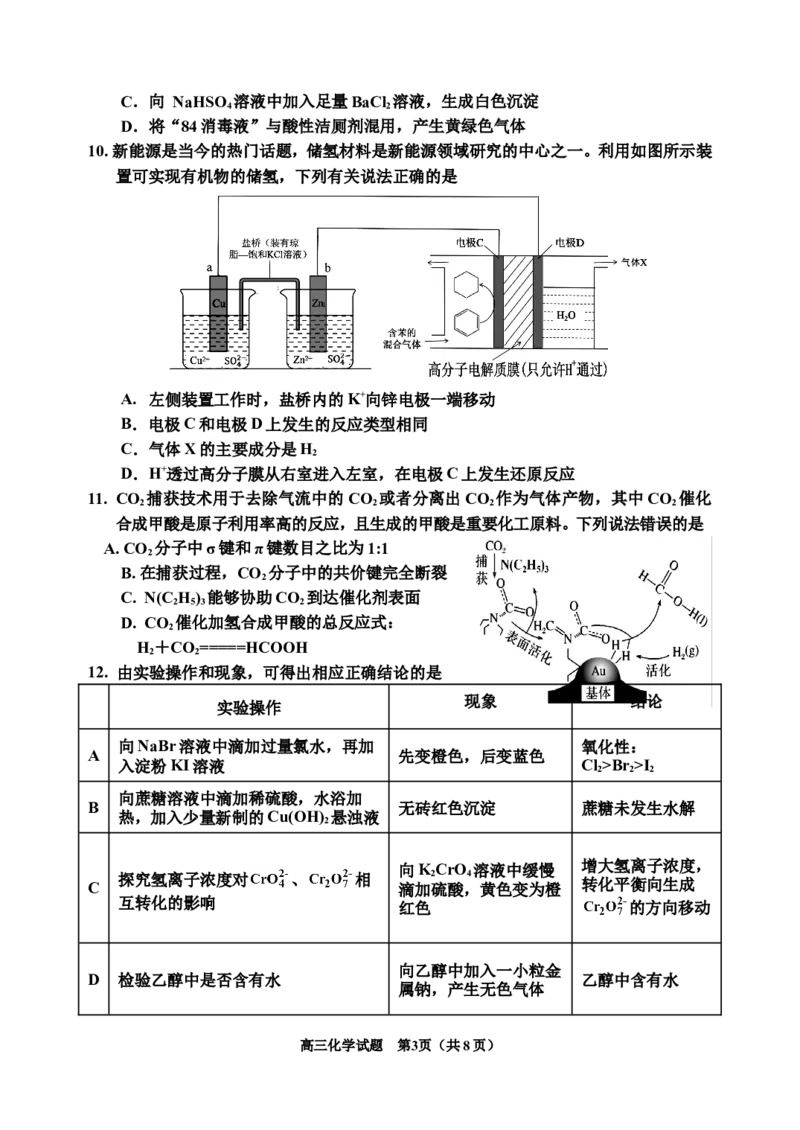
10. 新能源是当今的热门话题,储氢材料是新能源领域研究的中心之一。利用如图所示装
置可实现有机物的储氢,下列有关说法正确的是
A. 左侧装置工作时,盐桥内的K+向锌电极一端移动
B.电极C和电极D上发生的反应类型相同
C.气体X的主要成分是H
2
D.H+透过高分子膜从右室进入左室,在电极C上发生还原反应
11. CO 捕获技术用于去除气流中的CO 或者分离出CO 作为气体产物,其中CO 催化
2 2 2 2
合成甲酸是原子利用率高的反应,且生成的甲酸是重要化工原料。下列说法错误的是
A. CO 分子中σ键和π键数目之比为1:1
2
B. 在捕获过程,CO 分子中的共价键完全断裂
2
C. N(C H) 能够协助CO 到达催化剂表面
2 5 3 2
D. CO 催化加氢合成甲酸的总反应式:
2
H+CO =====HCOOH
2 2
12. 由实验操作和现象,可得出相应正确结论的是
现象 结论
实验操作
向NaBr溶液中滴加过量氯水,再加 氧化性:
A 先变橙色,后变蓝色
入淀粉KI溶液 Cl >Br >I
2 2 2
向蔗糖溶液中滴加稀硫酸,水浴加
B 无砖红色沉淀 蔗糖未发生水解
热,加入少量新制的Cu(OH) 悬浊液
2
向KCrO 溶液中缓慢 增大氢离子浓度,
探究氢离子浓度对 、 相 2 4
C 滴加硫酸,黄色变为橙 转化平衡向生成
互转化的影响
红色 的方向移动
向乙醇中加入一小粒金
D 检验乙醇中是否含有水 乙醇中含有水
属钠,产生无色气体
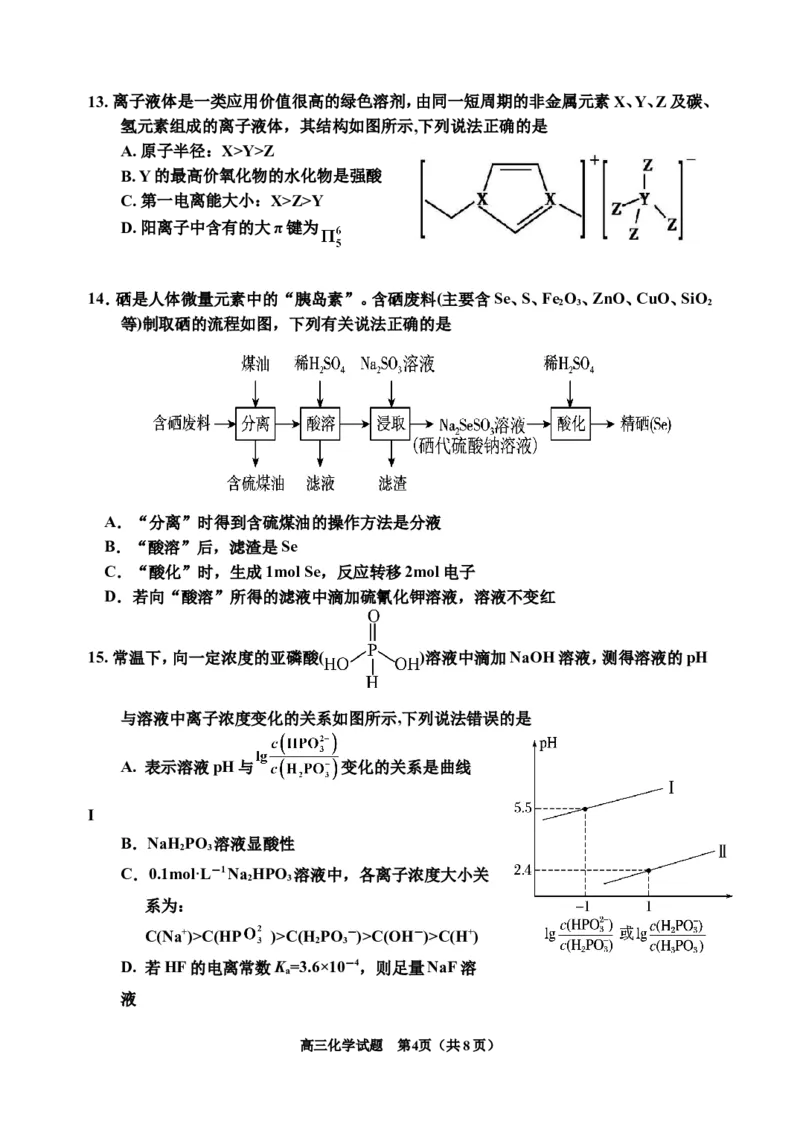
高三化学试题 第3页(共8页)13. 离子液体是一类应用价值很高的绿色溶剂,由同一短周期的非金属元素X、Y、Z及碳、
氢元素组成的离子液体,其结构如图所示,下列说法正确的是
A. 原子半径:X>Y>Z
B. Y的最高价氧化物的水化物是强酸
C. 第一电离能大小:X>Z>Y
D. 阳离子中含有的大π键为
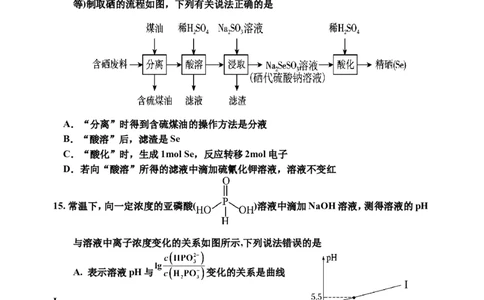
14.硒是人体微量元素中的“胰岛素”。含硒废料(主要含Se、S、FeO、ZnO、CuO、SiO
2 3 2
等)制取硒的流程如图,下列有关说法正确的是
A.“分离”时得到含硫煤油的操作方法是分液
B.“酸溶”后,滤渣是Se
C.“酸化”时,生成1mol Se,反应转移2mol电子
D.若向“酸溶”所得的滤液中滴加硫氰化钾溶液,溶液不变红
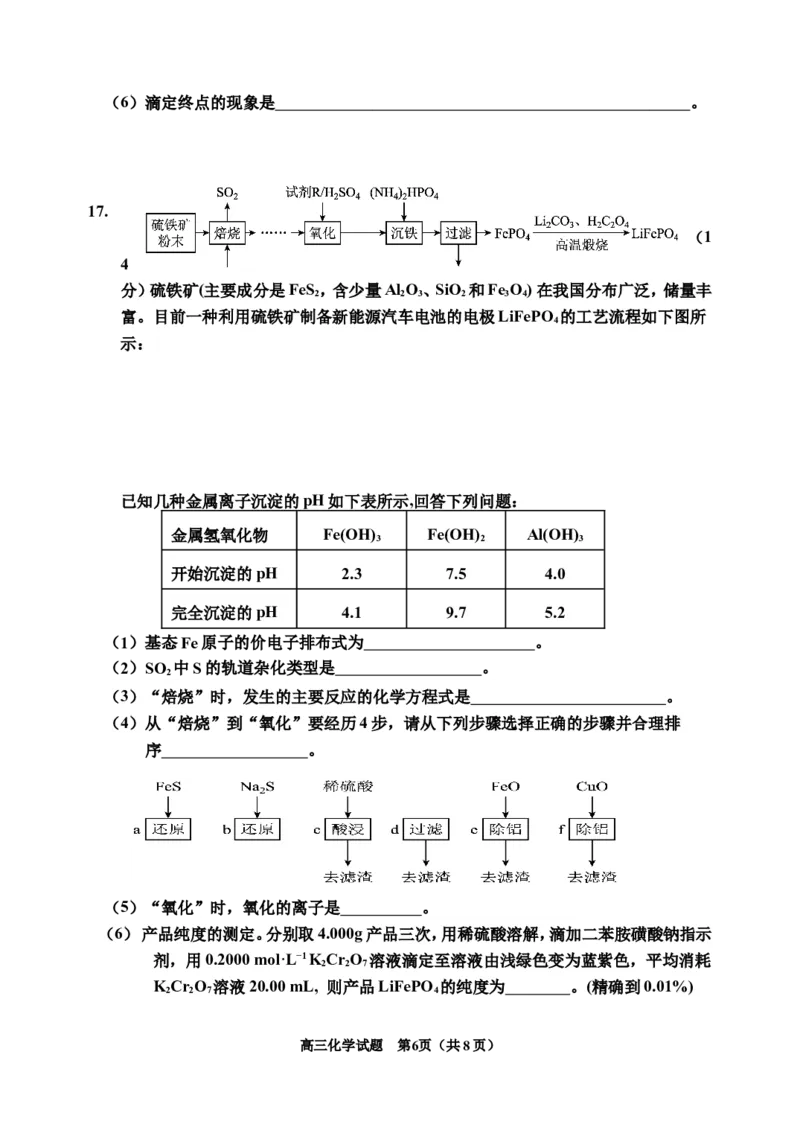
15. 常温下,向一定浓度的亚磷酸( )溶液中滴加NaOH溶液,测得溶液的pH
与溶液中离子浓度变化的关系如图所示,下列说法错误的是
A. 表示溶液pH与 变化的关系是曲线
I
B.NaH PO 溶液显酸性
2 3
C.0.1mol·L-1 Na HPO 溶液中,各离子浓度大小关
2 3
系为:
C(Na+)>C(HP )>C(H PO-)>C(OH-)>C(H+)
2 3
D. 若HF的电离常数K =3.6×10-4,则足量NaF溶
a
液
高三化学试题 第4页(共8页)和HPO 溶液反应的离子方程式为:F- + H PO = HF + H PO-
3 3 3 3 2 3
二、非选择题(本大题共4个小题,共55分)
16.( 14分)亚硝酰氯(NOCl)常用于合成洗涤剂、触媒及用作中间体,其熔点-64.5°C, 沸
点-5.5°C,气态时呈黄色,液态时呈红褐色,具有刺鼻恶臭气味,遇水易反应生成一
种氯化物和两种氮的常见氧化物,其中一种呈红棕色。NOCl可由NO与纯净的Cl
2
合成,相关实验装置如图所示(夹持装置略去)。请回答下列问题:
Ⅰ. Cl 的制备
2
(1)若用高锰酸钾制备Cl ,发生装置可选 (填大写字母),反应的离子方程式
2
为: 。
(2)欲收集一瓶纯净干燥的氯气,选择上图中的装置,其连接顺序为: _______
(按气
流方向填小写字母标 号)。
Ⅱ. 合成NOCl
(3)仪器m的名称为 , 写出NOCl中N的化合价 。
(4)-10°C冰盐水的作用是 。
(5)若实验中用NaOH溶液进行尾气处理,无水CaCl 的作用是 。
2
Ⅲ. 亚硝酰氯(NOCl)纯度测定:将所得亚硝酰氯(NOCl)产品14.00g溶于水,配制成
250ml溶液;取出25ml,以Na CrO 溶液为指示剂,用0.80mol·L−1 AgNO 标准溶液
2 4 3
滴定至终点,消耗标准溶液的体积为22.40ml。(已知:Ag CrO 为砖红色固体,样品
2 4
杂质不参与反应)
高三化学试题 第5页(共8页)(6)滴定终点的现象是 。
17.
(1
4
分)硫铁矿(主要成分是FeS ,含少量Al O、SiO 和FeO) 在我国分布广泛,储量丰
2 2 3 2 3 4
富。目前一种利用硫铁矿制备新能源汽车电池的电极LiFePO 的工艺流程如下图所
4
示:
已知几种金属离子沉淀的pH如下表所示,回答下列问题:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH)
3 2 3
开始沉淀的pH 2.3 7.5 4.0
完全沉淀的pH 4.1 9.7 5.2
(1)基态Fe原子的价电子排布式为 。
(2)SO 中S的轨道杂化类型是 。
2
(3)“焙烧”时,发生的主要反应的化学方程式是 。
(4)从“焙烧”到“氧化”要经历4步,请从下列步骤选择正确的步骤并合理排
序 。
(5)“氧化”时,氧化的离子是 。
(6) 产品纯度的测定。分别取4.000g产品三次,用稀硫酸溶解,滴加二苯胺磺酸钠指示
剂,用0.2000 mol·L−1 KCrO 溶液滴定至溶液由浅绿色变为蓝紫色,平均消耗
2 2 7
KCrO 溶液20.00 mL, 则产品LiFePO 的纯度为 。(精确到0.01%)
2 2 7 4
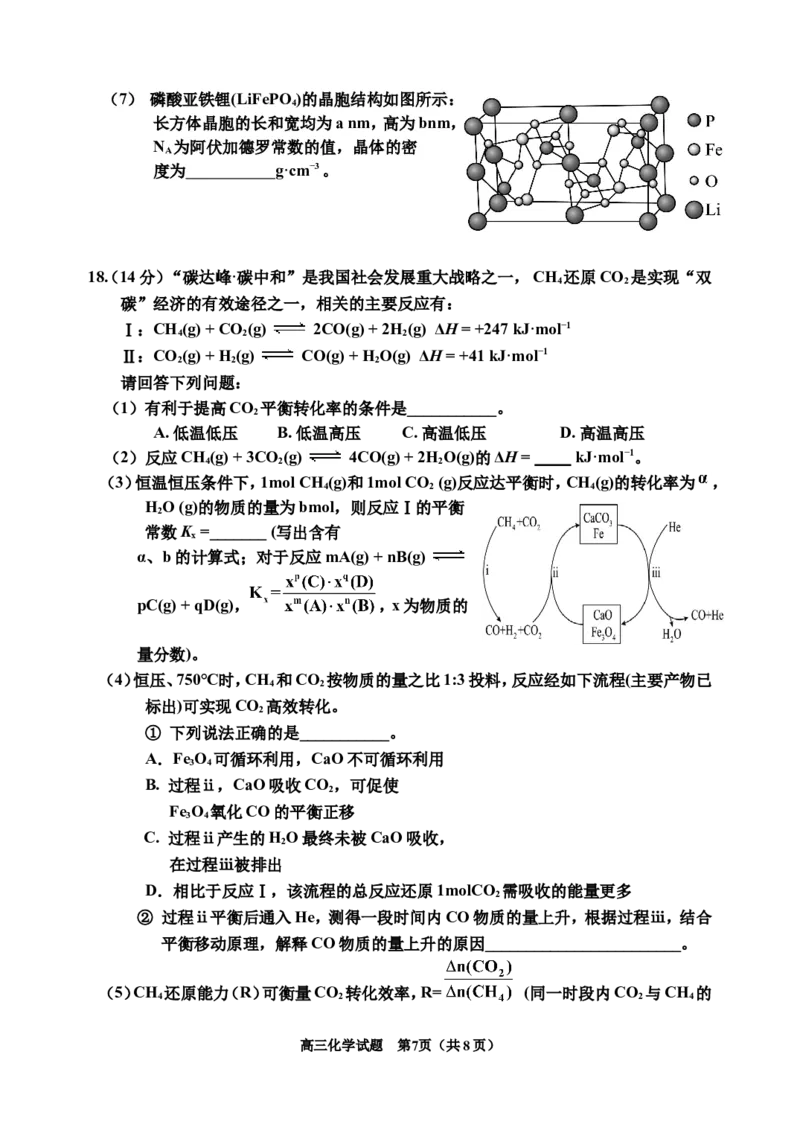
高三化学试题 第6页(共8页)(7) 磷酸亚铁锂(LiFePO )的晶胞结构如图所示:
4
长方体晶胞的长和宽均为a nm,高为bnm,
N 为阿伏加德罗常数的值,晶体的密
A
度为 g·cm−3 。
18(. 14分)“碳达峰·碳中和”是我国社会发展重大战略之一, CH 还原CO 是实现“双
4 2
碳”经济的有效途径之一,相关的主要反应有:
Ⅰ:CH (g) + CO (g) 2CO(g) + 2H (g) ΔH = +247 kJ·mol−1
4 2 2
Ⅱ:CO (g) + H (g) CO(g) + H O(g) ΔH = +41 kJ·mol−1
2 2 2
请回答下列问题:
(1)有利于提高CO 平衡转化率的条件是___________。
2
A. 低温低压 B. 低温高压 C. 高温低压 D. 高温高压
(2)反应CH (g) + 3CO (g) 4CO(g) + 2H O(g)的ΔH = kJ·mol−1。
4 2 2
(3)恒温恒压条件下,1mol CH (g)和1mol CO (g)反应达平衡时,CH (g)的转化率为 ,
4 2 4
HO (g)的物质的量为bmol,则反应Ⅰ的平衡
2
常数K =_______ (写出含有
x
α、b的计算式;对于反应mA(g) + nB(g)
pC(g) + qD(g), ,x为物质的
量分数)。
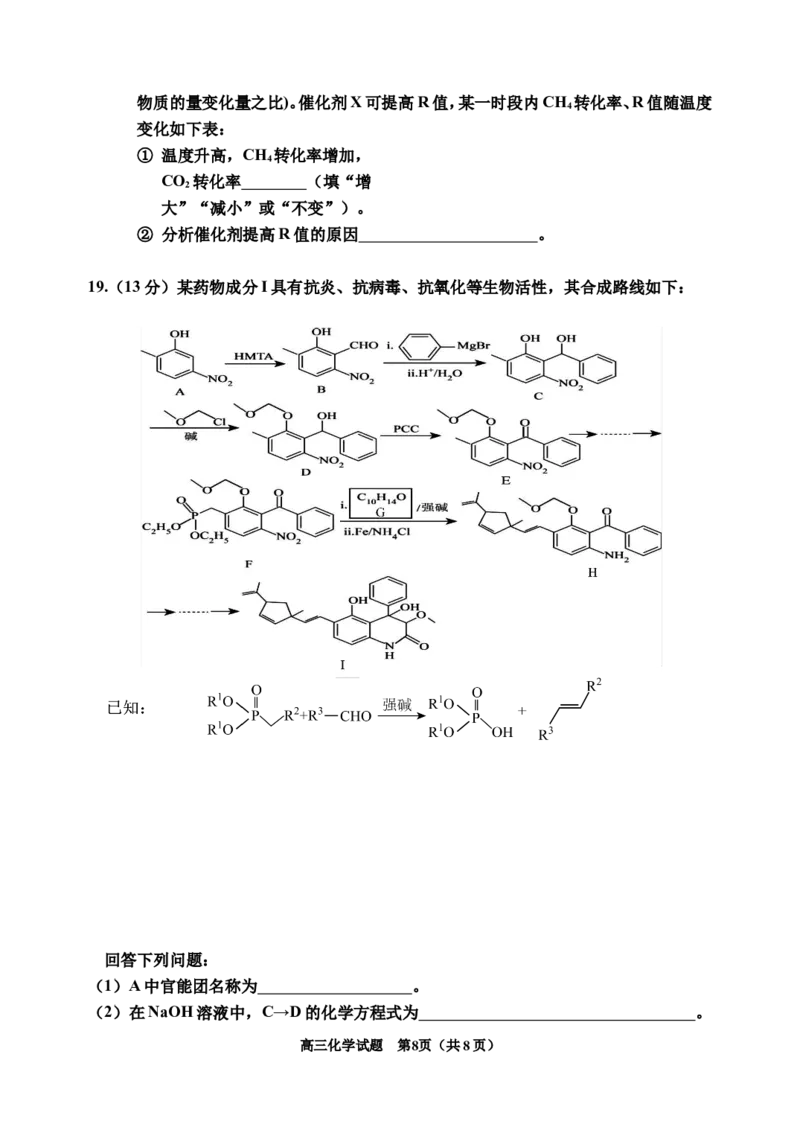
(4)恒压、750℃时,CH 和CO 按物质的量之比1:3投料,反应经如下流程(主要产物已
4 2
标出)可实现CO 高效转化。
2
① 下列说法正确的是___________。
A.FeO 可循环利用,CaO不可循环利用
3 4
B. 过程ⅱ,CaO吸收CO ,可促使
2
FeO 氧化CO的平衡正移
3 4
C. 过程ⅱ产生的HO最终未被CaO吸收,
2
在过程ⅲ被排出
D.相比于反应Ⅰ,该流程的总反应还原1molCO 需吸收的能量更多
2
② 过程ⅱ平衡后通入He,测得一段时间内CO物质的量上升,根据过程ⅲ,结合
平衡移动原理,解释CO物质的量上升的原因________________________。
(5)CH 还原能力(R)可衡量CO 转化效率,R= (同一时段内CO 与CH 的
4 2 2 4
高三化学试题 第7页(共8页)物质的量变化量之比)。催化剂X可提高R值,某一时段内CH 转化率、R值随温度
4
变化如下表:
① 温度升高,CH 转化率增加,
4
CO 转化率 (填“增
2
大”“减小”或“不变”)。
② 分析催化剂提高R值的原因 。
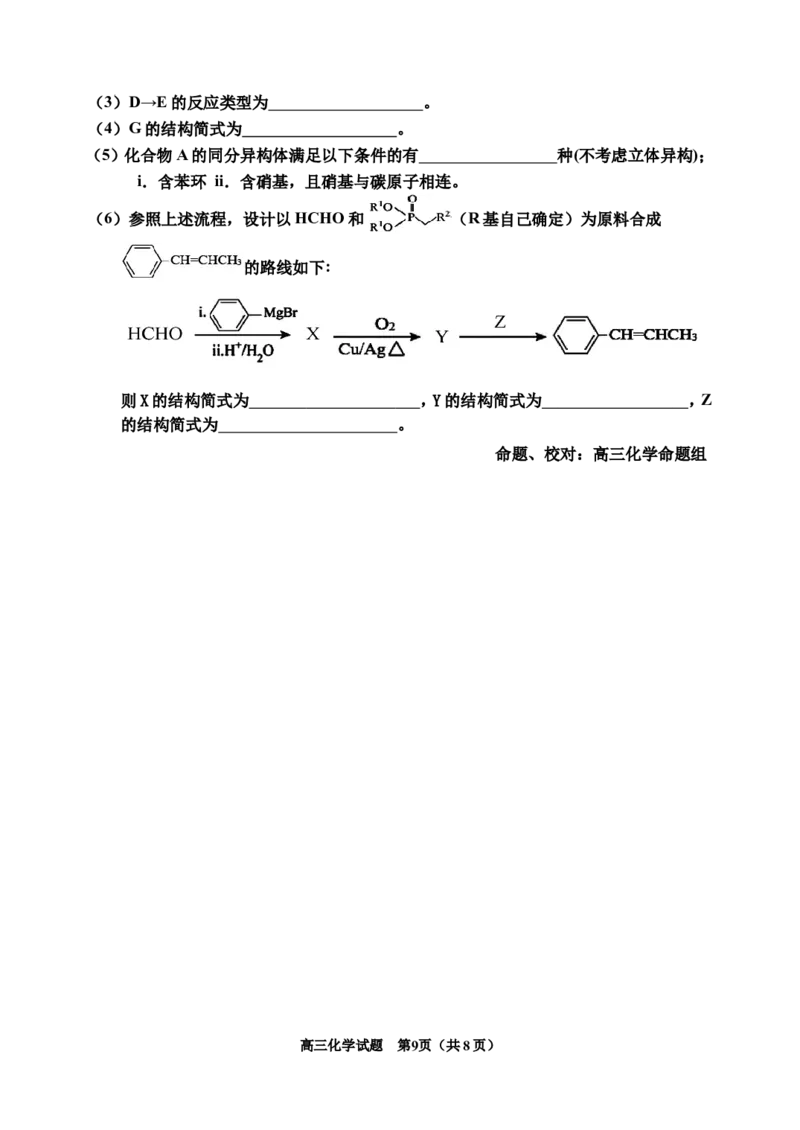
19.(13分)某药物成分I具有抗炎、抗病毒、抗氧化等生物活性,其合成路线如下:
回答下列问题:
(1)A中官能团名称为 。
(2)在NaOH溶液中,C→D的化学方程式为 。
高三化学试题 第8页(共8页)(3)D→E的反应类型为 。
(4)G的结构简式为 。
(5)化合物A的同分异构体满足以下条件的有 种(不考虑立体异构);
i.含苯环 ii.含硝基,且硝基与碳原子相连。
(6)参照上述流程,设计以HCHO和 (R基自己确定)为原料合成
的路线如下:
则X的结构简式为 ,Y的结构简式为 ,Z
的结构简式为 。
命题、校对:高三化学命题组
高三化学试题 第9页(共8页)