文档内容
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 王双奕
粉笔教师教育 粉笔教师目
录
content
1 化学反应与能量
2 化学反应速率和化学平衡
3 水溶液中的离子平衡
4 电化学基础水溶液中的离子平衡P151
(三)水解平衡常数
水解反应的平衡常数叫作水解平衡常数或水解常数,用 K 表示。
h
以NH ++H O NH ·H O+H+ 为例,NH +水解的水解平衡常数表
4 2 3 2 4
达式为:
K 数值越大,水解趋势越大。
hP151
【粉笔提示】
水解平衡常数与水的离子积常数和电离平衡常数的关系:P151
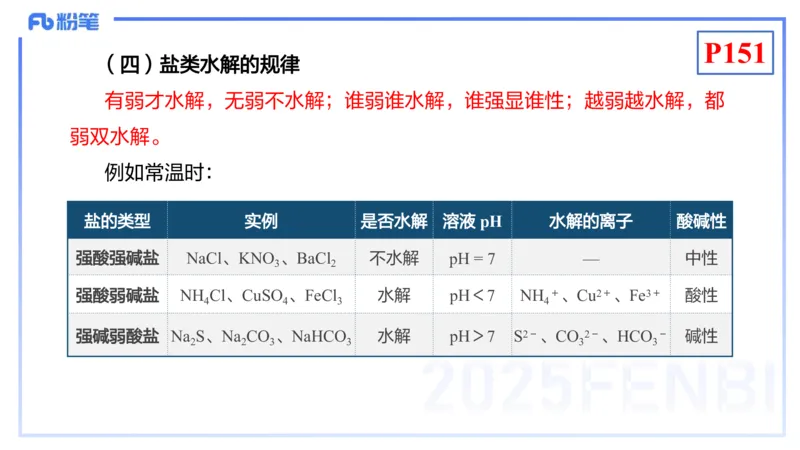
(四)盐类水解的规律
有弱才水解,无弱不水解;谁弱谁水解,谁强显谁性;越弱越水解,都
弱双水解。
例如常温时:
盐的类型 实例 是否水解 溶液 pH 水解的离子 酸碱性
强酸强碱盐 NaCl、KNO 、BaCl 不水解 pH = 7 — 中性
3 2
强酸弱碱盐 NH Cl、CuSO 、FeCl 水解 pH<7 NH +、Cu2+、Fe3+ 酸性
4 4 3 4
强碱弱酸盐 Na S、Na CO 、NaHCO 水解 pH>7 S2-、CO 2-、HCO - 碱性
2 2 3 3 3 3P151
【粉笔提示】
“越弱越水解”指的是盐对应的酸(或碱)越弱,水解程度越大,溶液碱性
(或酸性)越强。如果酸性:HA>HB,那么相同浓度的 NaA 和 NaB 溶液,后
者的碱性强。例如,CH COOH 的酸性比 HCN 强,则相同浓度时,CH COO-
3 3
的水解程度比 CN-小,NaCN 溶液的碱性比 CH COONa 的强。
3P152
(五)影响盐类水解平衡的因素
1.内因
主要因素是盐本身的性质,组成盐的酸根离子所对应的酸越弱或阳离子
对应的碱越弱,盐的水解程度就越大(越弱越水解)。P152
2.外因
(1)温度:水解过程一般是吸热过程,故升温使水解程度增大,反之则减小。
(2)浓度:盐溶液越稀,水解程度越大,反之越小。
【粉笔提示】
盐的浓度越大,水解程度越小,但其浓溶液的酸性(或碱性)比其稀溶液的酸
性(或碱性)强。
(3)溶液的酸碱性:组成盐的离子能与水发生水解反应。向盐溶液中加入 H+,
可抑制阳离子水解,促进阴离子水解;向盐溶液中加入OH-,能抑制阴离子水解,
促进阳离子水解。P152
例1: Fe3++3H O Fe(OH) +3H+(正反应吸热)
2 3
移动
改变条件 H +数 pH Fe3+水解率 现象
方向
升高温度 向右 增多 减小 增大 颜色变深(棕黄→红棕)
加 HCl 向左 增多 减小 减小 颜色变浅
加 H O 向右 增多 增大 增大 颜色变浅
2
加 Mg 粉 向右 减少 增大 增大 生成红褐色沉淀和无色气体
加 NaHCO 向右 减少 增大 增大 生成红褐色沉淀和无色气体
3
加少量 NaF 向右 减少 增大 增大 颜色变深
加少量 NaOH 向右 减少 增大 增大 生成红褐色沉淀P153
例2:CH COO-+H O CH COOH+OH-(正反应吸热)
3 2 3
改变条件 c (CH COO-) c (CH COOH) c (OH-) c (H+) pH 水解程度
3 3
升温 减小 增大 增大 — — 增大
加水 减小 减小 减小 增大 减小 增大
加醋酸 增大 增大 减小 增大 减小 减小
加醋酸钠 增大 增大 增大 减小 增大 减小
加 HCl 减小 增大 减小 增大 减小 增大
加 NaOH 增大 减小 增大 减小 增大 减小P153
(六)盐类水解的应用
遇到下列情况时,应从盐的水解角度进行分析。
1.实验室配制易水解的盐溶液
如配制 FeCl 、SnCl 溶液时加入一定量的酸(盐酸)防止水解,或直接
3 2
溶解在浓盐酸中再加水稀释。
Fe3++3H O Fe(OH) +3H+
2 3P153
2.某些活泼金属与强酸弱碱盐反应
镁条放入氯化铵、氯化铜、氯化铁溶液中产生氢气。
3.制备氢氧化铁胶体
向沸水中滴加饱和氯化铁溶液并继续煮沸,直至液体呈透明的红褐色:
Fe3++3H O Fe(OH) (胶体)+3H+
2 3P153
4.明矾[KAl(SO ) ·12H O]、三氯化铁(FeCl )等净水
4 2 2 3
Al3++3H O Al(OH) (胶体)+3H+
2 3
Fe3++3H O Fe(OH) (胶体)+3H+
2 3
原因:胶体吸附性强,可吸附水中悬浮的颗粒并沉降,从而起到净水作用。
5.苏打洗涤去油污
CO 2-+H O HCO -+OH-
3 2 3
原因:加热,促进碳酸根离子的水解,溶液碱性增强,去油污能力增强。P153
6.泡沫灭火器原理
成分:NaHCO 、Al (SO )
3 2 4 3
原理:当两盐混合时, Al3+水解产生的氢离子与 HCO - 水解产生的氢
3
氧根离子结合生成水,相互促进发生完全双水解。
3HCO -+Al3+ = Al(OH) ↓+3CO ↑
3 3 2P154
7.施用化肥
普钙 [Ca(H PO ) ] (又叫过磷酸钙) 、铵态氮肥不能与草木灰(主要成分
2 4 2
为K CO )混用。
2 3
原因:K CO 水解显碱性,其与 H PO -、NH + 发生反应,降低肥效。
2 3 2 4 4
CO 2-+H O HCO -+OH-
3 2 3
3Ca2+ + 6H PO - +12OH- = Ca (PO ) ↓+12H O+4PO 3-
2 4 3 4 2 2 4
NH ++OH- NH +H O
4 3 2P154
8.某些盐溶液加热蒸干的产物
将 FeCl 、AlCl 、CuCl 等 挥发性酸 的盐溶液蒸干不能制得纯净的盐。
3 3 2
原因:FeCl 易水解,FeCl +3H O Fe(OH) +3HCl。
3 3 2 3
加热时盐的水解程度增大,氯化氢易挥发离开反应体系,促使反应进行
到底,生成的 Fe(OH) 灼烧后得到红棕色的 Fe O 。
3 2 3
同理,蒸干 AlCl (或 CuCl )溶液并灼烧得到 Al O (或 CuO)。
3 2 2 3P154
【粉笔提示】
蒸干Al (SO ) 、Na CO 等溶液,因为产物 H SO 、NaOH 难挥发,因而能
2 4 3 2 3 2 4
得到 Al (SO ) 、Na CO 固体。
2 4 3 2 3
Al (SO ) +6H O 2Al(OH) +3H SO
2 4 3 2 3 2 4
Na CO +H O NaHCO +NaOH
2 3 2 3P154
9.判断盐溶液的酸碱性(如 FeCl 溶液显酸性)
3
10.某些试剂的实验室贮存
如 Na CO 溶液、Na PO 溶液、Na SiO 溶液等不能贮存于磨口玻璃瓶中。
2 3 3 4 2 3
11.采用促进溶液中某些盐的水解,使之生成氢氧化物沉淀的方法,以除去
溶液中的某些金属离子。
例如,向 MgCl 、FeCl 的混合溶液中加入 MgO 或 MgCO 除去 FeCl ,向
2 3 3 3
CuCl 、FeCl 的混合溶液中加入 CuO 或 Cu (OH) CO 除去 FeCl 。
2 3 2 2 3 3
(Fe3+ 在pH=3.7 时几乎可以沉淀完全)P155
【粉笔提示】
盐类水解中的三大守恒
1.电荷守恒
电解质溶液中不论存在多少种离子,溶液总是呈电中性的,即阳离子所
带的正电荷总数一定等于阴离子所带的负电荷总数。
例如 NaHCO 溶液中:
3
c (Na+)+c (H+ ) =c (HCO -)+c (OH-)+2c (CO 2-)
3 3P155
2.物料守恒(元素质量守恒)
在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生
了变化。但就该离子所含的某种元素来说,其质量在变化前后是守恒的,即
元素质量守恒,也称物料守恒。
例如在Na S 溶液中,S 元素以 S2-、HS-、H S 三种形式存在,但不管
2 2
如何,Na 原子的物质的量总是 S 原子物质的量的 2 倍。根据物料守恒,必
然有:
c (Na+)=2[ c (S2-)+c (HS-)+c (H S) ] = 2c (S2-)+2c (HS-)+2c (H S)
2 23.质子守恒 P155
任何溶液中,由水电离产生的 c (H+)=c (OH-) 。
如 Na S 溶液中的质子转移示意图:
2
c (H+)+c (HS-)+2c (H S)=c (OH-) 或 c (H O+)+c (HS-)+2c (H S)=c (OH-)
2 3 2
质子守恒式也可由电荷守恒式和物料守恒式联立得到。
电荷: c (Na+)+c (H+) = 2 c (S2-)+c (HS-)+c (OH-)
物料:2 c (S2-)+2c (HS-)+2c (H S)= c (Na+)
2P161P155
四、缓冲溶液
(一)同离子效应与盐效应
弱酸弱碱的电离平衡是一个暂时的、相对的动态平衡,当外界条件发
生改变时,电离平衡会像其他化学平衡一样,随即发生平衡移动,使弱酸
弱碱的电离程度有所改变。同离子效应和盐效应是影响弱酸弱碱电离的常
见因素。
1.同离子效应
在弱电解质溶液中,若加入与该弱电解质有共同离子的强电解质时,
弱电解质的电离平衡会向左移动,以致弱电解质的电离度减小。
CH COOH CH COO-+H+
3 3P156
2.盐效应
在弱电解质溶液中,若加入与弱电解质没有相同离子的强电解质时,
会增大溶液中离子的浓度,使溶液中离子间的相互牵制作用增强,即活度
降低,离子结合为分子的几率减少,弱电解质的电离平衡会向右移动,从
而使弱电解质分子浓度减小,以致弱电解质的电离度增加。
CH COOH CH COO-+H+
3 3P156
(二)缓冲溶液的概念
能够缓冲加入少量酸、碱和稀释的影响,使溶液的 pH 维持在一定范围
内的溶液称为缓冲溶液。
(三)缓冲原理
1.缓冲作用的原理
缓冲作用的原理是同离子效应的结果。缓冲溶液的作用实质是通过共
轭酸碱对之间的质子转移,消耗外来的酸和碱,即质子转移平衡的移动。
2.典型的缓冲溶液
典型的缓冲溶液由一对浓度接近的共轭酸碱组成,组成缓冲溶液的两
种物质(共轭酸碱对)称为缓冲对或缓冲系。如:HAc~Ac-、NH +~NH 。
4 3P156
常见的缓冲对:
(1)弱酸及其对应盐:HAc~NaAc 。
(2)弱碱及其对应盐:NH Cl~NH ·H O 。
4 3 2
(3)多元弱酸及其次级盐:H CO ~NaHCO 。
2 3 3
(4)酸式盐及其次级盐:NaH PO ~Na HPO 。
2 4 2 4P161P156
(四)缓冲溶液pH的计算
共轭酸碱对间的质子传递平衡,用通式表示:
HB+H O H O+ +B- (HB 表示共轭酸,B- 表示共轭碱)
2 3
计算缓冲溶液的 pH:
式中 pK 为弱酸电离常数的负对数,[HB] 和 [B-] 均为平衡浓度。
aP157
[B-] 与 [HB] 的比值称为缓冲比,[B-] 与 [HB] 之和称为缓冲溶液的
总浓度。
缓冲比在 0.1-10 间为宜,这时溶液的pH=pK ±1,若超过这个范围,
a
缓冲作用将明显减弱。
弱酸及其对应盐组成的缓冲溶液 pH 近似计算公式:
弱碱及其对应盐组成的缓冲溶液 pOH 近似计算公式:P157
五、难溶电解质的溶解平衡
(一)固体物质的溶解度
不同的固体物质在水中的溶解度差别很大,从溶解度这一角度来讲,可将物
质进行如下分类(常温下):
溶解性 易溶 可溶 微溶 难溶
溶解度 >10 g 1~10 g 0.01~1 g <0.01 g
绝大多数固体物质的溶解度随温度的升高而增大,如 KNO 、CuSO 等;
3 4
少数物质的溶解度随温度的变化不明显,如 NaCl 等;
极少数物质的溶解度随温度的升高反而减小,如 Ca(OH) 等。
2P157
(二)沉淀溶解平衡
1.沉淀溶解平衡的建立
将固体物质溶于水中时,一方面,在水分子的作用下,分子或离子脱离
固体表面进入水中,这一过程叫溶解(扩散)过程;另一方面,溶液中的分
子或离子又在未溶解的固体表面聚集成晶体,这一过程叫结晶(析出)过程。
当这两个相反的过程的速率相等时,物质的溶解达到最大限度,形成饱和溶
液,达到沉淀溶解平衡状态。P157
2.沉淀溶解平衡
绝对不溶解的物质是不存在的,任何难溶物质的溶解度都不为零。以难
溶物质氯化银为例,尽管其溶解度很小,但仍会有少量溶解,氯化银在水中
存在着溶解和沉淀两个过程,在一定温度下,当沉淀溶解和生成的速率相等
时,便得到氯化银的饱和溶液,建立动态平衡。P158
3.沉淀溶解平衡的特征
(1)等:ν(溶解) = ν(沉淀) 。
(2)动:ν(溶解) = ν(沉淀) ≠ 0,动态平衡,溶解和沉淀的过程仍
在不断进行。
(3)定:达到平衡时,固体质量和离子浓度保持不变。
(4)变:当温度、溶液中离子浓度等外界条件发生改变时,沉淀溶解
平衡将发生移动,达到新的平衡。P158
(三)沉淀溶解平衡常数——溶度积
1.定义
在一定条件下,难溶物质的饱和溶液中,存在沉淀溶解平衡,其平衡常
数叫作溶度积常数或溶度积。
2.表达式
以 PbI 的沉淀溶解平衡为例:
2
PbI (s) Pb2+(aq)+2I-(aq)
2
K = c(Pb2+)·c2(I-)
spP158
3.意义
溶度积(K )反映了难溶电解质在水中的溶解能力。对于阴阳离子个数
sp
比相同的电解质,K 的数值越大,电解质在水中的溶解能力越强。
sp
4.影响 K 的因素
sp
K 与其他化学平衡常数一样,只与难溶电解质的性质和温度有关,而与
sp
沉淀的量和溶液中离子浓度的变化无关。
【粉笔提示】
对于阴阳离子个数比不同的电解质,要确定其溶解能力的大小,不能直接
比较 K 的数值大小。
spP161P159
(四)影响沉淀溶解平衡的因素
1.内因:难溶电解质本身的性质。
2.外因
(1)浓度:加水稀释,沉淀溶解平衡向溶解的方向移动,但 K 不变。
sp
(2)温度:多数难溶电解质溶于水的过程是吸热的,所以对于此类难溶
电解质,升高温度,沉淀溶解平衡向溶解的方向移动,同时 K 增大。
spP159
(3)同离子效应:向沉淀溶解平衡体系中,加入与难溶电解质所含离子
相同的物质,平衡向生成沉淀的方向移动,K 不变。
sp
(4)其他:向沉淀溶解平衡体系中,加入可与体系中某些离子反应生成
更难溶的物质或气体,平衡向溶解的方向移动,K 不变。
spP159
(五)沉淀溶解平衡的应用
1.判断沉淀溶解平衡
利用 Q 与 K 的大小来判断沉淀的溶解与生成,在难溶电解质的溶解平
c sp
衡体系中:
当 Q > K 时,就会生成沉淀。
c sp
当 Q =K 时,体系处于平衡状态。
c sp
当 Q < K 时,沉淀就会溶解。
c spP159
2.沉淀的溶解方法
常用的方法有酸碱溶解法、氧化还原溶解法、配位溶解法和沉淀转化溶解法。
(1)酸碱溶解法
原理是通过生成某些可溶性弱电解质(水、弱酸或弱碱),使难溶物的离子
浓度降低而溶解,实质是发生复分解反应,沉淀溶解的过程实质是破坏沉淀溶解
平衡的过程。如难溶酸用强碱溶,难溶碱用强酸或较强酸溶,难溶弱酸盐用强酸
或较强酸溶等。
如 BaCO 的沉淀溶解平衡为 BaCO (s) Ba2+(aq)+CO 2- (aq),加入盐酸以
3 3 3
后发生反应 CO 2-+2H+ = H O+CO ↑,使沉淀溶解平衡向右移动,从而达到溶解沉
3 2 2
淀的目的。P159
(2)氧化还原溶解法
原理是通过氧化还原反应使难溶物的离子浓度降低,使平衡向右移动而
溶解。此法适用于具有明显氧化性或还原性的难溶物,如 Ag S 溶于稀HNO :
2 3
3Ag S+8HNO (稀) = 6AgNO +3S+2NO↑+4H O
2 3 3 2P160
(3)配位溶解法
在难溶物中加入配位剂,因形成配合物而降低难溶物的某种离子浓度,
使平衡向右移动而溶解。如AgCl 溶于氨水:
AgCl(s)+2NH ·H O = [Ag(NH ) ]++Cl-+2H O。
3 2 3 2 2
(4)沉淀转化溶解法
本法是将难溶物转化为能用上述三种方法之一溶解的沉淀,然后再进行
溶解。例如在 BaSO 中加入饱和 Na CO 溶液,使 BaSO 转化为 BaCO ,再
4 2 3 4 3
用盐酸溶解 BaCO 。
3P160
3.沉淀的转化
(1)定义
一般来说,沉淀的转化就是由一种难溶物转化为另一种更难溶物的过程。
(2)实质
沉淀转化的实质就是沉淀溶解平衡的移动。
一般来说,溶解度小的沉淀转化成溶解度更小的沉淀容易实现。对于组
成类似(阴、阳离子个数比相同)的难溶电解质,K 大的易转化为 K 小的。
sp spP160
(3)示例
根据难溶物质溶解度的大小,难溶物之间可以进行转化,例如:
NaCl NaBr NaI Na2S
AgNO AgCl (白色沉淀) AgBr (淡黄色沉淀) AgI (黄色沉淀)
3
Ag S (黑色沉淀)
2
(4)应用
沉淀转化在工业上应用普遍。例如,在工业废水处理过程中,用 FeS 等难溶物作沉
淀剂去除废水中的重金属离子,其原理是重金属离子的硫化物(如 CuS)的溶解度小于
FeS 的溶解度。P160电化学基础P162
一、原电池
(一)原电池的工作原理
1.定义
把化学能直接转化为电能的装置。
2.工作原理
如图是两种铜锌原电池装置的示意图。P162
在两个装置中锌片作负极、铜片作正极,Zn失去电子发生氧化反应而溶
解,电子经 Zn 片流入 Cu 片,Cu2+ 得电子发生还原反应变成 Cu 沉淀在铜片
上因此有电流产生,化学能转化为电能。电极反应和总反应如下:
锌片作负极:Zn-2e-= Zn2+(氧化反应)
铜片作正极:Cu2++2e-= Cu(还原反应)
总反应:Zn+Cu2+= Cu+Zn2+P162
(1)两极判断
负极:一般较活泼金属的电极为负极;
电子流出的电极为负极;
阴离子移向的电极为负极;
发生氧化反应的电极为负极。
正极:一般较不活泼金属的电极为正极;
电子流入的电极为正极;
阳离子移向的电极为正极;
发生还原反应的电极为正极。P163
【粉笔提示】
原电池中必须有自发的氧化还原反应发生,据此可以判断正负极。
1.Mg—Al—NaOH 溶液形成的原电池中,Al 作负极,Mg 作正极;
2.Fe—Cu—浓 HNO 形成的原电池中,Cu 作负极,Fe 作正极;
3
3.Fe—Cu (通入空气)—NaCl 溶液形成的原电池中,Fe 作负极,Cu 作正极。
(吸氧腐蚀)P163
(2)三向判断
电子流向:负极 正极
离子迁移:阳离子 正极
阴离子 负极
电流方向:正极→负极P163
(3)双液电池
①盐桥在双液原电池中的作用:使两个半电池中的溶液连成一个通路。
②盐桥成分:一般为琼脂和饱和 KCl、NH NO 或 KNO 溶液。
4 3 3
③盐桥的优点:使原电池中的氧化剂和还原剂近乎完全隔离,并在不同区域之
间实现了电子的定向移动,使原电池能持续、稳定地产生电流。
④两种原电池相比的能量变化情况
单液电池:化学能转化为电能、热能,反应过程中,溶液的温度升高。
双液电池:化学能转化为电能,反应过程中,溶液的温度不变。P163
3.工作条件
(1)两个活泼性不同的电极
(2)电解质溶液 缺一不可
(3)形成闭合回路