文档内容
专题 03 氧化还原反应
内容概览
考点01 氧化还原反应的定义和实质
考点02 氧化还原反应相关概念的判断
考点03 氧化剂与还原剂
考点04 氧化还原反应的规律
考点05 氧化还原反应的综合考查
考点01 氧化还原反应的定义和实质
1.(23-24高一上·安徽省皖北六校·期末)氧化还原反应广泛存在于生产和生活中,下列现象与氧化还原
无关的是
A.植物光合作用 B.食物腐败
C.易燃物的自燃 D.酸雨腐蚀大理石雕像
2.(23-24高一上·吉林省部分名校·期末)下列过程不涉及氧化还原反应的是
A.新切开的钠表面变暗 B.氯化钠溶液通电制
C.用铁矿石冶炼生铁 D. 受热分解
3.(23-24高一上·广东省广州市·期末)下列应用中不涉及氧化还原反应的是
A.用白醋清洗水壶中的水垢 B.发射火箭时燃料的燃烧
C. 用作呼吸面具的供氧剂 D.暖贴中的铁粉遇空气放热
4.(23-24高一上·福建省福州市·期末)古籍中有“银针验毒”的记载,其原理为
,该反应属于
A.化合反应 B.分解反应 C.离子反应 D.氧化还原反应
5.(23-24高一上·北京市朝阳区·期末)下列物质的应用中,与氧化还原反应无关的是
A.用 和 制取盐酸
B.用生石灰( )作干燥剂
C.用铝粉和 作管道疏通剂
D.用 漂白棉、麻、纸张
6.(23-24高一上·安徽省芜湖市·期末)下列生产、生活中的事例不涉及氧化还原反应的是
A.燃料的燃烧 B.钢铁的锈蚀 C.干冰用于人工降雨 D.食物的腐败
学科网(北京)股份有限公司 s考点02 氧化还原反应相关概念的判断
7.(23-24高一上·北京市东城区·期末)下列反应中,水只作还原剂的是
A.
B.
C.
D.
8.(23-24高一上·山东日照·期末)下列说法正确的是
A.多数酸性氧化物能与水反应生成相应的酸
B.非金属元素从化合态变为游离态一定被氧化
C.电解质的强弱取决于其在水溶液中的导电能力
D.具有还原性的物质在氧化还原反应中一定作还原剂
9.(23-24高一上·浙江丽水·期末)关于化学反应:SO +2H S=3S↓+2H O,下列说法不正确的是
2 2 2
A.HS是还原剂 B.HO是还原产物
2 2
C.SO 是氧化剂 D.S既是氧化产物,又是还原产物
2
10.(23-24高一上·湖南衡阳·期末)神舟十三号载人飞船所用的燃料为液态的偏二甲肼(C HN,其中H
2 8 2
元素显+1价) 和四氧化二氮(N O),反应的化学方程式为C HN+2N O=3N ↑+2CO ↑+4H O↑。下列关于该
2 4 2 8 2 2 4 2 2 2
反应的说法中正确的是
A.C HN 是氧化剂 B.属于置换反应
2 8 2
C.N 既是氧化产物,又是还原产物 D.每转移1.6 mol e-,生成11.2L气体
2
考点03 氧化剂与还原剂
11.(23-24高一上·广东省广州市·期末)下列转化中,需要加入氧化剂才能实现的是
A. B. C. D.
12.(23-24高一上·湖北省十堰市·期末)实现下列物质间的转化,需要加入氧化剂的是
A. B.
C. D.
13.(23-24高一上·湖北省十堰市·期末)下列变化过程需要加入还原剂才能实现的是
A.KMnO →MnO B.SO →S C.Fe→Fe O D.Na→NaOH
4 2 2 3 4
14.(23-24高一上·安徽省皖北六校·期末)氧化还原反应是一类重要的化学反应,下列转化必须加入氧化
剂才能实现的是
A. B.
学科网(北京)股份有限公司 sC. D.
考点04 氧化还原反应的规律
15.(23-24高一上·广东省东莞市·期末)由于高温条件下能发生反应: (未配平),当
火灾现场存放有大量金属Mg时,不能用 而应用干燥的沙土灭火。下列说法不正确的是
A.该反应属于置换反应 B.由该反应可知,Mg的还原性强于C
C.氧化产物与还原产物之比为2:1 D.每生成 ,转移电子的物质的量为2mol
16.(23-24高一上·广东省广州市·期末)钛合金是具有耐腐蚀性的重要金属材料,金属钠在高温时与四氯
化钛反应可制取金属钛,高温反应的化学方程式为: 。下列说法不正确的是
A.Na在反应中被还原 B. 在反应中得到电子
C.Ti是还原产物 D.每生成24gTi,转移 电子
17.(23-24高一上·福建省福州市·期末) 是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中
可通过以下反应制得: 。下列说法正确的是
A. 发生还原反应 B. 在反应中作氧化剂
C.该反应中 体现氧化性 D.每生成2mol ,转移的电子数为
18.(23-24高一上·湖北省A9高中联盟·期末)关于反应NaSO+HSO =Na SO +S↓+SO ↑+HO,下列
2 2 3 2 4 2 4 2 2
说法错误的是
A.HSO 没有参与氧化还原反应
2 4
B.NaSO 既是氧化剂又是还原剂
2 2 3
C.氧化剂与还原剂的物质的量之比为1∶1
D.1 mol Na SO 发生反应,转移4 mol电子
2 2 3
19.(23-24高一上·河南省洛阳市·期末)“绿水青山就是金山银山”,除尘脱硫在环境保护中有着重要的
作用。双碱法脱硫过程如图所示。下列说法错误的是
A.过程I中,SO 表现出酸性氧化物的性质
2
B.过程Ⅱ中,0.5molO 可氧化
2
C.双碱法脱硫过程中,Ca(OH) 可以循环利用
2
D.总反应为
考点05 氧化还原反应的综合考查
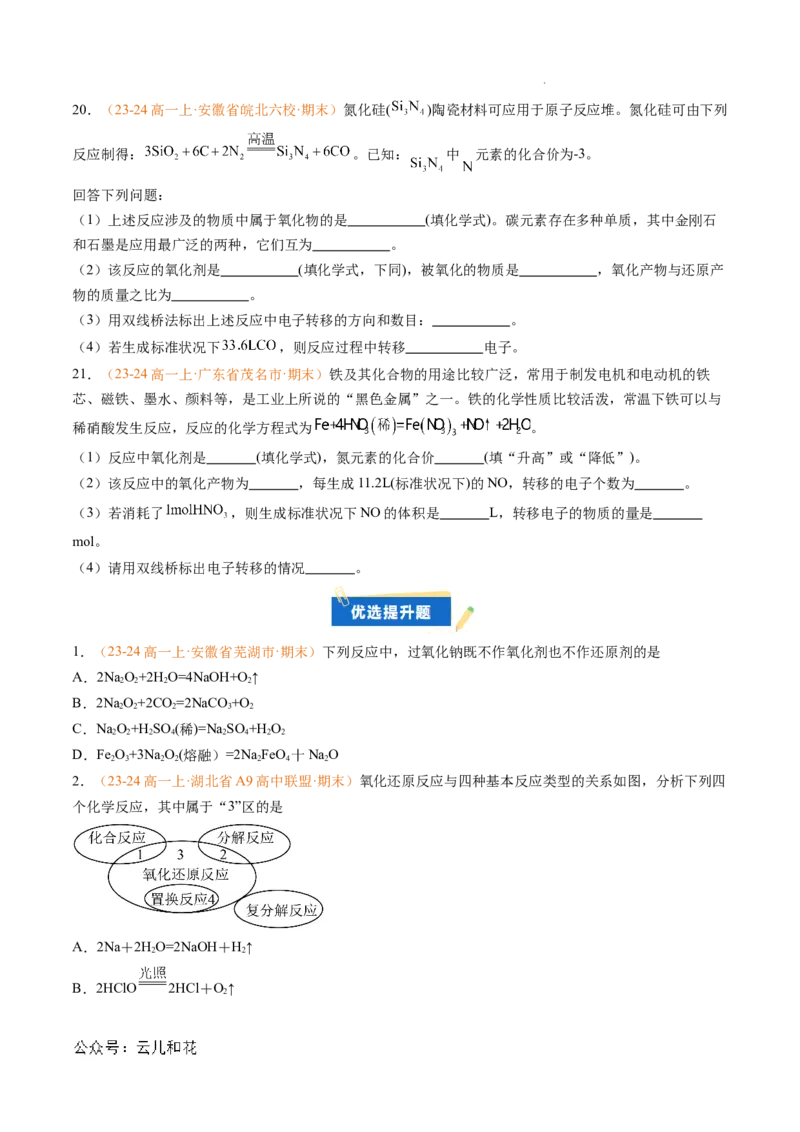
学科网(北京)股份有限公司 s20.(23-24高一上·安徽省皖北六校·期末)氮化硅( )陶瓷材料可应用于原子反应堆。氮化硅可由下列
反应制得: 。已知: 中 元素的化合价为-3。
回答下列问题:
(1)上述反应涉及的物质中属于氧化物的是 (填化学式)。碳元素存在多种单质,其中金刚石
和石墨是应用最广泛的两种,它们互为 。
(2)该反应的氧化剂是 (填化学式,下同),被氧化的物质是 ,氧化产物与还原产
物的质量之比为 。
(3)用双线桥法标出上述反应中电子转移的方向和数目: 。
(4)若生成标准状况下 ,则反应过程中转移 电子。
21.(23-24高一上·广东省茂名市·期末)铁及其化合物的用途比较广泛,常用于制发电机和电动机的铁
芯、磁铁、墨水、颜料等,是工业上所说的“黑色金属”之一。铁的化学性质比较活泼,常温下铁可以与
稀硝酸发生反应,反应的化学方程式为 。
(1)反应中氧化剂是 (填化学式),氮元素的化合价 (填“升高”或“降低”)。
(2)该反应中的氧化产物为 ,每生成11.2L(标准状况下)的NO,转移的电子个数为 。
(3)若消耗了 ,则生成标准状况下NO的体积是 L,转移电子的物质的量是
mol。
(4)请用双线桥标出电子转移的情况 。
1.(23-24高一上·安徽省芜湖市·期末)下列反应中,过氧化钠既不作氧化剂也不作还原剂的是
A.2NaO+2H O=4NaOH+O ↑
2 2 2 2
B.2NaO+2CO =2NaCO +O
2 2 2 3 2
C.NaO+H SO (稀)=Na SO +H O
2 2 2 4 2 4 2 2
D.Fe O+3Na O(熔融)=2Na FeO 十NaO
2 3 2 2 2 4 2
2.(23-24高一上·湖北省A9高中联盟·期末)氧化还原反应与四种基本反应类型的关系如图,分析下列四
个化学反应,其中属于“3”区的是
A.2Na+2HO=2NaOH+H↑
2 2
B.2HClO 2HCl+O↑
2
学科网(北京)股份有限公司 sC.4NH +5O 4NO+6HO
3 2 2
D.4Fe(OH) +O+2HO=4Fe(OH)
2 2 2 3
3.(23-24高一上·湖北省十堰市·期末) —铁纳米粉在现代电子工业上用途极为广泛,用赤铁矿石(含
、 ,也含有 、 、 等)制备纳米铁颗粒。下列说法正确的是
A.反应 中,氧化产物与还原产物的物质的量之比为1:2
B.实验室制氯气的方法为
C.少量 粉末与稀硫酸反应的离子方程式为
D.将 和 粉末溶于足量的稀盐酸中,加入高锰酸钾溶液,一段时间后,高锰酸钾溶液褪色,则使
高锰酸钾溶液褪色的离子仅为
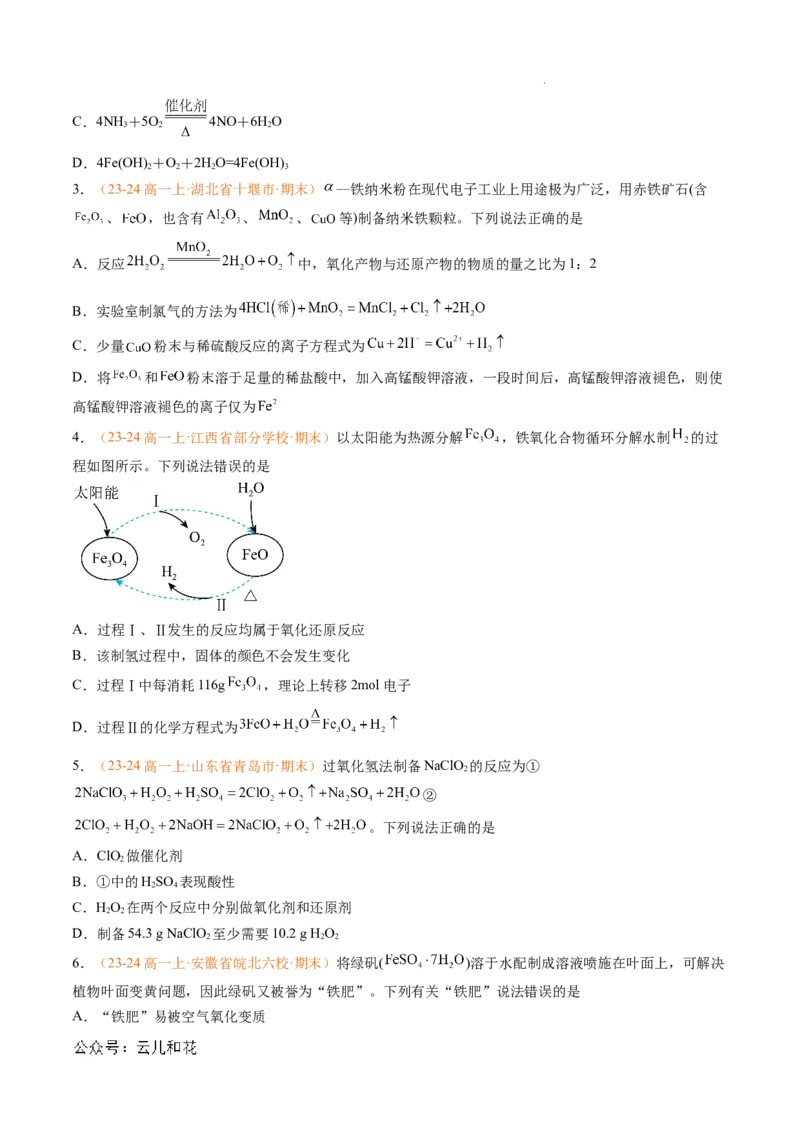
4.(23-24高一上·江西省部分学校·期末)以太阳能为热源分解 ,铁氧化合物循环分解水制 的过
程如图所示。下列说法错误的是
A.过程Ⅰ、Ⅱ发生的反应均属于氧化还原反应
B.该制氢过程中,固体的颜色不会发生变化
C.过程Ⅰ中每消耗116g ,理论上转移2mol电子
D.过程Ⅱ的化学方程式为
5.(23-24高一上·山东省青岛市·期末)过氧化氢法制备NaClO 的反应为①
2
②
。下列说法正确的是
A.ClO 做催化剂
2
B.①中的HSO 表现酸性
2 4
C.HO 在两个反应中分别做氧化剂和还原剂
2 2
D.制备54.3 g NaClO 至少需要10.2 g H O
2 2 2
6.(23-24高一上·安徽省皖北六校·期末)将绿矾( )溶于水配制成溶液喷施在叶面上,可解决
植物叶面变黄问题,因此绿矾又被誉为“铁肥”。下列有关“铁肥”说法错误的是
A.“铁肥”易被空气氧化变质
学科网(北京)股份有限公司 sB.可用 溶液检验“铁肥”是否发生变质
C.为保证“铁肥”的效果,可向配制后的溶液中加入少量铁粉
D. 的摩尔质量为
7.(23-24高一上·广东省东莞市·期末)方程式是世界通用的化学语言。下列方程式书写正确的是
A.钠和冷水反应:
B. 与浓盐酸制备 :
C.将碳酸钙加入过量盐酸中:
D.Fe在氯气中燃烧:
8.(23-24高一上·安徽省芜湖市·期末)废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH +完
4
全转化为N,该反应可表示为2NH ++3ClO-=N↑+3Cl-+2H++3H O。下列说法中,不正确的是
2 4 2 2
A.反应中氮元素被氧化,氯元素被还原
B.还原性NH +< Cl-
4
C.反应中每生成1 mol N ,转移6 mol电子
2
D.经此法处理过的废水不可以直接排放
9.(23-24高一上·湖北省荆门市·期末)分别是从海藻灰和智利硝石中提取碘的主要反应:
①
②
下列说法正确的是
A. 与 在一定条件下可生成
B.碘元素在反应(1)中被还原,在反应(2)中被氧化
C.氧化性:
D.反应①②中生成等量 时转移电子数为2:5
10.(23-24高一上·湖北省部分省级示范高中·期末)高铁酸钠 是一种新型绿色消毒剂,主要用
于饮用水的处理。工业上制备高铁酸钠的一种方法化学原理可以用离子方程式表示:
。下列说法正确的是
A. 能杀菌消毒,利用了其强还原性
B.每生成 ,转移电子为
C.离子方程式中涉及的元素都是短周期元素
D. 处理水时,既能杀菌消毒,生成的 胶体又能吸附水中的悬浮杂质
11.(23-24高一上·安徽省部分学校·期末)已知 某溶液(该溶液称为 )中仅含有两种溶质
和 ,且物质的量浓度依次为 和 ,向该溶液中投入 铁粉恰好完全反应,释放出
学科网(北京)股份有限公司 s的气体体积为 。下列叙述正确的是
A. 中 的物质的量为
B.
C.反应后所得溶液中氧化产物与还原产物的物质的量之比为
D.
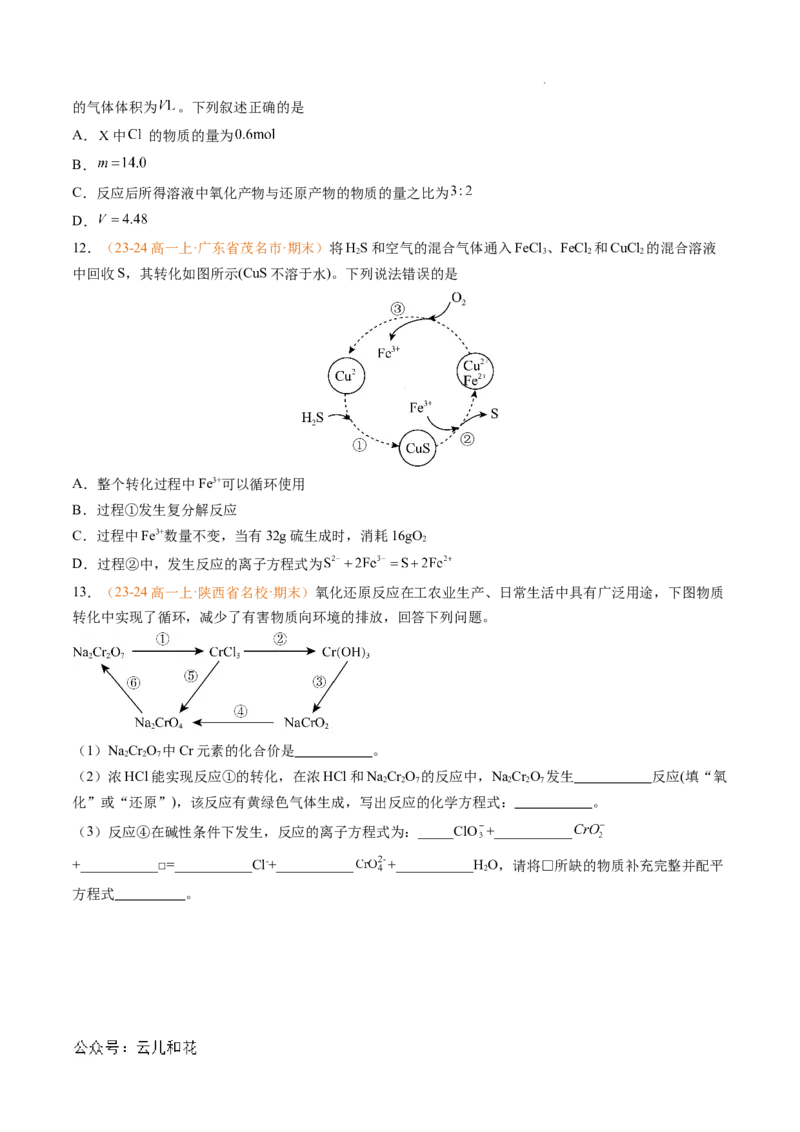
12.(23-24高一上·广东省茂名市·期末)将HS和空气的混合气体通入FeCl 、FeCl 和CuCl 的混合溶液
2 3 2 2
中回收S,其转化如图所示(CuS不溶于水)。下列说法错误的是
A.整个转化过程中Fe3+可以循环使用
B.过程①发生复分解反应
C.过程中Fe3+数量不变,当有32g硫生成时,消耗16gO
2
D.过程②中,发生反应的离子方程式为
13.(23-24高一上·陕西省名校·期末)氧化还原反应在工农业生产、日常生活中具有广泛用途,下图物质
转化中实现了循环,减少了有害物质向环境的排放,回答下列问题。
(1)NaCr O 中Cr元素的化合价是 。
2 2 7
(2)浓HCl能实现反应①的转化,在浓HCl和NaCr O 的反应中,NaCr O 发生 反应(填“氧
2 2 7 2 2 7
化”或“还原”),该反应有黄绿色气体生成,写出反应的化学方程式: 。
(3)反应④在碱性条件下发生,反应的离子方程式为:_____ClO +___________
+___________□=___________Cl-+___________ +___________H O,请将□所缺的物质补充完整并配平
2
方程式 。
学科网(北京)股份有限公司 s