文档内容
专题 05 物质的量
内容概览
考点01 物质的量与摩尔质量
考点02 气体摩尔体积与阿伏加德罗定律
考点03 物质的量浓度
考点04 一定物质的量浓度溶液的配制
考点05 有关阿伏加德罗常数的判断
考点01 物质的量与摩尔质量
1.(23-24高一上·福建莆田·期末)下列叙述错误的个数是
①摩尔是国际单位制中七个基本物理量之一
② 任何物质都含有约 个分子
③ 就是阿伏加德罗常数
④在标准状况下, 任何物质的体积均为
⑤ 的摩尔质量等于 分子的质量
⑥ 中含有 氢分子和 氧原子
A.①②④ B.①②③④ C.③⑤⑥ D.①②③④⑤⑥
【答案】D
【解析】①摩尔是物质的量的单位,物质的量是七个基本物理量之一,摩尔是七个基本物理量的单位之
一,故错误;
②物质不一定是由分子构成的,还可能是由原子或离子构成的,故错误;
③阿伏加德罗常数的单位为 ,阿伏加德罗常数用 表示,故错误;
④在标准状况下, 任何气体的体积约为 ,故错误;
⑤摩尔质量的单位为 ,质量的单位是 , 的摩尔质量和 分子的质量在数值上相等,故
错误;
⑥ 中含有 氢原子和 氧原子,没有氢分子,故错误。
故选D;
2.(23-24高一上·江苏宿迁·期末)下列叙述错误的是
A.物质的量是国际单位制中七个基本物理量之一
B.0.016kg 含有约6.02×1023个氧原子
C.单位物质的量的任何物质都含有约6.02×1023个原子
学科网(北京)股份有限公司D.对两种相同物质的量的气体,处于相同温度下,压强越大体积越小
【答案】C
【解析】A.物质的量是国际单位制中7个基本物理量之一,故A正确;
B.0.016kg 的物质的量是1mol,含有约6.02×1023个氧原子,故B正确;
C.并不是1mol任何物质都含有约6.02×1023个原子。如1molH 应该含有2×6.02×1023个氢原子并不是1mol
2
任何物质都含有约6.02×1023个原子。如1molH 应该含有2×6.02×1023个氢原子,故C错误;
2
D.对两种相同物质的量的气体,当温度相同时,压强越大,气体摩尔体积的数值越小,则气体的体积越
小,故D正确。
答案选C。
考点02 气体摩尔体积与阿伏加德罗定律
3.(23-24高一上·安徽省芜湖市·期末)下列选项中与17gNH 所含原子数相等的是
3
A.64gO B.2molCO C.22.4LCO D.2gH
2 2 2
【答案】A
【分析】17gNH 的物质的量为1mol,所含原子数为4N 。
3 A
【解析】A.64gO 的物质的量为2mol,所含原子数为4N ,A符合题意;
2 A
B.2molCO 中,所含原子数为6N ,B不符合题意;
2 A
C.22.4LCO的密度未知,无法求出其物质的量,也就无法求出其所含原子数,C不符合题意;
D.2gH 的物质的量为1mol,所含原子数为2N ,D不符合题意;
2 A
故选A。
4.(23-24高一上·安徽省芜湖市·期末)下列有关物质相关量的说法正确的是
A.同温同压下, 和 的密度相同
B. 氩气含有的质子数为
C.同温同压下,等质量的 和 的电子数相同
D.质量相同的 和 (重水)所含的质子数相同
【答案】C
【解析】A.由 可知,同温同压下,气体的密度之比等于其摩尔质量之比,故A项错误;
B.非标准状态下,22.4L氩气的物质的量不一定为1mol,则含有的质子数不一定为18N ,故B项错误;
A
C.等质量的O 和O 中所含氧原子数目相同,因此二者所含电子数相同,故C项正确;
2 3
D. 1molH O和1molD O均含有10个质子,M(H O)=18g/mol,M(D O)=20g/mol,质量相同的HO和DO
2 2 2 2 2 2
的物质的量不同,则质子数不同,故D项错误;
故本题选C。
5.(23-24高一上·湖北·期末)下列有关气体的说法正确的是
A.在非标准状况下,气体的摩尔体积不可能是22.4L/mol
学科网(北京)股份有限公司B.1molHCl气体溶于1LHO中,所得溶液物质的量浓度为1mol/L
2
C.在同温同容条件下,等质量的O 和SO 的压强比为2:1
2 2
D.在同温同压条件下,CO和CO 的密度比为11:7
2
【答案】C
【解析】A.影响气体物质的量的因素有温度、压强,因此在非标准状况下,气体的摩尔体积也可能是
22.4L/mol,A项错误;
B.1molHCl气体溶于1LHO中,所得溶液的体积不是1L,溶液物质的量浓度不是1mol/L,B项错误;
2
C.据PV=nRT可知,在同温同容条件下,气体的压强比等于物质的量之比,等质量的O 和SO 的压强比
2 2
为2:1,C项正确;
D.据PV=nRT有, ,进一步变化有: ,因此在同温、同压条件下,气体的密
度比等于摩尔质量之比,CO和CO 的密度比为7:11,故D错误;
2
故答案选C。
考点03 物质的量浓度
6.(23-24高一上·福建省福州市·期末)下列溶液中 浓度最大的是
A.50mL 的 溶液 B.50mL 的 溶液
C.100mL 的 溶液 D.100mL 的 溶液
【答案】B
【解析】 浓度大小与溶液体积无关, 的 溶液中 , 的 溶液中
, 的 溶液中 , 的 溶液中
,故 的 溶液 浓度最大,答案选B。
7.(23-24高一上·安徽省芜湖市·期末)下列溶液中 的物质的量浓度与其他三项不同的是
A. 的 溶液 B. 的 溶液
C. 的 溶液 D. 的
【答案】C
【解析】A.10mL0.30mol⋅L−1的NaCl溶液,含有Cl-物质的量浓度为:0.30mol⋅L−1;
B.20mL0.15mol⋅L−1的CaCl 溶液,含有Cl-物质的量浓度为:0.15mol⋅L−1×2=0.30mol⋅L−1;
2
C.30mL0.10mol⋅L−1的MgCl 溶液,含有Cl-物质的量浓度为:0.10mol⋅L−1×2=0.20mol⋅L−1;
2
D.40mL0.10mol⋅L−1的AlCl ,含有Cl-物质的量浓度为:0.10mol⋅L−1×3=0.30mol⋅L−1;
3
则30mL0.10mol⋅L−1的MgCl 溶液中的氯离子的物质的量浓度与其他三项不同,故本题选C。
2
考点04 一定物质的量浓度溶液的配制
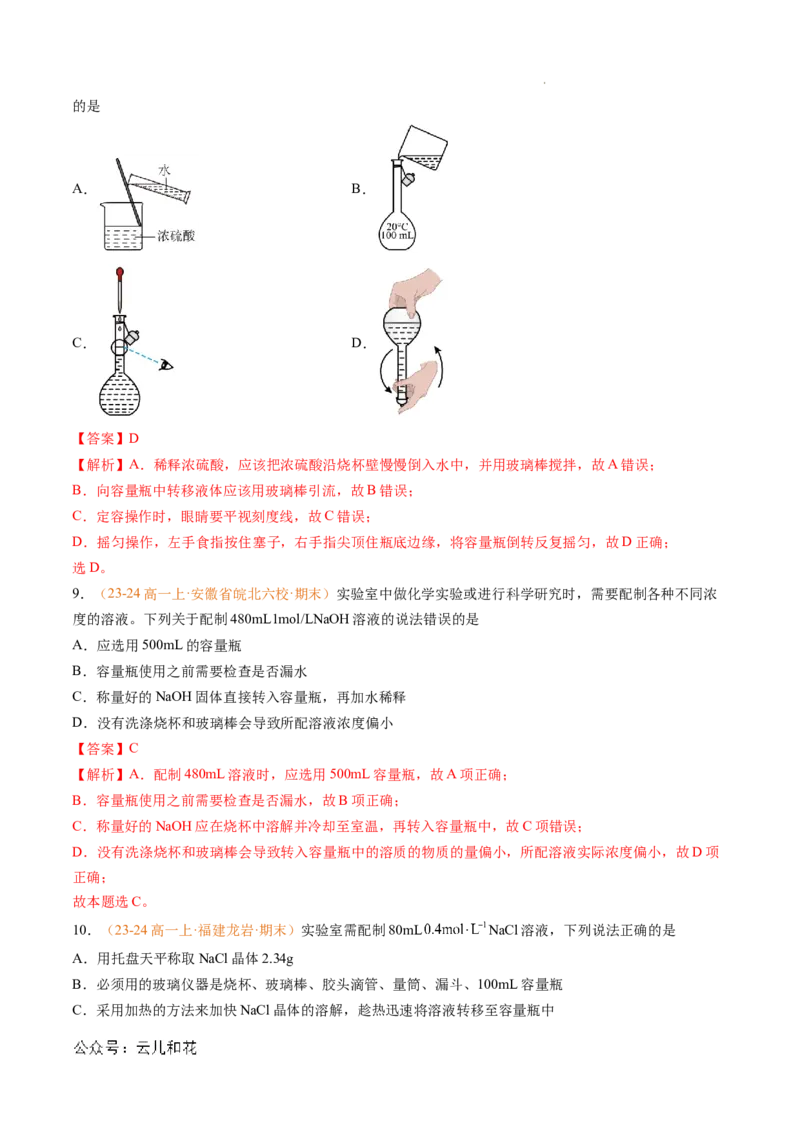
8.(23-24高一上·福建省福州市·期末)现需配制250mL 溶液,下列有关实验操作正确
学科网(北京)股份有限公司的是
A. B.
C. D.
【答案】D
【解析】A.稀释浓硫酸,应该把浓硫酸沿烧杯壁慢慢倒入水中,并用玻璃棒搅拌,故A错误;
B.向容量瓶中转移液体应该用玻璃棒引流,故B错误;
C.定容操作时,眼睛要平视刻度线,故C错误;
D.摇匀操作,左手食指按住塞子,右手指尖顶住瓶底边缘,将容量瓶倒转反复摇匀,故D正确;
选D。
9.(23-24高一上·安徽省皖北六校·期末)实验室中做化学实验或进行科学研究时,需要配制各种不同浓
度的溶液。下列关于配制480mL1mol/LNaOH溶液的说法错误的是
A.应选用500mL的容量瓶
B.容量瓶使用之前需要检查是否漏水
C.称量好的NaOH固体直接转入容量瓶,再加水稀释
D.没有洗涤烧杯和玻璃棒会导致所配溶液浓度偏小
【答案】C
【解析】A.配制480mL溶液时,应选用500mL容量瓶,故A项正确;
B.容量瓶使用之前需要检查是否漏水,故B项正确;
C.称量好的NaOH应在烧杯中溶解并冷却至室温,再转入容量瓶中,故C项错误;
D.没有洗涤烧杯和玻璃棒会导致转入容量瓶中的溶质的物质的量偏小,所配溶液实际浓度偏小,故D项
正确;
故本题选C。
10.(23-24高一上·福建龙岩·期末)实验室需配制80mL NaCl溶液,下列说法正确的是
A.用托盘天平称取NaCl晶体2.34g
B.必须用的玻璃仪器是烧杯、玻璃棒、胶头滴管、量筒、漏斗、100mL容量瓶
C.采用加热的方法来加快NaCl晶体的溶解,趁热迅速将溶液转移至容量瓶中
学科网(北京)股份有限公司D.定容时仰视会造成所配制溶液的物质的量浓度偏小
【答案】D
【解析】A.配制80mL NaCl溶液,需要选用100 mL容量瓶,所需称量的碳酸钠晶体的质量为
m=cVM=0.4mol/L×0.1L×58.5g/mol=2.34g,用托盘天平称取NaCl晶体2.3g,故A错误;
B.配制一定物质的量浓度的溶液,需要用托盘天平称量溶质的质量,溶质在烧杯中进行溶解,玻璃棒不
断搅拌,冷却到室温后,用玻璃棒把溶液转移到500 mL容量瓶,并洗涤烧杯和玻璃棒2-3次,洗涤液也转
移进容量瓶内,加水至刻度线1-2 cm时,用胶头滴管滴加,最后定容,所以配制操作必需的玻璃仪器是烧
杯、玻璃棒、胶头滴管、500 mL容量瓶,故B错误;
C.热的溶液转移到容量瓶内,待溶液冷却到室温后,根据“热胀冷缩”规律,溶液的体积偏小,造成所
配溶液的浓度偏大,故C错误;
D.定容时仰视容量瓶刻度线,造成溶液的体积偏大,会造成所配制溶液的物质的量浓度偏小,故D正
确;
故选D。
11.(23-24高一上·北京市朝阳区·期末)配制 溶液,下列说法不正确的是
A.将称量好的 固体放入 中,加入适量蒸馏水,使之全部溶解
B.将蒸馏水注入容量瓶,当液面离刻度线 时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线
相切
C.若俯视容量瓶的刻度线,则所配 溶液的浓度大于
D.摇匀后发现液面低于刻度线,无须继续加水,直接将所配溶液倒入试剂瓶中,并贴好标签
【答案】A
【解析】A.称量好的 固体放入烧杯中加入适量蒸馏水,使之全部溶解,A符合题意;
B.注入蒸馏水到容量瓶中至液面离刻度线 时改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相
切,B不符合题意;
C.若俯视容量瓶的刻度线,导致容量瓶中溶液的实际体积小于100mL,由 可知所配 溶液的浓
度大于 ,C不符合题意;
D.摇匀后发现液面低于刻度线是因为溶液残留在橡皮塞与瓶口的缝隙中,无须继续加水,直接将所配溶
液倒入试剂瓶中,并贴好标签,D不符合题意;
故选A。
12.(23-24高一上·安徽省芜湖市·期末)实验室配制 的 溶液,回答下列问题。
(1)用托盘天平称取胆矾晶体的质量为 g。
学科网(北京)股份有限公司(2)所需仪器除药匙、烧杯、托盘天平、量筒、胶头滴管、玻璃棒外,还需要 (填仪器名称)。
(3)实验步骤如下,请补全操作(填操作的图示序号) (计算→称量→溶解
→_______→_______→_______→摇匀、装瓶、贴标签)。
(4)在配制过程中,如果其他操作都正确,而没有洗涤烧杯和玻璃棒,会使配制结果 (填“偏大”
“偏小”或“不变”)。
(5)定容时,若不慎加水超过了刻度线,处理方式是 。
【答案】(1)12.5
(2) 容量瓶
(3)B、C、A
(4)偏小
(5)重新配制
【解析】(1)配制460mL硫酸铜溶液,需要500mL的容量瓶,则用托盘天平称取胆矾晶体的质量为:
500×10-3L×0.1mol/L×250g/mol=12.5g,故答案为:12.5;
(2)所需仪器除药匙、烧杯、托盘天平、量筒、胶头滴管、玻璃棒、500mL容量瓶,故答案为:500mL
容量瓶;
(3)实验步骤为计算→称量→溶解→移液→洗涤→定容→摇匀、装瓶、贴标签,故答案为:B、C、A;
(4)在配制过程中,如果其他操作都正确,而没有洗涤烧杯和玻璃棒,则溶质的物质的量减小,配制硫
酸铜溶液的物质的量浓度偏小,故答案为:偏小;
(5)定容时,若不慎加水超过了刻度线,需要重新配制,故答案为:重新配制。
13.(23-24高一上·广东省广州市·期末)学习小组探究硫酸在双氧水与铜的反应中的作用。
(1)配制 的稀硫酸
(a)配制 的稀硫酸,需要 硫酸的体积为 mL。
(b)配制溶液时,需要的仪器有100mL容量瓶、玻璃棒、胶头滴管、 (从下图中选择,写出名
称)。
(c)下列关于100mL容量瓶的操作,正确的是 。
学科网(北京)股份有限公司(d)用胶头滴管滴加蒸馏水至刻度线时,某同学仰视容量瓶上的刻度线,最后配成的溶液中 的实际浓
度比所要求的 (填“偏大”、“偏小”或“不变”)。
(2)开展实验探究
该学习小组进行如下图所示的实验:
(a)写出②中Cu溶解的离子方程式 。
(b)比较实验①和②,从氧化还原角度说明 的作用是 。
【答案】(1)27.8 烧杯、量筒 CD 偏小
(2) 增强 的氧化性
【解析】(1)(a)根据稀释前后溶质物质的量不变,即100×10-3 L×5.0mol/L=18mol/L×V,
V=0.0278L=27.8mL,故答案为:27.8;
(b)配制溶液时,需要的仪器有100mL容量瓶、玻璃棒、胶头滴管、烧杯、量筒,故答案为:烧杯、量
筒;
(c)A.摇匀要在定容后,且要盖紧玻璃塞上下颠倒摇匀,故A项错误;
B.定容时,视线应该与容量瓶凹液面最低处相平,故B项错误;
C.转移时,应该用玻璃棒引流,玻璃棒下端接触容量瓶刻度线下方,故C项正确;
D.摇匀时要一只手托住瓶底,另一只手按紧玻璃塞,反复上下颠倒,故D项正确;
故答案为:CD;
(d)仰视容量瓶上的刻度线,导致所加入的水量偏大,最后配成的溶液中HSO 的实际浓度比所要求的偏
2 4
小,故答案为:偏小;
(2)(a)过氧化氢、铜片、稀硫酸反应生成硫酸铜和水,离子方程式为:Cu+H O+2H+=Cu2++2H O,故答
2 2 2
案为:Cu+H O+2H+=Cu2++2H O;
2 2 2
(b)结合实验①和②,从氧化还原角度的说明H+的作用是增强HO 的氧化性,故答案为:增强HO 的氧化
2 2 2 2
性。
考点05 有关阿伏加德罗常数的判断
学科网(北京)股份有限公司14.(23-24高一上·北京市朝阳区·期末) 为阿伏加德罗常数的值。下列说法正确的是
A. 的摩尔质量是
B. 中含有氢原子的数目为
C.常温常压下, 中含有氯分子的数目为
D. 溶液中,含有 的数目为
【答案】B
【解析】A.摩尔质量的单位为g/mol,A错误;
B. 即1mol水中含有氢原子的数目为 ,B正确;
C.非标况, 的气体体积不能计算物质的量,C错误;
D.未告知溶液的体积,不能计算溶液中离子数目,D错误;
故选B。
15.(23-24高一上·广东省茂名市·期末)下列说法不正确的是
A. 的 的质量为
B.物质的量是国际单位中七个基本物理量之一
C. 中含有 个原子
D.在标准状况下, 的气体摩尔体积为
【答案】A
【解析】A. 的 的质量为 ,A错误;
B.物质的量是国际单位制中七个基本物理量之一,B正确;
C. 中含有1molO原子和0.5molS原子,则 中含有 个原子,C正确;
D.在标准状况下,任何气体的气体摩尔体积都为 ,D正确;
故选A。
16.(23-24高一上·福建省福州市·期末)设 为阿伏加德罗常数的值,下列说法错误的是
A.1.8g 的质子数为
B.14g 的分子数为
C. 溶液中, 的数目为
D.标准状况下,22.4L 的电子数为
【答案】C
【解析】A. 为0.1mol,每个水分子中含有10个质子,则总含质子数为 ,故A正确;
B.14g 为 ,因此0.5molCO含有的分子数为 ,故B正确;
学科网(北京)股份有限公司C.未说明溶液体积,无法计算硫酸根数目,故C错误;
D.标准状况下,22.4L 为1mol,每个甲烷分子中含有10个电子,则总含电子数为 ,故D正确;
故答案选C。
17.(23-24高一上·安徽省皖北六校·期末)用 表示阿伏加德罗常数的值,下列叙述正确的是
A. 由 与 组成的混合气体中含有的原子数为
B.1mol 发生反应,转移电子数一定为
C.标准状况下,11.2L 含有分子数为
D. 的 溶液中含 数为
【答案】A
【解析】A. 和 的混合物可看作氧原子的集合体, ,即原子数目为 ,A项
正确;
B.若与水或碱反应,1mol 发生反应,转移电子数为1mol,B项错误;
C.标准状况下, 为液体,不能用 进行计算,C项错误;
D.缺少体积,无法计算出 数,D项错误;
故答案为:A。
18.(23-24高一上·安徽省部分学校·期末)设N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.常温常压下,18g H O中含有的电子数为9N
2 A
B.100mL 1mol·L-1KClO 溶液中含有的Cl-数为0.1N
3 A
C.7.1gCl 与足量铁在加热条件下完全反应时转移的电子数为0.3N
2 A
D.标准状况下,5.6LCO和O 的混合气体中含有的原子数为0.5N
2 A
【答案】D
【解析】A.常温常压下,18gHO的物质的量是 ,而1个HO分子含有10个电子,故
2 2
1molH O中所含电子总数为10 N ,A项错误;
2 A
B.KClO 溶液中含有K+和ClO ,不含Cl-,B项错误;
3
C.7.1gCl 的物质的量为 ,0.1molCl 与足量铁完全反应生成氯化铁,生成0.2mol Cl-,转
2 2
移的电子数为0.2 N ,C项错误;
A
D.标准状况下,5.6LCO和O 的所含的原子数为: ×2×N mol-1=0.5N ,D项正确;
2 A A
答案选D。
学科网(北京)股份有限公司1.(23-24高一上·安徽省合肥市六校联盟·期末)用 表示阿伏加德罗常数的值,下列说法正确的是
A.13gZn与足量稀 完全反应,生成的 所含原子数目为
B.0.5mol/L 溶液中含有 和 总物质的量为1mol
C. 气体溶于水,所得溶液中含有的氯化氢分子为
D. 的铁与足量 反应失去电子数为
【答案】A
【解析】A.13gZn与足量稀 发生反应Zn+H SO =ZnSO +H ,生成的 所含原子数目为
2 4 4 2
,故A正确;
B.没有明确溶液体积,不能计算0.5mol/L 溶液中含有 和 总物质的量,故B错误;
C. 气体溶于水,氯化氢完全电离为氢离子和氯离子,所得溶液中不含氯化氢分子,故C错
误;
D. 的铁与足量 反应生成1molFeCl ,铁元素化合价由0升高为+3,失去电子数为 ,故D错
3
误;
选A。
2.(23-24高一上·福建龙岩·期末)监测 含量是否达到排放标准的反应原理是
. 表示阿伏加德罗常数的值,下列说法正确的是
A.0.1mol 固体中所含离子总数为
B.25℃时, 的HCl溶液中含有 的数目为
C.17g 中含有的原子数目为
D.2.24L 中含有的分子数目为
【答案】C
【解析】A.BaCl 是离子化合物,0.1molBaCl 含0.1molBa2+和0.2molCl-,所含离子总数为0.3N ,故A错
2 2 A
误;
B.缺少溶液的体积,无法计算溶液中的数目,故B错误;
C.17gHO 物质的量为0.5mol,每个HO 分子中含4个原子,共含有的原子数目为2N ,故C正确;
2 2 2 2 A
D.没有指明标况,2.24L的数据无法使用,故D错误;
故选C。
3.(23-24高一上·河南省开封市联考·期末)下列说法中,正确的是
A. 的摩尔质量是
学科网(北京)股份有限公司B.标准状况下, 的体积是
C. 中含有的氧原子数约为
D. 溶液中 是
【答案】D
【解析】A.金属钠的摩尔质量为23g/mol,故A错误;
B.标准状况下,水为液态,无法计算1mol水的体积,故B错误;
C.二氧化碳分子中含有2个氧原子,则44g二氧化碳中含有的氧原子数约为 ×2×6.02×1023mol—
1=2×6.02×1023,故C错误;
D.0.5mol/L碳酸钠溶液中钠离子的浓度为0.5mol/L×2=1mol/L,故D正确;
故选D。
4.(23-24高一上·湖北省A9高中联盟·期末)N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.11.2LNH 含有的分子数目为0.5N
3 A
B.0.1mol/LNaCl溶液中含有Na+数目为0.1N
A
C.1molCl 和铁在一定条件下完全反应,转移电子数目为3N
2 A
D.1 mol H O+中含有电子数为10 N
3 A
【答案】D
【解析】A.未说明11.2LNH 所处的温度和压强,无法计算11.2LNH 含有的分子数目,A错误;
3 3
B.未说明0.1mol/LNaCl溶液的体积,无法计算含有Na+的数目,B错误;
C.1molCl 和铁在一定条件下完全反应生成FeCl ,Cl元素由0价下降到-1价,转移电子数目为2N ,C错
2 3 A
误;
D.1个HO+含10个电子,则1 mol H O+中含有电子数为10 N ,D正确;
3 3 A
故选D。
5.(23-24高一上·北京市东城区·期末) 为阿伏加德罗常数的值。下列说法不正确的是
A. 中氢原子数目为
B.常温常压下, 中氮分子数目为
C. 溶液中 数目为
D. 铝与足量盐酸完全反应,转移的电子数目为
【答案】B
【解析】A.0.5molCH 中氢原子数目为:0.5mol×4×N mol-1=2N ,故A正确;
4 A A
B.常温常压下,V 大于22.4L/mol,常温常压下,2.24LN 中氮分子数目小于0.1N ,故B错误;
m 2 A
C.2L0.1mol⋅L-1NaSO 溶液中Na+数目为:2L×0.2mol/L×N mol-1=0.4N ,故C正确;
2 4 A A
D.2.7g铝物质的量为: ,与足量盐酸完全反应生成0.1mol铝离子,转移的电子数目为
学科网(北京)股份有限公司0.3N ,故D正确;
A
故选:B。
6.(23-24高一上·广东省广州市·期末)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中一定含有
B. 中含有 的数目为
C. 中含有共价键的数目为
D. 溶解在1L水中,所得溶液中溶质的物质的量浓度为
【答案】B
【解析】A.没有标准状况,无法计算其物质的量,故A错误;
B.1个KSO 中含有2个K+,故 中含有 的数目为 ,故B正确;
2 4
C. 的物质的量为1mol,故 中含有共价键的数目为2 ,故C错误;
D.物质的量浓度应该是溶质的物质的量与溶液体积的比值,而题目中1L为水的体积,不能确定溶液的体
积,故无法计算其物质的量溶度,故D错误;
故选B。
7.(23-24高一上·湖南省名校联考联合体·期末)设 为阿伏加德罗常数的值,下列说法正确的是
A. 溶于适量水中,所得溶液中 和 微粒总数为
B. 的盐酸中含有的氯化氢分子数为
C.常温常压下, 氘气 含有的中子数为
D.已知 ,如果有 参加反应,则由水还原的 分子数目为
【答案】C
【解析】A. 氯气的物质的量为 ,含氯原子数共为 ,氯气和水的反应为可逆反应,溶液中含
氯微粒为: 和 ,故 少于 ,A错误;
B. 是强酸,在水中完全电离,溶液中无氯化氢分子,B错误;
C.1个氘原子 含有1个中子, 氘气 的物质的量为 ,含有的中子数为 ,C正确;
D.根据反应 可知,当有 水参加反应时,消耗
,由于 中 元素发生了歧化反应,故由水还原的 分子数小于 ,D错误;
本题选C。
学科网(北京)股份有限公司8.(23-24高一上·湖北省A9高中联盟·期末)下列有关气体的说法正确的是
A.在非标准状况下,气体的摩尔体积不可能是22.4L/mol
B.1molHCl气体溶于1LHO中,所得溶液物质的量浓度为1mol/L
2
C.在同温同容条件下,等质量的O 和SO 的压强比为2:1
2 2
D.在同温同压条件下,CO和CO 的密度比为11:7
2
【答案】C
【解析】A.影响气体物质的量的因素有温度、压强,因此在非标准状况下,气体的摩尔体积也可能是
22.4L/mol,A项错误;
B.1molHCl气体溶于1LHO中,所得溶液的体积不是1L,溶液物质的量浓度不是1mol/L,B项错误;
2
C.据PV=nRT可知,在同温同容条件下,气体的压强比等于物质的量之比,等质量的O 和SO 的压强比
2 2
为2:1,C项正确;
D.据PV=nRT有, ,进一步变化有: ,因此在同温、同压条件下,气体的密
度比等于摩尔质量之比,CO和CO 的密度比为7:11,故D错误;
2
故答案选C。
9.(23-24高一上·北京市东城区·期末)配制 溶液,某同学的实验记录如下。
Ⅰ.将称量好的 固体放入烧杯中,用适量蒸馏水溶解。
Ⅱ.将烧杯中的溶液注入 容量瓶,再用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入
容量瓶。
Ⅲ.将蒸馏水注入容量瓶,当液面离容量瓶颈部的刻度线 时,改用胶头滴管滴加蒸馏水,至溶液的
凹液面与刻度线相切。
Ⅳ.盖好瓶塞,反复上下颠倒,摇匀。
下列是该同学的实验分析,其中不正确的是
A.步骤Ⅰ中称量的 固体为
B.步骤Ⅰ和Ⅱ用到同一支玻璃棒,其作用分别是搅拌和引流
C.步骤Ⅱ中洗涤液不慎酒到容量瓶外,则配成的溶液中 的实际浓度比所要求的小
D.步骤Ⅳ摇匀后,发现容量瓶中液面比刻度线低,应该再滴加少量蒸馏水
【答案】D
【解析】A.配制100mL溶液需选用100mL容量瓶且计算时按所选容量瓶规格计算, 100mL 1.00mol/L
NaCl溶液需要NaCl的物质的量为1.00mol/L×0.1L=0.1mol,质量为0.1mol×58.5g/mol=5.85g,故A正确;
B.步骤Ⅰ中将称好的NaCl固体放入烧杯中,加入适量蒸馏水,此步骤玻璃棒作用是搅拌,加速溶解,步
骤Ⅱ是移液和洗涤,需要用玻璃棒引流,故B正确;
C.步骤Ⅱ中洗涤液不慎酒到容量瓶外,则溶质偏少,所配制溶液浓度偏低,故C正确;
D.步骤Ⅳ摇匀后,发现容量瓶中液面比刻度线低,若再滴加少量蒸馏水,会导致所配制溶液浓度偏低,
故D错误;
故选D。
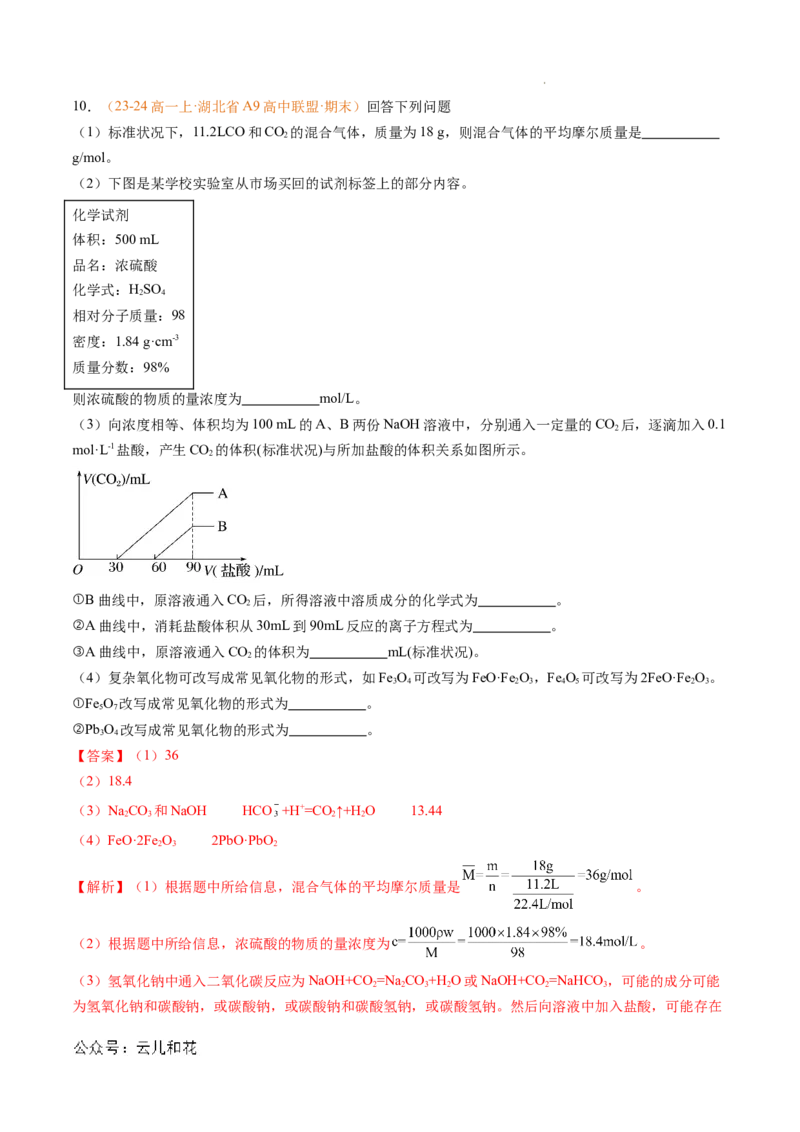
学科网(北京)股份有限公司10.(23-24高一上·湖北省A9高中联盟·期末)回答下列问题
(1)标准状况下,11.2LCO和CO 的混合气体,质量为18 g,则混合气体的平均摩尔质量是
2
g/mol。
(2)下图是某学校实验室从市场买回的试剂标签上的部分内容。
化学试剂
体积:500 mL
品名:浓硫酸
化学式:HSO
2 4
相对分子质量:98
密度:1.84 g·cm-3
质量分数:98%
则浓硫酸的物质的量浓度为 mol/L。
(3)向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO 后,逐滴加入0.1
2
mol·L-1盐酸,产生CO 的体积(标准状况)与所加盐酸的体积关系如图所示。
2
①B曲线中,原溶液通入CO 后,所得溶液中溶质成分的化学式为 。
2
②A曲线中,消耗盐酸体积从30mL到90mL反应的离子方程式为 。
③A曲线中,原溶液通入CO 的体积为 mL(标准状况)。
2
(4)复杂氧化物可改写成常见氧化物的形式,如Fe O 可改写为FeO·Fe O,Fe O 可改写为2FeO·Fe O。
3 4 2 3 4 5 2 3
①Fe O 改写成常见氧化物的形式为 。
5 7
②Pb O 改写成常见氧化物的形式为 。
3 4
【答案】(1)36
(2)18.4
(3)NaCO 和NaOH HCO +H+=CO ↑+H O 13.44
2 3 2 2
(4)FeO·2Fe O 2PbO·PbO
2 3 2
【解析】(1)根据题中所给信息,混合气体的平均摩尔质量是 。
(2)根据题中所给信息,浓硫酸的物质的量浓度为 。
(3)氢氧化钠中通入二氧化碳反应为NaOH+CO =Na CO+H O或NaOH+CO =NaHCO,可能的成分可能
2 2 3 2 2 3
为氢氧化钠和碳酸钠,或碳酸钠,或碳酸钠和碳酸氢钠,或碳酸氢钠。然后向溶液中加入盐酸,可能存在
学科网(北京)股份有限公司的反应为:NaOH+HCl=NaCl+H O;NaCO+HCl=NaCl+NaHCO ;NaHCO +HCl=NaCl+H O+CO↑。分析
2 2 3 3 3 2 2
若只含有碳酸钠,则前后两个阶段消耗的盐酸的量相等,若前者消耗盐酸的量多,则溶液成分为氢氧化钠
和碳酸钠,若后者消耗的盐酸的量多,则溶质的成分为碳酸钠和碳酸氢钠。所以A为碳酸钠和碳酸氢钠,
B为氢氧化钠和碳酸钠;
①根据分析可知,B曲线中,原溶液通入CO 后,所得溶液中溶质成分的化学式为NaCO 和NaOH;
2 2 3
②据分析可知,A曲线中,消耗盐酸体积从30mL到90mL反应的离子方程式为HCO +H+=CO ↑+H O;
2 2
③A曲线中,原溶液通入CO 的体积与A曲线最终产生的CO 体积相等,消耗盐酸体积从30mL到90mL
2 2
反应的离子方程式为:HCO +H+=CO ↑+H O,n(CO)=n(HCl)=
2 2 2
0.06L×0.1mol/L=0.006mol,V(CO )=0.006mol×22.4×103mL/mol=13.44mL。
2
(4)改写后的化学和原化学式原子数相等,
①铁元素常见的价态为+2、+3价,因此Fe O 改写成常见氧化物的形式为FeO·2Fe O;
5 7 2 3
②Pb O 中Pb有+2、+4价,Pb O 改写成常见氧化物的形式为2PbO·PbO。
3 4 3 4 2
11.(23-24高一上·安徽省部分学校·期末)物质的量在实验与科研中应用广泛。请回答下列问题:
(1)实验室欲用 的浓硫酸配制 稀硫酸 。
①下列操作正确的是 (填序号)。
操
作
选
项
②用量筒量取浓硫酸的体积为 。
③配制溶液的过程中,其他操作都正确,下列不当操作对所配溶液浓度的影响:
用量筒量取浓硫酸时俯视读数: (填“偏大”“偏小”或“无影响”,下同)。
稀释浓硫酸时,未冷却到室温即转移到容量瓶中: 。
将量取浓硫酸后的量筒进行洗涤,并将洗涤液转移到容量瓶中: 。
(2)室温下测得 的密度为 ,则室温下 的气体摩尔体积为 (用含 的代
数式表示)。
(3)为测定 溶液的浓度,某同学设计了如下实验方案。
实验原理: 。
学科网(北京)股份有限公司实验步骤:
ⅰ.按图安装装置(夹持仪器略去),并检查装置气密性;
ⅱ.在各仪器中加入图示试剂;
ⅲ.调整 中两液面使其相平,使 中液面保持在0或略低于0刻度位置,读数并记录;
ⅳ.将 液全部滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
ⅴ.待体系恢复到室温,移动 管,保持 中两液面相平,读数并记录、处理数据。
①步骤ⅲ需“调整 中两液面使其相平”的原因是 。
②将实验过程中测得的数据转化为 的质量时,其质量为 ,则 为
(列出计算式)。
③有同学认为用同样的装置和方法不能测定 溶液的浓度,其原因为 。
【答案】(1)a 6.8 小 大 大
(2)
(3)保持C、D中的压强与大气压相同,保证所测氢气的体积准确
由于硫酸镁不能与锌反应,故不能用此方法测定硫酸镁溶液的浓度
【分析】测定 溶液浓度的实验中,先发生反应 ,剩余的锌继续与稀硫酸反
应, ,通过装置D和E测定生成氢气的体积,由此可计算得到与稀硫酸反应的
锌的质量,参与反应的锌的总质量减去与稀硫酸反应的锌的质量,即为与硫酸铜反应的锌的质量,由此可
知参与反应的硫酸铜的物质的量,继而计算得到硫酸铜的浓度。
【解析】(1)配制稀硫酸溶液时,正确的操作是;
a.转移过程:用玻璃棒引流,a正确;
b.未定容前不需要摇匀,更不能用手指堵住容量瓶的瓶口摇匀,b错误;
c.定容过程:定容时不应仰视,c错误,
d.摇匀过程:盖好瓶塞,用食指顶住瓶塞,另一只手的手指托住瓶底,反复上下颠倒,使溶液混合均
学科网(北京)股份有限公司匀,d错误;
故选a;
用 的浓硫酸配制 稀硫酸 ,浓硫酸的体积为 ;
a.配制溶液的过程中,用量筒量取浓硫酸时俯视读数,所量取浓硫酸的体积偏小,所配溶液浓度偏小;
b.稀释浓硫酸时,未冷却到室温即转移到容量瓶中,冷却后溶液体积偏小,所配溶液浓度偏大;
c.将量取浓硫酸后的量筒进行洗涤,并将洗涤液转移到容量瓶中,所取的浓硫酸的体积偏大,所配溶液
浓度大;
(2)室温下测得 的密度为 ,则室温下 的气体摩尔体积为 ;
(3)①步骤ⅲ需调整 中两液面使其相平的原因是,保持C、D中的压强与大气压相同,保证所测氢
气的体积准确;
②消耗的锌的物质的量为 ,实验过程中所得 的质量为 ,则生产氢气的物质的量为 ,因
此与硫酸铜反应的锌的物质的量为 ,故 ;
③由于硫酸镁不能与锌反应,故不能用此方法测定硫酸镁溶液的浓度。
学科网(北京)股份有限公司