文档内容
江苏省连云港市 2023-2024 届高三第一次调研考试
化学试题
注意事项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷共8页,包含选择题(第1题~第13题,共13题)、非选择题(第14题~第17题,共4
题)共两部分。本卷满分100分,考试时间为75分钟。考试结束后,请将答题卡交回。
2.答题前,请务必将自己的姓名、考试证号用书写黑色字迹的0.5毫米签字笔填写在答题卡上。
3.作答选择题,必须用2B铅笔把答题卡上对应题目的答案标号涂黑涂满;如需改动,请用橡
皮擦干净后,再选涂其它答案。答非选择题必须用书写黑色字迹的0.5毫米签字笔写在答题
卡上的指定位置,在其它位置作答一律无效。
4.如有作图需要,可用2B铅笔作答,并请加黑加粗,描写清楚。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Co 59
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 第19届亚运会秉持“绿色、智能、节俭、文明”办会理念。下列说法不正确的是
A. 亚运村餐厅“竹餐具”中含有丰富的多糖
B. 火炬燃料“零碳甲醇”燃烧不产生二氧化碳
C. 吉祥物“江南忆”机器人所用芯片的主要成分为硅
D. 火炬使用的“1070”铝合金具有硬度高、耐高温的特点
【答案】B
【解析】
【详解】A.“竹餐具”的主要成分是纤维素,纤维素属于多糖,故A正确;
B.“零碳甲醇”是利用焦炉气中的副产氢气与从工业尾气中捕集的二氧化碳合成的“绿色甲醇”,甲醇
的结构简式为CHOH,甲醇中含有碳元素,燃烧会产生二氧化碳,故B错误;
3
C.计算机芯片的主要成分为晶体硅,故C正确;
D.铝合金材料具有硬度高、耐高温的特性,符合火炬材料的需求,故D正确;
选B。
2. 反应 可以除去天然气中的 。下列说法正确的是
A. 为极性分子 B. 的电子式为
第1页/共24页
学科网(北京)股份有限公司C. 的空间构型为平面正方形 D. 反应中 仅作还原剂
【答案】A
【解析】
【详解】A.硫最外层有6个电子,它和两个氢形成两对共用电子对后还有2对孤对电子,一共有4对电
子在硫周围,这四对电子呈四面体型结构,其中两个方向被氢占据,还有2个方向被孤电子对占据,所以
为
分子呈V型,正负电荷中心不能重合, 极性分子,A符合题意;
B. 与CO 为等电子体,电子式为 ,B不符合题意;
2
C. 的空间构型为正四面体,C不符合题意;
D.反应中 中H的化合价由+1→0价,化合价降低,作氧化剂,D不符合题意;
故选A。公众号:高中试卷君
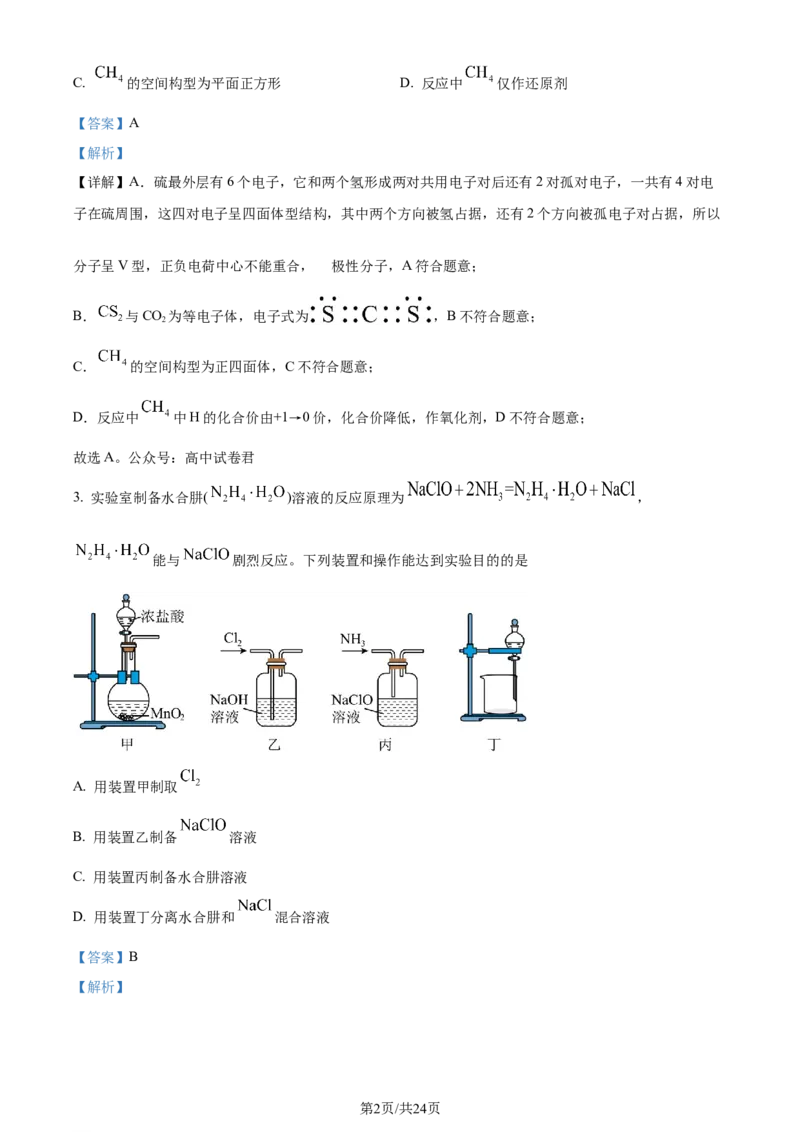
3. 实验室制备水合肼( )溶液的反应原理为 ,
能与 剧烈反应。下列装置和操作能达到实验目的的是
A. 用装置甲制取
B. 用装置乙制备 溶液
C. 用装置丙制备水合肼溶液
D. 用装置丁分离水合肼和 混合溶液
【答案】B
【解析】
第2页/共24页
学科网(北京)股份有限公司【
详解】A.浓盐酸与二氧化锰制取氯气需要加热,A装置不满足条件,A不符合题意;
B.氯气与氢氧化钠溶液反应生成次氯酸钠、氯化钠,B装置可达到实验目的,B符合题意;
C.氨气可被次氯酸钠氧化,反应剧烈,NaClO过量,可氧化生成的NH·HO,应将NaClO注入氨水,
2 4 2
C装置不能达到实验目的 ,C不符合题意;
D.NH·HO沸点较低,溶于水,应该采取蒸馏的方式提纯,蒸馏时温度计测定馏分的温度、冷凝管中
2 4 2
冷水下进上出,D装置不能达到实验目的,D不符合题意;
故选B。
4. 元素 、 、 位于周期表中ⅤA族。下列说法正确的是
A. 原子半径:
B. 第一电离能:
C. 、 、 的键角逐渐增大
D. 、 、 的酸性逐渐减弱
【答案】D
【解析】
【详解】A.同主族元素,从上到下原子半径依次增大,则 、 、 的原子半径依次增大,
,故A错误;
B.同主族元素,从上到下第一电离能依次减小,则N、P、As的第一电离能依次减小,
,故B错误;
C.元素 、 、 位于周期表中ⅤA族,元素非金属性大于H,从上到下原子半径依次增大,它们与H
形成共价键的极性逐渐减弱,因此极性键间的排斥力逐渐减小, 、 、 的键角逐渐减小,故
C错误;
D.同主族元素,从上到下非金属性依次减弱,最高价氧化物对应水化物的酸性依次减弱,则硝酸、磷酸、
砷酸的酸性依次减弱,故D正确;
第3页/共24页
学科网(北京)股份有限公司故选D。
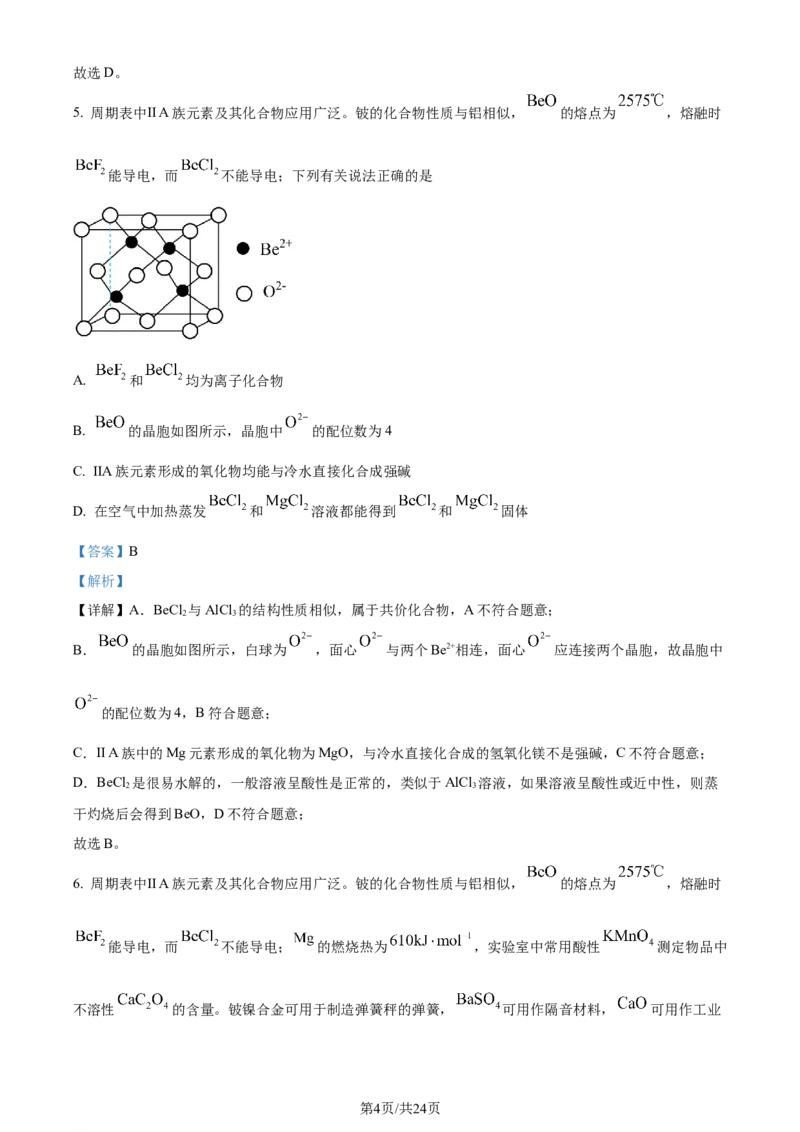
5. 周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似, 的熔点为 ,熔融时
能导电,而 不能导电;下列有关说法正确的是
A. 和 均为离子化合物
B. 的晶胞如图所示,晶胞中 的配位数为4
C. ⅡA族元素形成的氧化物均能与冷水直接化合成强碱
D. 在空气中加热蒸发 和 溶液都能得到 和 固体
【答案】B
【解析】
【详解】A.BeCl 与AlCl 的结构性质相似,属于共价化合物,A不符合题意;
2 3
B. 的晶胞如图所示,白球为 ,面心 与两个Be2+相连,面心 应连接两个晶胞,故晶胞中
的配位数为4,B符合题意;
C.ⅡA族中的Mg元素形成的氧化物为MgO,与冷水直接化合成的氢氧化镁不是强碱,C不符合题意;
D.BeCl 是很易水解的,一般溶液呈酸性是正常的,类似于AlCl 溶液,如果溶液呈酸性或近中性,则蒸
2 3
干灼烧后会得到BeO,D不符合题意;
故选B。
6. 周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似, 的熔点为 ,熔融时
能导电,而 不能导电; 的燃烧热为 ,实验室中常用酸性 测定物品中
不溶性 的含量。铍镍合金可用于制造弹簧秤的弹簧, 可用作隔音材料, 可用作工业
第4页/共24页
学科网(北京)股份有限公司废气脱硫剂。下列化学反应表示正确的是
A. 与 溶液反应:
B. 镁的燃烧:
C. 向 溶液中滴加足量 溶液:
D. 用酸性 测定 的含量:
【答案】C
【解析】
【详解】A.铍的化合物性质与铝相似, 与 溶液反应: ,
A不符合题意;
B.燃烧热1mol纯物质燃烧所放出 热的量,镁的燃烧:
,B不符合题意;
C.向 溶液中滴加足量 溶液:化学方程式为
Mg(HCO )+4NaOH=Mg(OH)↓+2Na CO+2H O,离子反应方程式为:
3 2 2 2 3 2
,C符合题意;
D.用酸性 测定 的含量, 属于难溶物质不能拆分:
,D不符合题意;
故选C。
7. 周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似, 的熔点为 ,熔融时
能导电,而 不能导电; 的燃烧热为 ,实验室中常用酸性 测定物品中
第5页/共24页
学科网(北京)股份有限公司不溶性 的含量。铍镍合金可用于制造弹簧秤的弹簧, 可用作隔音材料, 可用作工业
废气脱硫剂。下列物质结构与性质或物质性质与用途具有对应关系的是
A. 难溶于水,可用作隔音材料
B. 能与水反应,可作工业废气脱硫剂
C. 的半径比 小, 的熔点比 高
的
D. 铍镍合金具有导电性,可以用于制造弹簧秤 弹簧
【答案】C
【解析】
【详解】A.BaSO 具有高吸音性能,可用作隔音材料,与BaSO 难溶于水无关,A错误;
4 4
B.氧化钙和二氧化硫反应得到亚硫酸钙,亚硫酸钙被氧化得到硫酸钙,避免生成污染气体,可以用作脱
硫剂,B错误;
C.离子晶体的熔点取决于金属的半径和电荷,通常半径小电荷大的熔点高,Mg2+和Ca2+所带的电荷数一
样,Mg2+的半径比Ca2+小,MgO的熔点比CaO高,C正确;
D.铍镍具有延展性,可以用于制造弹簧秤的弹簧,D错误;
故选C。
8. 硫及其化合物的转化具有重要应用。下列说法不正确的是
A. 工业制 :
B. 回收烟气中 获得 :
C. 工业废液中通入 除 :
D. 热的 溶液除S:
【答案】A
【解析】
【详解】A.工业制硫酸过程中的物质转化是将二氧化硫氧化为三氧化硫:
,A符合题意;
第6页/共24页
学科网(北京)股份有限公司B.回收烟气中 获得 : ,该反应节约成本,简化反应步骤,该反
应正确,B不符合题意;
C. 是难溶于水与酸的物质,工业废液中通入 除 : ,该反应
正确,C不符合题意;
D.在加热条件下,硫能与强碱溶液发生反应,热的 溶液除S:
,该反应正确,D不符合题意;
故选A。
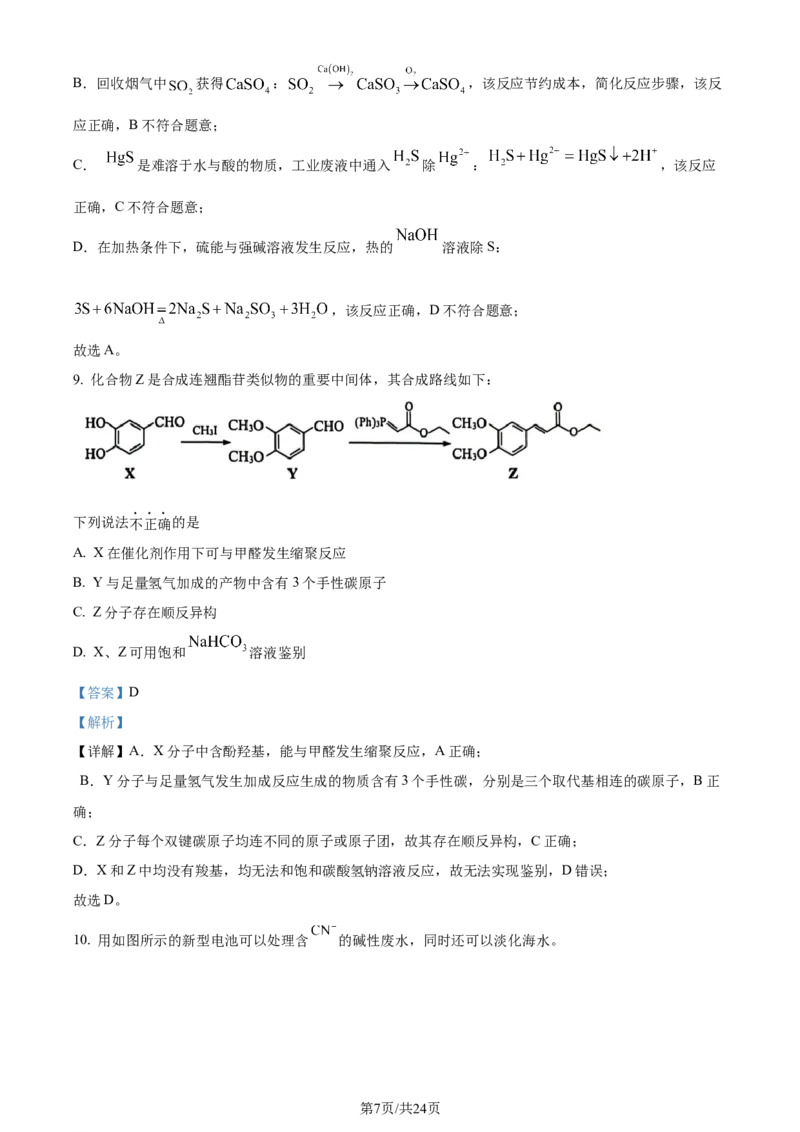
9. 化合物Z是合成连翘酯苷类似物的重要中间体,其合成路线如下:
下列说法不正确的是
A. X在催化剂作用下可与甲醛发生缩聚反应
B. Y与足量氢气加成的产物中含有3个手性碳原子
C. Z分子存在顺反异构
D. X、Z可用饱和 溶液鉴别
【答案】D
【解析】
【详解】A.X分子中含酚羟基,能与甲醛发生缩聚反应,A正确;
B.Y分子与足量氢气发生加成反应生成的物质含有3个手性碳,分别是三个取代基相连的碳原子,B正
确;
C.Z分子每个双键碳原子均连不同的原子或原子团,故其存在顺反异构,C正确;
D.X和Z中均没有羧基,均无法和饱和碳酸氢钠溶液反应,故无法实现鉴别,D错误;
故选D。
10. 用如图所示的新型电池可以处理含 的碱性废水,同时还可以淡化海水。
第7页/共24页
学科网(北京)股份有限公司下列说法正确的是
A. a极电极反应式:
B. 电池工作一段时间后,右室溶液的 减小
C. 交换膜Ⅰ为阳离子交换膜,交换膜Ⅱ为阴离子交换膜
D. 若将含有 的废水完全处理,理论上可除去 的质量为
【答案】D
【解析】
【 分 析 】 由 图 可 知 , a 电 极 在 碱 性 条 件 下 失 去 电 子 生 成 氮 气 , 电 极 反 应 为
,a为负极,则b为正极,电极反应为:2H++2e-=H ↑,以
2
此解题。
【详解】A.由分析可知,a极电极反应式: ,A错误;
B.由分析可知,b为正极,电极反应为:2H++2e-=H ↑,则消耗氢离子,pH增大,B错误;
2
C.由A分析可知,a电极附近负电荷减少,则阴离子通过交换膜Ⅰ向左移动,由B分析可知,b电极附近
正电荷减少,则阳离子通过交换膜Ⅱ向右移动,C错误;
D. 的物质的量为1mol,根据选项A分析可知,消耗1mol CN-时转移5mol电子,根据电荷守恒
可知,可同时处理5mol ,其质量为 ,D正确;
故选D。
11. 室温下,下列实验方案能达到探究目的的是
第8页/共24页
学科网(北京)股份有限公司选
实验方案 探究目的
项
向 、 混合溶液中依次加入少量氯水和 ,振荡后
A 氧化性:
静置,观察 层颜色
向溶液 中加入盐酸,将产生的气体通入品红溶液中,观察溶
B 溶液 中是否含有 或
液颜色变化
测定浓度均为 的 、 溶液的 和 的电离
C
能力
用饱和 溶液浸泡一段时间后过滤、洗涤,向
D
所得滤渣上滴加盐酸,产生无色气体
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.向 、 混合溶液中依次加入少量氯水和 ,振荡后静置,少量氯水先将KI氧化为
碘单质,仅能证明氧化性: , ,无法证明氧化性 ,A不符合题意;
B.若溶液X为次氯酸钠溶液,则向溶液X中加入盐酸会产生氯气,也可以使品红溶液褪色,不能判断溶
液X中是否含有 或 ,B不符合题意;
C.室温下,测定浓度均为0.1mol⋅L−1的CHCOONa溶液、NH Cl溶液的pH,可对比 和
3 4
的水解程度,进而判断CHCOOH和NH ⋅HO的电离程度,C符合题意;
3 3 2
D.将BaSO 投入饱和NaCO 溶液中充分反应,Q(BaCO)>K (BaCO),是沉淀的生成,不能证明
4 2 3 c 3 sp 3
K (BaSO)>K (BaCO),D不符合题意;
sp 4 sp 3
故选C。
12. 室温下,用含少量 和 的 溶液制备 的过程如下。
第9页/共24页
学科网(北京)股份有限公司已知: , ; ,
下列说法正确的是
A. 溶液中:
B. “除钴镍”后得到的上层清液中 为 ,则 为
C. 溶液中:
D. “沉铁”后的滤液中:
【答案】A
【解析】
【分析】该工艺流程的原料为含少量 和 的 溶液,产品为 ,加入 溶
液,使 和 转化为 、 沉淀过滤除去,滤液中加入 溶液,与 反应生成
。
【详解】A. 溶液中, 发生水解 、 ,水解程度
较大, ,以
第一步水解为主,设发生水解的 为xmol/L,
,则
,解得 ,故 ,A正确;
第10页/共24页
学科网(北京)股份有限公司B.“除钴镍”后得到的上层清液中 为 ,
,则
,B错误;
C. 溶液存在电荷守恒 及物料守恒
,则质子守恒为
,C错误;
D.除去 和 的 溶液,加入 溶液 “沉铁”后,滤液中含有 、少量
及可能过量的 ,故电荷守恒,因为阴离子种类不全,
,D错误;
答案选A。
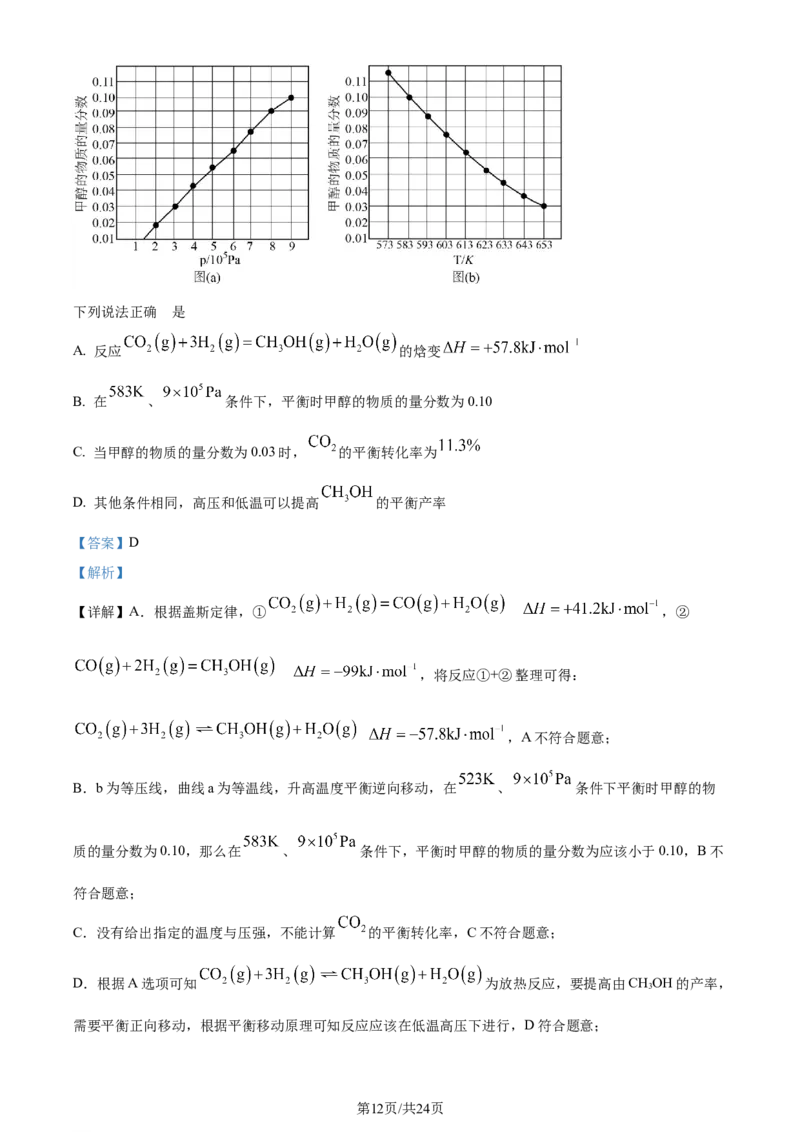
13. 二氧化碳加氢制甲醇过程中的主要反应为
在密闭容器中,起始时 ,分别在 、 条件下测得平衡时甲醇的物
质的量分数与压强、甲醇的物质的量分数与温度的关系如图所示。
第11页/共24页
学科网(北京)股份有限公司下列说法正确 的是
A. 反应 的焓变
B. 在 、 条件下,平衡时甲醇的物质的量分数为0.10
C. 当甲醇的物质的量分数为0.03时, 的平衡转化率为
D. 其他条件相同,高压和低温可以提高 的平衡产率
【答案】D
【解析】
【详解】A.根据盖斯定律,① ,②
,将反应①+②整理可得:
,A不符合题意;
B.b为等压线,曲线a为等温线,升高温度平衡逆向移动,在 、 条件下平衡时甲醇的物
质的量分数为0.10,那么在 、 条件下,平衡时甲醇的物质的量分数为应该小于0.10,B不
符合题意;
C.没有给出指定的温度与压强,不能计算 的平衡转化率,C不符合题意;
D.根据A选项可知 为放热反应,要提高由CHOH的产率,
3
需要平衡正向移动,根据平衡移动原理可知反应应该在低温高压下进行,D符合题意;
第12页/共24页
学科网(北京)股份有限公司故选D。
二、非选择题:共4题,共61分。
14. 以含钼( )废催化剂(含 ,以及 、 、 等)为原料制备 ,其过程表示如下:
(1)焙烧。将废催化剂和足量 固体置于焙烧炉中,通入足量空气加热至 充分反应。焙烧过
程中 转化为 的化学方程式为___________。
(2)浸取。将焙烧所得固体加水浸泡,然后过滤、洗涤。过滤后所得滤液中存在的阴离子有 、
、___________。欲提高单位时间内钼的浸取率,可以采取的措施有___________(任写一点)。
(3)除杂。向浸取后的滤液中通入过量 ,过滤。通入过量 的目的___________。
(4)制备。向上述(3)所得滤液中加入硝酸调节溶液的 小于6,使 转化为 ,然后加入
充分反应,析出 ,灼烧后可得到 。灼烧
得到 的化学方程式为___________。
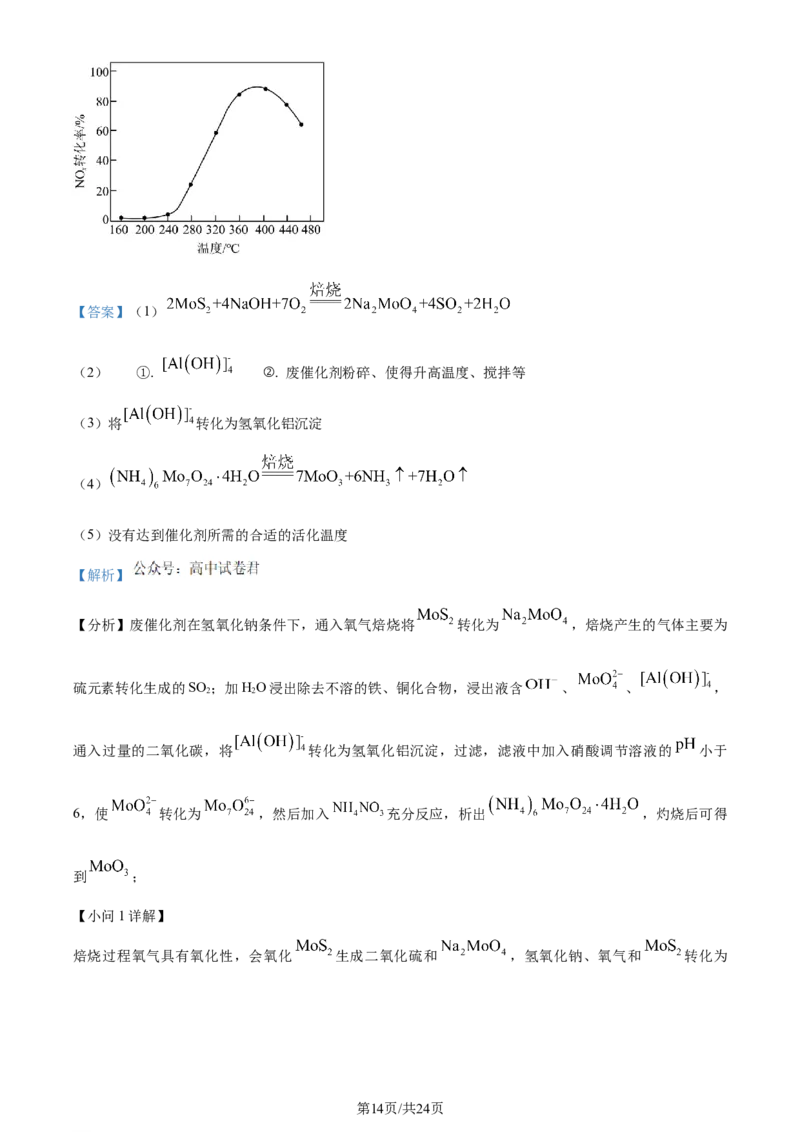
(5)应用。将 制成 催化剂,用于氨催化还原氮氧化物,一定压强下,
将氨氮比为1.0的混合气体按一定流速通入装有上述催化剂的反应装置,测得 的转化率随温度的变化
关系如图所示。在温度 之间, 转化率不高的原因是___________。
第13页/共24页
学科网(北京)股份有限公司【答案】(1)
(2) ①. ②. 废催化剂粉碎、使得升高温度、搅拌等
(3)将 转化为氢氧化铝沉淀
(4)
(5)没有达到催化剂所需的合适的活化温度
【解析】
【分析】废催化剂在氢氧化钠条件下,通入氧气焙烧将 转化为 ,焙烧产生的气体主要为
硫元素转化生成的SO ;加HO浸出除去不溶的铁、铜化合物,浸出液含 、 、 ,
2 2
通入过量的二氧化碳,将 转化为氢氧化铝沉淀,过滤,滤液中加入硝酸调节溶液的 小于
6,使 转化为 ,然后加入 充分反应,析出 ,灼烧后可得
到 ;
【小问1详解】
焙烧过程氧气具有氧化性,会氧化 生成二氧化硫和 ,氢氧化钠、氧气和 转化为
第14页/共24页
学科网(北京)股份有限公司、二氧化硫,水,化学方程式为 ;
【小问2详解】
氧化铝会和氢氧化钠生成可溶性的 ,故过滤后所得滤液中存在的阴离子有 、 、
。欲提高单位时间内钼的浸取率,可以采取的措施有废催化剂粉碎、使得升高温度、搅拌等;
【小问3详解】
通入过量的二氧化碳,将 转化为氢氧化铝沉淀,除去铝元素;
【小问4详解】
,灼烧后可得到 ,结合质量守恒可知,还生成氨气和水,反应为
;
【小问5详解】
催化剂催化需要一定的活化温度,在温度 之间, 转化率不高的原因是:。此时温度较低,
没有达到催化剂所需的合适的活化温度,导致反应速率较慢,单位时间内 转化率不高。
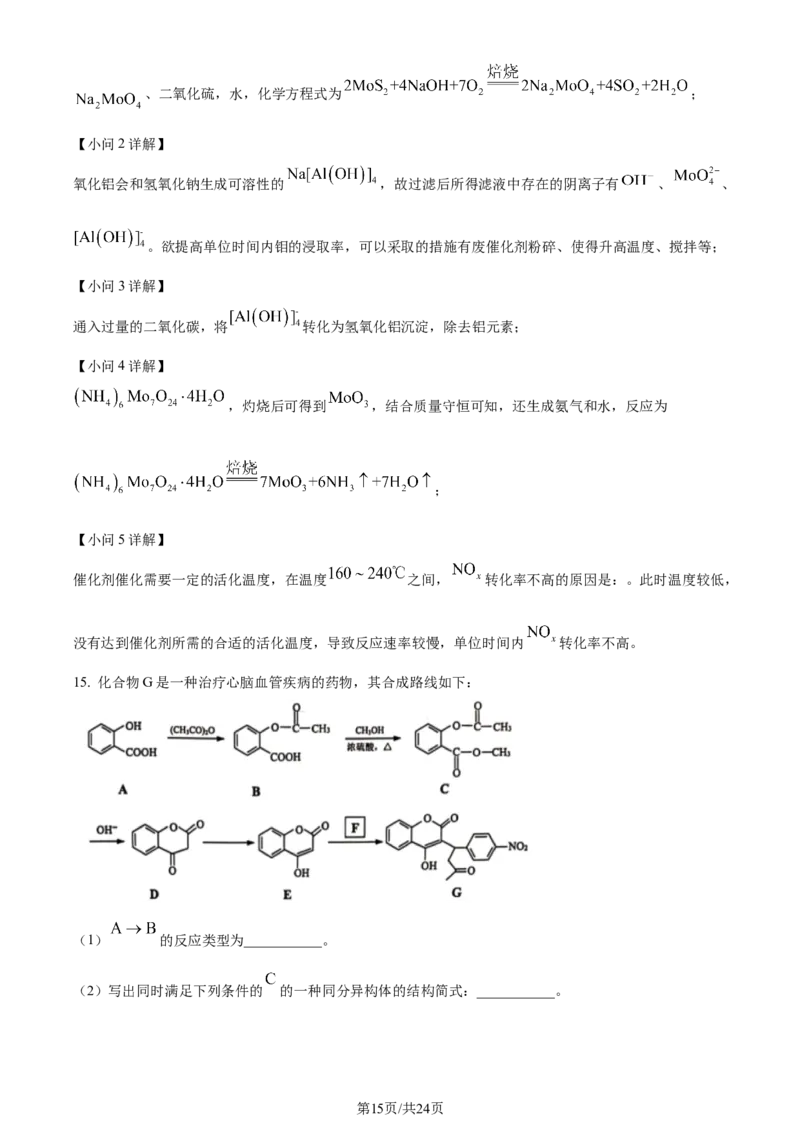
15. 化合物G是一种治疗心脑血管疾病的药物,其合成路线如下:
(1) 的反应类型为___________。
(2)写出同时满足下列条件的 的一种同分异构体的结构简式:___________。
第15页/共24页
学科网(北京)股份有限公司①能与 溶液反应生成 ;
②酸性条件下能水解,水解产物之一能与 溶液发生显色反应;
③分子中不同化学环境的氢原子个数比是 。
(3)下列关于化合物D、E的说法正确的是___________(填序号)。
a.D和E互为同分异构体
b.D和E分子中所有原子均可共平面
c.D和E分子中以 杂化的碳原子个数比为
(4)F的分子式为 ,则F的结构简式为___________。
(5)已知: ( 、 、 、 为烃基或H),写
出以 、 和 为原料制备 的合成路线流程图___________(无
机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
【答案】(1)取代反应
(2) 或 (3)ac
(4) (5)
第16页/共24页
学科网(北京)股份有限公司。
【解析】
【分析】结合合成路线分析可知,A B发生与乙酸酐的取代反应,B C发生酯化反应生成酯,C D
成环,D E为异构化反应,由酮羰基异构为醇烯,结合E和G的结构简式分析可知,F与E发生了加成
反应生成了G,故F的结构简式为: 。
【小问1详解】
结合分析可知,A→B发生与乙酸酐的取代反应;
【小问2详解】
同时满足下列条件的 的一种同分异构体①能与 溶液反应生成 ,说明此异构体有-COOH;
②酸性条件下能水解,水解产物之一能与 溶液发生显色反应,说明此异构体含酚酯的结构;③分子
中不同化学环境的氢原子个数比是 ,说明此异构体高度对称且含甲基。分析C可知,侧链4个碳,
少4个氢,故可拆出羧基、甲酸酚酯基、两个甲基,放在苯环对称位置上,故满足条件的有:
或 。
【小问3详解】
结合分析及化合物D、E的结构可知,D和E互为同分异构体;
且D和E分子中以 杂化的碳原子个数比为 ;但D存在饱和碳原子,故不可能所有原子同平面。故
第17页/共24页
学科网(北京)股份有限公司选ac。
【小问4详解】
结合分析可知F的结构为: 。
【小问5详解】
结合已知: ( 、 、 、 为烃基或H),可知,
合成目标分子需要先在苯酚上引入酯基,同时烯烃需要转化成酮羰基,二者发生已知条件的反应即可,故
可设计合成路线如下:
。
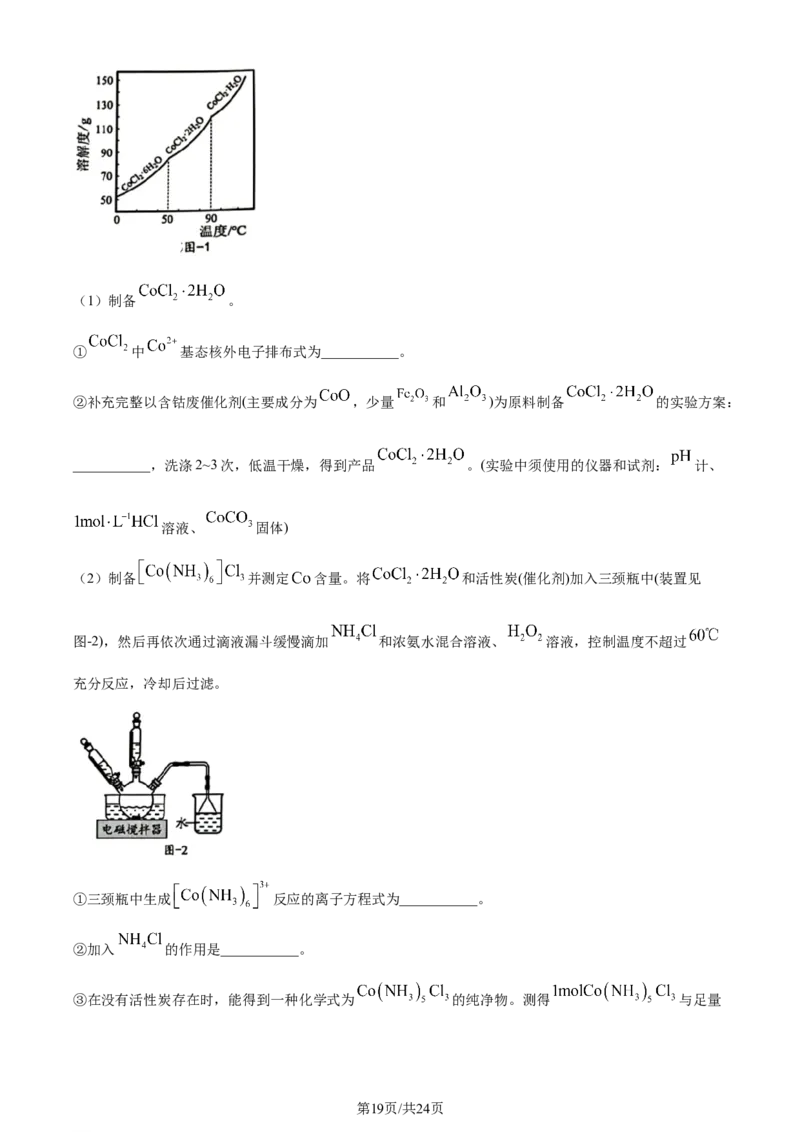
16. 实验室利用含钴废催化剂制备 ,并利用其制备 。已知: 完
全沉淀的 为 , 完全沉淀的 为 , 开始沉淀的 为 , 的溶解
度曲线如图-1所示。
第18页/共24页
学科网(北京)股份有限公司(1)制备 。
① 中 基态核外电子排布式为___________。
②补充完整以含钴废催化剂(主要成分为 ,少量 和 )为原料制备 的实验方案:
___________,洗涤2~3次,低温干燥,得到产品 。(实验中须使用的仪器和试剂: 计、
溶液、 固体)
(2)制备 并测定 含量。将 和活性炭(催化剂)加入三颈瓶中(装置见
图-2),然后再依次通过滴液漏斗缓慢滴加 和浓氨水混合溶液、 溶液,控制温度不超过
充分反应,冷却后过滤。
①三颈瓶中生成 反应的离子方程式为___________。
②加入 的作用是___________。
③在没有活性炭存在时,能得到一种化学式为 的纯净物。测得 与足量
第19页/共24页
学科网(北京)股份有限公司的硝酸银溶液反应生成 ,该配合物内界的化学式为___________。
④准确称取 样品于烧杯中,加入足量 溶液充分反应,微沸加热至无 放出。冷却至室
温后,加入过量的 固体和盐酸,充分摇荡。将所得溶液定容至 ,然后取出 溶液放入
锥形瓶中,滴加少量淀粉溶液,用 溶液滴定至终点,消耗 溶液的体积为
。计算样品中钴元素的质量分数。___________。已知:
, ,
。
【答案】(1) ①. 1s22s22p63s23p63d7 ②. 用 溶解含钴废催化剂,加 固体调节
pH,用pH计控制4.2≤pH<6.5生成氢氧化铁、氢氧化铝沉淀除Fe3+、Al3+,过滤,滤液加热浓缩、冷却到
50-90℃结晶析出 ,过滤
(2) ①. ②. 抑制氨
水电离,防止生成Co(OH) 沉淀 ③. ④. 20%
2
【解析】
【分析】含钴废催化剂主要成分为 ,少量 和 。用盐酸溶解得到含有Co2+、Al3+、Fe3+的溶
液,加碳酸钴调节pH为4.2~6.5生成氢氧化铁、氢氧化铝沉淀除Fe3+、Al3+,过滤,滤液加热浓缩、冷却
到50-90℃结晶析出 。
【小问1详解】
①Co是27号元素,Co失去4s上的2个电子得到 , 基态核外电子排布式为1s22s22p63s23p63d7。
②补充完整以含钴废催化剂(主要成分为 ,少量 和 )为原料制备 的实验方
第20页/共24页
学科网(北京)股份有限公司案:用 溶解含钴废催化剂,加 固体调节pH,用pH计控制4.2≤pH<6.5生成氢氧化
铁、氢氧化铝沉淀除Fe3+、Al3+,过滤,滤液加热浓缩、冷却到50-90℃结晶析出 ,过滤,
加洗涤2~3次,低温干燥,得到产品 。
【小问2详解】
①三颈瓶中,Co2+被双氧水氧化生成 反应的离子方程式为
。
② 能抑制氨水电离,防止生成Co(OH) 沉淀。
2
③ 与足量的硝酸银溶液反应生成 ,说明外界只有2个氯离子,该配合物内
界的化学式为 。
④根据 、
, 建立关系式
,样品中n(Co=)=0.1mol/L×0.024L
0.024mol,样品中钴元素的质量分数为 。
17. 氮氧化物( 、 等)的处理和资源化利用具有重要意义。
(1) 的处理。研究证明: 能提高 的分解速率, 参与了第Ⅱ步、第Ⅲ步反应。反应历
程( 为反应活化能):
第21页/共24页
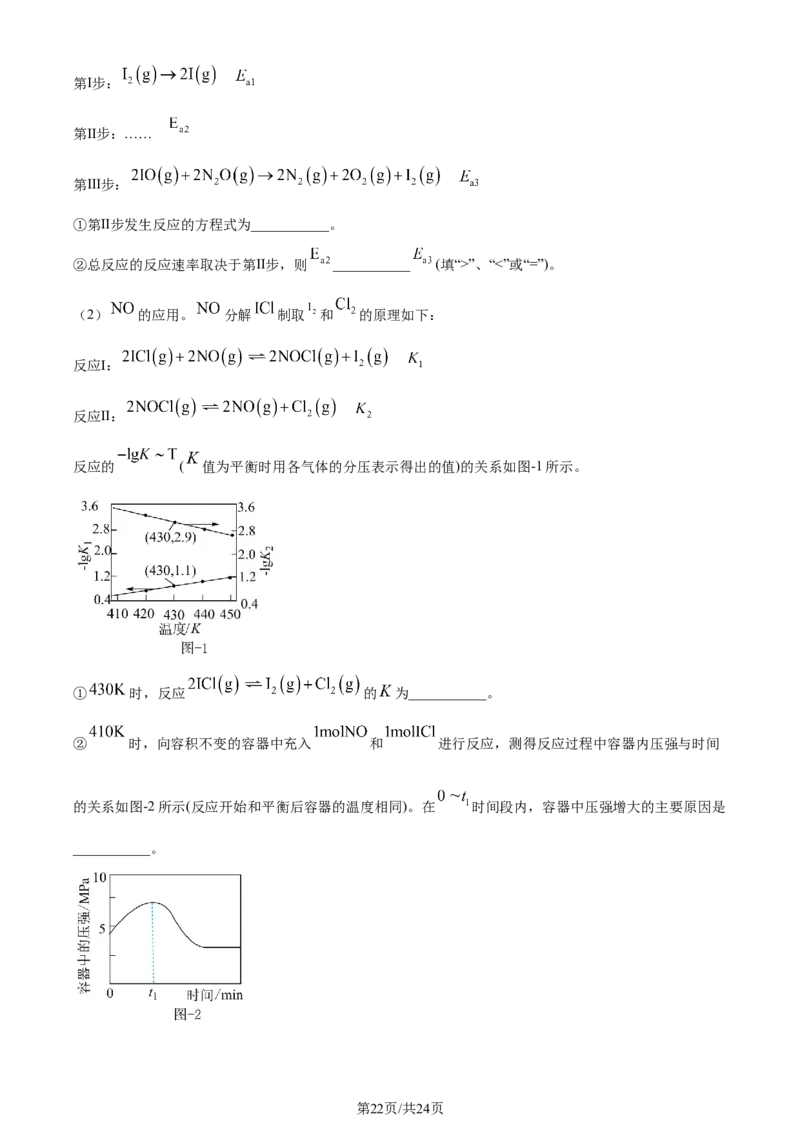
学科网(北京)股份有限公司第Ⅰ步:
第Ⅱ步:……
第Ⅲ步:
①第Ⅱ步发生反应的方程式为___________。
②总反应的反应速率取决于第Ⅱ步,则 ___________ (填“>”、“<”或“=”)。
(2) 的应用。 分解 制取 和 的原理如下:
反应Ⅰ:
反应Ⅱ:
反应的 ( 值为平衡时用各气体的分压表示得出的值)的关系如图-1所示。
① 时,反应 的 为___________。
② 时,向容积不变的容器中充入 和 进行反应,测得反应过程中容器内压强与时间
的关系如图-2所示(反应开始和平衡后容器的温度相同)。在 时间段内,容器中压强增大的主要原因是
___________。
第22页/共24页
学科网(北京)股份有限公司(3)催化电解 吸收液可将 还原为 ,其催化机理如图-3所示。在相同条件下,恒定通过电解
池的电量,电解得到部分还原产物的法拉第效率( )随电解电压的变化如图-4所示。已知 ,
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数; 表示电解过程中通
过的总电量。
①当电解电压为 时,电解生成的 和 的物质的量之比为___________。
②当电解电压为 时,催化电解 生成 的电极反应式为___________。
③电解电压大于 后,随着电解电压的不断增大, 的法拉第效率迅速增大,可能原因是
___________(吸附在催化剂上的物种加“*”表示,如 、 等)。
【答案】(1) ①. I(g)+NO(g)→N (g)+IO(g) ②. >
2 2
(2) ①. 10-4 ②. 反应Ⅰ为放热反应,随着反应的进行容器中的温度上升,导致容器内的压强增大
(3) ①. 15∶2 ②. NO+5e-+5H+=NH+H O ③. 随着电解电压的不断增大,*NO结合H+与e-得
3 2
到 *NOH ( 或 *NO+H++e-=*NOH ) 的 量 增 多 , *NOH 在 催 化 剂 表 面 失 水 转 化 成 NO ( 或
2
2*NOH=N O↑+HO)的选择性增大,导致NO的量增多,使NO的法拉第效率迅速增大
2 2 2 2
【解析】
【小问1详解】
①I(g)能提高NO的分解速率,I(g)是NO分解反应的催化剂,NO参与了第Ⅱ、Ⅲ步的反应,结合题给第
2 2 2 2 2
Ⅰ、Ⅲ步的反应和NO的分解反应[2N O(g) 2N(g)+O(g)]可知,第Ⅱ步发生反应的方程式为I(g)
2 2 2 2
第23页/共24页
学科网(北京)股份有限公司+N O(g)→N (g)+IO(g)。
2 2
②总反应的反应速率取决于第Ⅱ步,说明第Ⅱ步的反应速率最慢,活化能越小、反应速率越慢,则E >
a2
E 。
a3
【小问2详解】
①由图-1可知,430K时,-lgK =1.1、-lgK =2.9,则K= =10-1.1、K= =10-2.9,
1 2 1 2
反应2ICl(g) I(g)+Cl (g)的K= =K K=10-1.1×10-2.9=10-4。
2 2 1 2
②由图-1可知,随着温度的升高-lgK 逐渐增大、-lgK 逐渐减小,即随着温度的升高K 逐渐减小、K 逐渐
1 2 1 2
增大,说明反应Ⅰ为放热反应、反应Ⅱ为吸热反应,结合PV=nRT,故图-2在0~t 时间段内,容器中压强增
1
大的主要原因是:反应Ⅰ为放热反应,随着反应的进行容器中的温度上升,导致容器内的压强增大。
【小问3详解】
①由图-4知,当电解电压为U 时,H、NH 的法拉第效率分别为60%、20%,根据FE%= 知,电解生
1 2 3
成H 和NH 转移电子物质的量之比为60%∶20%=3∶1,生成H、NH 的电极反应式分别为2H++2e-=H ↑、
2 3 2 3 2
NO+5e-+5H+=NH+H O,则电解生成的H 和NH 的物质的量之比为 ∶ =15∶2。
3 2 2 3
②结合图-3,当电解电压为U 时,催化电解NO生成NH 的电极反应式为NO+5e-+5H+=NH+H O。
2 3 3 2
③电解电压大于U 后,随着电解电压的不断增大,NO的法拉第效率迅速增大,可能原因是:随着电解电
3 2
压的不断增大,*NO结合H+与e-得到*NOH(或*NO+H++e-=*NOH)的量增多,*NOH在催化剂表面失水
转化成NO(或2*NOH=N O↑+HO)的选择性增大,导致NO的量增多,使NO的法拉第效率迅速增大。
2 2 2 2 2
第24页/共24页
学科网(北京)股份有限公司