文档内容
2026 届高三第一学期期中考试
化学试题
时量:75min 分值:100分
命题人:
可能用到的相对原子质量:H~1 Be~9 C~12 N~14 O~16 Mg~24 Si~28 Cl~35.5
一、单项选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合要求)
1.化学品在人们生活中用途广泛。下列说法错误的是
A.维生素C 可用作抗氧化剂 B.硫酸铝可用于杀菌、净水
C.苯甲酸钠可用作防腐剂 D.CaCO 、FeSO 、ZnSO 等可用作奶粉营养强化剂
3 4 4
2.关于实验安全与实验事故处理,下列说法错误的是
A.金属钠、钾失火后,用沙土扑灭
B.苯酚需要标注: ,若不慎将苯酚沾到皮肤上,先后用乙醇、水冲洗
C.实验室制备氯气的实验中,需要注意:
D.检验铁和水蒸气反应的气体产物前应该先验纯,再点燃
3.下列化学用语表示正确的是
A.基态氧原子的轨道表示式:
B.用电子式表示HCl的形成过程为
C.NaCl溶液中的水合离子为
D.中子数为21的钾核素:21K
19
4.物质微观结构决定宏观性质,并影响用途。下列结构或性质不能解释其用途的是
选项 结构 性质 用途
有良好的导电性和
A 等离子体含电子、阳离子和电中性粒子 可制造显示器
流动性
大多数离子液体含有体积很大的阴、阳 有良好的导电性,难挥
B 可用作原电池的电解质
离子 发
C 碳化硅中Si原子与C原子通过共价键相连 硬度高、熔点高、耐腐蚀 可用作砂纸和砂轮的磨料
D 石墨中层与层之间存在微弱的范德华力 质地软,层间易滑动 可用作导电材料
第 1 页 共 8 页
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#} 5.枫叶所含鞣酸在铁锅中加热后会形成黑色色素,故能用于制作黑色糯米饭。下列有关鞣酸的
说法正确的是
A.不能使FeCl 溶液显紫色 B.能与溴水发生取代反应
3
C.有 4个手性碳原子 D.可与NaHCO 溶液反应
3
6.设N 为阿伏加德罗常数的值,下列判断正确的是
A
A.标准状况下,2.24LHF含有的电子数为N
A
B.室温下,pH=9的CH COONa溶液中,水电离出的H+数目为10-5N
3 A
C.1.2g金刚石中含有共价键的数目为0.2N
A
D.等体积、等物质的量浓度的NaCl 和 KCl 溶液中,阴、阳离子数目之和均为2N
A
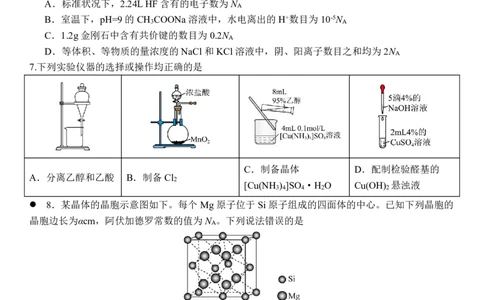
7.下列实验仪器的选择或操作均正确的是
C.制备晶体 D.配制检验醛基的
A.分离乙醇和乙酸 B.制备Cl
2
[Cu(NH ) ]SO ·H O Cu(OH) 悬浊液
3 4 4 2 2
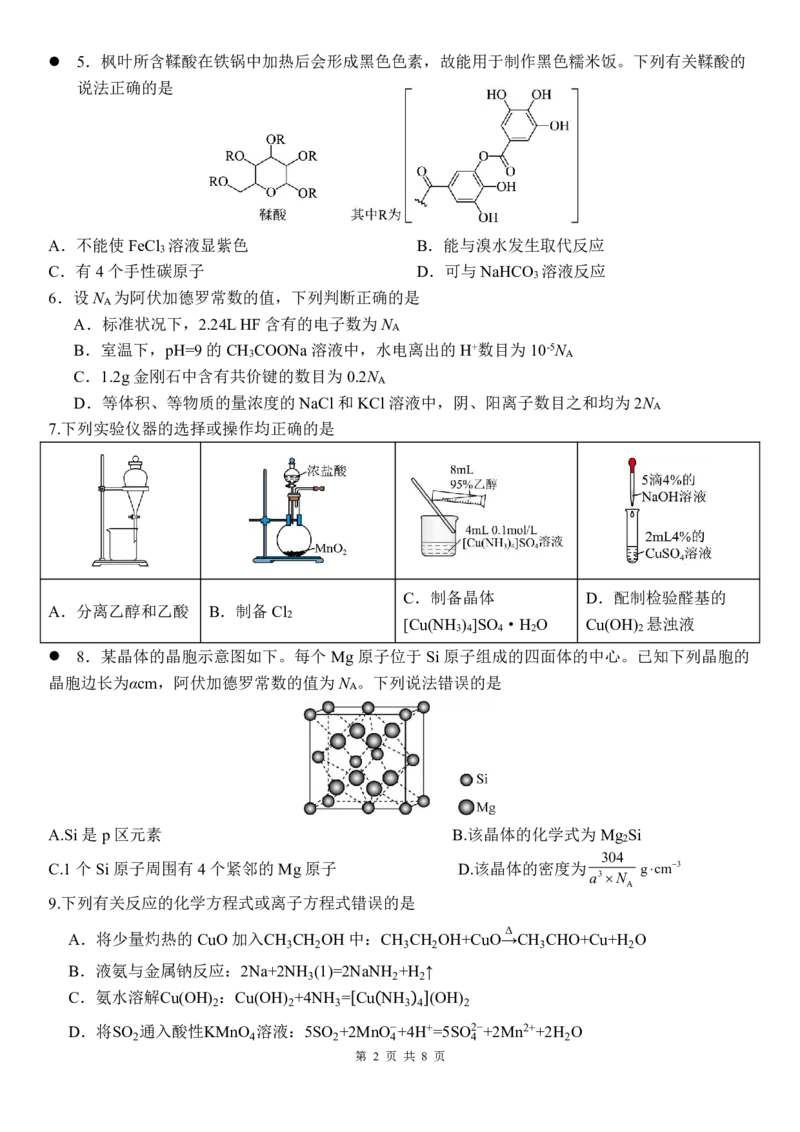
8.某晶体的晶胞示意图如下。每个Mg 原子位于Si原子组成的四面体的中心。已知下列晶胞的
晶胞边长为αcm,阿伏加德罗常数的值为N 。下列说法错误的是
A
A.Si是p区元素 B.该晶体的化学式为Mg Si
2
304
C.1个 Si原子周围有4个紧邻的Mg 原子 D.该晶体的密度为 gcm3
a3N
A
9.下列有关反应的化学方程式或离子方程式错误的是
Δ
A.将少量灼热的CuO加入CH CH OH中:CH CH OH+CuO→CH CHO+Cu+H O
3 2 3 2 3 2
B.液氨与金属钠反应:2Na+2NH (1)=2NaNH +H ↑
3 2 2
C.氨水溶解Cu(OH) :Cu(OH) +4NH = Cu NH (OH)
2 2 3 3 4 2
D.将SO 通入酸性KMnO 溶液:5SO +2MnO−+4H+=5SO2−+2Mn2++2H O
2 4 2 4 4 2
第 2 页 共 8 页
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#}10.利用丙烷制备丙烯的机理如图所示,下列说法正确的是
A.M-H 改变了丙烷制备丙烯的反应历程
B.升高温度不利于提高丙烷转化率
C.该反应是一个最理想的“原子经济性反应”
D.反应决速步涉及的变化过程为M-H+C H CH CH CH MH
3 8 3 2 2 2
11.根据下列实验操作和现象所得到的结论不正确的是( )
选项 实验操作和现象 结论
向沸水中滴加少量饱和 FeCl 溶液,得到红褐色液体,用激光
3
A 所得红褐色液体是胶体
笔照射可观察到光亮的“通路”
将银和AgNO 溶液与铜和NaSO 溶液组成原电池。连通后
3 4
B Cu 的金属性比Ag 强
银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝
向等物质的量浓度的 KF和KSCN混合溶液中滴加几滴
C 结合Fe3+的能力:F->SCN-
FeCl 溶液,振荡,溶液颜色无明显变化
3
在酸性KMnO 溶液中滴加足量FeCl 溶液,溶液的紫红色逐
4 2
D 体现Fe2+的还原性
渐褪去
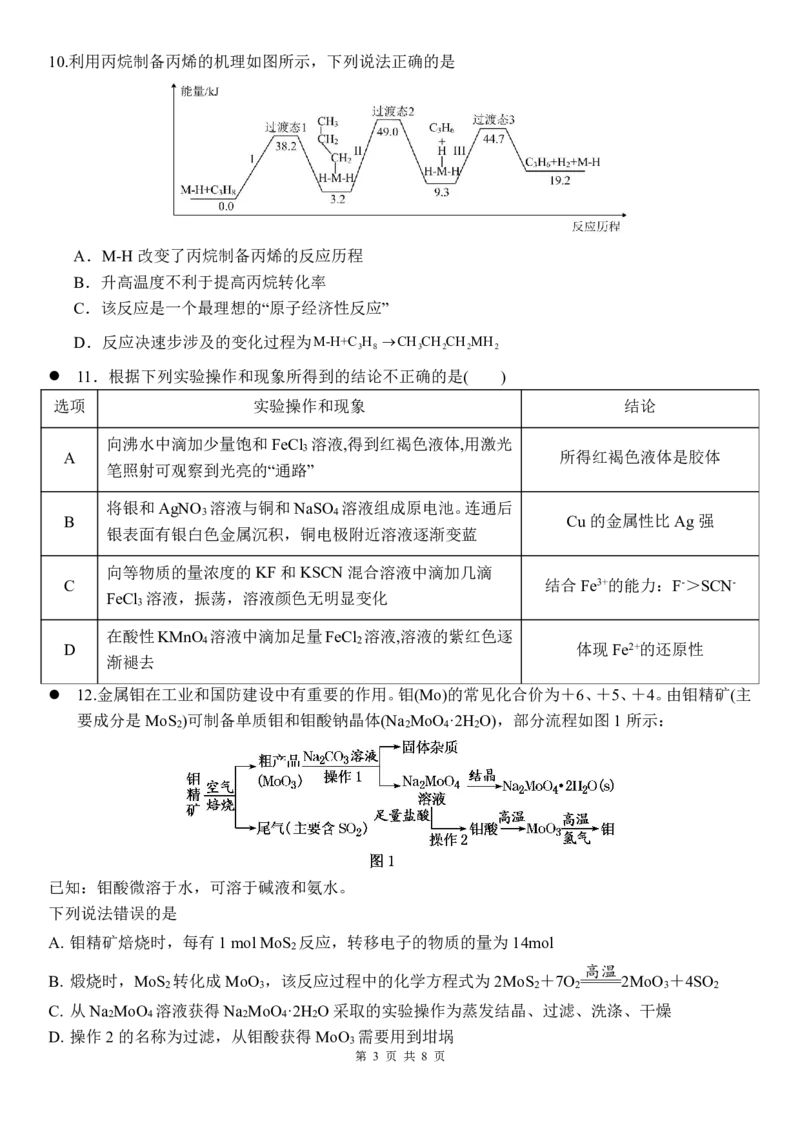
12.金属钼在工业和国防建设中有重要的作用。钼(Mo)的常见化合价为+6、+5、+4。由钼精矿(主
要成分是MoS )可制备单质钼和钼酸钠晶体(Na MoO ·2H O),部分流程如图1所示:
2 2 4 2
已知:钼酸微溶于水,可溶于碱液和氨水。
下列说法错误的是
A. 钼精矿焙烧时,每有1molMoS 反应,转移电子的物质的量为14mol
2
高温
B. 煅烧时,MoS 转化成MoO ,该反应过程中的化学方程式为2MoS +7O =====2MoO +4SO
2 3 2 2 3 2
C. 从Na MoO 溶液获得Na MoO ·2H O采取的实验操作为蒸发结晶、过滤、洗涤、干燥
2 4 2 4 2
D. 操作2的名称为过滤,从钼酸获得MoO 需要用到坩埚
3
第 3 页 共 8 页
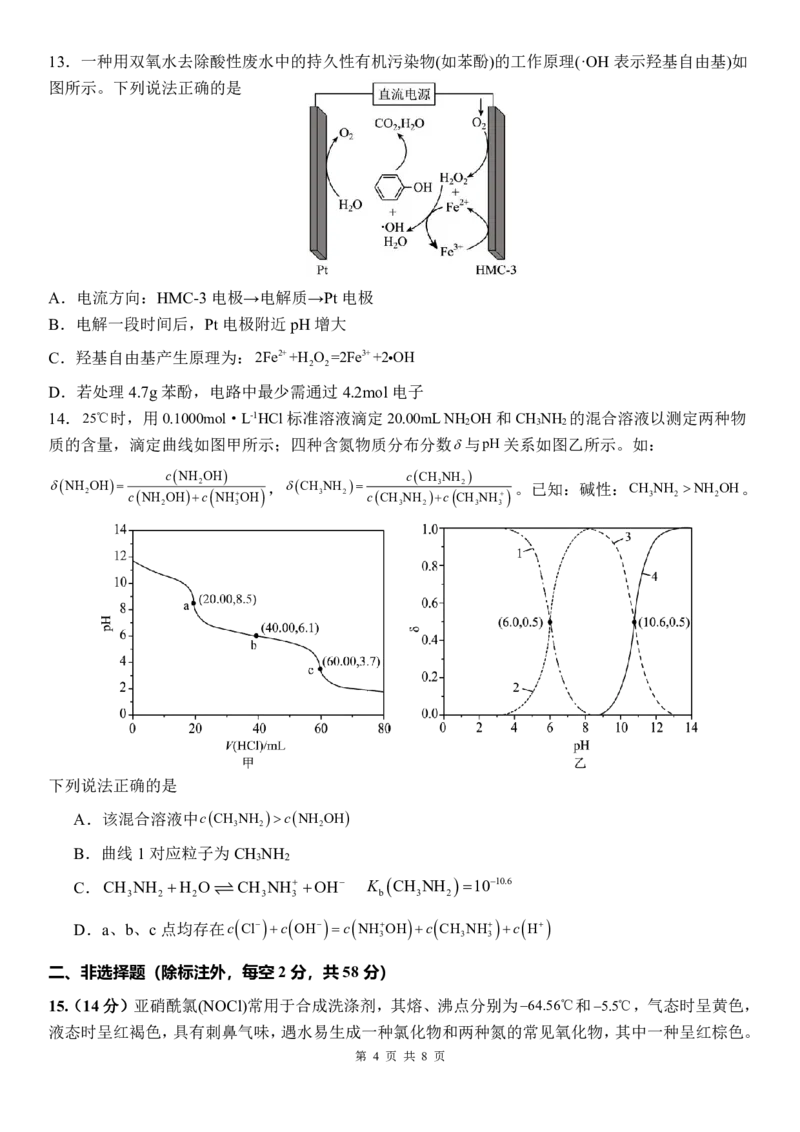
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#}13.一种用双氧水去除酸性废水中的持久性有机污染物(如苯酚)的工作原理(·OH表示羟基自由基)如
图所示。下列说法正确的是
A.电流方向:HMC-3 电极→电解质→Pt 电极
B.电解一段时间后,Pt电极附近pH增大
C.羟基自由基产生原理为:2Fe2++H O =2Fe3++2OH
2 2
D.若处理4.7g苯酚,电路中最少需通过4.2mol电子
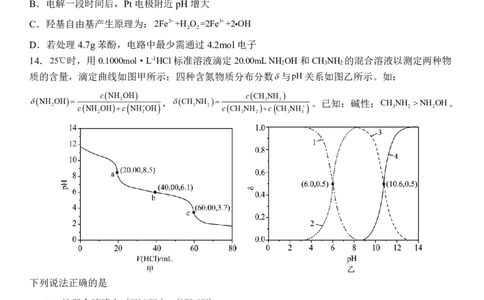
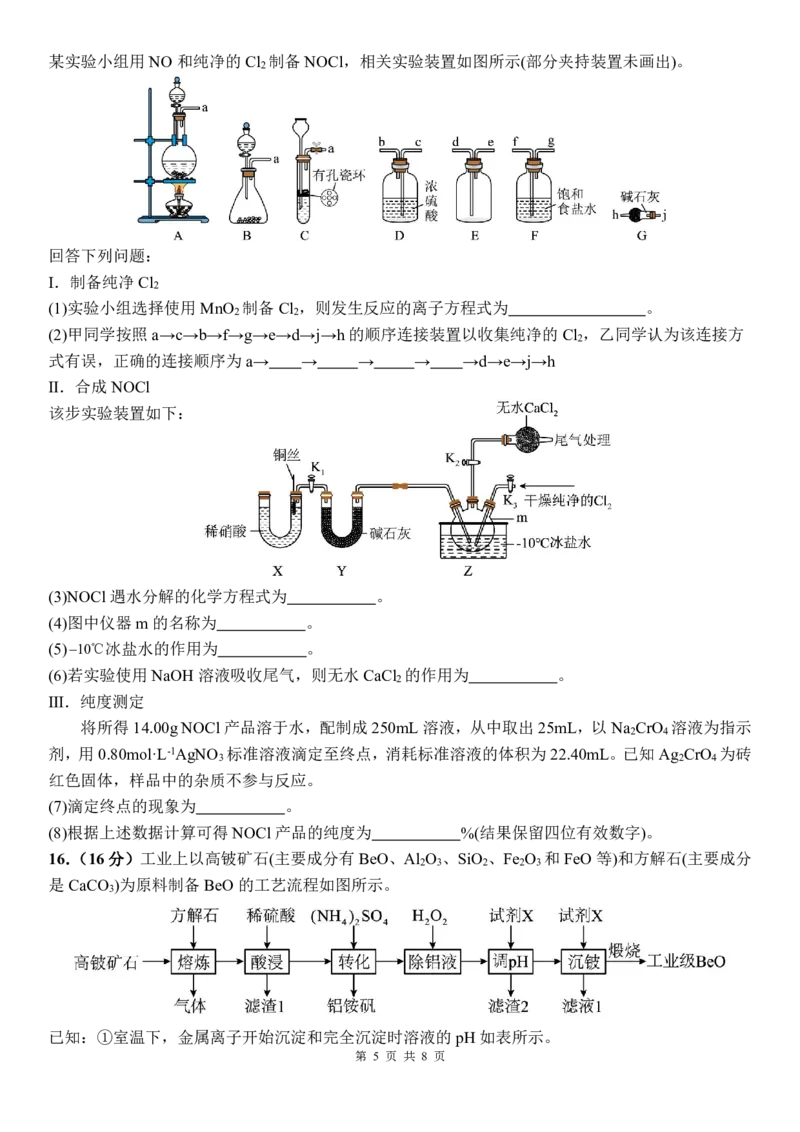
14.25℃时,用0.1000mol·L-1HCl标准溶液滴定20.00mLNH OH和CH NH 的混合溶液以测定两种物
2 3 2
质的含量,滴定曲线如图甲所示;四种含氮物质分布分数与pH关系如图乙所示。如:
cNH OH cCH NH
NH 2 OH cNH OH 2 c NHOH ,CH 3 NH 2 cCH NH 3 c C 2 H NH 。已知:碱性:CH 3 NH 2 NH 2 OH。
2 3 3 2 3 3
下列说法正确的是
A.该混合溶液中cCH NH cNH OH
3 2 2
B.曲线1对应粒子为CH NH
3 2
C.CH NH H O CH NH OH K CH NH 1010.6
3 2 2 3 3 b 3 2
D.a、b、c点均存在c Cl c OH c NHOH c CH NH c H
3 3 3
二、非选择题(除标注外,每空2分,共58分)
15.(14分)亚硝酰氯(NOCl)常用于合成洗涤剂,其熔、沸点分别为64.56℃和5.5℃,气态时呈黄色,
液态时呈红褐色,具有刺鼻气味,遇水易生成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。
第 4 页 共 8 页
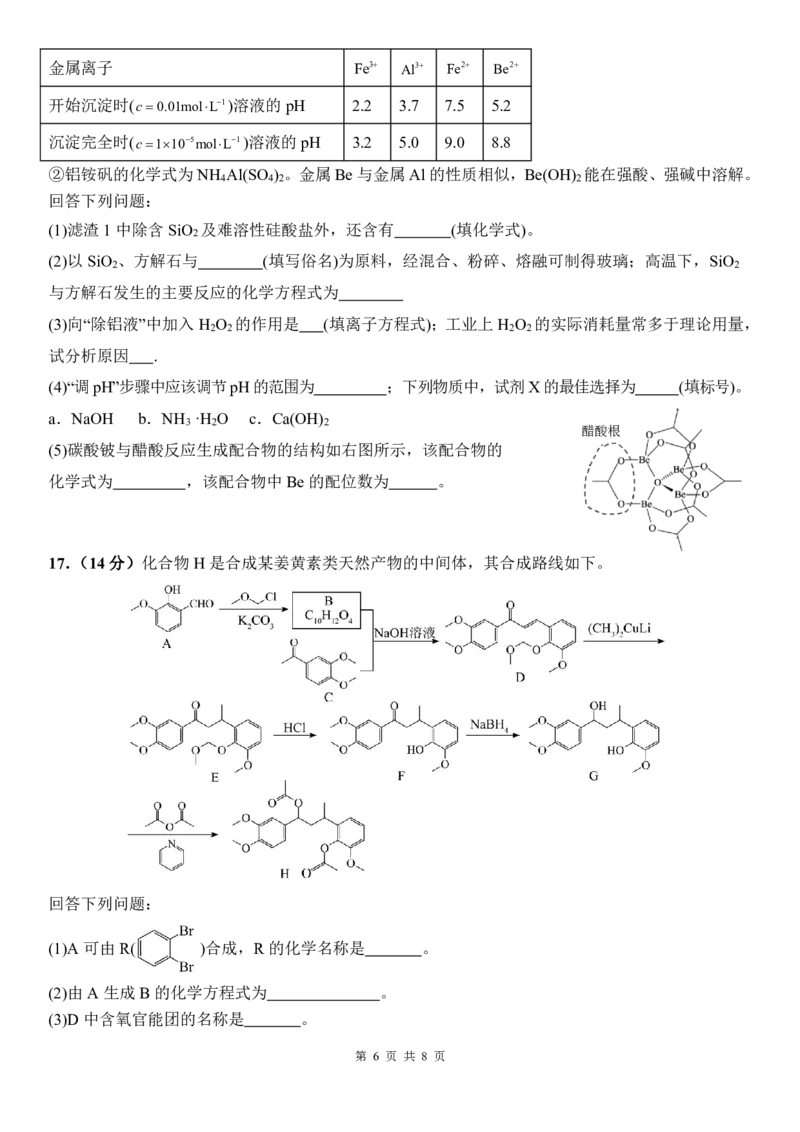
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#}某实验小组用NO和纯净的Cl 制备NOCl,相关实验装置如图所示(部分夹持装置未画出)。
2
回答下列问题:
Ⅰ.制备纯净Cl
2
(1)实验小组选择使用MnO 制备Cl ,则发生反应的离子方程式为 。
2 2
(2)甲同学按照a→c→b→f→g→e→d→j→h的顺序连接装置以收集纯净的Cl ,乙同学认为该连接方
2
式有误,正确的连接顺序为a→ → → → →d→e→j→h
Ⅱ.合成NOCl
该步实验装置如下:
(3)NOCl遇水分解的化学方程式为 。
(4)图中仪器m 的名称为 。
(5)10℃冰盐水的作用为 。
(6)若实验使用NaOH 溶液吸收尾气,则无水CaCl 的作用为 。
2
Ⅲ.纯度测定
将所得14.00gNOCl 产品溶于水,配制成250mL 溶液,从中取出25mL,以Na CrO 溶液为指示
2 4
剂,用0.80mol·L-1AgNO 标准溶液滴定至终点,消耗标准溶液的体积为22.40mL。已知Ag CrO 为砖
3 2 4
红色固体,样品中的杂质不参与反应。
(7)滴定终点的现象为 。
(8)根据上述数据计算可得NOCl 产品的纯度为 %(结果保留四位有效数字)。
16.(16分)工业上以高铍矿石(主要成分有BeO、Al O 、SiO 、Fe O 和FeO 等)和方解石(主要成分
2 3 2 2 3
是CaCO )为原料制备BeO 的工艺流程如图所示。
3
已知:①室温下,金属离子开始沉淀和完全沉淀时溶液的pH如表所示。
第 5 页 共 8 页
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#}金属离子 Fe3 Al3 Fe2 Be2
开始沉淀时(c0.01molL1)溶液的pH 2.2 3.7 7.5 5.2
沉淀完全时(c1105molL1)溶液的pH 3.2 5.0 9.0 8.8
②铝铵矾的化学式为NH Al(SO ) 。金属Be 与金属Al 的性质相似,Be(OH) 能在强酸、强碱中溶解。
4 4 2 2
回答下列问题:
(1)滤渣1中除含SiO 及难溶性硅酸盐外,还含有 (填化学式)。
2
(2)以SiO 、方解石与 (填写俗名)为原料,经混合、粉碎、熔融可制得玻璃;高温下,SiO
2 2
与方解石发生的主要反应的化学方程式为
(3)向“除铝液”中加入H O 的作用是 (填离子方程式);工业上H O 的实际消耗量常多于理论用量,
2 2 2 2
试分析原因 .
(4)“调pH”步骤中应该调节pH的范围为 ;下列物质中,试剂X的最佳选择为 (填标号)。
a.NaOH b.NH ·H O c.Ca(OH)
3 2 2
醋酸根
(5)碳酸铍与醋酸反应生成配合物的结构如右图所示,该配合物的
化学式为 ,该配合物中Be 的配位数为 。
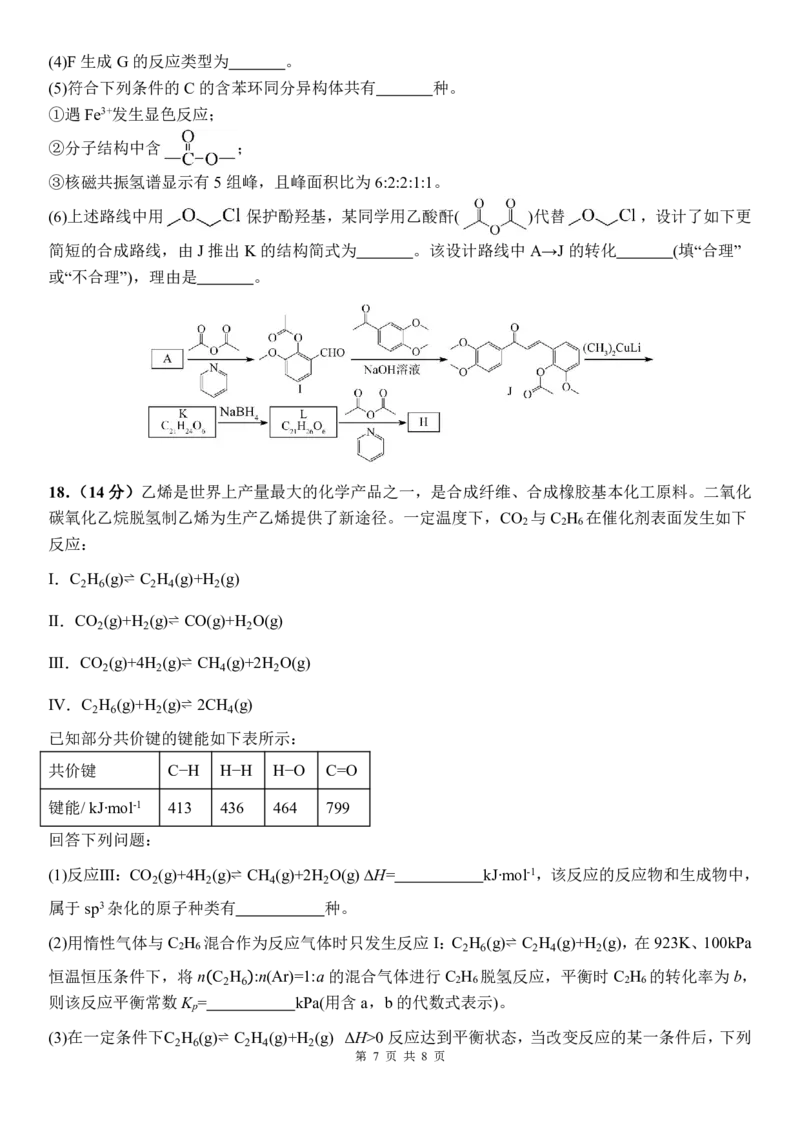
17.(14分)化合物H是合成某姜黄素类天然产物的中间体,其合成路线如下。
回答下列问题:
(1)A 可由R( )合成,R 的化学名称是 。
(2)由A 生成B的化学方程式为 。
(3)D 中含氧官能团的名称是 。
第 6 页 共 8 页
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#}(4)F 生成G的反应类型为 。
(5)符合下列条件的C 的含苯环同分异构体共有 种。
①遇Fe3+发生显色反应;
②分子结构中含 ;
③核磁共振氢谱显示有5组峰,且峰面积比为6:2:2:1:1。
(6)上述路线中用 保护酚羟基,某同学用乙酸酐( )代替 ,设计了如下更
简短的合成路线,由J 推出K的结构简式为 。该设计路线中A→J 的转化 (填“合理”
或“不合理”),理由是 。
18.(14分)乙烯是世界上产量最大的化学产品之一,是合成纤维、合成橡胶基本化工原料。二氧化
碳氧化乙烷脱氢制乙烯为生产乙烯提供了新途径。一定温度下,CO 与C H 在催化剂表面发生如下
2 2 6
反应:
I.C H (g)⇌ C H (g)+H (g)
2 6 2 4 2
Ⅱ.CO (g)+H (g)⇌ CO(g)+H O(g)
2 2 2
Ⅲ.CO (g)+4H (g)⇌ CH (g)+2H O(g)
2 2 4 2
Ⅳ.C H (g)+H (g)⇌ 2CH (g)
2 6 2 4
已知部分共价键的键能如下表所示:
共价键 C−H H−H H−O C=O
键能/kJ∙mol-1 413 436 464 799
回答下列问题:
(1)反应Ⅲ:CO (g)+4H (g)⇌ CH (g)+2H O(g) ∆H= kJ∙mol-1,该反应的反应物和生成物中,
2 2 4 2
属于sp3杂化的原子种类有 种。
(2)用惰性气体与C H 混合作为反应气体时只发生反应I:C H (g)⇌ C H (g)+H (g),在923K、100kPa
2 6 2 6 2 4 2
恒温恒压条件下,将n C H :n(Ar)=1:a的混合气体进行C H 脱氢反应,平衡时C H 的转化率为b,
2 6 2 6 2 6
则该反应平衡常数K = kPa(用含 a,b的代数式表示)。
p
(3)在一定条件下C H (g)⇌ C H (g)+H (g) ΔH>0 反应达到平衡状态,当改变反应的某一条件后,下列
2 6 2 4 2
第 7 页 共 8 页
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#}变化能说明平衡一定向正反应方向移动的是___________。
A.正反应速率先增大后减小 B.混合气体密度增大
C.反应物的体积百分数增大 D.化学平衡常数K值增大
(4)反应Ⅱ:CO (g)+H (g)⇌ CO(g)+H O(g) ΔH>0是提高乙烯产率的关键,但同时发生副反应Ⅲ。
2 2 2
①为提高反应Ⅱ的平衡转化率,应选择的反应条件为 。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
②基于上述反应,在催化剂表面C H 与CO 发生脱氢制乙烯的总反应为:16C H (g)+9CO (g)⇌
2 6 2 2 6 2
14C H (g)+12H (g)+6H O(g)+CH (g)+12CO(g),该反应温度常控制在600℃左右,其原因
2 4 2 2 4
是 。
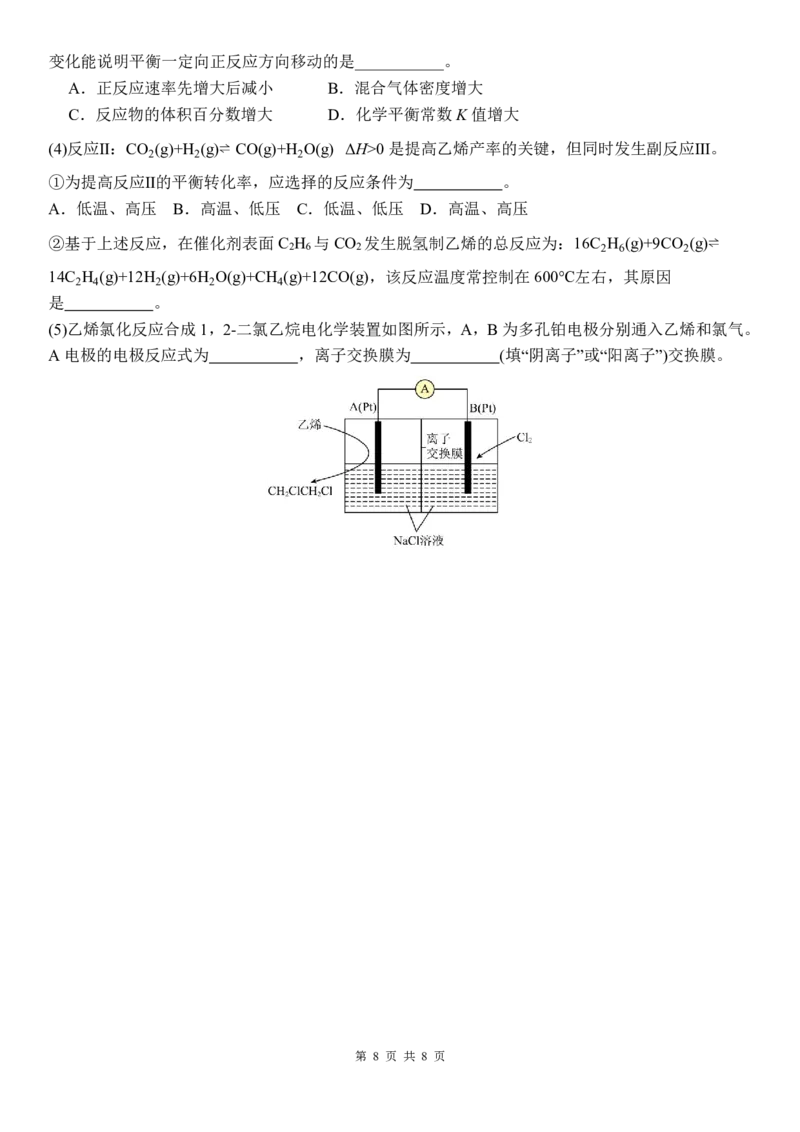
(5)乙烯氯化反应合成1,2-二氯乙烷电化学装置如图所示,A,B 为多孔铂电极分别通入乙烯和氯气。
A电极的电极反应式为 ,离子交换膜为 (填“阴离子”或“阳离子”)交换膜。
第 8 页 共 8 页
{#{QQABLQC54giQkMRACQ6KRQ0QCUkYsIETLCgOAUAaOAZDQRNIBAA=}#}