文档内容
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
…
学
校
:
______________
姓
名
:
_____________
班
级
:
_______________
考
号
:
______________________
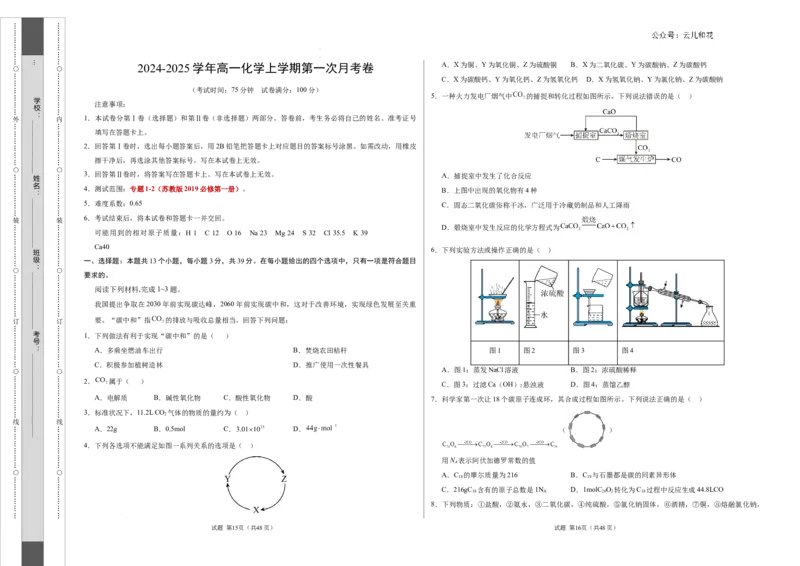
2024-2025 学年高一化学上学期第一次月考卷 A.X为铜、Y为氧化铜、Z为硫酸铜 B.X为二氧化碳、Y为碳酸钠、Z为碳酸钙
C.X为碳酸钙、Y为氧化钙、Z为氢氧化钙 D.X为氢氧化钠、Y为氯化钠、Z为碳酸钠
(考试时间:75分钟 试卷满分:100分)
5.一种火力发电厂烟气中 的捕捉和转化过程如图所示。下列说法错误的是( )
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。 A.捕捉室中发生了化合反应
4.测试范围:专题1-2(苏教版2019必修第一册)。 B.上图中出现的氧化物有4种
5.难度系数:0.65 C.固态二氧化碳俗称干冰,广泛用于冷藏奶制品和人工降雨
6.考试结束后,将本试卷和答题卡一并交回。
D.煅烧室中发生反应的化学方程式为
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Mg 24 S 32 Cl 35.5 K 39
Ca40
6.下列实验方法或操作正确的是( )
一、选择题:本题共13个小题,每小题3分,共39分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
阅读下列材料,完成1~3题。
我国提出争取在2030年前实现碳达峰,2060年前实现碳中和,这对于改善环境,实现绿色发展至关重
要。“碳中和”指 的排放与吸收总量相当。回答下列问题:
1.下列做法有利于实现“碳中和”的是( )
A.多乘坐燃油车出行 B.焚烧农田秸秆 图1 图2 图3 图4
C.积极参加植树造林 D.推广使用一次性餐具
A.图1:蒸发NaCl溶液 B.图2:浓硫酸稀释
2. 属于( )
C.图3:过滤Ca(OH) 悬浊液 D.图4:蒸馏乙醇
2
A.电解质 B.碱性氧化物 C.酸性氧化物 D.酸 7.科学家第一次让18个碳原子连成环,其合成过程如图所示。下列说法正确的是( )
3.标准状况下,11.2L CO 气体的物质的量约为( )
2
A.22g B.0.5mol C. D. ( )
4.下列各选项不能满足如图一系列关系的选项是( )
用N 表示阿伏加德罗常数的值
A
A.C 的摩尔质量为216 B.C 与石墨都是碳的同素异形体
18 18
C.216gC 含有的原子总数是1N D.1molC O 转化为C 过程中反应生成44.8LCO
18 A 20 2 18
8.下列物质:①盐酸,②氨水,③二氧化碳,④纯硫酸,⑤氯化钠固体,⑥酒精,⑦铜,⑧熔融氯化钠,
试题 第15页(共48页) 试题 第16页(共48页)
学学科科网网((北北京京))股股份份有有限限公公司司………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
⑨氢氧化铁胶体,⑩五水硫酸铜,以下叙述不正确的是
A.能导电的有4种 B.属于纯净物的有7种
C.属于非电解质的有2种 D.属于电解质的有4种
9.下列实验所采取的分离方法与对应原理都正确的是( )
选
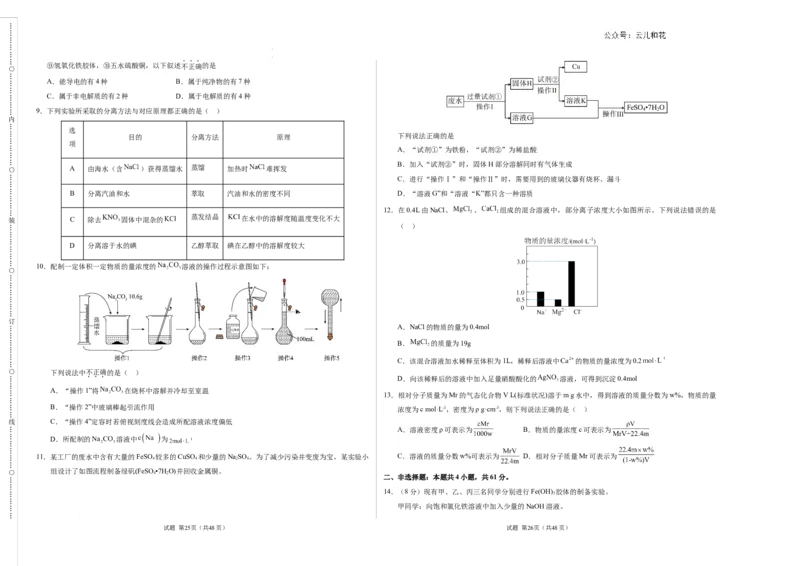
目的 分离方法 原理 下列说法正确的是
项
A.“试剂①”为铁粉,“试剂②”为稀盐酸
B.加入“试剂②”时,固体H部分溶解同时有气体生成
A 由海水(含 )获得蒸馏水 蒸馏 加热时 难挥发
C.进行“操作Ⅰ”和“操作Ⅱ”时,需要用到的玻璃仪器有烧杯、漏斗
B 分离汽油和水 萃取 汽油和水的密度不同 D.“溶液G”和“溶液“K”都只含一种溶质
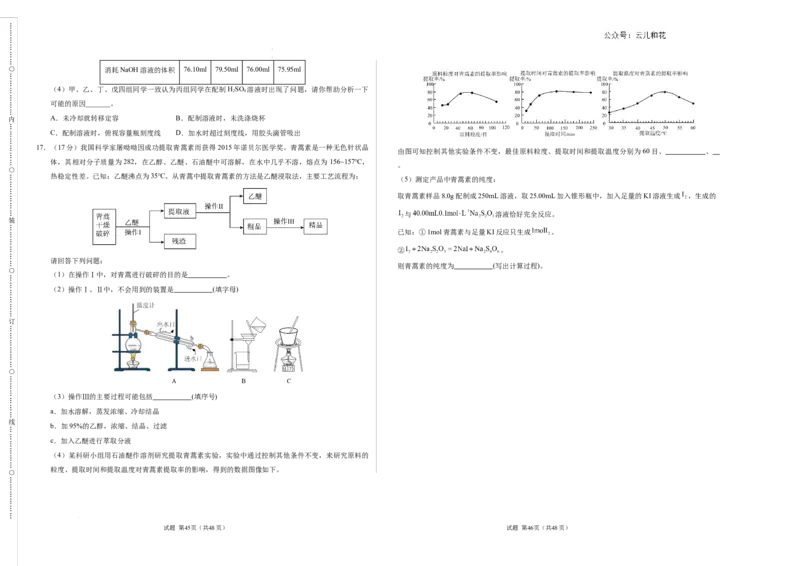
12.在0.4L由NaCl、 、 组成的混合溶液中,部分离子浓度大小如图所示。下列说法错误的是
C 除去 固体中混杂的 蒸发结晶 在水中的溶解度随温度变化不大
( )
D 分离溶于水的碘 乙醇萃取 碘在乙醇中的溶解度较大
10.配制一定体积一定物质的量浓度的 溶液的操作过程示意图如下:
A.NaCl的物质的量为0.4mol
B. 的质量为19g
C.该混合溶液加水稀释至体积为1L,稀释后溶液中 的物质的量浓度为0.2
下列说法中不正确的是( )
D.向该稀释后的溶液中加入足量硝酸酸化的 溶液,可得到沉淀0.4mol
A.“操作1”将 在烧杯中溶解并冷却至室温
13.相对分子质量为Mr的气态化合物V L(标准状况)溶于m g水中,得到溶液的质量分数为w%,物质的量
B.“操作2”中玻璃棒起引流作用 浓度为c mol·L-1,密度为ρ g·cm-3,则下列说法正确的是( )
C.“操作4”定容时若俯视刻度线会造成所配溶液浓度偏低
A.溶液密度ρ可表示为 B.物质的量浓度c可表示为
D.所配制的 溶液中 为
11.某工厂的废水中含有大量的FeSO 较多的CuSO 和少量的NaSO 。为了减少污染并变废为宝,某实验小 C.溶液的质量分数w%可表示为 D.相对分子质量Mr可表示为
4 4 2 4
组设计了如图流程制备绿矾(FeSO •7H O)并回收金属铜。 4 2
二、非选择题:本题共4小题,共61分。
14.(8分)现有甲、乙、丙三名同学分别进行Fe(OH) 胶体的制备实验。
3
甲同学:向饱和氯化铁溶液中加入少量的NaOH溶液。
试题 第25页(共48页) 试题 第26页(共48页)
学学科科网网((北北京京))股股份份有有限限公公司司………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
…
学
校
:
______________
姓
名
:
_____________
班
级
:
_______________
考
号
:
______________________
乙同学:直接加热饱和FeCl 溶液。
3
丙同学:向25mL沸水中逐滴加入5~6滴FeCl 饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
3
试回答下列问题:
(1)其中操作正确的同学是 (填“甲”“乙”或“丙”)。该同学想证明Fe(OH) 胶体已经
3
制备成功,他可以利用 (最简单的方法)进行鉴别。
(2)制备氢氧化铁胶体的化学方程式为 。
II.新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯 Fe(OH) 3 胶体 毒剂:①“84”消毒液;②H 2 O 2 ;③ClO 2 ;④O 3 ;⑤碘酒;⑥75%酒精;⑦过氧乙酸(CH 3 COOOH);⑧
的装置是可用下列中的 (填选项)。 高铁酸钠(Na FeO)。回答下列问题:
2 4
(7)上述杀菌消毒剂属于电解质的是 (填序号):属于非电解质的是 (填序号)。
16.(14分)HSO 和NaOH是实验室里常用的试剂。已知浓硫酸应密封保存,否则吸水而使浓度降低。
2 4
A. B. C.
名称 硫酸
化学式 HSO
2 4
体积 500mL
15.(22分)I.根根据所学知识,回答下列问题:
(1)在同温同压下,NO和SO 两种气体,密度比为 ,若两者质量相等,其体积比为 质量分数 98%
2
。
密度 1.8g/mL
(2)30gRO 中,核外电子总数比质子总数多6.02×1023,则R的摩尔质量为 。
I.HSO 溶液的配制
2 4
(3)实验室利用反应2KClO 3 2KCl+3O 2 ↑制取氧气,现有12.25gKClO 3 参加反应,计算得到标准状况 (1)某次实验中五组同学每组都要用250mL1mol/LH 2 SO 4 的溶液,现有浓硫酸一瓶,瓶上标签如图,
请帮助他们计算该浓硫酸的物质的量浓度为 mol/L。配制250mL1mol/LH SO 溶液时需此浓硫酸
2 4
下的氧气的体积是 L。
的体积为 mL。(保留一位小数)
(4)某元素G的一种含氧酸化学式为HGO ,属于二元酸,则HGO 与过量氢氧化钠溶液反应生成的
3 3 3 3
II.NaOH溶液的配制
产物NaHGO 为 (填“酸式盐”或“正盐”)。
2 3
实验室需配制490mL0.5mol/L的NaOH溶液
(5)某密闭容器,中间有一可自由滑动的隔板(厚度忽略不计)将容器分成两部分,装置如图所示(左、
(2)配制过程中用到的玻璃仪器有量筒、烧杯、玻璃棒、 和胶头滴管,配制前要称量NaOH固
右两侧温度相同)。左边充入1mol氦气,右边充入CO和NO的混合气体,原子总数为共1.6mol,则左
体 g。
右两室体积比为 。
III.某同学认为上述浓硫酸可能因保存不当而使浓度降低,甲小组同学重新测定配制的 HSO 溶液的物
2 4
质的量浓度。
(3)甲组同学用配制的标准NaOH溶液来测定20mLH SO 溶液的浓度,消耗0.5mol/L的NaOH溶液
2 4
76.00mL。则HSO 的实际物质的量浓度为 mol/L。
2 4
IV.乙丙丁戊四组同学也模仿甲同学进行实验,他们测定时所消耗的NaOH溶液的体积如下表
(6)2.76gCaO ·8H O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140°C时完全脱水,杂
2 2
组别 乙 丙 丁 戊
质受热不分解)如图所示。试确定60°C时CaO·xHO中x= 。
2 2
试题 第35页(共48页) 试题 第36页(共48页)
学学科科网网((北北京京))股股份份有有限限公公司司………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
消耗NaOH溶液的体积 76.10ml 79.50ml 76.00ml 75.95ml
(4)甲、乙、丁、戊四组同学一致认为丙组同学在配制 HSO 溶液时出现了问题,请你帮助分析一下
2 4
可能的原因_______。
A.未冷却就转移定容 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
17.(17分)我国科学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔医学奖。青蒿素是一种无色针状晶
由图可知控制其他实验条件不变,最佳原料粒度、提取时间和提取温度分别为60目、 、
体,其相对分子质量为282,在乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为 156~157℃,
。
热稳定性差。已知:乙醚沸点为35℃。从青蒿中提取青蒿素的方法是乙醚浸取法,主要工艺流程为:
(5)测定产品中青蒿素的纯度:
取青蒿素样品8.0g配制成250mL溶液,取25.00mL加入锥形瓶中,加入足量的KI溶液生成 ,生成的
与 溶液恰好完全反应。
已知:①1mol青蒿素与足量KI反应只生成 。
② 。
请回答下列问题:
则青蒿素的纯度为 (写出计算过程)。
(1)在操作Ⅰ中,对青蒿进行破碎的目的是 。
(2)操作Ⅰ、Ⅱ中,不会用到的装置是 (填字母)
(3)操作Ⅲ的主要过程可能包括 (填序号)
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%的乙醇,浓缩、结晶、过滤
c.加入乙醚进行萃取分液
(4)某科研小组用石油醚作溶剂研究提取青蒿素实验,实验中通过控制其他条件不变,来研究原料的
粒度、提取时间和提取温度对青蒿素提取率的影响,得到的数据图像如下。
试题 第45页(共48页) 试题 第46页(共48页)
学学科科网网((北北京京))股股份份有有限限公公司司