文档内容
2025-2026 学年高一化学上学期第一次月考卷
(考试时间:60 分钟,试卷满分:100 分)
注意事项:
1.答题前,考生务必将自己的学校、班级、姓名、准考证号填写清楚,并将条形码粘贴在规定位置。
2.本试卷设试卷和答题纸两部分。试卷包括试题与答题要求;所有答案必须涂或写在答题纸上;做在
试卷上一律不得分。答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
3.选择类试题中,标注“不定项”的试题,每小题有 1~2 个正确选项,只有 1 个正确选项的,多选不给
分,有 2 个正确选项的,漏选一个给一半分,错选不给分;未特别标注的试题,每小题只有一个正确选项。
4.测试范围:沪科版必修 1 第一章、第二章第一节。
5.考试结束后,将本试卷和答题卡一并交回。
6.难度系数:0.70。
可能用到的相对原子质量:H-1;C-12;O-16;Na-23;Mg-24;Al-27;Cl-35.5;Ti-48;Cu-64;Fe-56;
Mn-55;Fe-56;Zn-65;
一、从新鲜薰衣草中提取精油(22 分)
薰衣草精油常用作芳香剂、驱虫剂的原料。某小组在实验室从新鲜薰衣草中提取少量精油。
【查阅资料】薰衣草精油成分复杂,沸点范围 100℃~220℃,相同温度时在水中溶解度小于在苯、四氯
化碳(有毒、沸点 76.8℃)等溶剂中的溶解度。
【方案实施】
(1)步骤①:在研钵中将薰衣草捣碎,转移至小烧杯中并加入适量蒸馏水,搅拌使充分溶解,然后
。(单选题,选择上图装置的字母)
(2)将薰衣草捣碎的目的: 。
(3)步骤②:在薰衣草水中加入适量 CCl 利用 B 装置进行 , (填写操作)。
4
1 / 12(4)溶有精油的 CCl 层在 层。
4
A.上 B.下
(5)步骤③:将分离出的 CCl 层利用 (单选题,选择图中装置的字母)进行蒸馏。
4
(6)蒸馏收集温度在 ℃的馏分(该馏分可循环使用)。
A.100~220 B.76.8
(7)仪器 e 的名称是 。瓶中加入沸石的目的是 。温度计感温泡的位置是 。
(8)冷凝水的进水口为 。
A.g B.f
(9)为进一步检验薰衣草溶解液中的其他物质,配制 500 mL 0.5000 mol/L 的 NaOH 溶液。配制时,应用
电子天平称取 NaOH 的质量为 。
(10)(不定项)下列说法错误的是______。
A.称量 NaOH 固体的时间不宜过长
B.摇匀后发现液面低于刻度线,应及时加水至刻度线
C.定容时,仰视容量瓶刻度线会使配制的 NaOH 溶液浓度偏低
D.容量瓶可存放配好的 NaOH 溶液
【答案】(1)D(2 分)
(2)扩大物质的接触面积,使物质充分溶解(2 分)
(3)萃取(1 分) 分液(1 分)
(4)B(2 分)
(5)C(2 分)
(6)B(2 分)
(7)蒸馏烧瓶(1 分) 防止爆沸(1 分) 蒸馏烧瓶支管口下沿(2 分)
(8)A(2 分)
(9)10.0 g(2 分)
(10)BD(2 分)
【解析】要从新鲜薰衣草中提取少量精油,首先将薰衣草在研钵中捣碎,然后将其转移至小烧杯中并
加入适量蒸馏水,搅拌使充分溶解,再进行过滤,分离固、液混合物,弃去滤渣,然后根据薰衣草精油易
溶于四氯化碳等有机物,而四氯化碳与水又互不相溶、密度比水大的性质,向水溶液中加入四氯化碳,充
分振荡、静置、分液,得到精油的 CCl 溶液,再根据精油、CCl 是互溶的沸点不同的液体混合物,采用蒸
4 4
馏方法,收集 100-220℃的馏分,就分离出薰衣草精油。配制一定体积、一定物质的量浓度的溶液需使用容
2 / 12量瓶,根据 c= 、m=n·M 计算配制溶液需称量的溶质的质量。容量瓶不能稀释浓溶液、不能用于溶解固体、
储存溶液等。根据配制溶液的步骤确定使用的仪器种类,结合物质的量浓度定义式,根据操作对配制溶液
的体积及溶质的物质的量的影响分析实验误差。
(1)步骤①在研钵中将薰衣草捣碎,转移至小烧杯中并加入适量蒸馏水,搅拌使其充分溶解后过滤,分
离滤渣与滤液,故该步操作名称为过滤,操作装置图为图 D;
(2)在研钵中将薰衣草捣碎,目的是扩大水与薰衣草中的固体物质的接触面积,使物质充分接触,并将
可溶性物质充分溶解在水中;
(3)步骤②中在薰衣草水中加入适量 CCl 充分振荡。由于薰衣草精油在水中的溶解度小于在 CCl 的溶
4 4
解度,再根据四氯化碳的密度大于水的密度,利用装置 B 进行萃取、分液,薰衣草精油就存在于下层的 CCl
4
层中;故这两步操作分别为:萃取、分液;
(4)由于薰衣草精油在水中的溶解度小于在 CCl 的溶解度,CCl 密度大于水,所以萃取时 CCl 在下层;
4 4 4
(5)精油与四氯化碳互溶,但二者的沸点不同,相差较大,因此可知步骤③将 CCl 层利用装置 C 进行蒸
4
馏操作;
(6)薰衣草精油成分复杂,沸点范围 100℃~220℃,则收集温度在 76.8℃,得到的 CCl 可以循环使用;
4
(7)根据图示可知:仪器 e 为蒸馏烧瓶;
液体混合物进行加热时,为防止液面剧烈跳动,避免产生爆沸现象,应该加入碎瓷片;进行蒸馏时要
使温度计测量收集的馏分的温度,因此温度计水银球应该在蒸馏烧瓶支管口下沿附近;
(8)同时为增强冷凝效果,使物质被充分冷凝收集,要采用逆流原理,使冷凝管内的冷却水的方向是下
口 g 进上口 f 出,故选 A;
(9)要配制 500 mL 0.5000 mol/L 的 NaOH 溶液,需要溶质 NaOH 的物质的量 n=c·V=0.5000 mol/L×0.5
L=0.2500 mol,其质量 m=n·M=0.2500 mol×40 g/mol=10.0 g;
(10)A 项,NaOH 具有吸湿性,因此在称量 NaOH 固体时要避免其吸水潮解,故称量 NaOH 固体的时间
不宜过长,A 正确;B 项,配制 NaOH 溶液时,若摇匀后发现液面低于刻度线,这是由于部分溶液黏在容
量瓶的瓶颈上,由于溶液具有均一性,溶液的浓度与溶液体积大小无关,因此不能再加水至刻度线,否则
会对配制好的溶液起到稀释作用,使溶液浓度变小,B 错误;C 项,在定容时,仰视容量瓶刻度线,则溶液
的体积偏大,由于溶质的物质的量不变,最终会使配制的 NaOH 溶液浓度偏低,C 正确;D 项,容量瓶是
准确配制一定体积一定物质的量浓度的溶液的仪器,不可用于存放配好的 NaOH 溶液,而应该将配制好的
NaOH 溶液转移至试剂瓶中,D 错误;故选 BD。
二、测量锌的相对原子质量(18 分)
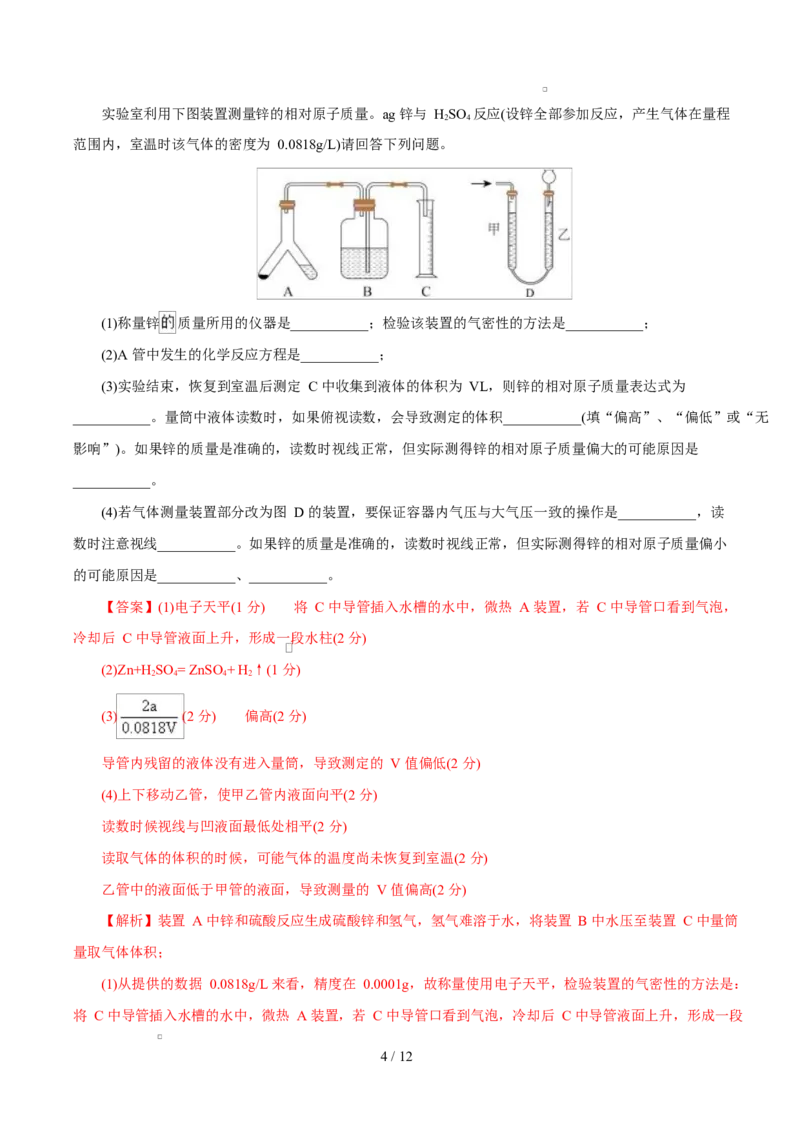
3 / 12实验室利用下图装置测量锌的相对原子质量。ag 锌与 HSO 反应(设锌全部参加反应,产生气体在量程
2 4
范围内,室温时该气体的密度为 0.0818g/L)请回答下列问题。
(1)称量锌 质量所用的仪器是___________;检验该装置的气密性的方法是___________;
(2)A 管中发生的化学反应方程是___________;
(3)实验结束,恢复到室温后测定 C 中收集到液体的体积为 VL,则锌的相对原子质量表达式为
___________。量筒中液体读数时,如果俯视读数,会导致测定的体积___________(填“偏高”、“偏低”或“无
影响”)。如果锌的质量是准确的,读数时视线正常,但实际测得锌的相对原子质量偏大的可能原因是
___________。
(4)若气体测量装置部分改为图 D 的装置,要保证容器内气压与大气压一致的操作是___________,读
数时注意视线___________。如果锌的质量是准确的,读数时视线正常,但实际测得锌的相对原子质量偏小
的可能原因是___________、___________。
【答案】(1)电子天平(1 分) 将 C 中导管插入水槽的水中,微热 A 装置,若 C 中导管口看到气泡,
冷却后 C 中导管液面上升,形成一段水柱(2 分)
(2)Zn+H SO = ZnSO+ H ↑(1 分)
2 4 4 2
(3) (2 分) 偏高(2 分)
导管内残留的液体没有进入量筒,导致测定的 V 值偏低(2 分)
(4)上下移动乙管,使甲乙管内液面向平(2 分)
读数时候视线与凹液面最低处相平(2 分)
读取气体的体积的时候,可能气体的温度尚未恢复到室温(2 分)
乙管中的液面低于甲管的液面,导致测量的 V 值偏高(2 分)
【解析】装置 A 中锌和硫酸反应生成硫酸锌和氢气,氢气难溶于水,将装置 B 中水压至装置 C 中量筒
量取气体体积;
(1)从提供的数据 0.0818g/L 来看,精度在 0.0001g,故称量使用电子天平,检验装置的气密性的方法是:
将 C 中导管插入水槽的水中,微热 A 装置,若 C 中导管口看到气泡,冷却后 C 中导管液面上升,形成一段
4 / 12水柱;
(2)A 中锌与硫酸反应制取氢气,方程式为:Zn+H SO = ZnSO+ H ↑;
2 4 4 2
(3)设锌的相对原子质量为 x,氢气的质量=VL×0.0818g/L =0.0818Vg,根据 Zn+H SO =ZnSO +H ↑,可
2 4 4 2
得关系式
,解得 x= ;量筒中液体如果俯视读数时,测定气体的体积偏高;如果锌的质
量是准确的,但实际测得锌的相对原子质量偏小的可能原因是:导管内残留的液体没有进入量筒,导致测
定的 V 值偏低;
(4)若气体测量装置部分改为图 D 的装置,要保证容器内气压与大气压一致的操作是:通过上下移动乙
管,使甲乙管内液面向平,读数时注意视线要与凹液面的最低处保持水平;如果锌的质量是准确的,但实
际测得锌的相对原子质量偏小的可能原因是 V 值偏大,体积与压强和温度有关,故可能得原因是读取气体
的体积的时候,可能气体的温度尚未恢复到室温或乙管中的液面低于甲管的液面,导致测量的 V 值偏高。
三、高效消毒剂(18 分)
某“消毒液”是一种以 NaClO 为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭
等的卫生消毒,某“消毒液”瓶体部分标签如图 1 所示,该“消毒液”通常稀释 100 倍(体积之比)后使用。
(1)此“消毒液”主要溶质的物质的量浓度约为 mol/L(计算结果保留一位小数)。某同学量取此“消
毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中 c(Na+)= mol/L。
该同学参照该“消毒液”的配方,用 NaClO 固体配制 480mL2.0mol/LNaClO 消毒液。
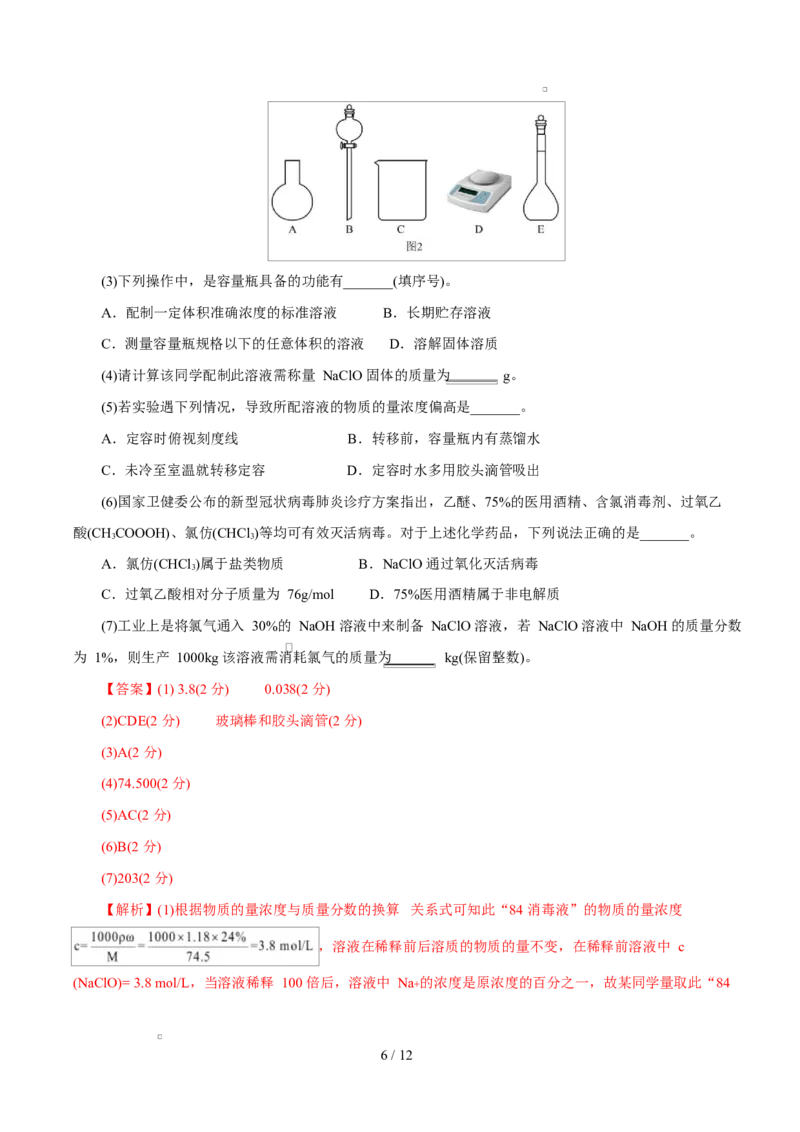
(2)如图 2 所示的仪器中,配制该溶液需要使用的是 (填仪器序号),还缺少的玻璃仪器是
。
5 / 12(3)下列操作中,是容量瓶具备的功能有_______(填序号)。
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.测量容量瓶规格以下的任意体积的溶液 D.溶解固体溶质
(4)请计算该同学配制此溶液需称量 NaClO 固体的质量为 g。
(5)若实验遇下列情况,导致所配溶液的物质的量浓度偏高是_______。
A.定容时俯视刻度线 B.转移前,容量瓶内有蒸馏水
C.未冷至室温就转移定容 D.定容时水多用胶头滴管吸出
(6)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%的医用酒精、含氯消毒剂、过氧乙
酸(CHCOOOH)、氯仿(CHCl )等均可有效灭活病毒。对于上述化学药品,下列说法正确的是_______。
3 3
A.氯仿(CHCl )属于盐类物质 B.NaClO 通过氧化灭活病毒
3
C.过氧乙酸相对分子质量为 76g/mol D.75%医用酒精属于非电解质
(7)工业上是将氯气通入 30%的 NaOH 溶液中来制备 NaClO 溶液,若 NaClO 溶液中 NaOH 的质量分数
为 1%,则生产 1000kg 该溶液需消耗氯气的质量为 kg(保留整数)。
【答案】(1) 3.8(2 分) 0.038(2 分)
(2)CDE(2 分) 玻璃棒和胶头滴管(2 分)
(3)A(2 分)
(4)74.500(2 分)
(5)AC(2 分)
(6)B(2 分)
(7)203(2 分)
【解析】(1)根据物质的量浓度与质量分数的换算 关系式可知此“84 消毒液”的物质的量浓度
,溶液在稀释前后溶质的物质的量不变,在稀释前溶液中 c
(NaClO)= 3.8 mol/L,当溶液稀释 100 倍后,溶液中 Na+ 的浓度是原浓度的百分之一,故某同学量取此“84
6 / 12消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中 c(Na+)= ;
(2)①配制一定物质的量浓度的溶液,需使用托盘天平称量固体药品,然后用烧杯溶解药品,并用玻璃
棒进行搅拌溶解,待溶液冷却后转移至 500 mL 的容量瓶中,用蒸馏水洗涤烧杯、玻璃棒,洗涤液也转移至
容量瓶中,当加水至液面接近刻度线 1-2 cm 时,改用胶头滴管滴加至凹液面与刻度线相平,故如图所示的
仪器中配制溶液需要使用的仪器序号是 CDE;还缺少的仪器有玻璃棒和胶头滴管;
(3)A 项,容量瓶是准确配制一定体积准确浓度的溶液的仪器,A 正确;B 项,容量瓶只能用于配制溶
液,不能用于贮存溶液,B 错误;C 项,容量瓶只能配制容量瓶规格的体积的溶液,而不能量取任意体积的
溶液,C 错误;D 项,容量瓶不能用来溶解固体溶质,D 错误;故选 A;
(4)配制 480mLNaClO 溶液,必须使用 500 mL 的容量瓶,所以实际是配制 500mL2.0mol/LNaClO 溶液,
需称量 NaClO 的质量 m(NaClO)=2.0 mol/L×0.5 L×74.5 g/mol=74.500g;
(5)A 项,定容时俯视刻度线读数,溶液的体积偏小,由于溶质的物质的量不变,因此配制溶液的判断
偏高,A 符合题意;B 项,转移前,容量瓶内有蒸馏水,不影响溶液的体积及溶质的物质的量,因此对配
制溶液的浓度无影响,B 不符合题意;C 项,未冷却至室温就转移定容,当溶液恢复至室温时,液面低于刻
度线,溶液体积偏小,最终导致配制溶液的浓度偏高,C 符合题意;D 项,定容时水多,用胶头滴管吸出,
则会导致配制溶液浓度偏低,D 不符合题意;故选 AC;
(6)A 项,氯仿(CHCl )不属于盐类物质,故 A 错误;B 项,NaClO 具有强氧化性,通过其强氧化性使病
3
毒失活,故 B 正确;C 项,过氧乙酸的分子式为 CHCOOOH,所以其相对分子质量为:12×2+4+16×3=76,
3
故 C 错误;D 项,75%医用酒精属于混合物,不是电解质,也不是非电解质,属于非电解质,故 D 错误;
故选 B;
(7)设氯气为 xkg,根据化学反应方程式 Cl+2NaOH=NaClO+NaCl+H O,则消耗氢氧化钠为 ,原
2 2
氢氧化钠质量为 +1000kg×1%,由氢氧化钠守恒定律可知,原溶液为 1000 kg-x kg,则 +
1000kg×1%=(1000 kg-x kg) ×0.3,解得 x=203kg。
四、制备氯化碘(19 分)
ICl(氯化碘)是红棕色液体,易挥发,熔点为 13.9℃,沸点为 974℃,易与水反应,接触空气时能形成五
氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组同学拟用下列仪器制备氯化
碘。
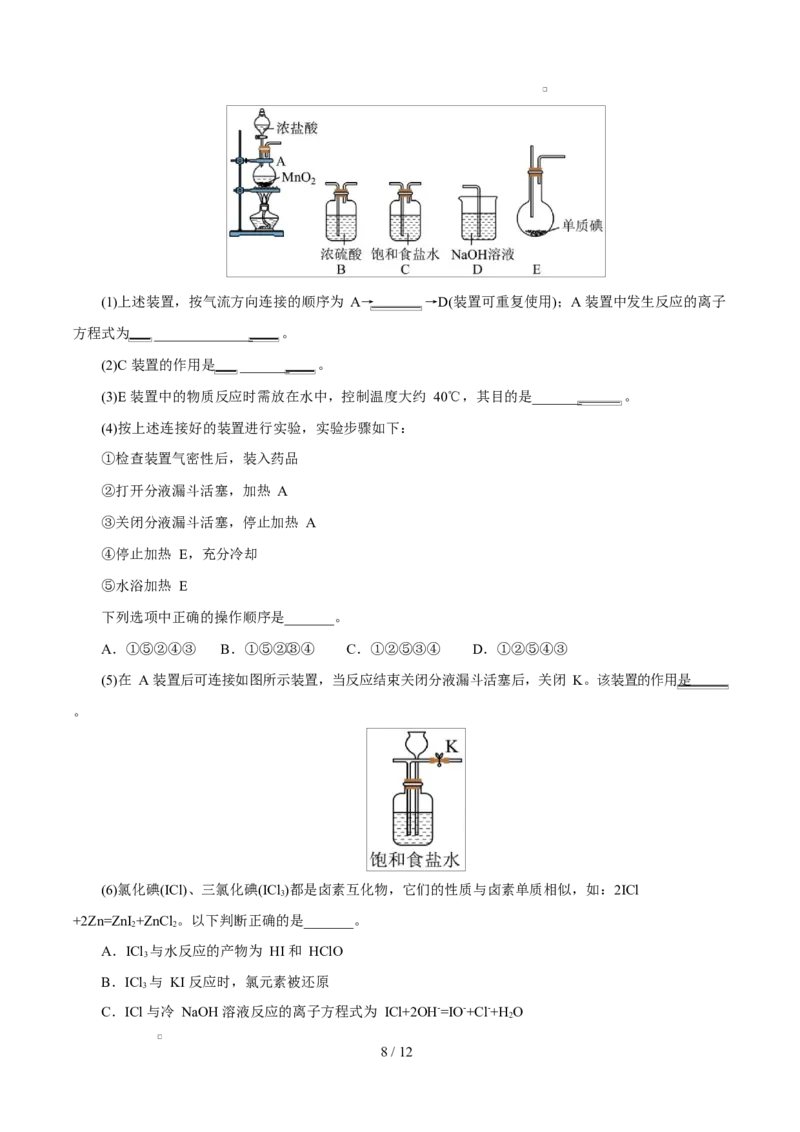
7 / 12(1)上述装置,按气流方向连接的顺序为 A→ →D(装置可重复使用);A 装置中发生反应的离子
方程式为 ______________ 。
(2)C 装置的作用是 _______ 。
(3)E 装置中的物质反应时需放在水中,控制温度大约 40℃,其目的是_______ 。
(4)按上述连接好的装置进行实验,实验步骤如下:
①检查装置气密性后,装入药品
②打开分液漏斗活塞,加热 A
③关闭分液漏斗活塞,停止加热 A
④停止加热 E,充分冷却
⑤水浴加热 E
下列选项中正确的操作顺序是_______。
A.①⑤②④③ B.①⑤②③④ C.①②⑤③④ D.①②⑤④③
(5)在 A 装置后可连接如图所示装置,当反应结束关闭分液漏斗活塞后,关闭 K。该装置的作用是
。
(6)氯化碘(ICl)、三氯化碘(ICl )都是卤素互化物,它们的性质与卤素单质相似,如:2ICl
3
+2Zn=ZnI+ZnCl 。以下判断正确的是_______。
2 2
A.ICl 与水反应的产物为 HI 和 HClO
3
B.ICl 与 KI 反应时,氯元素被还原
3
C.ICl 与冷 NaOH 溶液反应的离子方程式为 ICl+2OH-=IO-+Cl-+H O
2
8 / 12D.ICl 与水的反应属于氧化还原反应
(7)已知硫氰[(SCN) ]的化学性质与 Cl 的类似,被称为“拟卤素”,如:(SCN)
2 2
+2NaOH=NaSCN+NaSCNO+H O。阴离子的还原性顺序为 I->SCN->Br->Cl-。下列说法中不正确的是_______。
2 2
A.若 Cl、(SCN) 发生泄漏,均可喷洒石灰水进行处理
2 2
B.(SCN) +2NaOH=NaSCN+NaSCNO+H O 是氧化还原反应
2 2
C.Cl 与 KSCN 溶液发生反应的离子方程式为 Cl+2SCN-=(SCN) +2Cl-
2 2 2
D.(SCN) 可以与 KBr 溶液反应:(SCN) +2KBr=2KSCN+Br
2 2 2
【答案】(1) A→CBEB→D(2 分) MnO
2
+4H++2Cl- Mn2++ Cl
2
↑+ 2H
2
O(2 分)
(2)除去 Cl 中的 HCl(2 分)
2
(3)适当提高温度,增加反应速率;减少 I 的升华和 ICl 的挥发(2 分)
2
(4)D(3 分)
(5)储存多余的 Cl(2 分)
2
(6)C(3 分)
(7)D(3 分)
【解析】利用二氧化锰与浓盐酸加热制备氯气,氯气中含有氯化氢、水蒸气杂质,因此混合气体先通
过饱和食盐水溶液,除去氯化氢,再通过浓硫酸除去水蒸气,得到干燥纯净的氯气,氯气进入到装置 E 中,
与碘进行反应,由于 ICl(氯化碘)红棕色液体,易水解,所以还必须连接装置 B,最后多余的尾气被碱液吸
收,按气流方向连接的顺序为 ACBEBD。
(1)由分析可知,上述装置,按气流方向连接的顺序为 A→C→B→E→B→D;A 装置中二氧化锰和浓盐
酸在受热条件下反应生成氯气,发生反应的离子方程式为:MnO
2
+4H++2Cl- Mn2++ Cl
2
↑+ 2H
2
O。
(2)由分析可知,C 装置中盛有饱和食盐水,作用是除去 Cl₂中的 HCl。
(3)I 易升华,ICl 易挥发,E 装置中的物质反应时需放在水中,控制温度大约 40℃,其目的是:适当提
2
高温度,增加反应速率;减少 I₂的升华和 ICl 的挥发。
(4)置连接好后,首先检查装置的气密性,不漏气后,加入药品,打开分液漏斗活塞,反应开始进行,
用水浴法给装置 E 加热,反应结束后,停止加热 E,充分冷却,待到室温后,分液漏斗活塞在关闭, 正确
实验步骤为①②⑤④③,故选 D。
(5)在 A 装置后可连接如图的装置,当反应结束关闭分液漏斗活塞后,关闭 K,该装置可以用来储存多
余的 Cl,避免释放到空气中污染空气。
2
(6)A 项,由题意可知,ICl 与水反应 I 元素非金属性弱显正价,故应结合水电离出的 OH-,产物为 HIO
3 2
,氯元素显负价结合水电离出的 H+ ,产物为 HCl,故 A 错误;B 项,ICl
3
与 KI 反应时,ICl
3
中的+3 价 I
9 / 12被还原,故 B 错误;C 项,ICl 中 I 元素为+1 价 I,Cl 为-1 价氯,故 ICl 与冷 NaOH 溶液反应:ICl
+2OH-=IO-+Cl-+H O,故 C 错误;D 项,ICl 与水发生反应:ICl+ HO=HIO+HCl,反应中没有化合价的改变,
2 2
故不属于氧化还原反应,D 项错误;故选 C。
(7)A 项,石灰水是氢氧化钙的水溶液,显碱性,Cl 可以和碱溶液反应:2Cl
2 2
+2Ca(OH) =CaCl +Ca(ClO) +2H O,(SCN) 和氢氧化钙的反应和 Cl 相似:2
2 2 2 2 2 2
(SCN) +2Ca(OH) =Ca(SCN) +Ca(SCNO) +2H O。所以可以用石灰水处理,故 A 正确;B 项,Cl 与 NaOH
2 2 2 2 2 2
反应属于氧化还原反应,(SCN) 和氢氧化钠的反应与 Cl 类似,(SCN) +2NaOH = NaSCN+NaSCNO+H O 也
2 2 2 2
是氧化还原反应,B 正确;C 项,根据阴离子的还原性顺序为 SCN->Cl-,还原性强的物质可以生成还原性
弱的物质,所以该反应可以发生,故 C 正确;D 项,根据阴离子的还原性顺序为 SCN->Br-,还原性强的物
质可以生成还原性弱的物质,则该反应不能发生,故 D 错误;故选 D。
五、由钛铁矿制备钛流程(23 分)
钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为 FeTiO )制备钛的流程如下。
3
(1)作为“航空金属”,推测钛(Ti)最不可能具有的性质是_______。
A.硬度大 B.密度大 C.熔点高 D.抗腐蚀
(2)对上述流程认识正确的是_______。
A.四家工厂中发生的主反应都属于氧化还原反应 B.生产工艺中需要消耗热能和电能
C.合成厂中消耗的原料比为 1:1 D.氯化厂中被氧化的元素是 Ti
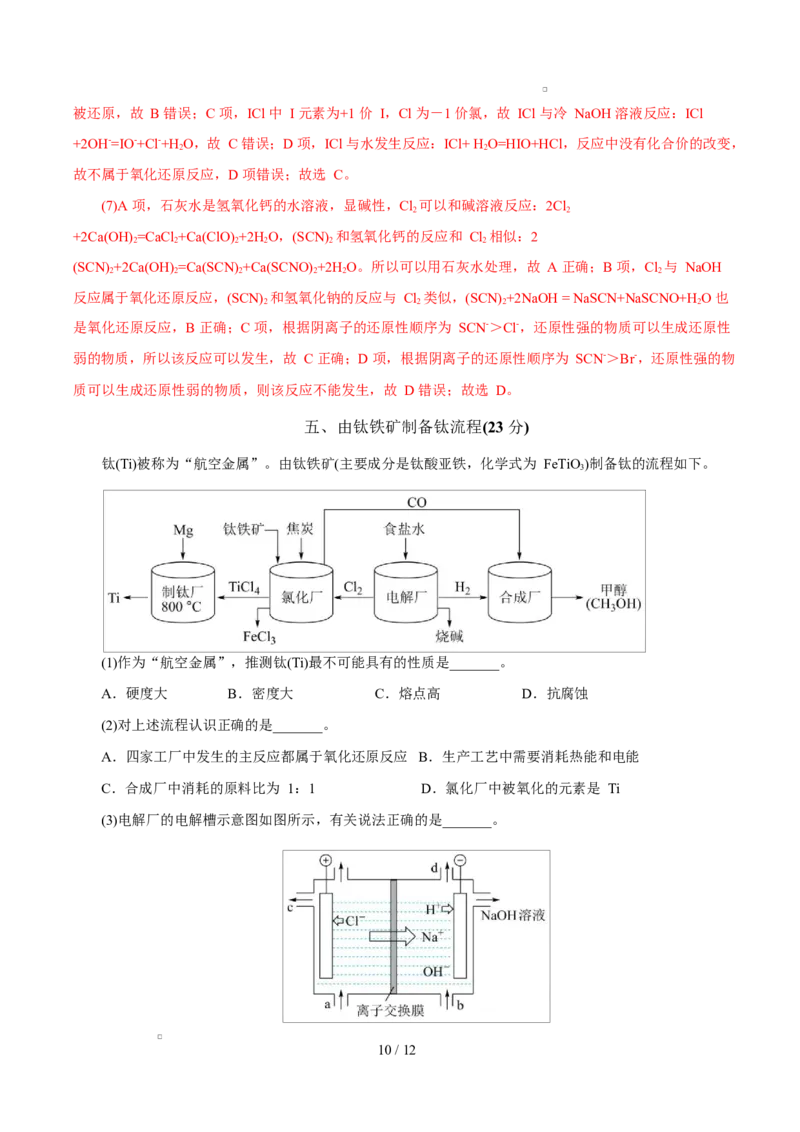
(3)电解厂的电解槽示意图如图所示,有关说法正确的是_______。
10 / 12A.a 口进水 B.b 口进精制饱和食盐水
C.c 口出的是 Cl-,OH-是由 b 口进入的 D.d 口出的是 H
2
(4)下列关于氯气的说法正确的是_______。
A.氯气的密度比空气小 B.氯气在化学反应中只能作氧化剂
C.液氯是将氯气溶于水后的分散系 D.液氯常温下不与单质铁反应
(5)氯化厂副产品 FeCl 还可通过 (任写化学方程式)制得。写出它的一种用途______________ 。
3
(6)制钛厂实际生产中,需在氩气环境下操作。其目的是 ______________ ;已知金属钛常温下不
与强酸反应,为提高金属钛的产率,制钛时常使用过量的镁。现有一份钛与镁的混合样品,设计实验去除
镁以得到纯净的钛:____________________________ 。
(7)在某些工艺过程中,需要控制条件以形成 TiO ·nH O 溶胶,该溶胶的分散质颗粒直径大小在
2 2
_______ 范围。利用 _______效应的实验,可迅速判断生产条件是否控制合理。
(8)依据“绿色化学”理念,该工艺存在的优点有(任写一项) ______________ 。
(9)四氯化钛(TiCl)是上述流程中的重要中间产物,依据下表信息,要精制含少量 SiCl 杂质的 ,可
4 4
采用 _______ 方法。
TiCl SiCl
4 4
熔点/℃ -23.2 -68.8
沸点/℃ 136.4 57.6
【答案】(1)B(2 分)
(2)AB(2 分)
(3)D(2 分)
(4)D(2 分)
(5)2Fe+3Cl FeCl(2 分) 制备胶体、作催化剂、腐蚀铜板(2 分)
2 3
(6)避免金属被氧化(2 分) 将钛与镁的混合物溶解在稀硫酸中,过滤,洗涤烘干(2 分)
(7)1~100nm(2 分) 丁达尔(1 分)
(8)成本低、综合利用 CO、氯气等废气不给环境造成污染(2 分)
(9)分馏(蒸馏) (2 分)
【解析】钛铁矿和焦炭、氯气氯化生成氯化铁、氯化钛,氯化钛被镁还原为钛单质;电解食盐水生成
氯气和氢气和氢氧化钠,氢气和 CO 合成甲醇。
11 / 12(1)作为“航空金属”,推测钛(Ti)硬度大、熔点高、抗腐蚀,性能优良,其用于航空,则其密度不会太大,
故选 B;
(2)A 项,电解食盐水生成氯气和氢气和氢氧化钠,氢气和 CO 合成甲醇,钛铁矿和焦炭、氯气氯化生
成氯化铁、氯化钛,氯化钛被镁还原为钛单质,四家工厂中发生的主反应中都存在元素化合价改变,都属
于氧化还原反应,正确;B 项,电解需要电能,氯化生成氯化钛、合成甲醇、高温置换镁需要消耗热能,
正确;C 项,由碳氢守恒,则合成厂中消耗的原料一氧化碳、氢气物质的量比为 1:2,错误;D 项,FeTiO
3
中钛为+4、铁为+2,氯化生成氯化铁、氯化钛,则氯化厂中被氧化的元素是铁,错误;故选 AB;
(3)A 项,由图,钠离子向右侧移动,右侧为阴极室,则 a 口进精制饱和食盐水,错误;B 项,结合 A
分析,b 口进水,钠离子迁移过来后生成氢氧化钠,错误;C 项,电解过程中,左侧氯离子生成氯气,c 口
出的是稀氯化钠溶液,右侧电极生成氢气和氢氧根离子,错误;D 项,右侧生成氢气,则 d 口出的是 H,
2
正确;故选 D;
(4)A 项,氯气的密度比空气大,错误;B 项,氯气和水生成氯化氢和次氯酸,在化学反应中做氧化剂
和还原剂,错误;C 项,液氯是液态氯气,不是溶液,错误;D 项,液氯常温下不与单质铁反应,点燃和
铁生成氯化铁,正确;故选 D。
(5)液氯常温下不与单质铁反应,点燃和铁生成氯化铁,2Fe+3Cl FeCl;氯化铁可用制备胶体、作催
2 3
化剂、腐蚀铜板等;
(6)镁和钛高温容易和空气中氧气反应,则在氩气环境下操作,其目的是避免金属被氧化;已知金属钛
常温下不与强酸反应,则钛与镁的混合样品,设计实验去除镁以得到纯净的钛,方案为:将钛与镁的混合
物溶解在稀硫酸中,过滤,洗涤烘干;
(7)胶体是分散质粒子大小在 1nm~100nm 的分散系;光束通过胶体时,光线能够发生散射作用而产生
丁达尔效应,而通入其它分散系时不能产生丁达尔效应;
故该溶胶的分散质颗粒直径大小在 1nm~100nm 范围。利用丁达尔效应的实验,可迅速判断生产条件是
否控制合理。
(8)该工艺多种工艺联合进行,使得生产成本低、综合利用 CO、氯气等废气不给环境造成污染;
(9)利用物质的沸点不同,制含少量 SiCl 杂质的 TiCl ,可采用蒸馏方法。
4 4
12 / 12