文档内容
.2019 年镇江市化学中考试卷(ZH-05)
(满分:100分考试时间:100分钟)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 C1-35.5 Na-23 Ca-40 Fe-56
Cu-64 Ag-108 Ba-137
一、单项选择题(本题包括15小题,每小题2分,共30分。每小题只有一个选项符合题
意)
1.下列属于纯净物的是( )
A. 食用醋 B. 葡萄酒 C. 蒸馏水 D. 酸牛奶
2.下列物质的用途主要与其化学性质有关的是( )
A. 金刚石用于切割玻璃 B. 高粱常用于酿制白酒
C. 铜常用来做电线电缆 D. 干冰可用作人工降雨
3.下列化学用语正确的是( )
A. 二个氮分子---- B. 氦气----
C. 二硫化碳--- D. 锌离子---
4.下列做法正确的是( )
.
A 高温煮沸,杀菌消毒 B. 霉变大米,清洗食用
C. 深埋电池,消除污染 D. 食品防腐,硫磺熏蒸
5.下列归类正确的是( )
选项 归类 内容
A 常见的碱 纯碱、氨水、火碱
B 挥发性酸 浓盐酸、浓硫酸、浓硝酸
C 大气污染物 、二氧化硫、二氧化碳
D 有机高分子材料 聚乙烯、聚氯乙烯、有机玻璃
A. A B. B C. C D. D
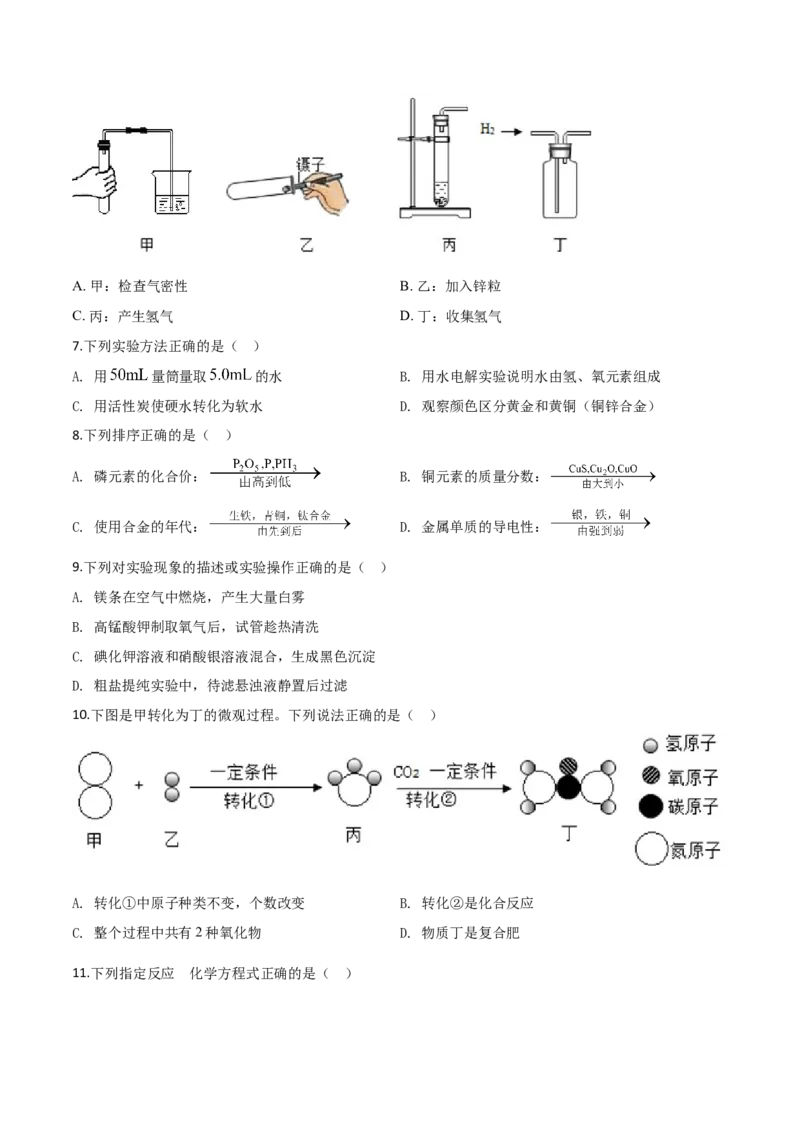
6.下图是实验室制取并收集氢气的主要操作,其中不正确的是( )A. 甲:检查气密性 B. 乙:加入锌粒
C. 丙:产生氢气 D. 丁:收集氢气
7.下列实验方法正确的是( )
A. 用 量筒量取 的水 B. 用水电解实验说明水由氢、氧元素组成
C. 用活性炭使硬水转化为软水 D. 观察颜色区分黄金和黄铜(铜锌合金)
8.下列排序正确的是( )
A. 磷元素的化合价: B. 铜元素的质量分数:
C. 使用合金的年代: D. 金属单质的导电性:
9.下列对实验现象的描述或实验操作正确的是( )
A. 镁条在空气中燃烧,产生大量白雾
B. 高锰酸钾制取氧气后,试管趁热清洗
C. 碘化钾溶液和硝酸银溶液混合,生成黑色沉淀
D. 粗盐提纯实验中,待滤悬浊液静置后过滤
10.下图是甲转化为丁的微观过程。下列说法正确的是( )
A. 转化①中原子种类不变,个数改变 B. 转化②是化合反应
C. 整个过程中共有2种氧化物 D. 物质丁是复合肥
的
11.下列指定反应 化学方程式正确的是( )A. 酸雨形成的原因
B. 证明铜的活动性大于银:
C. 用含氢氧化铝的药物治疗胃酸过多:
D. 超氧化钾( )与二氧化碳反应生成碳酸钾和氧气:
12.电解饱和氯化钾溶液的化学方程式: 下列说法中不正确的
是( )
A. 可用于自来水生产中杀菌消毒 B. 农业上常用 改良酸性土壤
C. 反应中有2中元素化合价发生改变 D. 可由海水蒸发结晶、精制获得
13.下列物质的转化在给定条件下均能实现的是( )
A.
B.
C.
D.
14.下列实验操作能达到实验目的的是( )
选项 物质 目的 主要实验操作
A 和 鉴别 分别用燃着的木条试验,观察现象
B 溶液中混有少量盐酸 检验 取样,滴加 溶液,观察是否产生沉淀
溶液中混有少量
C 除杂 加入 溶液至不再产生沉淀,过滤
加入过量的 溶液,过滤、洗涤,再分别向滤
D 和 的混合溶液 分离
渣和滤液中加入适量稀盐酸A. A B. B C. C D. D
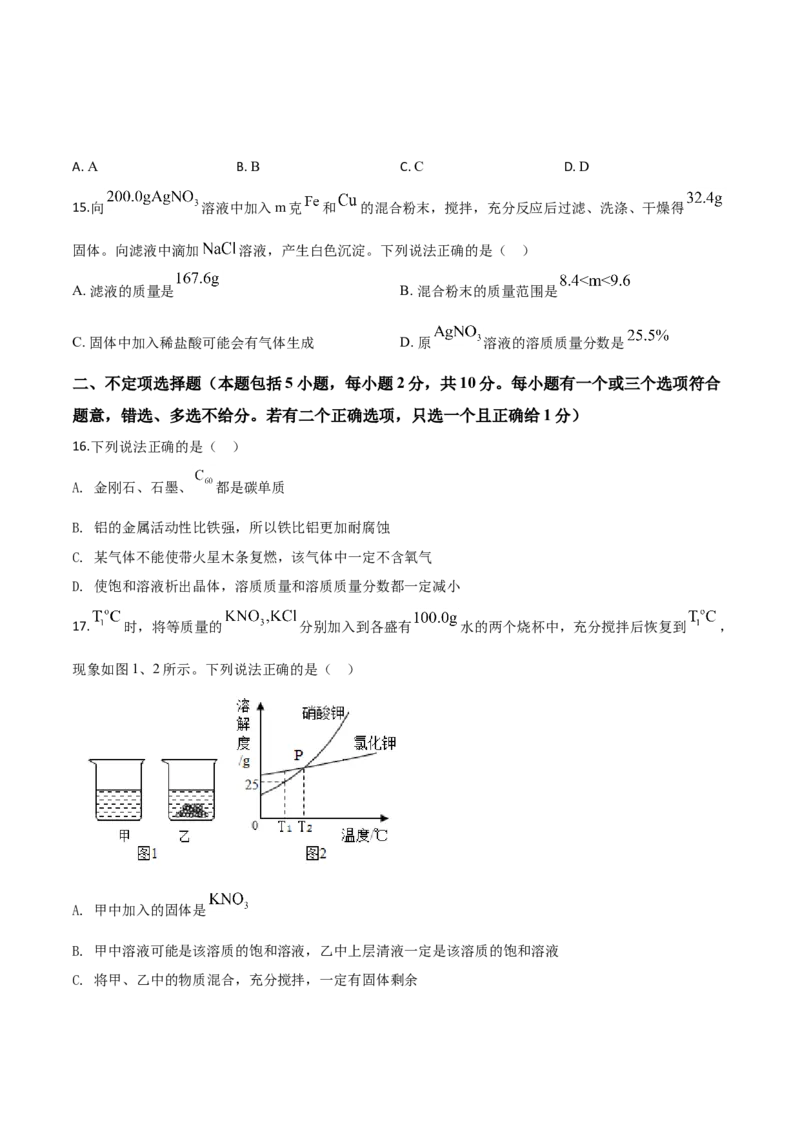
15.向 溶液中加入m克 和 的混合粉末,搅拌,充分反应后过滤、洗涤、干燥得
固体。向滤液中滴加 溶液,产生白色沉淀。下列说法正确的是( )
A. 滤液的质量是 B. 混合粉末的质量范围是
C. 固体中加入稀盐酸可能会有气体生成 D. 原 溶液的溶质质量分数是
二、不定项选择题(本题包括5小题,每小题2分,共10分。每小题有一个或三个选项符合
题意,错选、多选不给分。若有二个正确选项,只选一个且正确给1分)
16.下列说法正确的是( )
A. 金刚石、石墨、 都是碳单质
B. 铝的金属活动性比铁强,所以铁比铝更加耐腐蚀
C. 某气体不能使带火星木条复燃,该气体中一定不含氧气
D. 使饱和溶液析出晶体,溶质质量和溶质质量分数都一定减小
17. 时,将等质量的 分别加入到各盛有 水的两个烧杯中,充分搅拌后恢复到 ,
现象如图1、2所示。下列说法正确的是( )
A. 甲中加入的固体是
B. 甲中溶液可能是该溶质的饱和溶液,乙中上层清液一定是该溶质的饱和溶液
C. 将甲、乙中的物质混合,充分搅拌,一定有固体剩余D. 若将甲、乙的温度从 升高到 ,两溶液中的溶质质量分数相等
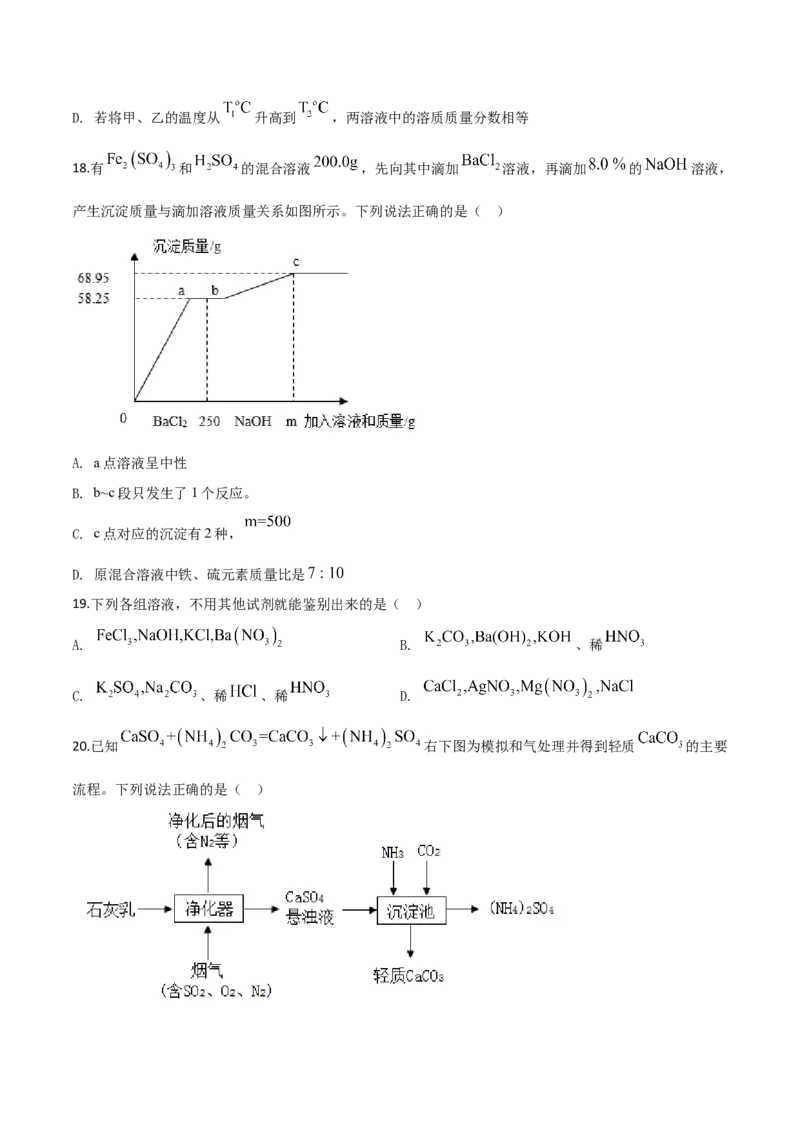
18.有 和 的混合溶液 ,先向其中滴加 溶液,再滴加 的 溶液,
产生沉淀质量与滴加溶液质量关系如图所示。下列说法正确的是( )
A. a点溶液呈中性
B. b~c段只发生了1个反应。
C. c点对应的沉淀有2种,
D. 原混合溶液中铁、硫元素质量比是
19.下列各组溶液,不用其他试剂就能鉴别出来的是( )
A. B. 、稀
C. 、稀 、稀 D.
20.已知 右下图为模拟和气处理并得到轻质 的主要
流程。下列说法正确的是( )A. 净化时用石灰乳而不用石灰水,是为了充分吸收
B. 净化时反应的化学方程式:
C. 沉淀时应先通入 后,再通入 ,有利于 的生成
D. 由沉淀池中发生的反应可知,溶解性:
三、填空题(本题包括5小题,共18分)
21.用化学符号表示:
(1)水银______________________ (2)2个钠离子______________________
(3)人体缺少___________元素会导致甲状腺疾病。 (4)最常用的溶剂_____________
22.选择下列适当的物质填空(选填序号):
A 明矾 B 硝酸 C 洗洁精 D 熟石灰 E 硫酸 F 食盐 G 维生素 H 硝酸铵
(1)溶于水温度降低的是______________.
(2)生活中作乳化剂的是_______________
(3)铅蓄电池含有的酸是_______________.
(4)厨房中作调味品的是__________________.
(5)可配制波尔多液的是______________________
(6)蔬菜,水果中富含有__________________
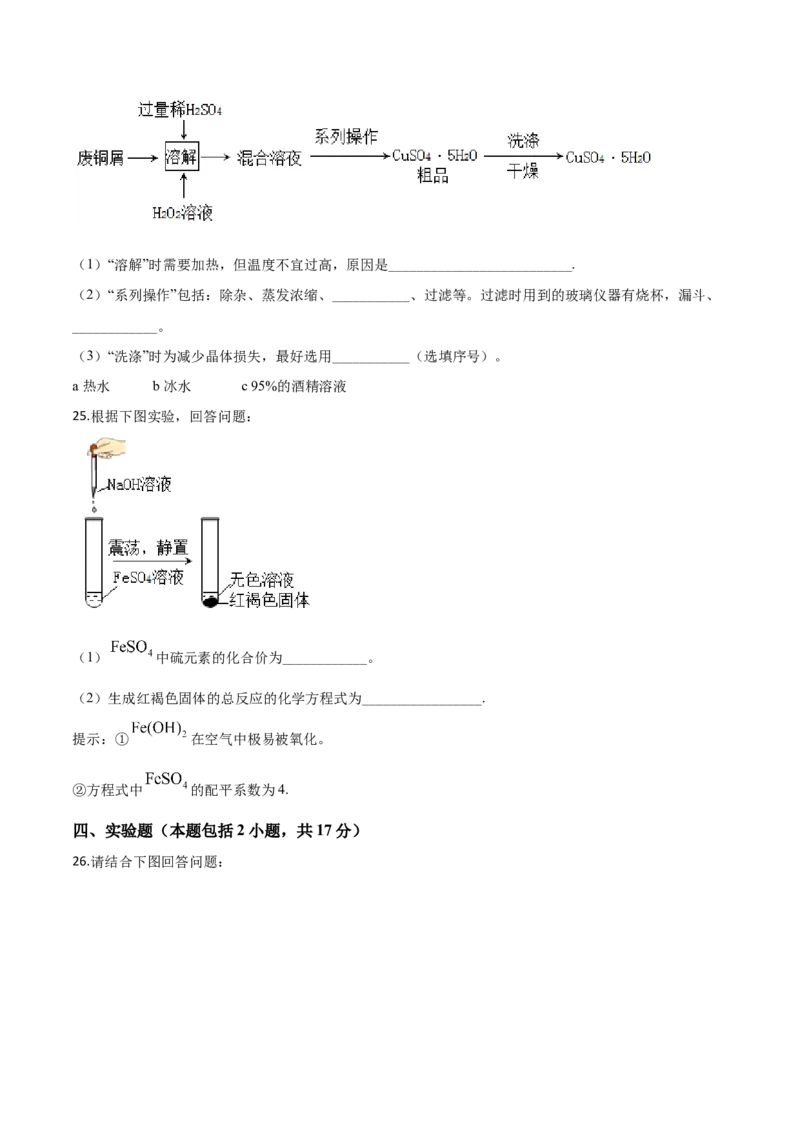
23.合金是重要的金属材料.
(1) 按其一定比例熔合后冷却可得到储氢合金材料。该过程属于__________变化(选填“物理”或
“化学”)
(2)图中能表示锡铅合金的是___________(选填“a”“b”或“c”)
24.用废铜屑生产硫酸铜晶体 的流程如下:(1)“溶解”时需要加热,但温度不宜过高,原因是__________________________.
(2)“系列操作”包括:除杂、蒸发浓缩、___________、过滤等。过滤时用到的玻璃仪器有烧杯,漏斗、
____________。
(3)“洗涤”时为减少晶体损失,最好选用___________(选填序号)。
a 热水 b 冰水 c 95%的酒精溶液
25.根据下图实验,回答问题:
(1) 中硫元素的化合价为____________。
(2)生成红褐色固体的总反应的化学方程式为_________________.
提示:① 在空气中极易被氧化。
②方程式中 的配平系数为4.
四、实验题(本题包括2小题,共17分)
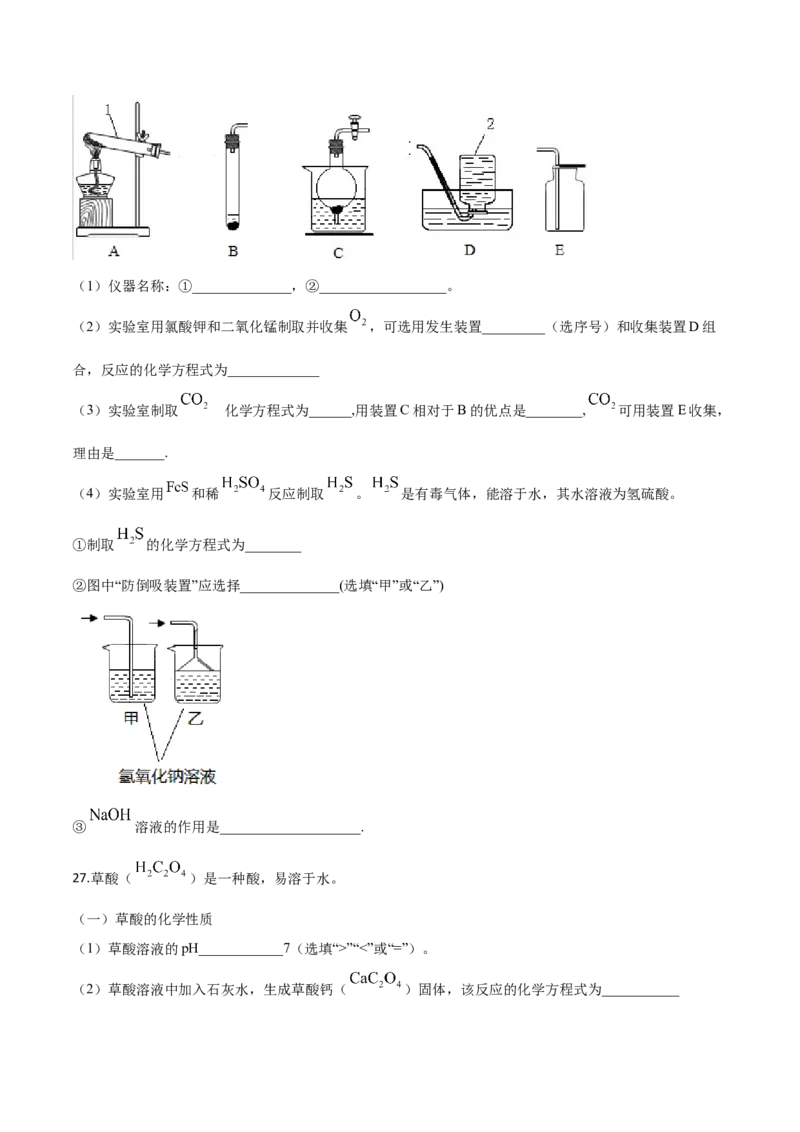
26.请结合下图回答问题:(1)仪器名称:①______________,②__________________。
(2)实验室用氯酸钾和二氧化锰制取并收集 ,可选用发生装置_________(选序号)和收集装置D组
合,反应的化学方程式为_____________
的
(3)实验室制取 化学方程式为______,用装置C相对于B的优点是________, 可用装置E收集,
理由是_______.
(4)实验室用 和稀 反应制取 。 是有毒气体,能溶于水,其水溶液为氢硫酸。
①制取 的化学方程式为________
②图中“防倒吸装置”应选择______________(选填“甲”或“乙”)
③ 溶液的作用是____________________.
27.草酸( )是一种酸,易溶于水。
(一)草酸的化学性质
(1)草酸溶液的pH____________7(选填“>”“<”或“=”)。
(2)草酸溶液中加入石灰水,生成草酸钙( )固体,该反应的化学方程式为___________(二) 热分解探究
资料:
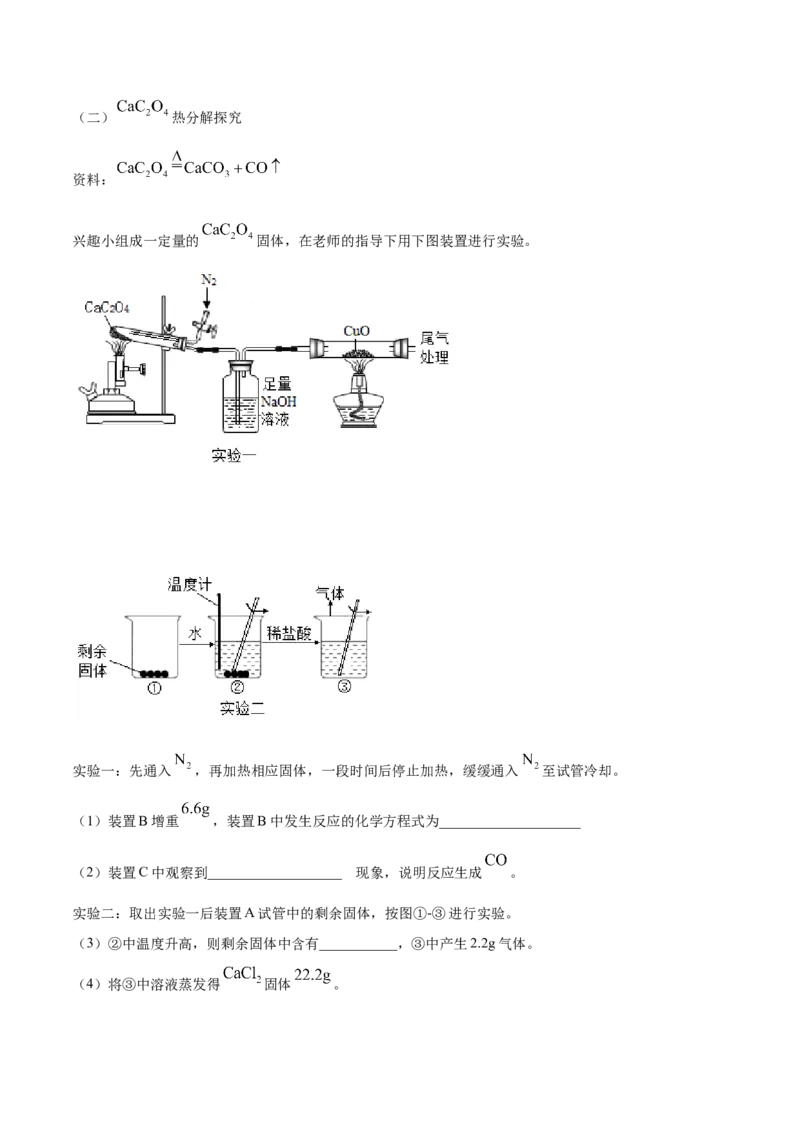
兴趣小组成一定量的 固体,在老师的指导下用下图装置进行实验。
实验一:先通入 ,再加热相应固体,一段时间后停止加热,缓缓通入 至试管冷却。
(1)装置B增重 ,装置B中发生反应的化学方程式为____________________
的
(2)装置C中观察到___________________ 现象,说明反应生成 。
实验二:取出实验一后装置A试管中的剩余固体,按图①-③进行实验。
(3)②中温度升高,则剩余固体中含有___________,③中产生2.2g气体。
(4)将③中溶液蒸发得 固体 。结论:(1)取用的 固体的质量为____________g。
(2)结合实验及相关数据,本实验中 分解的总反应化学方程式为_____________
五、推断题(本题包括2小题,共11分)
28.现有一包固体粉末,可能含有 中的一种或几种。
进行如下实验:
(1)取少量固体溶于足量水中,过滤得到白色固体A和无色滤液B,则原固体中一定不含有________.
(2)向固体A中加入足量稀盐酸,固体全部溶解,无气泡产生,则原固体中一定含有____________一定
不含有______________。
(3)向滤液B中通入 ,产生白色沉淀,则原固体中一定还含有_______,一定不含有______。
29.如图为某些物质间的转化关系(部分反应条件省略)。A、B、E、F、G均为气体,B能使稀高锰酸钾
溶液退色,E、F组成元素相同,且F有毒,G是一种最轻的气体;乙、丁均为黑色的固体氧化物,反应④
是工业炼铁的原理;反应②是光合作用。
(1)化学式:G_________,丙____________.
(2)反应①、④的化学方程式:①_________________;④________________________
(3)甲一定含有的元素是____________________.
(4)Fe与蓝色溶液的反应属于____________________反应(填基本反应类型)。
六、综合题(本题包括1小题,共14分)
30.金属及其化合物在生产生活中有广泛的应用。(一)金属的应用和防护
(1)用不锈钢、合成橡胶、氧化镁等材料制造的飞机轮胎属于___________________材料。
(2)航空煤油是飞机的燃料,它主要是由___________炼制的。
(3)铁易生锈,提出防止铁生锈的一种方法__________。
(4)特种钢中含有少量 。 和 粉混合在高温下反应可得到 ,该反应的化学方程式为
_______.
(5) 受热分解生成高熔点的 。 可用作阻燃剂,其主要原理是__________(选
填序号)。
a 分解吸热,降低可燃物着火点 b 覆盖燃烧物,隔绝氧气
(二)制备还原性铁粉
实验室利用废铁屑(含少量 )为原料制备还原性铁粉的流程如下:
(1) 粉可使“酸溶”产生的 转化为 ,该反应的化学方程式为_________.
(2)检验 已洗净的方法:取最后一次洗涤后的滤液,先加入一定量稀盐酸,再滴加_______溶液,
无明显现象。
(3)“干燥”时有少量 发生下列转化: ,该转化的化学方程式为
____________________.
(4)“焙烧”前,应将炭粉与“干燥”所得固体均匀混合,目的是_______________.(三)测定还原性铁粉的组成
还原性铁粉中含有少量 ,小组同学在老师的指导下进行以下实验。
资料:① 在加热时与 反应能生成相应氧化物。
② 不与酸反应。
实验1:取 样品,加入足量稀 ,充分反应后生成 。
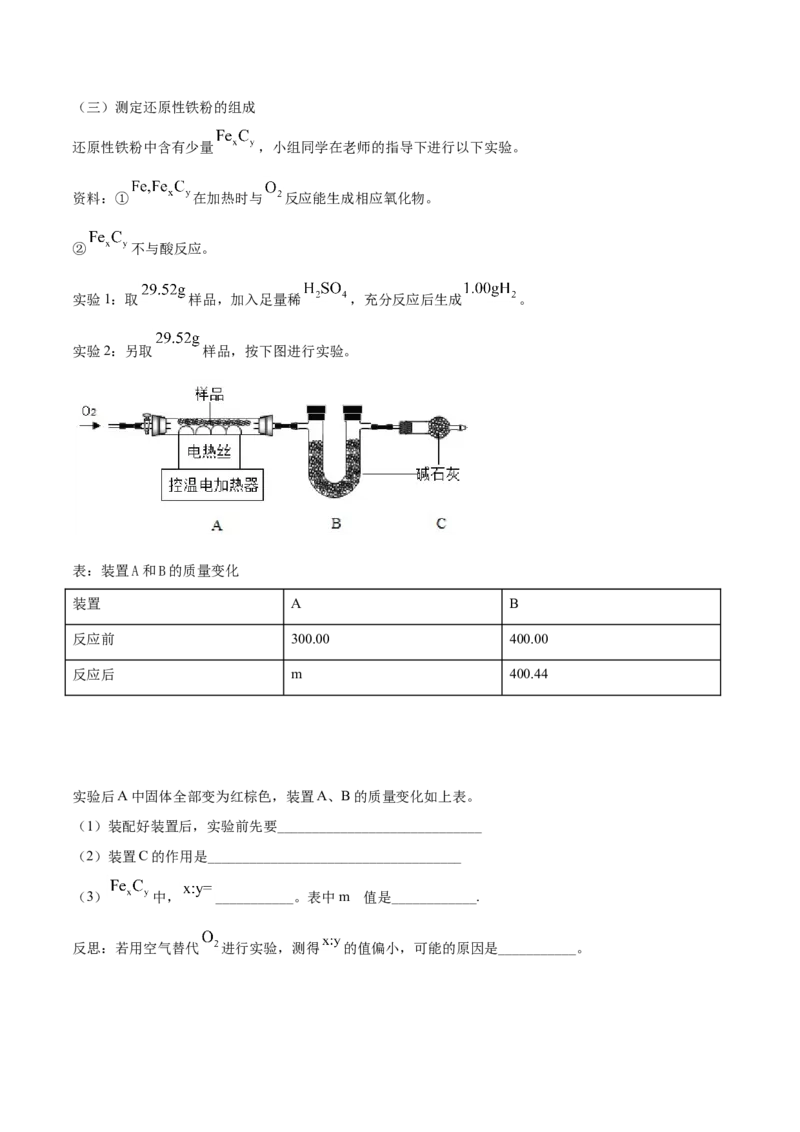
实验2:另取 样品,按下图进行实验。
表:装置A和B的质量变化
装置 A B
反应前 300.00 400.00
反应后 m 400.44
实验后A中固体全部变为红棕色,装置A、B的质量变化如上表。
(1)装配好装置后,实验前先要_____________________________
(2)装置C的作用是____________________________________
的
(3) 中, ___________。表中m 值是____________.
反思:若用空气替代 进行实验,测得 的值偏小,可能的原因是___________。