文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:75 分钟,分值:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第一章、第二章1~2节(人教版2019选择性必修1)。
5.考试结束后,将本试卷和答题卡一并交回。
6.难度系数:0.68。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Fe 56 Cu 64
第Ⅰ卷(选择题 共 42 分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.已知化学反应 的能量变化如图所示,下列叙述中正确的是
A.每生成2分子AB吸收bkJ热量
B.断裂 键和 键,放出akJ能量
C.该反应中反应物的总能量高于生成物的总能量
D.该反应的
2.下列说法中错误的是
A.活化分子之间发生的碰撞一定是有效碰撞
B.对有气体参加的化学反应,增大压强使容器容积减小,可使单位体积内活化分子数增多,因而化学
反应速率增大
1 / 10C.升高温度,可使反应物分子中活化分子的百分数增大,因而增大化学反应速率
D.加入适宜的催化剂,可使反应物分子中活化分子的百分数增大,因而增大化学反应速率
3.以 为原料合成 的相关反应为:①
;② 。部分键能数据如下表所示,
则 共价键的键能是
共价键
键能/ 803 414 326 464
A. B. C. D.
4.下列事实能说明反应物本身性质是影响化学反应速率的决定性因素的是
A.银能与浓HNO 反应,而不与浓盐酸反应
3
B.Cu与浓HNO 反应的速率比与稀HNO 反应快
3 3
C.N 与O 在常温、常压下不反应,放电时可反应
2 2
D.Fe与热的浓硫酸反应,而不与冷的浓硫酸反应
5.可逆反应 在不同条件下的化学反应速率如下,其中表示的反应速率最快
的是
A.v(B)=0.4 mol/(L·s) B.v(A)=5 mol/(L·min)
C.v(C)=0.2 mol/(L·s) D.v(D)=6 mol/(L·min)
6.已知分解1molH O 放出热量98kJ。在含有少量 的溶液中,HO 分解机理为:
2 2 2 2
慢
快
下列说法正确的是
A. 是该反应的催化剂 B.反应的速率与 浓度有关
C. D.反应活化能等于
7.丙二醇脱氧脱水反应的循环机理如图所示。下列说法错误的是
2 / 10A.若将原料换为乙二醇,有乙烯生成
B.反应历程中存在极性键、非极性键的断裂和形成
C.反应③属于氧化还原反应
D. 降低了反应的焓变,加快了反应速率
8.已知HO(g)=H O(1) ΔH=-QkJ•mol-1,
2 2 1
C HOH(g)=C HOH(1) ΔH=-QkJ•mol-1,
2 5 2 5 2
C HOH(g)+3O (g)=2CO (g)+3HO(g) ΔH=-QkJ•mol-1
2 5 2 2 2 3
若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为 kJ
A.Q+Q +Q B.0.5(Q +Q +Q )
1 2 3 1 2 3
C.0.5Q -1.5Q +0.5Q D.1.5Q -0.5Q +0.5Q
1 2 3 1 2 3
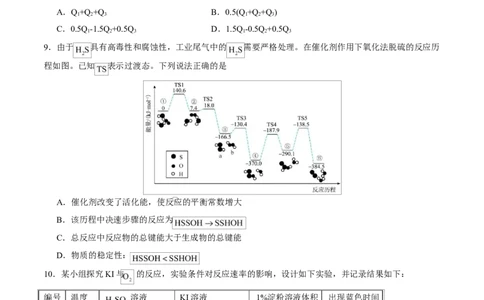
9.由于 具有高毒性和腐蚀性,工业尾气中的 需要严格处理。在催化剂作用下氧化法脱硫的反应历
程如图。已知 表示过渡态。下列说法正确的是
A.催化剂改变了活化能,使反应的平衡常数增大
B.该历程中决速步骤的反应为
C.总反应中反应物的总键能大于生成物的总键能
D.物质的稳定性:
10.某小组探究KI与 的反应,实验条件对反应速率的影响,设计如下实验,并记录结果如下:
编号 温度 溶液 KI溶液 1%淀粉溶液体积 出现蓝色时间
1mL 40s
①
1mL 20s
②
1mL 5s
③
1mL 未见蓝色
④下列说法正确的是
3 / 10A.由实验①②可知, 增大,反应速率加快
B.实验②③是探究浓度对反应速率的影响
C.在 被 氧化过程中, 不参加反应
D.由实验①③④可知,温度升高,反应速率越慢
11.下列热化学方程式正确的是
A.甲烷的燃烧热为 ,则甲烷燃烧的热化学方程式可表示为
:
B. 下,将 和 置于密闭容器中充分反应生成 ,放热 ,其
热化学方程式为 :
C.已知在 下, 燃烧生成水蒸气放出 热量,其热化学方程式为
:
D. 时,强酸与强碱的稀溶液发生中和反应的中和热为 ,硫酸溶液与氢氧化
钾溶液反应的热化学方程式为 :
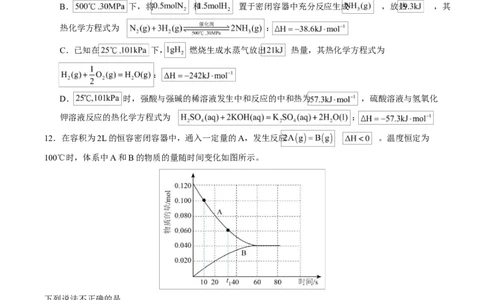
12.在容积为2L的恒容密闭容器中,通入一定量的A,发生反应 。温度恒定为
100℃时,体系中A和B的物质的量随时间变化如图所示。
下列说法不正确的是
A.0~10s时段,反应速率 为
B. 时刻体系内 为
C.若 ,则反应达到平衡状态
D.欲测定A的相对分子质量,应采用的适宜条件为高温低压
13.为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计和结论都正
确的是
4 / 10选 影响
方案设计 现象 结
论 项 因素
向恒温恒容密闭玻璃容器中充入100mLHI气 气体颜色 对于反应前后气体总体积不变的
A 压强
体,分解达到平衡后再充入100mLAr 不变 可逆反应,改变压强平衡不移动
将封装有 和 混合气体的烧瓶浸泡 气体颜色 升高温度,平衡向吸热反应方
向 B 温度
在热水中 变深 移动
催化 向1mL乙酸乙酯中加入1mL0.3mol·L-1 上层液体 使用合适的催化剂可使平衡向
正 C
剂 溶液,水浴加热 逐渐减少 反应方向移动
向1mL0.1mol·L-1 溶液中加入 黄色溶液 增大反应物浓度,平衡向正反应
D 浓度
1mL1.0mol·L-1HBr溶液 变橙色 方向移动
14.向恒容密闭容器中充入 和 ,发生反应: ,测
得 的平衡转化率与温度、投料比 的关系如图所示。下列叙述正确的是
A.该反应低温条件下自发
B.增大体积, 增大, 减小
C.投料比 ,且平衡常数
D.当 ,温度为 时,氨气的平衡转化率为
第 II 卷(非选择题 共 58 分)
二、非选择题:本题共4个小题,共58分(除标注外,每空2分)。
15.(14分)能源是现代社会物质文明的原动力,研究化学反应能量变化意义重大。回答下列问题:
(1)下列反应中,属于放热反应的是___________
5 / 10A.碳与 反应 B.铝和氧化铁反应
C. 受热分解 D.锌与盐酸反应
(2)已知,在 和101kPa下,部分化学键的键能数据如表所示。
化学键
键能 391 946 803 462 193
科学家发现了一种新的气态分子 ( ),有关反应为 。在 和101ka下,
转化为 的热化学方程式为 ,由此可知 与 中更稳定的 是
(填化学式)。
(3)甲醇是重要的能源以及化工原料。已知:
(I )
(Ⅱ
(Ⅲ)
时,甲醇的燃烧热的热化学方程式为 ,反应中转移 个电子时,放出 的热
量。
(4)工业上利用 和 制甲醇:
(Ⅳ) 。
①借助高分子选择性吸水膜可有效提高 平衡利用率。其原因是 。
②下列关于反应IV的说法不正确的是 (填序号)。
A.有利于减少碳排放,体现了绿色化学思想
B.降低温度可提高 含量,工业生产时应控制低温
C.充分反应后,放出热量可能大于49kJ
D.当气体密度保持不变时,反应一定达到平衡状态
16.(15分)工业上常采用催化氧化的方法将 转化为 ,涉及反应如下:
。
部分化学键的键能如下表所示。
化学键
6 / 10键能/( ) 946 498 464
回答下列问题:
(1)氮气和氧气谁更稳定,从化学键的角度简述原因? 。
(2) 的 (填“<”、“>“或“=”)。
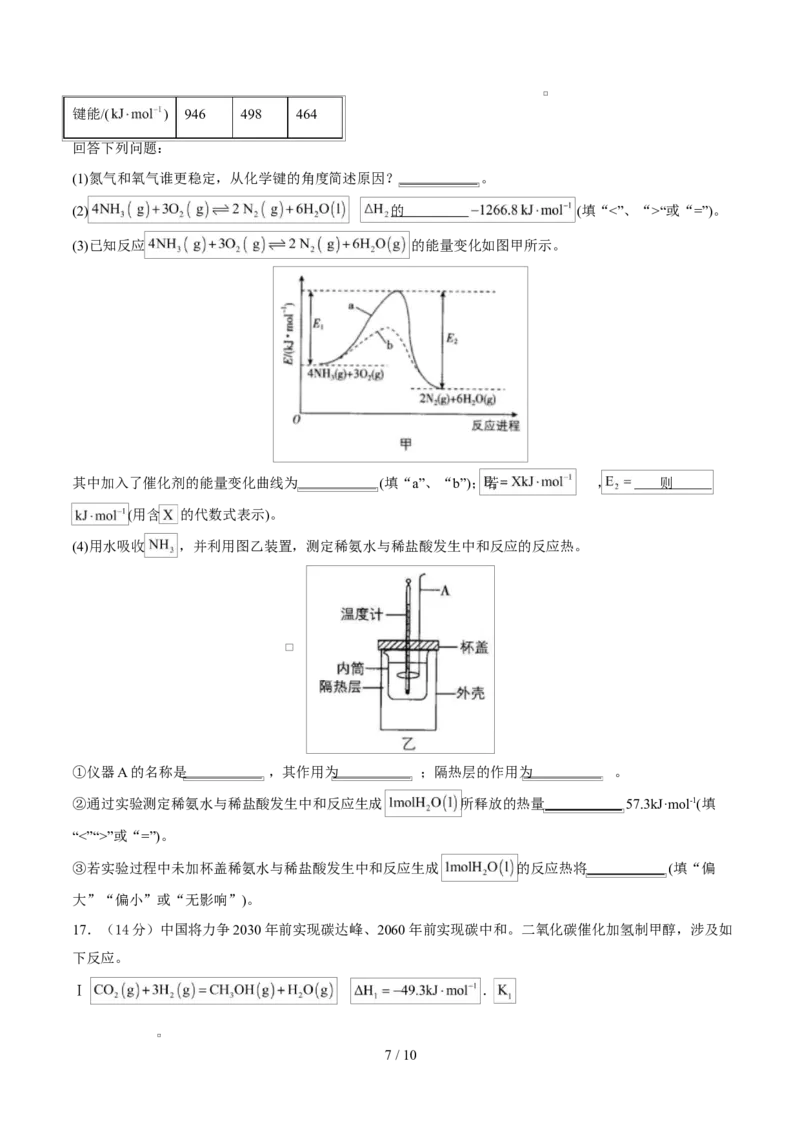
(3)已知反应 的能量变化如图甲所示。
其中加入了催化剂的能量变化曲线为 (填“a”、“b”);若 , 则
(用含 的代数式表示)。
(4)用水吸收 ,并利用图乙装置,测定稀氨水与稀盐酸发生中和反应的反应热。
①仪器A的名称是 ,其作用为 ;隔热层的作用为 。
②通过实验测定稀氨水与稀盐酸发生中和反应生成 所释放的热量 57.3kJ·mol-1(填
“<”“>”或“=”)。
③若实验过程中未加杯盖稀氨水与稀盐酸发生中和反应生成 的反应热将 (填“偏
大”“偏小”或“无影响”)。
17.(14分)中国将力争2030年前实现碳达峰、2060年前实现碳中和。二氧化碳催化加氢制甲醇,涉及如
下反应。
Ⅰ .
7 / 10Ⅱ .
Ⅲ .
回答下列问题:
(1)反应Ⅰ的平衡常数 (用平衡常数 表示) , ;一般认为反
应Ⅰ通过反应Ⅱ和反应Ⅲ两步来实现,若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的 是
(填标号)。
A. B .
C. D.
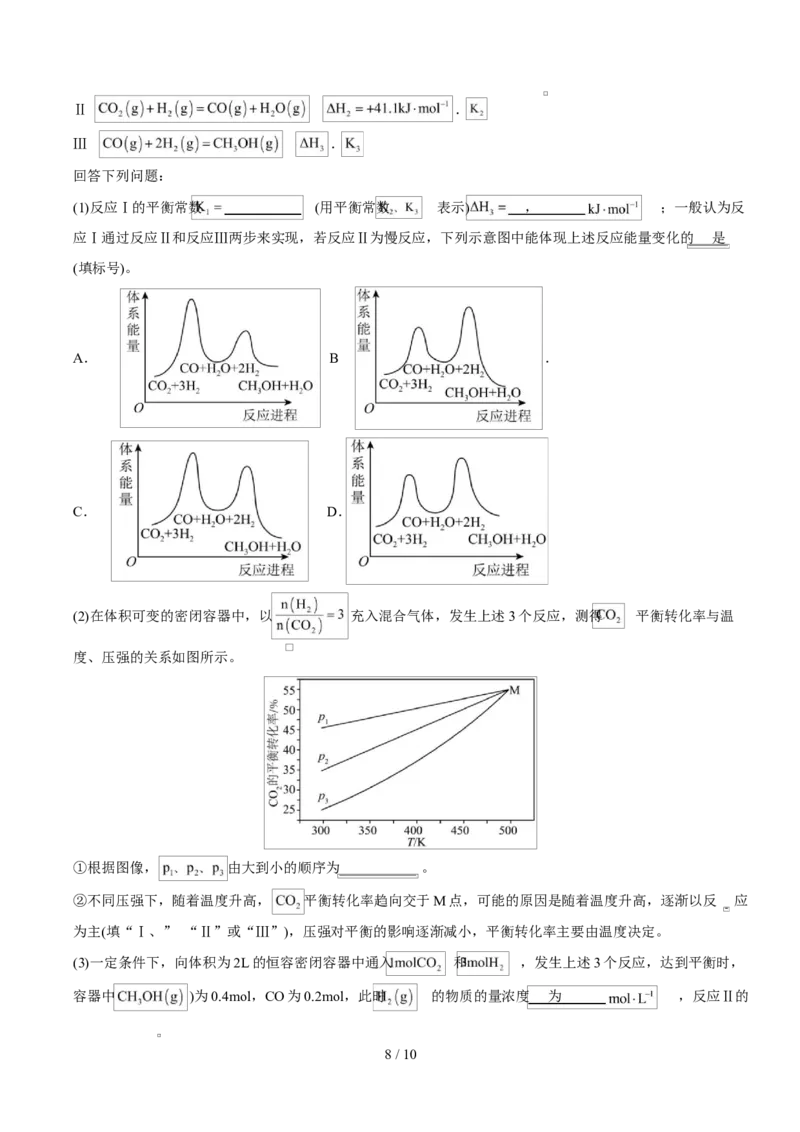
(2)在体积可变的密闭容器中,以 充入混合气体,发生上述3个反应,测得 平衡转化率与温
度、压强的关系如图所示。
①根据图像, 由大到小的顺序为 。
②不同压强下,随着温度升高, 平衡转化率趋向交于M点,可能的原因是随着温度升高,逐渐以反 应
为主(填“Ⅰ、” “Ⅱ”或“Ⅲ”),压强对平衡的影响逐渐减小,平衡转化率主要由温度决定。
(3)一定条件下,向体积为2L的恒容密闭容器中通入 和 ,发生上述3个反应,达到平衡时,
容器中 )为0.4mol,CO为0.2mol,此时 的物质的量浓度 为 ,反应Ⅱ的
8 / 10物质的量分数平衡常数 ( 为用物质的量分数替代浓度计算的平衡常数)。
18.(15分)I.某化学小组安装两套如图所示的相同装置,用以探究影响HO 分解速率的因素。
2 2
(1)仪器b的名称为是 。
(2)MnO 催化下HO 分解的化学方程式为 。
2 2 2
(3)有如下实验设计方案,请帮助他们完成表格中未填部分。
实验编号 实验目的 T/K 催化剂 浓度
甲组实验I 作实验参照 298 3滴FeCl 溶液 10mL2%H O
3 2 2
甲组实验Ⅱ 298 10mL5%H O
2 2
Ⅱ.某研究性学习小组利用HC O 溶液和酸性KMnO 溶液的反应探究“外界条件的改变对化学反应速率的影
2 2 4 4
响”,进行了如下实验:
室温下溶液颜色褪至无
室温下,试管中所加试剂及其用量/mL
实验
色所需时间/min
编号 2.0mol∙L-1 H 0.2mol∙L-1 3mol∙L-1稀
2
HC O 溶液 O KMnO 硫酸
2 2 4 4
1 3.0 2.0 3.0 V 4.0
1
2 2.0 V 3.0 2.0 5.2
2
3 1.0 4.0 3.0 2.0 6.4
(4)补全方程式: 。
(5)实验过程使用了“控制变量法”,则V= ,V= ;根据上表中的实验数据,可以得到的结论
1 2
是 。
(6)该小组同学查阅已有的资料后,提出假设:生成物中的MnSO 为该反应的催化剂,请你帮助该小组同学
4
完成实验方案验证假设。
实 室温下,试管中所加试剂及其用量/mL 再向试 室温下
9 / 10验 管中加 溶液颜
编 入少量 色褪至
2.0mol∙L-1 HC O 0.2mol∙L-1 3mol∙L-1稀
2 2 4
号 HO 固体 无色所
溶液 2 KMnO 溶液 硫酸
4
需时间
/min
4 3.0 2.0 3.0 2.0 _______ t
①再向试管中加入的少量固体的化学式为 。
②若该小组同学提出的假设成立,应观察到的现象是 。
10 / 10