文档内容
2024-2025 学年高二化学上学期期中模拟卷
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:选择性必修1(不含电化学部分)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第Ⅰ卷(选择题 共 40 分)
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.合理利用某些盐能水解的性质,可以解决许多生产、生活中的问题。下列叙述的事实与盐水解的性质
无关的是
A.配制FeSO 溶液时,加入一定量 Fe粉
4
B.沸水中加入饱和的氯化铁溶液制备Fe(OH) 胶体
3
C.长期施用铵态氮肥会使土壤酸化
D.热碱水清洗厨房里的油污
【答案】A
【解析】A.亚铁离子容易被氧化生成铁离子,加入Fe粉,Fe可与铁离子反应生成亚铁离子,从而防止亚
铁离子被氧化,与盐类水解无关,A正确;B.沸水中加入饱和氯化铁溶液,升高温度,铁离子水解平衡
正向移动,因此能制备氢氧化铁胶体,与盐水解有关,B错误;C.长期使用铵态氮肥,铵根离子水解生
成氢离子,从而使土壤酸化,与盐水解有关,C错误;D.升高温度,碱水中的碳酸根离子水解程度增
大,溶液的碱性增强,去油污的能力也随之增强,与盐水解有关,D错误;故答案选A。
2.下列事实一定能说明HF是弱酸的是
A.用HF溶液做导电性实验,灯泡很暗
B.1mol/L的HF水溶液能使紫色石蕊试液变红
C.常温下0.1mol/L的HF溶液的pH为2.3
D.HF能与NaCO 溶液反应,产生CO 气体
2 3 2
【答案】C
【解析】A.溶液的导电性强弱与溶液中离子浓度大小有关,溶液中离子浓度大,溶液的导电能力强,则
用氢氟酸溶液做导电性实验,灯泡很暗只能说明溶液中的离子浓度小,不能说明氢氟酸是弱酸,故A错
学科网(北京)股份有限公司 学科网(北京)股份有限公司误;B.1mol/L的氢氟酸溶液能使紫色石蕊试液变红只能说明氢氟酸溶液显酸性,不能说明氢氟酸是弱
酸,故B错误;C.0.1mol/L的氢氟酸溶液的pH为2.3说明氢氟酸在溶液中部分电离出氢离子,溶液中存
在电离平衡,属于弱酸,故C正确;D.氢氟酸溶液能与碳酸钠溶液反应生成二氧化碳气体只能说明氢氟
酸的酸性强于碳酸,不能说明氢氟酸是弱酸,故D错误;故选C。
3.工业上由CO 和H 合成气态甲醇的热化学方程式为CO(g)+3H(g)=CH OH(g)+HO(g) ΔH<0。已知
2 2 2 2 3 2
该反应是放热反应。下列表示合成甲醇的反应的能量变化示意图正确的是
A. B.
C. D.
【答案】A
【解析】由热化学方程式可知,反应物、生成物均为气态,焓变为负,为放热反应,且生成物为液态时放
出热量更多,选项A中图符合。故答案选A。
4.已知: ; ; ;
。
下列叙述正确的是
A. B.
C. D. 代表 的燃烧热
【答案】C
【解析】A.氢气生成等量液态水放出热量比生成等量气态水多,反应热更小,A错误;B.等物质的量的
C(s)生成CO时放出的热量比生成CO 时少,反应热更大,B错误;C.根据盖斯定律,选项中的方程式
2
可由(反应②-反应①)×2得到,ΔH=2(ΔH-ΔH ),C正确;D.氢气的燃烧热化学方程式中,氢气前系数为
2 1
1,表示1mol氢气在氧气中完全燃烧生成液态水放出的热量,D错误;故答案选C。
5.下列说法正确的是
A.凡是放热反应都是自发的,因为吸热反应都是非自发的
B.非自发反应在任何情况下都不会发生反应
C.常温下,反应 不能自发进行,则该反应的
D.标准状况下,熵值:1mol <1mol CO
【答案】C
学科网(北京)股份有限公司 学科网(北京)股份有限公司【分析】判断化学反应进行的方向从焓变和熵变两个维度去判断,当 ,反应可自发进
行;即当ΔH<0,ΔS>0时,一定能够自发进行;当ΔH<0,ΔS<0时低温下能够自发进行,当ΔH>0,
ΔS>0时,高温下能够自发进行,当ΔH>0,ΔS<0时,一定不能自发进行,据此分析解题。
【解析】A.由分析可知,放热反应不一定都是自发的,吸热反应也不都是非自发的,A错误;B.由分析
可知,非自发反应在外界条件改变时可能会自发进行反应,B错误;C.常温下
,反应该反应的ΔS>0,故其常温下不能自发进行,是因为该反应的ΔH>0,必须高温时才能自发进行,
C正确;D.相同条件下,气体相对分子质量越大,熵值越大,标准状况下,熵值:1mol CO>1mol CO,
2
D错误;故选C。
6.某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列说法正确的是
2 2 2 3 2
A.恒容下,再充入一定量的HO(g),平衡向正反应方向移动,v 加快、v 减慢
2 正 逆
B.缩小容器的体积,v >v
正 逆
C.恒容下,再充入一定量的Ar气,平衡向正反应方向移动
D.恒容下,再充入一定量的CH=CH (g),CH=CH (g)的平衡转化率增大
2 2 2 2
【答案】B
【解析】A.恒容下,再充入一定量的水蒸气,反应物的浓度增大,平衡向正反应方向移动,正、逆反应
速率均增大,故A错误;B.该反应是气体体积减小的反应,缩小容器的体积,气体压强增大,平衡向正
反应方向移动,正反应速率大于逆反应速率,故B正确;C.恒容下,再充入一定量的不参与反应的氩
气,反应体系中各物质浓度不变,反应速率不改变,化学平衡不移动,故C错误;D.恒容下,再充入一
定量的乙烯,反应物的浓度增大,平衡向正反应方向移动,但的转化率减小,故D错误;故选B。
7.已知反应① 和反应② 在T℃时的
平衡常数分别为 和 ,该温度下反应③ 的平衡常数为 ,则下列
说法正确的是
A.反应①的平衡常数
B.反应②中,增大氢气浓度,平衡正移, 增大
C.对于反应②,T℃时,
D.对于反应②,恒容时,温度升高,K值减小,则该反应为放热反应
【答案】D
【解析】A.反应①的平衡常数 ,故A错误;B.平衡常数只与温度有关,所以温度不变时增
大氢气浓度,平衡常数不变,故B错误;C.由盖斯定律,反应③=反应①-反应②,所以 ,故C错
误;D.对于反应②,恒容时升高温度,K值减小,说明升温平衡逆向移动,所以该反应为放热反应,故
学科网(北京)股份有限公司 学科网(北京)股份有限公司D正确;故答案为:D。
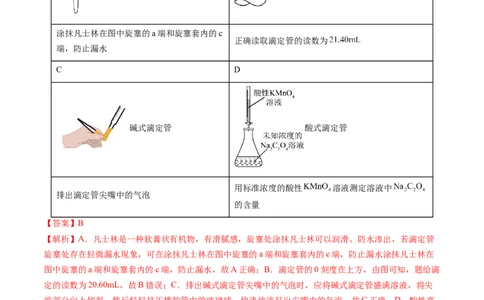
8.酸碱中和滴定是一种重要的实验方法,需要用到酸式滴定管和碱式滴定管,下列有关滴定管的判断、
使用或操作有误的是
A B
酸式滴定管 酸式/碱式滴定管
涂抹凡士林在图中旋塞的a端和旋塞套内的c
正确读取滴定管的读数为
端,防止漏水
C D
碱式滴定管 酸式滴定管
用标准浓度的酸性 溶液测定溶液中
排出滴定管尖嘴中的气泡
的含量
【答案】B
【解析】A.凡士林是一种软膏状有机物,有滑腻感,旋塞处涂抹凡士林可以润滑、防水渗出,若滴定管
旋塞处存在轻微漏水现象,可在涂抹凡士林在图中旋塞的a端和旋塞套内的c端,防止漏水涂抹凡士林在
图中旋塞的a端和旋塞套内的c端,防止漏水,故A正确;B.滴定管的0刻度在上方,由图可知,题给滴
定的读数为20.60mL,故B错误;C.排出碱式滴定管尖嘴中的气泡时,应将碱式滴定管盛满溶液,将尖
端部分向上倾斜,然后轻轻挤压橡胶管中的玻璃球,快速放液赶出尖嘴中的气泡,故C正确;D.酸性高
锰酸钾溶液具有强氧化性会腐蚀碱式滴定管的橡胶管,所以用标准浓度的酸性高锰酸钾溶液测定溶液中草
酸钠的含量时,应将草酸钠溶液放入锥形瓶中,酸性高锰酸钾溶液用酸式滴定管盛装,故D正确;故选
B。
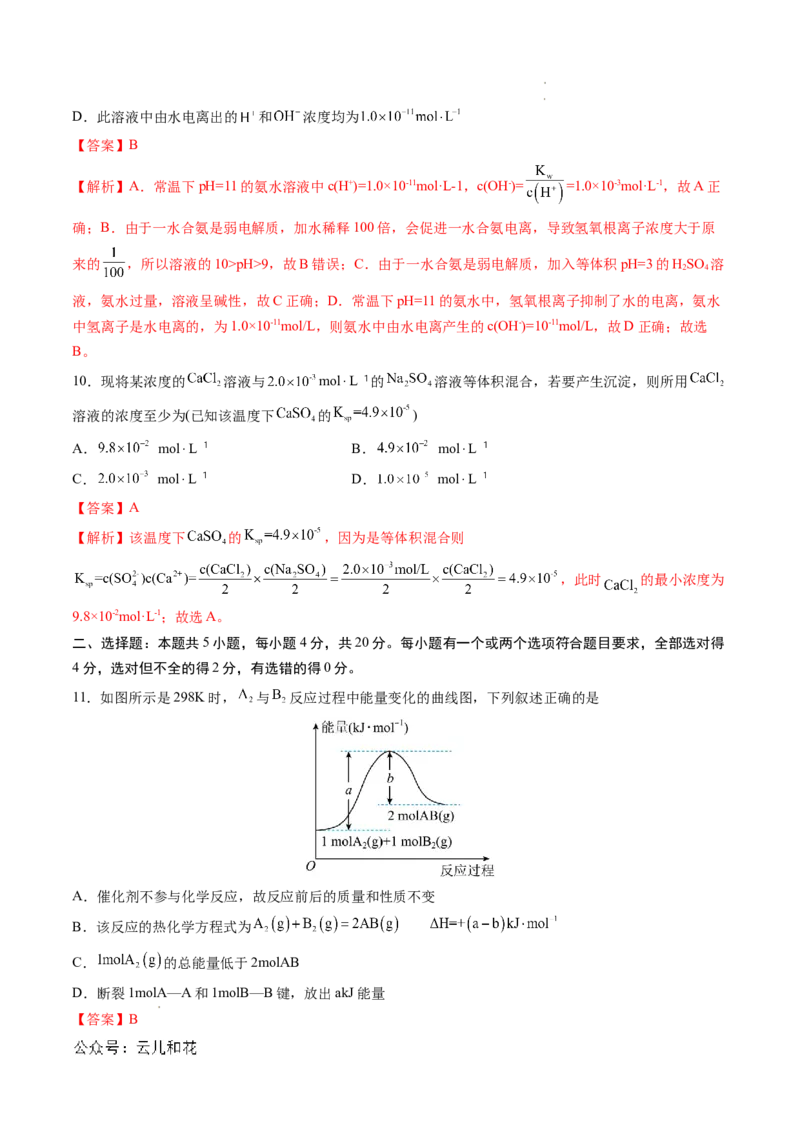
9.常温下,关于pH=11的氨水溶液,下列说法不正确的是
A.溶液中
B.加水稀释100倍后,溶液的
C.与等体积pH=3的 溶液充分混合后,溶液呈碱性
学科网(北京)股份有限公司 学科网(北京)股份有限公司D.此溶液中由水电离出的 和 浓度均为
【答案】B
【解析】A.常温下pH=11的氨水溶液中c(H+)=1.0×10-11mol·L-1,c(OH-)= =1.0×10-3mol·L-1,故A正
确;B.由于一水合氨是弱电解质,加水稀释100倍,会促进一水合氨电离,导致氢氧根离子浓度大于原
来的 ,所以溶液的10>pH>9,故B错误;C.由于一水合氨是弱电解质,加入等体积pH=3的HSO 溶
2 4
液,氨水过量,溶液呈碱性,故C正确;D.常温下pH=11的氨水中,氢氧根离子抑制了水的电离,氨水
中氢离子是水电离的,为1.0×10-11mol/L,则氨水中由水电离产生的c(OH-)=10-11mol/L,故D正确;故选
B。
10.现将某浓度的 溶液与 mol⋅L 的 溶液等体积混合,若要产生沉淀,则所用
溶液的浓度至少为(已知该温度下 的 )
A. mol⋅L B. mol⋅L
C. mol⋅L D. mol⋅L
【答案】A
【解析】该温度下 的 ,因为是等体积混合则
,此时 的最小浓度为
9.8×10-2mol·L-1;故选A。
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.如图所示是298K时, 与 反应过程中能量变化的曲线图,下列叙述正确的是
A.催化剂不参与化学反应,故反应前后的质量和性质不变
B.该反应的热化学方程式为
C. 的总能量低于2molAB
D.断裂1molA—A和1molB—B键,放出akJ能量
【答案】B
学科网(北京)股份有限公司 学科网(北京)股份有限公司【分析】由图可知,该反应为反应物总能量小于生成物总能量的吸热反应,反应的热化学方程式为A(g)
2
+B (g)=2AB(g) =+(a-b)kJ•mol-1。
2
【解析】A.催化剂能改变反应途径、降低反应的活化能,所以催化剂参与化学反应,A错误;B.由分析
可知,反应的热化学方程式为A(g)+B (g)=2AB(g) =+(a-b)kJ•mol-1,B正确;C. 的总能量
2 2
低于2molAB(g)的总能量,C错误;D.破坏化学键时,需要吸收能量,则断裂1molA—A和1molB—B
键,吸收akJ能量,D错误;故选B。
12.在一密闭容器中发生反应 ,3min达到平衡状态, 增加了
0.6mol∙L-1,下列说法正确的是
A.0~3min,
B.在2min末,
C.第4min时, 和 表示的反应速率的值相等
D.若相同时间内, ,则这两段时间内反应速率相等
【答案】C
【解析】A.由反应方程式可知,A呈固态,不能用A的浓度变化表示反应速率,A不正确;B.反应进行
3min时,达到平衡状态, 增加了0.6mol∙L-1,则 ,此速率表
示反应进行3min内的平均速率,不等于2min末的速率,B不正确;C.3min达到平衡状态,此时 =
= ,第4min时反应仍保持平衡状态,所以 和 表示的反应速率的值相等,C正
确;D.由于B、D的化学计量数不等,所以 表示反应进行到不同阶段时的
反应速率,则这两段时间内反应速率不相等,D不正确;故选C。
13.在酸催化作用下,丙烯水化法合成2-丙醇的反应历程如图所示。下列说法正确的是
A.总反应的活化能等于各步反应活化能之和
B.步骤③是该反应的决速步骤
C.丙烯水化法合成2-丙醇反应的
D.升高温度可以同时加快步骤①②③的反应速率
学科网(北京)股份有限公司 学科网(北京)股份有限公司【答案】CD
【解析】A.总反应的活化能不等于各步反应活化能之和,A错误;B.步骤①是该反应的决速步骤,B错
误;C.丙烯水化法合成2-丙醇反应的 ,C正确;D.升高温度可以加快所有反应的速率,即同时
加快步骤①②③的反应速率,D正确;答案选CD。
14.下列实验操作能达到实验目的的是
选项 实验操作 实验目的
探究2NO
2
(g)⇌N
2
O
4
(g)的热效
A 将盛有NO 气体的玻璃球放入热水浴中
2
应
向各盛有5mLH O 溶液的两支试管中分别滴入2滴0.1mol/L的 比较Fe3+与Cu2+对HO 分解的
2 2 2 2
B
FeCl 溶液和0.1mol/L的CuSO 溶液 催化效果
3 4
取少量久置的亚硫酸钠样品溶于除氧蒸馏水中,加入足量的稀
C 验证久置的NaSO 是否变质
2 3
盐酸,再滴加氯化钡溶液,观察是否有白色沉淀出现
向5mL0.1mol/LAgNO 溶液中滴加几滴0.1mol/L NaCl溶液,再
3
D 验证Ksp(AgCl)>Ksp(AgI)
滴加几滴0.1mol/LKI溶液
【答案】AC
【解析】A.NO 为红棕色气体,NO 为无色气体,将盛有NO 气体的玻璃球放入热水浴中,红棕色加
2 2 4 2
深,平衡逆向移动,即2NO
2
(g)⇌N
2
O
4
(g)为放热反应,故A正确;
B.比较Fe3+与Cu2+对HO 分解的催化效果要控制变量,即保证阴离子相同,而实验中所用的为浓度相同
2 2
的FeCl 溶液和CuSO 溶液,故B错误;
3 4
C.加入盐酸除去NaSO ,再加入BaCl 溶液,若有白色沉淀生成则说明NaSO 中含有NaSO ,从而证明
2 3 2 2 3 2 4
NaSO 已氧化变质,故C正确;
2 3
D.向5mL0.1mol/LAgNO 溶液中滴加几滴0.1mol/L NaCl溶液生成AgCl沉淀,硝酸银过量,此时再滴加
3
几滴0.1mol/LKI溶液,生成AgI沉淀,无法证明AgCl和AgI溶度积的大小,故D错误;
故选AC。
15.某温度下,在容积为2L的密闭容器中,X(g)、Y(g)、Z(g)三种物质的物质的量随时间变化的曲线如图
所示,已知4min时改变了一个条件。下列说法正确的是
A.反应进行到a点时,Z的转化率为10%
学科网(北京)股份有限公司 学科网(北京)股份有限公司B.此温度下,3min时向容器中再通入1molX(g)和1molY(g),此时
C.该温度下,反应的平衡常数为
D.该反应的化学方程式为
【答案】B
【分析】由图可知,反应中,X的物质的量增大,Y、Z的物质的量减小,则Y、Z为反应的反应物,X为
生成物,3min反应达到平衡时,X、Y、Z的物质的量之比为(1.0-0.4) mol:(1.2-1.0) mol:(2.0-1.6)
mol=3:1:2,则反应的化学方程式为Y(g)+2Z(g) 3X(g)。
【解析】A. 由图可知,a点时,X的物质的量为0.82mol,则X的变化量为0.42mol,由方程式可知,Z的
变化量为0.28mol,Z的转化率为 ×100%=14%,A项错误;B. 由图可知:3min时达到平衡状态,
由此可列三段式:
则该温度下平衡常数 ,此温度下,3min时向容器中再通入1mol X(g)和1mol Y(g),可得
此时浓度商 ,平衡逆向移动,因此 ,B项正确;C. 由B可知,该温度
下,反应的平衡常数为 ,C项错误;D. 由分析可知,方程式为:Y(g)+2Z(g) 3X(g),D项错误;故选
B。
第 II 卷(非选择题 共 60 分)
三、非选择题:本题共5小题,共60分。
16.(12分)乙烯是重要的有机化工原料,最经济的方法是以乙烷为原料制得。一种乙烷脱氢制乙烯的原
理为C H (g) = C H (g)+H(g) ΔH。
2 6 2 4 2
(1)已知C H、C H、H 的燃烧热ΔH分别为-1560 kJ/mol、-1411 kJ/mol和-286 kJ/mol,则乙烯脱氢的反
2 6 2 4 2
应△H为 kJ/mol。
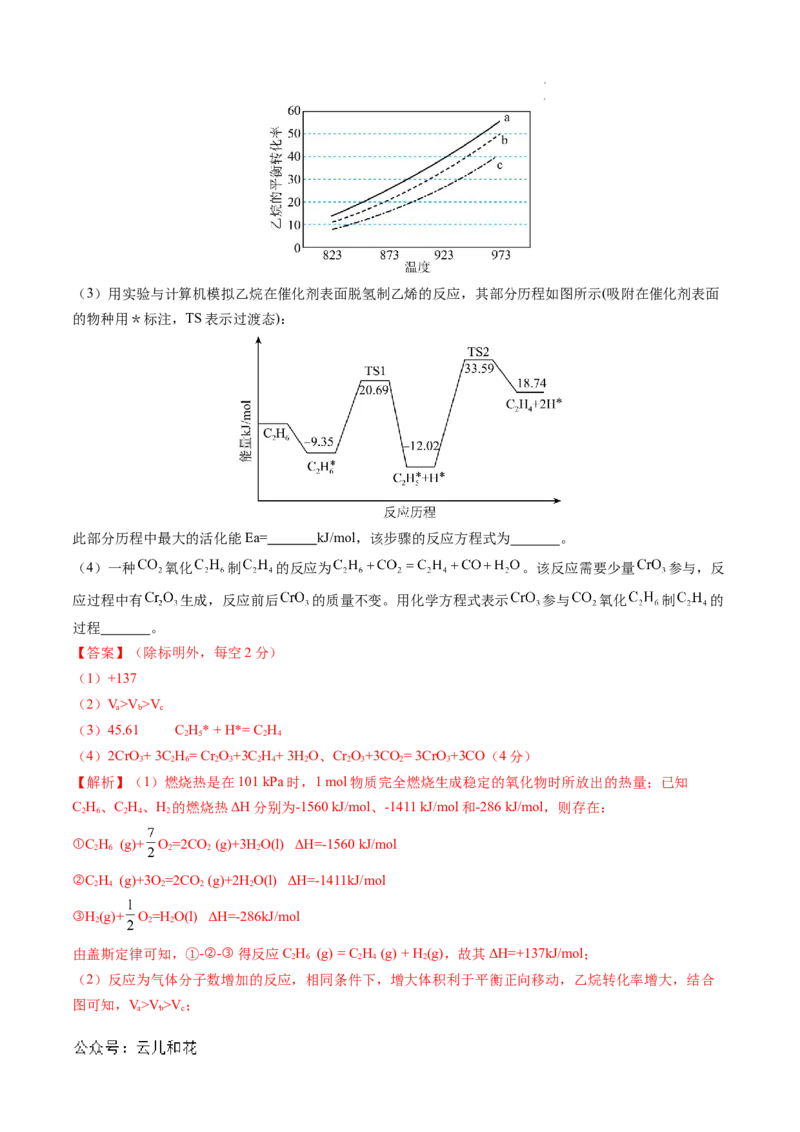
(2)向a、b、c三个容器中各充入1mol乙烷,乙烷的平衡转化率与温度变化的关系如图所示,则V、
a
V、V 的大小关系为 。
b c
学科网(北京)股份有限公司 学科网(北京)股份有限公司(3)用实验与计算机模拟乙烷在催化剂表面脱氢制乙烯的反应,其部分历程如图所示(吸附在催化剂表面
的物种用*标注,TS表示过渡态):
此部分历程中最大的活化能Ea= kJ/mol,该步骤的反应方程式为 。
(4)一种 氧化 制 的反应为 。该反应需要少量 参与,反
应过程中有 生成,反应前后 的质量不变。用化学方程式表示 参与 氧化 制 的
过程 。
【答案】(除标明外,每空2分)
(1)+137
(2)V>V >V
a b c
(3)45.61 C H*+ H*= C H
2 5 2 4
(4)2CrO+ 3C H= CrO+3C H+ 3H O、Cr O+3CO = 3CrO +3CO(4分)
3 2 6 2 3 2 4 2 2 3 2 3
【解析】(1)燃烧热是在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出的热量;已知
C H、C H、H 的燃烧热ΔH分别为-1560 kJ/mol、-1411 kJ/mol和-286 kJ/mol,则存在:
2 6 2 4 2
①C H (g)+ O=2CO (g)+3HO(l) ΔH=-1560 kJ/mol
2 6 2 2 2
②C H (g)+3O=2CO (g)+2HO(l) ΔH=-1411kJ/mol
2 4 2 2 2
③H(g)+ O=H O(l) ΔH=-286kJ/mol
2 2 2
由盖斯定律可知,①-②-③得反应C H (g) = C H (g)+H(g),故其ΔH=+137kJ/mol;
2 6 2 4 2
(2)反应为气体分子数增加的反应,相同条件下,增大体积利于平衡正向移动,乙烷转化率增大,结合
图可知,V>V >V;
a b c
学科网(北京)股份有限公司 学科网(北京)股份有限公司(3)过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,此部分历程
中最大的活化能Ea=(33.59-(-12.02))kJ/mol=45.61kJ/mol,该步骤为C H*和H*反应生成C H,反应方程式
2 5 2 4
为C H*+ H*= C H;
2 5 2 4
(4)该反应需要少量 参与,反应过程中有 生成,反应前后 的质量不变,则 为反应的
催化剂,结合总反应可知,初始 和乙烷反应转化为 和乙烯、水, 再和二氧化碳转化为CO
和 ,反应历程为:2CrO+ 3C H= CrO+3C H+ 3H O、Cr O+3CO = 3CrO +3CO。
3 2 6 2 3 2 4 2 2 3 2 3
17.(12分)化学反应伴随有能量的变化,获取反应能量变化有多条途径。
(1)通过测定反应过程中所放出的热量可计算中和热。某学生分别取50mL的0.50mol/L盐酸与0.55mol/L
氢氧化钠溶液进行中和反应,实验记录数据如下:
起始温度 ℃ 终止温度 ℃
实验序
号
盐酸 氢氧化钠 混合溶液
1 20.0 20.2 23.3
2 20.2 20.4 23.5
3 20.6 20.6 25.6
①已知热量计算 ,盐酸和氢氧化钠溶液的密度都是 ,又知中和后生成溶液的比热容
c=4.180J/(g・℃),依据该学生的实验数据计算,该实验测得的 ℃, J;该实验数
据测出的中和热 (保留1位有效数字)。
②上述实验得出的 大于-57.3 ,产生偏差的原因不可能是 (填字母)。
a.实验装置保温、隔热效果差
b.量取HCl溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
③若改用60mL 0.25 和50mL 0.55 NaOH溶液进行反应与上述实验相比,所放出的
热量 (填“相等”或“不相等”),若实验操作均正确,则是否影响中和热的计算结果 (填
“偏大”、“偏小”或“不影响”)。
④若改用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热 会 (填“偏
大”、“偏小”或“不影响”)。
学科网(北京)股份有限公司 学科网(北京)股份有限公司(2)通过化学键的键能计算。已知:
化学键种类
键能/ 436 496 463.4
计算可得: 。
(3)通过盖斯定律计算。氧化亚铜()常用于制船底防污漆,已知反应:
则 的 (用 和 表达)。
【答案】(除标明外,每空1分)
(1)①3.2℃ 1337.6 −53.5(2分)
②b
③不相等 不影响 ④偏大
(2) (2分)
(3) (2分)
【解析】(1)①依据该学生的实验数据分析,三次温度差分别为3.2℃、3.2℃、5.0℃,第三次是错误数
据,因此只能求前两次的数据平均值,则该实验测得的 3.2℃,
;该实验数据测出的中和热
;故答案为:3.2℃;1337.6;−53.5。
②上述实验得出的 大于-57.3 ,a.实验装置保温、隔热效果差,温度差较低,计算放出的热量
减小,焓变变大,故a不符合题意;b.量取HCl溶液的体积时仰视读数,盐酸体积偏多,放出的热量偏
多,焓变减小,故b符合题意;c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中,温度差减小,计算出的
热量减小,焓变变大,故c不符合题意;d.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度,所
得温度差减小,得到焓变变大,故d不符合题意;综上所述,答案为:b。
③若改用60mL 0.25 和50mL 0.55 NaOH溶液进行反应与上述实验相比,生成的水
的量不相同,所放出的热量不相等,若实验操作均正确,则是否影响中和热的计算结果不影响,其原因是
中和热是指生成1mol液态是放出的热量;故答案为:不相等;不影响。
④若改用相同浓度和体积的氨水代替NaOH溶液进行上述实验,由于氨水电离会吸收热量,因此温度差减
小,测得的中和热 会偏大;故答案为:偏大。
(2)
;故答案为: 。
学科网(北京)股份有限公司 学科网(北京)股份有限公司(3)根据盖斯定律,第一个方程式的0.5倍减去第二个方程式的0.5倍,则 的
;故答案为: 。
18.(12分)合成氨工艺是人工固氮最重要的途径。回答下列问题:
(1)工业合成氨的反应为 。在容积为2L的密闭容器中,通入amolN 和
2
bmolH ,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN 。
2 2
①达到平衡时,H 的转化率为 。
2
②在t min内以NH 的浓度变化表示的化学反应速率为 。
3
③若把容器的容积缩小一半,则正反应速率 (填“增大”、“减小”或“不变”,下同),N
2
的转化率 。
(2)在合成氨工业中,原料气(N 、H 及少量CO、NH 的混合气)在进入合成塔前需经过铜氨液处理,目
2 2 3
的是除去其中的CO,其反应为: 。铜氨液吸收CO
适宜的生产条件是 。
(3)合成氨工业中采用循环操作,主要是为了 (填序号)。
a.增大化学反应速率 b.提高平衡混合物中氨的含量
c.降低氨的沸点 d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为 ,该反应自发的条件是 (填
“低温自发”、“高温自发”或“任意温度自发”)。
②为提高CH 的平衡转化率,可采用的措施是 (填序号)。
4
a.使用合适的催化剂 b.采用较高的温度
c.采用较高的压强 d.延长反应时间
【答案】(除标明外,每空2分)
(1)① ② ③增大(1分) 增大(1分)
(2)低温和高压
(3)d
(4)高温自发(1分) b(1分)
【解析】(1)①该反应的平衡常数表达式 ;②根据已知条件列出“三段式”
学科网(北京)股份有限公司 学科网(北京)股份有限公司达到平衡时,H 的转化率为 ;③在tmin内以NH 的浓度变化表示的化学反应速率为
2 3
= ;④若把容器的容积缩小一半,反应物浓度增大,则正反应速率增大,平
衡正向移动,N 的转化率增大。
2
(2) 是气体体积减小的放热反应,则铜氨液吸收CO适宜的
生产条件是低温和高压。
(3)合成氨工业中采用循环操作,主要是为了提高氮气和氢气的利用率,故选d。
(4)① 的 、 ,当 时,反应能自发进行,该
反应自发的条件是高温自发;②a.催化剂不改变平衡状态,使用合适的催化剂不能提高CH 的平衡转化
4
率,故a不选;b.该反应为吸热反应,采用较高的温度,平衡正向移动,能提高CH 的平衡转化率,故b
4
选;c.该反应是气体体积增大的反应,采用较高的压强,平衡逆向移动,CH 的平衡转化率减小,故c不
4
选;d.延长反应时间,不能提高CH 的平衡转化率,故d不选;故选b。
4
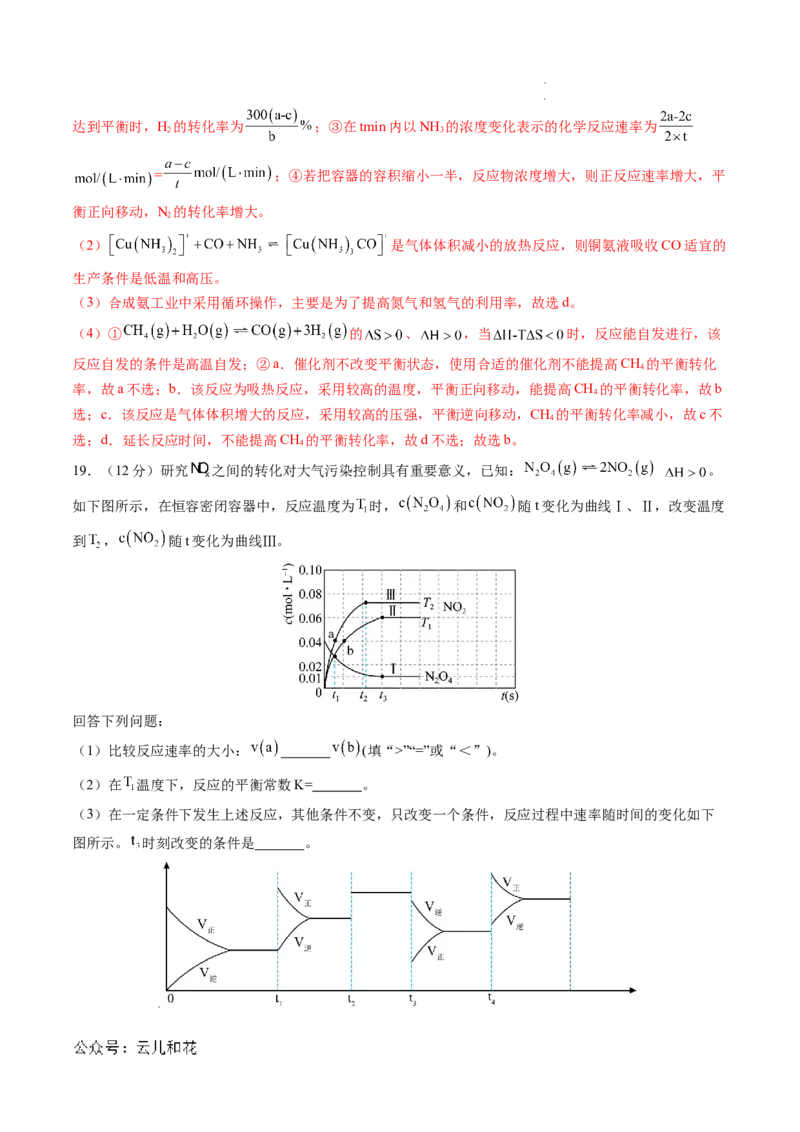
19.(12分)研究 之间的转化对大气污染控制具有重要意义,已知: 。
如下图所示,在恒容密闭容器中,反应温度为 时, 和 随t变化为曲线Ⅰ、Ⅱ,改变温度
到 , 随t变化为曲线Ⅲ。
回答下列问题:
(1)比较反应速率的大小: (填“>”“=”或“<”)。
(2)在 温度下,反应的平衡常数K= 。
(3)在一定条件下发生上述反应,其他条件不变,只改变一个条件,反应过程中速率随时间的变化如下
图所示。 时刻改变的条件是 。
学科网(北京)股份有限公司 学科网(北京)股份有限公司(4)反应体系达平衡后,若在恒温恒容条件下,再加入 ,再次达平衡后, 的体积分数
(填“增大”“减小”或“不变”)。
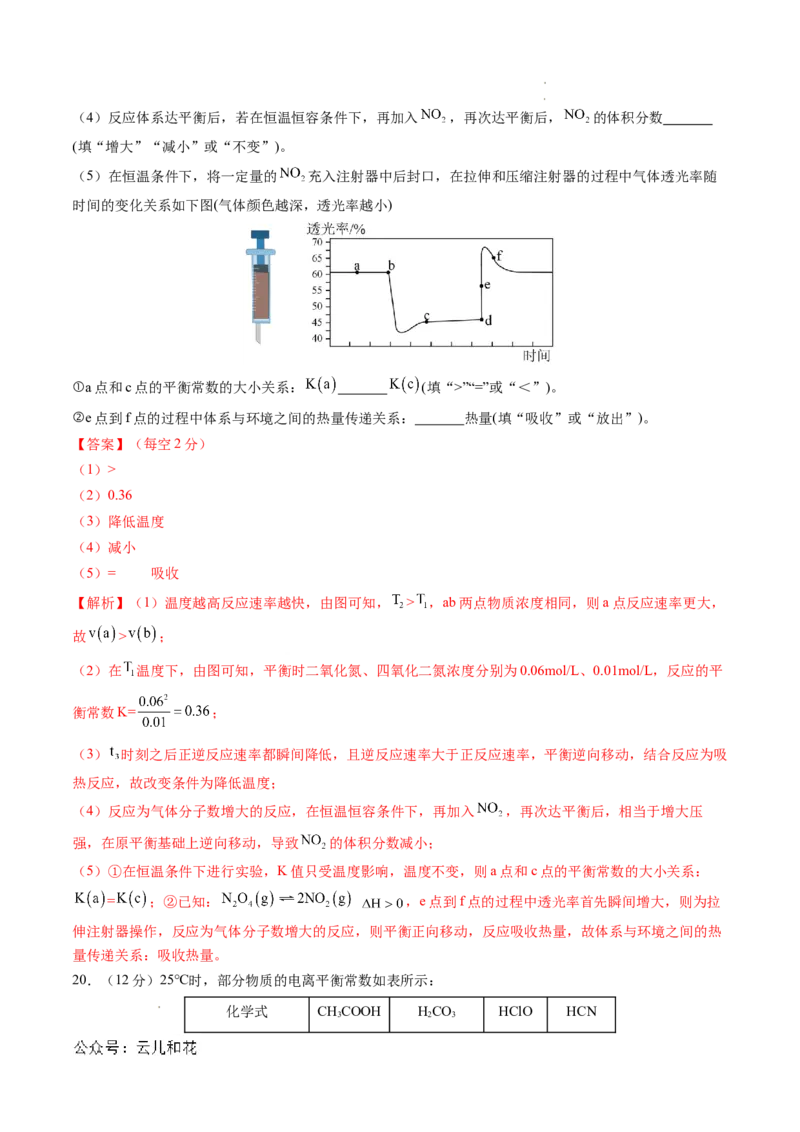
(5)在恒温条件下,将一定量的 充入注射器中后封口,在拉伸和压缩注射器的过程中气体透光率随
时间的变化关系如下图(气体颜色越深,透光率越小)
①a点和c点的平衡常数的大小关系: (填“>”“=”或“<”)。
②e点到f点的过程中体系与环境之间的热量传递关系: 热量(填“吸收”或“放出”)。
【答案】(每空2分)
(1)>
(2)0.36
(3)降低温度
(4)减小
(5)= 吸收
【解析】(1)温度越高反应速率越快,由图可知, > ,ab两点物质浓度相同,则a点反应速率更大,
故 > ;
(2)在 温度下,由图可知,平衡时二氧化氮、四氧化二氮浓度分别为0.06mol/L、0.01mol/L,反应的平
衡常数K= ;
(3) 时刻之后正逆反应速率都瞬间降低,且逆反应速率大于正反应速率,平衡逆向移动,结合反应为吸
热反应,故改变条件为降低温度;
(4)反应为气体分子数增大的反应,在恒温恒容条件下,再加入 ,再次达平衡后,相当于增大压
强,在原平衡基础上逆向移动,导致 的体积分数减小;
(5)①在恒温条件下进行实验,K值只受温度影响,温度不变,则a点和c点的平衡常数的大小关系:
= ;②已知: ,e点到f点的过程中透光率首先瞬间增大,则为拉
伸注射器操作,反应为气体分子数增大的反应,则平衡正向移动,反应吸收热量,故体系与环境之间的热
量传递关系:吸收热量。
20.(12分)25℃时,部分物质的电离平衡常数如表所示:
化学式 CHCOOH HCO HClO HCN
3 2 3
学科网(北京)股份有限公司 学科网(北京)股份有限公司K =4.3×10-7
a1
电离平衡常数(K) 1.8×10-5 3.0×10-8 5.0×10-10
a
K =5.6×10-11
a2
请回答下列问题:
(1)CHCOOH、HCO、HClO、HCN的酸性由强到弱的顺序 。
3 2 3
(2)向NaCN中通入少量的CO,发生反应的离子方程式为 。
2
(3)体积相同、pH相同的① ;②HCl;③ 三种酸溶液分别与同浓度的NaOH溶液完全
中和时,消耗NaOH溶液的体积由大到小的排列顺序是 (填序号);若是体积相同,物质的量浓度相
同的以上三种酸分别和足量的Zn反应,生成氢气的量由大到小的排列顺序是 (填序号)。
(4)H+浓度相同等体积的两份溶液A(盐酸)和B(CHCOOH)分别与不同质量的锌粉反应,若最后仅有一份
3
溶液中存在锌,放出氢气的质量相同,则下列说法正确的是 (填代号)。
a.反应所需要的时间:B>A b.开始反应时的速率:A>B
c.参加反应的锌物质的量:A=B d.A中有锌剩余
(5)25°C 时常压下,在 pH=5 的稀醋酸溶液中,c(CHCOO- )= mol· L -1(写出精确值的表示
3
式)。下列方法中,可以使 0.10mol·L -1CHCOOH 的电离程度增大的是 (填代号)。
3
a.加少入量0.10mol·L -1的稀盐酸 b.加热该CHCOOH溶液
3
c.加入少量冰醋酸 d.加水稀释至0.010mol·L -1
e.加入少量氯化钠晶体 f.加入少量0.10mol·L -1的NaOH溶液
【答案】(除标明外,每空2分)
(1)CHCOOH>H CO>HClO>HCN
3 2 3
(2)CN-+CO +H O=HCN+ HCO
2 2
(3)①>②=③(1分) ③>②=①(1分)
(4)cd
(5)10-5-10-9 bdf
【解析】(1)根据表中数据可知,酸的电离平衡常数大小为:CHCOOH>HCO>HClO>HCN>
3 2 3
,电离平衡常数越大,酸性越强,所以酸性由强到弱的顺序为:CHCOOH>H CO>HClO>HCN;
3 2 3
(2)向NaCN溶液中通入少量CO,由于酸性HCO>HCN> ,则反应生成HCN和碳酸氢钠,该
2 2 3
反应的离子方程式为:CN-+CO +H O═HCN+ HCO ;
2 2
(3)pH相同即c(H+)相同的盐酸和硫酸中和碱的能力相同,而盐酸和醋酸,因为醋酸是弱电解质,所以醋
酸中和碱的能力强,所以消耗NaOH溶液的体积由大到小的排列顺序为:①>②=③;若是体积相同,物
质的量浓度相同的以上三种酸,由于硫酸是二元强酸,另外两种酸是一元酸,则硫酸提供氢离子能力最
多,而盐酸和醋酸能够提供氢离子总量相同,所以加入足量锌,相同状况产生的气体体积由大到小的顺序
为:③>②=①;
(4)氢离子浓度相同的等体积的A、B两份溶液(A为盐酸,B为醋酸)分别与锌粉反应,若最后仅有一份
溶液中存在锌粉,且放出氢气的质量相同,由于醋酸部分电离,其酸的浓度大于氢离子浓度,盐酸中HCl
学科网(北京)股份有限公司 学科网(北京)股份有限公司的浓度等于氢离子的浓度,所以醋酸的浓度大于HCl的浓度,则盐酸中锌粉剩余;a.由于醋酸中酸过
量,醋酸会进一步电离出氢离子,则反应较快,所以反应所需的时间A>B,故a错误;b.开始pH相
同,则氢离子浓度相同,所以开始时反应速率A=B,故b错误;c.由于生成的氢气的质量相同,所以参
加反应的锌粉物质的量A=B,故c正确;d.醋酸的浓度大于盐酸的浓度,醋酸有剩余,则盐酸中有锌粉
剩余,故d正确,故答案为:cd;
(5)25℃时常压下,在pH=5的稀醋酸溶液中,c(H+)=10-5mol/L,由于该温度下水的离子积K =1.0×10-14,
w
则该温度下c(OH-)= =10-9 mol/L。在醋酸溶液中存在电荷守恒:c(H+)=c(OH-)+c(CHCOO-),所以
3
c(CHCOO-)=c(H+)-c(OH-)=(10-5-10-9) mol/L;a.加入少量0.10 mol/L的稀盐酸,溶液中c(H+)增大,电离平
3
衡逆向移动,导致醋酸电离程度减小,a不符合题意;b.CHCOOH电离过程会吸收热量,加热该
3
CHCOOH溶液,会使醋酸的电离平衡正向移动,因而会促进醋酸的电离,使其电离程度增大,b符合题
3
意;c.加入少量冰醋酸,电离平衡正向移动,但平衡移动趋势是微弱的,总的来说CHCOOH浓度增大,
3
故CHCOOH的电离程度减小,c不符合题意;d.加水稀释至0.010 mol/L,电离平衡正向移动,导致醋酸
3
电离程度增大,d符合题意;e.加入少量氯化钠晶体,对溶液中各种离子浓度无影响,因此醋酸的电离平
衡不移动,e不符合题意;f.加入少量0.10 mol/L的NaOH溶液,会反应消耗溶液中的H+,使溶液中c(H+)
减小,电离平衡正向移动,导致醋酸的电离平衡正向移动,电离程度增大,f符合题意;综上所述可知可
知:能够使醋酸电离程度增大的序号是bdf。
学科网(北京)股份有限公司 学科网(北京)股份有限公司