文档内容
树德中学高 2022 级高三下学期 4 月阶段性测试化学试题 5.科研人员开发了一种生产药物中间体三氟甲苯的方法:
考试时间:75分钟 满分:100分 命题人:刘发春 审题人:袁玉红、佘海丽、唐建华
可能用到的原子量:H-1 C-12 O-16 Cu-64 Re-186
第 I 卷 选择题(共 45 分) 设N 为阿伏加德罗常数的值,已知25℃时三氟乙酸的-lgKa=0.23,下列叙述正确的是
A
一、选择题(本大题包含15个小题,每题有且只有一个选项符合题意,每小题3分,共45分) A.1mol苯中σ键数目为6N
A
1.“挖掘文物价值,讲好中国故事”。下列有关文物的叙述错误的是 B.25℃时1L1mol·L-1三氟乙酸溶液中,H+的数目为N
A
C.1mol三氟甲苯中含有极性键数目为8N
A
D.标准状况下,2.24LH 和CO 组成的混合气体中,氢、氧原子总数为0.2N
2 2 A
6.ATP(腺苷三磷酸)是细胞生命活动所需能量的直接来源,也是生物体内重要的能量转换中间体,
ATP其分子结构如下图所示,ATP逐步水解可以生成AMP(腺嘌呤核苷酸)等磷酸酯,核苷酸
是组成核酸的基本单元。下列说法不正确的是
北齐·汉白玉佛像 唐·红陶生肖俑 清·缂丝朝袍 西汉·铜朱雀衔环杯
A.汉白玉佛像耐酸雨腐蚀 B.陶俑以黏土为主要原料,经高温烧结而成
C.缂丝的主要材质为蛋白质 D.为减缓铜朱雀衔环杯腐蚀,可将其置于铁质托盘上
2.下列有关化学用语或表述正确的是
A.BCl 的空间结构: A.ATP分子中含有4个手性碳原子
3
B.理论上1molATP最多能与6molNaOH反应
C.核酸DNA和RNA分子水解出的戊糖不同,碱基也不同
B. 用质谱法能区分NH 3 和ND 3 D.AMP分子能发生氧化反应、酯化反应、水解反应、加成反应
7.甲、乙、丙、丁、戊、已为短周期元素组成的常见物质,其中甲、乙、丙、戊在常温下均为气体,
C. 用核磁共振氢谱能鉴别 和 两种同分异构体 甲和丁为原子总数不大于4的10e-分子,乙为单质。它们之间的转化关系如图。下列正确的是
D. 甲胺的电子式:
3.下列装置和操作能达到实验目的的是 A.甲和丙均为极性分子,甲易溶于水,丙难溶于水 B.丙与乙反应时无明显现象
C.气体丙和戊均可通过排水法收集
A B C D
D.根据物质的氧化性和还原性可知,甲与己混合时发生氧化还原反应
8.环糊精是一类环状低聚糖,常见的环糊精结构和空间模型如图1所示,环糊精的空腔与某些药物
形成包合物如图2所示。下列说法正确的是
制备Al (SO ) 固体 比较金属M和N的活泼性 完成喷泉实验 探究小苏打的热稳定性
2 4 3
4.下列方程式的书写与所给事实相符合的是
A.常温下,醋酸和氢氧化钠溶液反应的热化学方程式:H+(aq)+OH-(aq)==H O(l) △H=-57.3kJ·mol-1
2
B.煅烧黄铁矿制SO 的反应方程式:4FeS+7O 2Fe O +4SO
2 2 2 3 2
C.镁溶于氯化铵浓溶液的离子方程式:Mg+2NH +==Mg2++2NH ↑+H ↑ A.图1中3种环糊精属于同系物 B.环糊精空腔的内壁具有亲水性
4 3 2
D.向硫酸铜溶液中加足量氨水和乙醇制得深蓝色晶体的离子方程式: C.环糊精与药物形成包合物能增大药物的水溶性,控制药物的释放速度
Cu2++4NH +SO 2- [Cu(NH ) ]SO ↓
D.药物分子与环糊精之间的作用力是一种配位键
3 4 3 4 4
2025-4 高三化月4 第1页共4页9.结构决定性质,性质决定用途。下列事实对应的解释不合理的是 13.某研究团队设计了一种可穿戴汗液传感器用于检测汗液中的葡萄糖浓度,该传感器同时集成了供
选项 事实 解释
电与检测两个模块。下图是葡萄糖供电模块工作原理(其中GOD为电极表面修饰的葡萄糖氧化
酶)。下列说法错误的是
A 石墨能导电 未参与杂化的2p电子可在整个石墨层中运动 A.使用高活性GOD,可提高酶促反应速率,增强电信号强度
B 二氧化硅的熔点低于碳化硅
氧原子半径比碳原子半径小,Si-O键键能比Si-C键键 B.利用纳米材料修饰电极表面可提供更多的活性位点,有利于提高
能强
传感器的灵敏度
C 2-丁烯存在顺反异构 碳碳双键连接的原子或原子团不能绕碳碳键键轴旋转
C.GOD区域的电极反应式:C H O +2e—+H O=C H O +2H+
6 12 6 2 6 12 7
CH =CHCH Cl中Cl的电负性较大,使双键电子云向
D CH 2 =CHCH 2 Cl与HClO加成的 中心 2 碳原子偏 2 移,HClO中带正电性的Cl易连在带负 D.供电模块中1×10-5mmolC 6 H 12 O 6 参与反应,消耗O 2 约为
主要产物是ClCH 2 CHClCH 2 OH 电性中心碳原子上 2.24×10-4mL(标准状况)
10.中科院课题组报道了空穴掺杂型铜氧化物超导体,其四方晶胞(晶胞参数:a=b≠c,α=β=γ=90°) 14.NO的氧化反应2NO+O
2
2NO
2
分两步进行:I.2NO N
2
O
2
;II.N
2
O
2
+O
2
2NO
2
,其能
的结构如图所示,设N
A
为阿伏加德罗常数的值。下列说法正确的是 量变化示意图如下图1。向恒容密闭容器中充入一定量的NO和O
2
,控制反应温度为T
1
和T
2
,
测得c(NO)随时间t的变化曲线如下图2。下列说法正确的是
A. 晶胞的俯视图为
B. 与Re等距离且最近的Cu有8个
C.Cu位于O构成的四面体的体心
1
D. 该超导体的密度为 g/cm3
a2c1033N
A
11.化合物M可作为一种废水处理剂,去除废水中的金属离子,其结构如图所示。W、X、Y和Z均
为短周期主族元素,X、Y和Z位于同一周期。W原子核外的电子只有一种自旋取向,基态Z原
子s轨道上的电子数和p轨道上的电子数相等。下列说法正确的是
A. 反应1在高温下自发进行
B. 氧化反应的决速步骤为过程I
C. 结合图2信息可知:T >T ,转化相同量的NO,T 温度条件下耗时更长
2 1 1
A.X、Y、Z的氢化物中沸点最高的是Z的氢化物 D. 引起图2变化的可能原因:升温I反应平衡逆移,c(N O )减小对Ⅱ反应速率的影响大于温度
2 2
B. 第二电离能:Z>Y 的影响
C.X分别与W、Y形成的化合物均为分子晶体 15.常温下,向20mL0.1mol/L的H A溶液中缓慢加入相同浓度的NaOH溶液,忽略溶液混合时的体
2
D. 化合物M中所有原子均满足8电子结构 积变化,混合溶液中含A微粒的分布系数δ与c(Na+)的变化关系如图。下列说法正确的是
12.下列实验操作及现象对应的结论正确的是 c(H A)
实验操作及现象 结论
[已知:δ(H
2
A)
c(H A)c(H
2
A-)c(A2- )
]。
2
向盛有 2mL0.1 mol/L 的 MgCl 2 溶液的试管中滴加 2~4 滴 A.Ka 1 的数量级为10-3
0.2mol/L 的 NaOH 溶液,振荡,再向上述试管中滴加 4 滴
A 说明Ksp:Fe(OH) c(H
2
A)>c(A2-)
沉淀
B 向CO还原Fe 2 O 3 所得到的固体物质中加入稀盐酸溶解,再 说明Fe O 已全部被还原 C.Ka 2 >1×10-7
滴加KSCN溶液,溶液未变红 2 3
D.c(Na+)=0.06mol/L时,
向某碱性溶液中滴加过量稀硫酸,产生淡黄色固体,并有无
C 说明该溶液中一定含有S O 2-
色有刺激性气体产生,将气体通入品红溶液,品红褪色 2 3 c(H A)+c(HA-)+c(A2-)=0.09mol/L
2
D 将KCl固体溶于水,进行导电性实验,KCl溶液导电性较强 说明KCl属于离子晶体
2025-4 高三化月4 第2页共4页II卷 非选择题(共 55分) 17.(14分)钒、钛、钨等金属的回收具有重要的经济和战略价值。利用废钒-钛系脱硝催化剂粉末(含
V O 、TiO 、WO 及少量的Si、P、Al等的化合物)回收钒、钛、钨的工艺流程如下图。
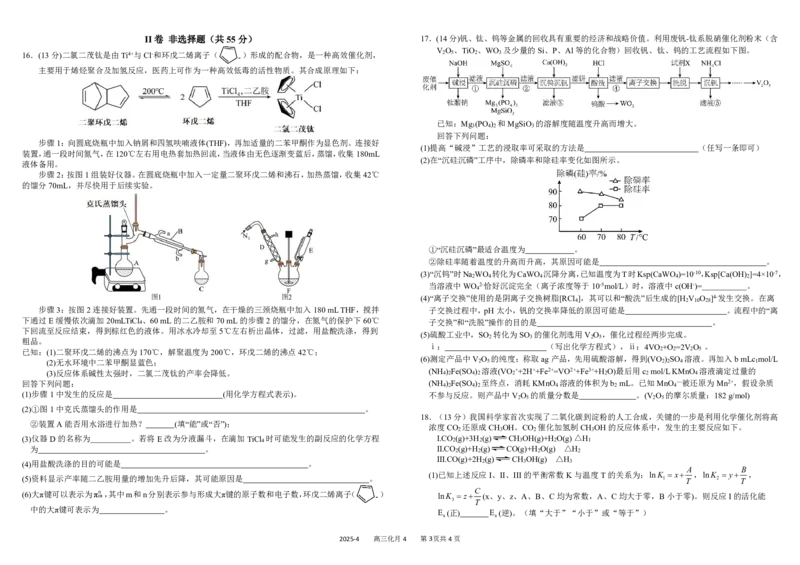
16.(13分)二氯二茂钛是由Ti4+与Cl-和环戊二烯离子( )形成的配合物,是一种高效催化剂, 2 5 2 3
主要用于烯烃聚合及加氢反应,医药上可作为一种高效低毒的活性物质。其合成原理如下:
已知:Mg (PO ) 和MgSiO 的溶解度随温度升高而增大。
3 4 2 3
回答下列问题:
步骤1:向圆底烧瓶中加入钠屑和四氢呋喃液体(THF),再加适量的二苯甲酮作为显色剂。连接好
(1)提高“碱浸”工艺的浸取率可采取的方法是 (任写一条即可)
装置,通一段时间氮气,在120℃左右用电热套加热回流,当液体由无色逐渐变蓝后,蒸馏,收集180mL
(2)在“沉硅沉磷”工序中,除磷率和除硅率变化如图所示。
液体备用。
步骤2:按图1组装好仪器。在圆底烧瓶中加入一定量二聚环戊二烯和沸石,加热蒸馏,收集42℃
的馏分70mL,并尽快用于后续实验。
①“沉硅沉磷”最适合温度为 。
②除硅率随着温度的升高而升高,其原因可能是 。
(3)“沉钨”时Na WO 转化为CaWO 沉降分离,已知温度为T时Ksp(CaWO )=10-10,Ksp[Ca(OH) ]=4×10-7,
2 4 4 4 2
当溶液中WO 2-恰好沉淀完全(离子浓度等于10-5mol/L)时,溶液中c(OH-)= 。
4
(4)“离子交换”使用的是阴离子交换树脂[RCl ],其可以和“酸洗”后生成的[H V O ]4-发生交换。在离
4 2 10 28
步骤3:按图2连接好装置。先通一段时间的氮气,在干燥的三颈烧瓶中加入180mLTHF,搅拌 子交换过程中,pH太小,钒的交换率降低的原因可能是 。流程中的“离
下通过E缓慢依次滴加20mLTiCl 4 、60mL的二乙胺和70mL的步骤2的馏分,在氮气的保护下60℃ 子交换”和“洗脱”操作的目的是 。
下回流至反应结束,得到棕红色的液体。用冰水冷却至5℃左右析出晶体,过滤,用盐酸洗涤,得到
(5)硫酸工业中,SO 转化为SO 的催化剂选用V O ,催化过程经两步完成。
2 3 2 5
粗品。
ⅰ: (写出化学方程式),ⅱ:4VO +O =2V O 。
已知:(1)二聚环戊二烯的沸点为170℃,解聚温度为200℃,环戊二烯的沸点42℃; 2 2 2 5
(6)测定产品中V O 的纯度:称取ag产品,先用硫酸溶解,得到(VO ) SO 溶液。再加入bmLc mol/L
(2)无水环境中二苯甲酮显蓝色; 2 5 2 2 4 1
(3)反应体系碱性太强时,二氯二茂钛的产率会降低。 (NH 4 ) 2 Fe(SO 4 ) 2 溶液(VO 2 ++2H++Fe2+=VO2++Fe3++H 2 O)最后用c 2 mol/LKMnO 4 溶液滴定过量的
回答下列问题: (NH ) Fe(SO ) 至终点,消耗KMnO 溶液的体积为b mL。已知MnO —被还原为Mn2+,假设杂质
4 2 4 2 4 2 4
(1)步骤1中发生的反应是 (用化学方程式表示)。 不参与反应。则产品中V O 的质量分数是 。(V O 的摩尔质量:182g/mol)
2 5 2 5
(2)①图1中克氏蒸馏头的作用是 。
18.(13分)我国科学家首次实现了二氧化碳到淀粉的人工合成,关键的一步是利用化学催化剂将高
②装置A能否用水浴进行加热? (填“能”或“否”);
浓度CO 还原成CH OH。CO 催化加氢制CH OH的反应体系中,发生的主要反应如下。
2 3 2 3
(3)仪器D的名称为 。若将E改为分液漏斗,在滴加TiCl
4
时可能发生的副反应的化学方程 I.CO
2
(g)+3H
2
(g) CH
3
OH(g)+H
2
O(g)△H
1
为 。 II.CO (g)+H (g) CO(g)+H O(g) △H
2 2 2 2
III.CO(g)+2H (g) CH OH(g) △H
(4)用盐酸洗涤的目的可能是 。 2 3 3
A B
(1)已知上述反应I、II、III的平衡常数K与温度T的关系为:lnK x ,lnK y ,
(5)资料显示产率随二乙胺用量的增加先升后降,其可能原因是 。 1 T 2 T
C
(6)大π键可以表示为 ,其中m和n分别表示参与形成大π键的原子数和电子数,环戊二烯离子( ) lnK z (x、y、z、A、B、C均为常数,A、C均大于零,B小于零)。则反应I的活化能
3 T
中的大π键可表示为 。
E (正) E (逆)。(填“大于”“小于”或“等于”)
a a
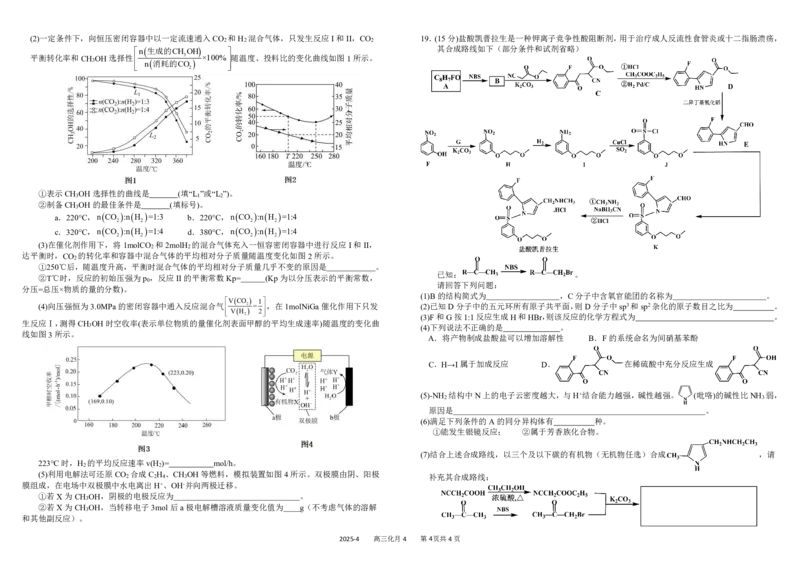
2025-4 高三化月4 第3页共4页(2)一定条件下,向恒压密闭容器中以一定流速通入CO 和H 混合气体,只发生反应I和II,CO 19.(15分)盐酸凯普拉生是一种钾离子竞争性酸阻断剂,用于治疗成人反流性食管炎或十二指肠溃疡,
2 2 2
n 生成的CH OH 其合成路线如下(部分条件和试剂省略)
平衡转化率和CH OH选择性 3 ×100%随温度、投料比的变化曲线如图1所示。
3
n
消耗的CO
2
①表示CH OH选择性的曲线是 (填“L ”或“L ”)。
3 1 2
②制备CH OH的最佳条件是 (填标号)。
3
a.220°C,nCO :nH =1:3 b.220°C,nCO :nH =1:4
2 2 2 2
c.320°C,nCO :nH =1:4 d.380°C,nCO :nH =1:4
2 2 2 2
(3)在催化剂作用下,将1molCO 和2molH 的混合气体充入一恒容密闭容器中进行反应I和II,
2 2
达平衡时,CO 的转化率和容器中混合气体的平均相对分子质量随温度变化如图2所示。
2
①250℃后,随温度升高,平衡时混合气体的平均相对分子质量几乎不变的原因是 。
已知: 。
②T℃时,反应的初始压强为p ,反应II的平衡常数Kp= (Kp为以分压表示的平衡常数,
0
请回答下列问题:
分压=总压×物质的量的分数)。
(1)B的结构简式为 ,C分子中含氧官能团的名称为 。
VCO 1
(4)向压强恒为3.0MPa的密闭容器中通入反应混合气 2 = ,在1molNiGa催化作用下只发 (2)已知D分子中的五元环所有原子共平面,则D分子中sp3和sp2杂化的原子数目之比为 。
VH
2
2
(3)F和G按1:1反应生成H和HBr,则该反应的化学方程式为 。
生反应Ⅰ,测得CH OH时空收率(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度的变化曲
3 (4)下列说法不正确的是 。
线如图3所示。
A.将产物制成盐酸盐可以增加溶解性 B.F的系统命名为间硝基苯酚
C.H→I属于加成反应 D. 在稀硫酸中充分反应生成
(5)-NH 结构中N上的电子云密度越大,与H+结合能力越强,碱性越强。 (吡咯)的碱性比NH 弱,
2 3
原因是 。
(6)满足下列条件的A的同分异构体有 种。
①能发生银镜反应; ②属于芳香族化合物。
(7)结合上述合成路线,以三个及以下碳的有机物(无机物任选)合成 ,请
223°C时,H 的平均反应速率v(H )= mol/h。
2 2
(5)利用电解法可还原CO 2 合成C 2 H 4 、CH 3 OH等燃料,模拟装置如图4所示。双极膜由阴、阳极 补充其合成路线:
膜组成,在电场中双极膜中水电离出H+、OH-并向两极迁移。
①若X为CH OH,阴极的电极反应为 。
3
②若X为CH OH,当转移电子3mol后a极电解槽溶液质量变化值为 g(不考虑气体的溶解
3
和其他副反应)。
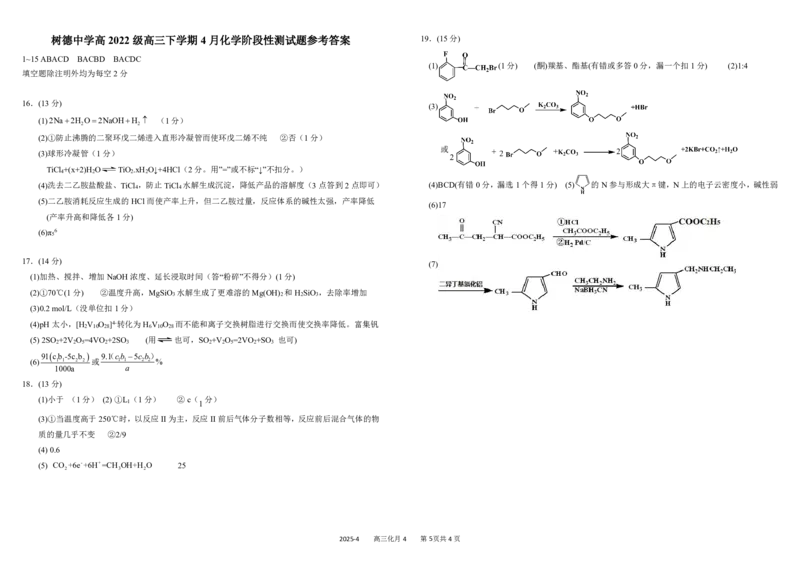
2025-4 高三化月4 第4页共4页树德中学高 2022 级高三下学期 4 月化学阶段性测试题参考答案 19.(15分)
1~15ABACD BACBD BACDC
(1) (1分) (酮)羰基、酯基(有错或多答0分,漏一个扣1分) (2)1:4
填空题除注明外均为每空2分
16.(13分)
(3)
(1)2Na2H O2NaOHH (1分)
2 2
(2)①防止沸腾的二聚环戊二烯进入直形冷凝管而使环戊二烯不纯 ②否(1分)
或
(3)球形冷凝管(1分)
TiCl +(x+2)H O TiO .xH O↓+4HCl(2分。用”=”或不标“↓”不扣分。)
4 2 2 2
(4)洗去二乙胺盐酸盐、TiCl ,防止TiCl 水解生成沉淀,降低产品的溶解度(3点答到2点即可) (4)BCD(有错0分,漏选1个得1分) (5) 的N参与形成大π键,N上的电子云密度小,碱性弱
4 4
(5)二乙胺消耗反应生成的HCl而使产率上升,但二乙胺过量,反应体系的碱性太强,产率降低
(6)17
(产率升高和降低各1分)
(6)π 6
5
17.(14分)
(7)
(1)加热、搅拌、增加NaOH浓度、延长浸取时间(答“粉碎”不得分)(1分)
(2)①70℃(1分) ②温度升高,MgSiO 水解生成了更难溶的Mg(OH) 和H SiO ,去除率增加
3 2 2 3
(3)0.2mol/L(没单位扣1分)
(4)pH太小,[H V O ]4-转化为H V O 而不能和离子交换树脂进行交换而使交换率降低。富集钒
2 10 28 6 10 28
(5)2SO +2V O =4VO +2SO (用 也可,SO +V O =2VO +SO 也可)
2 2 5 2 3 2 2 5 2 3
91cb -5c b 9.(1 cb 5c b)
(6) 1 1 2 2 或 1 1 2 2 %
1000a a
18.(13分)
(1)小于 (1分) (2)①L (1分) ②c( 分)
1 1
(3)①当温度高于250℃时,以反应II为主,反应II前后气体分子数相等,反应前后混合气体的物
质的量几乎不变 ②2/9
(4)0.6
(5) CO +6e-+6H+=CH OH+H O 25
2 3 2
2025-4 高三化月4 第5页共4页