文档内容
2024-2025 学年高二化学上学期期中模拟卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准
考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第1章~第3章第2节(人教版2019选择性必修1)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:Ca 40
第Ⅰ卷(选择题 共 42 分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学与生活、社会发展息息相关。下列说法正确的是
A.食品加工时不可添加任何防腐剂
B.合成不粘锅涂层聚四氟乙烯的单体属于不饱和烃
C.长期服用阿司匹林可预防某些疾病,没有副作用
D.侯氏制碱法的工艺过程中应用了物质溶解度的差异
2.商朝青铜器双羊尊是中国青铜器的代表作品。下列关于青铜的说法正确的是
A.青铜的熔点比纯铜要高
B.青铜、黄铜和紫铜都是铜的同素异形体
C.青铜与稀硝酸溶液共热,会产生NO气体
D.青铜表面的铜绿的主要成分是碳酸铜
3.通过以下反应均可获取H。下列有关说法不正确的是
2
①太阳光催化分解水制氢:2HO(l)=2H(g)+O(g) ΔH=+571.6kJ·mol–1
2 2 2 1
②焦炭与水反应制氢:C(s)+HO(g)=CO(g)+H (g) ΔH=+131.3kJ·mol–1
2 2 2
③甲烷与水反应制氢:CH(g)+HO(g)=CO(g)+3H (g) ΔH=+206.1kJ·mol–1
4 2 2 3
A.H 的燃烧热为285.8kJ·mol-1
2
B.反应②中E(反应物键能总和)>E(生成物键能总和)
C.C(s)+2H(g)=CH (g) ΔH=+74.8kJ·mol–1
2 4
D.2HO(g)=2H (g)+O(g) ΔH<+571.6kJ·mol-1
2 2 2
4.若 表示阿伏加德罗常数的值,下列说法正确的是
A.2 L 0.5 mol/L HF溶液中含有的 数目为
1
学学科科网网((北北京京))股股份份有有限限公公司司B.1 mol NH Cl中所含共价键的数目为
4
C.标准状况下22.4 L N 与足量H 充分反应后,所得氨分子的数目为
2 2
D.pH=1的硫酸溶液中含有的 数目为
5.温度为 时,在容积为 的恒容密闭容器中发生反应: 。实验
测得: , 为速率
常数,受温度影响。不同时刻测得容器中 如表:
时间/s 0 1 2 3 4 5
0.20 0.10 0.08 0.065 0.06 0.06
0.10 0.05 0.04 0.0325 0.03 0.03
下列说法正确的是
A. 内,该反应的平均速率
B.其他条件不变,往原容器中再通入 和 ,则达到新的平衡时 体积分数减小
C.其他条件不变,移走部分 ,则平衡正向移动,平衡常数增大
D.当温度改变为 时,若 ,则
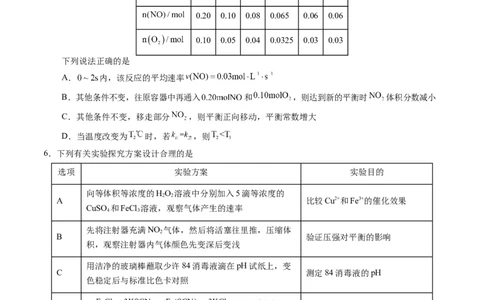
6.下列有关实验探究方案设计合理的是
选项 实验方案 实验目的
向等体积等浓度的HO 溶液中分别加入5滴等浓度的
2 2
A 比较Cu2+和Fe3+的催化效果
CuSO 和FeCl 溶液,观察气体产生的速率
4 3
先将注射器充满NO 气体,然后将活塞往里推,压缩体
2
B 验证压强对平衡的影响
积,观察注射器内气体颜色先变深后变浅
用洁净的玻璃棒蘸取少许84消毒液滴在pH试纸上,变
C 测定84消毒液的pH
色稳定后与标准比色卡对照
在 平衡体系中加入
D 探究离子浓度对平衡移动的影响
KCl晶体,观察并比较实验现象
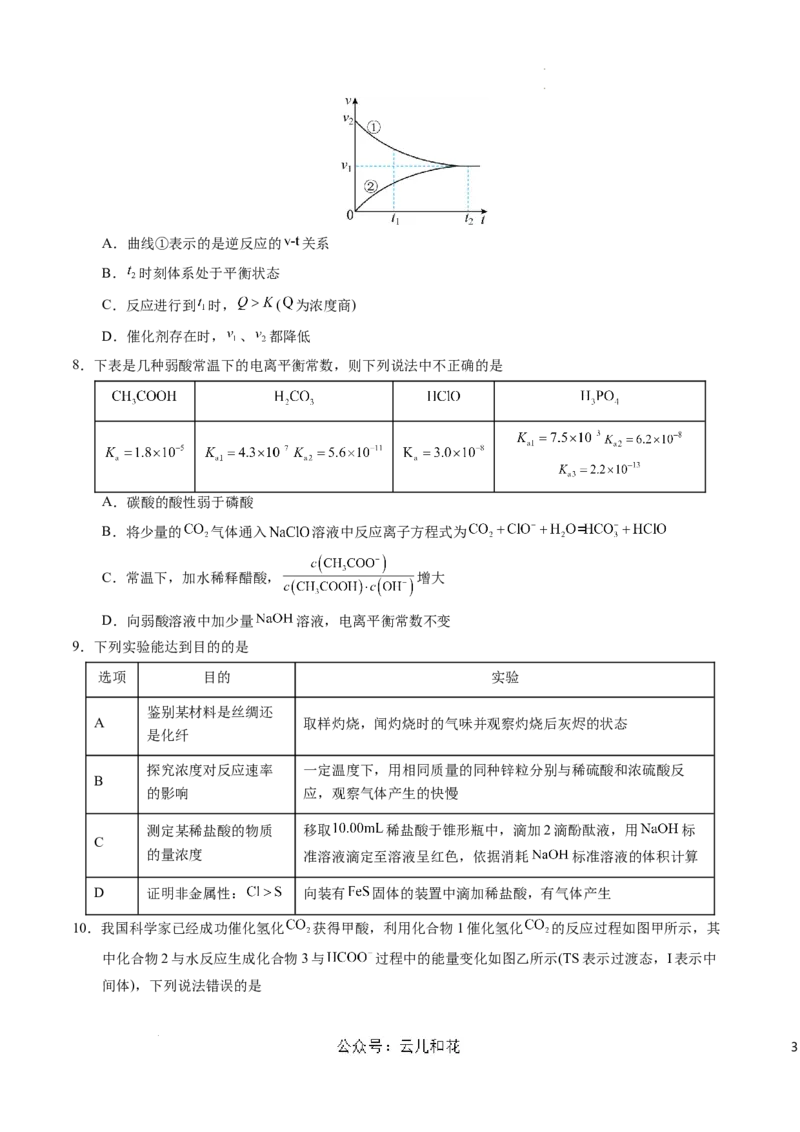
7.工业上苯乙烯的生产主要采用乙苯脱氢工艺: 。某条件下
无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
2
学学科科网网((北北京京))股股份份有有限限公公司司A.曲线①表示的是逆反应的 关系
B. 时刻体系处于平衡状态
C.反应进行到 时, ( 为浓度商)
D.催化剂存在时, 、 都降低
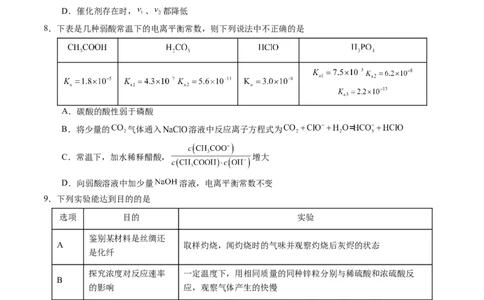
8.下表是几种弱酸常温下的电离平衡常数,则下列说法中不正确的是
A.碳酸的酸性弱于磷酸
B.将少量的 气体通入 溶液中反应离子方程式为
C.常温下,加水稀释醋酸, 增大
D.向弱酸溶液中加少量 溶液,电离平衡常数不变
9.下列实验能达到目的的是
选项 目的 实验
鉴别某材料是丝绸还
A 取样灼烧,闻灼烧时的气味并观察灼烧后灰烬的状态
是化纤
探究浓度对反应速率 一定温度下,用相同质量的同种锌粒分别与稀硫酸和浓硫酸反
B
的影响 应,观察气体产生的快慢
测定某稀盐酸的物质 移取 稀盐酸于锥形瓶中,滴加2滴酚酞液,用 标
C
的量浓度 准溶液滴定至溶液呈红色,依据消耗 标准溶液的体积计算
D 证明非金属性: 向装有 固体的装置中滴加稀盐酸,有气体产生
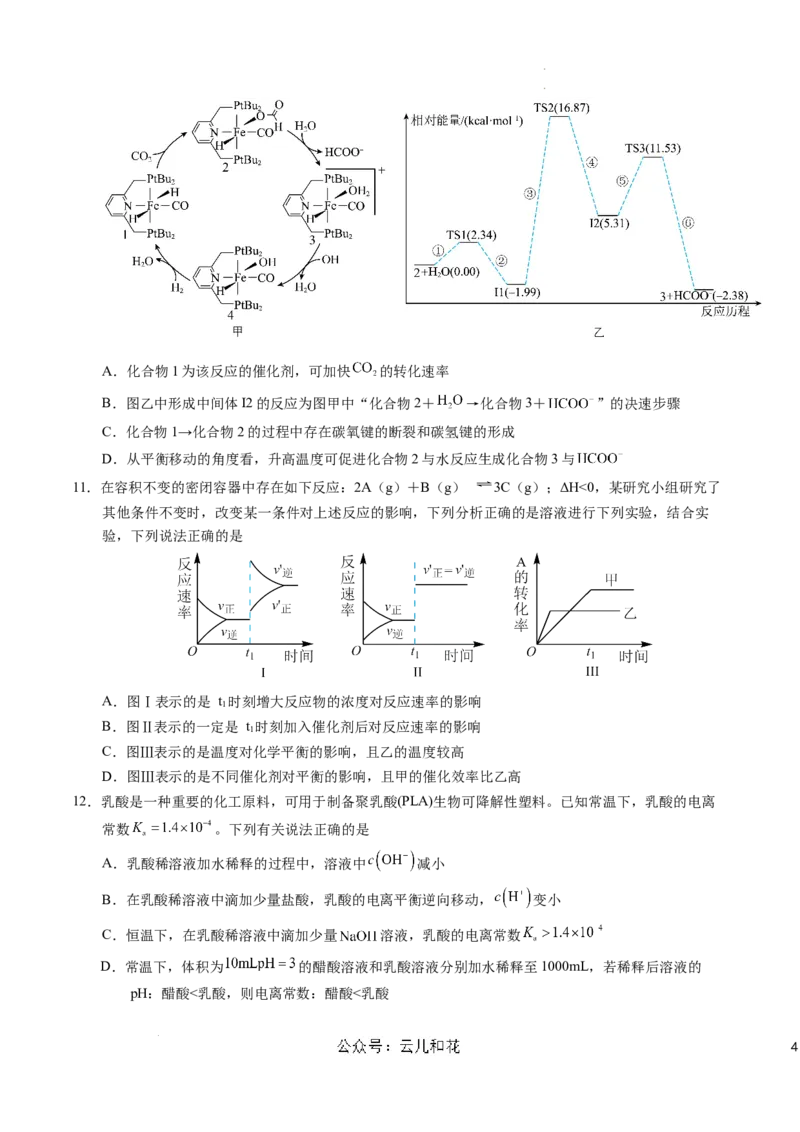
10.我国科学家已经成功催化氢化 获得甲酸,利用化合物1催化氢化 的反应过程如图甲所示,其
中化合物2与水反应生成化合物3与 过程中的能量变化如图乙所示(TS表示过渡态,I表示中
间体),下列说法错误的是
3
学学科科网网((北北京京))股股份份有有限限公公司司A.化合物1为该反应的催化剂,可加快 的转化速率
B.图乙中形成中间体I2的反应为图甲中“化合物2+ →化合物3+ ”的决速步骤
C.化合物1→化合物2的过程中存在碳氧键的断裂和碳氢键的形成
D.从平衡移动的角度看,升高温度可促进化合物2与水反应生成化合物3与
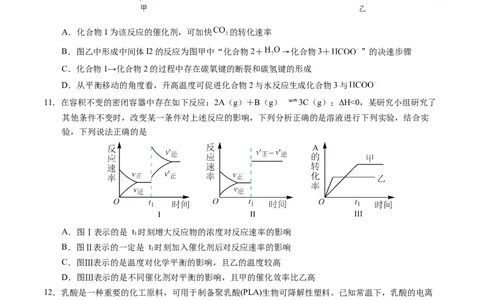
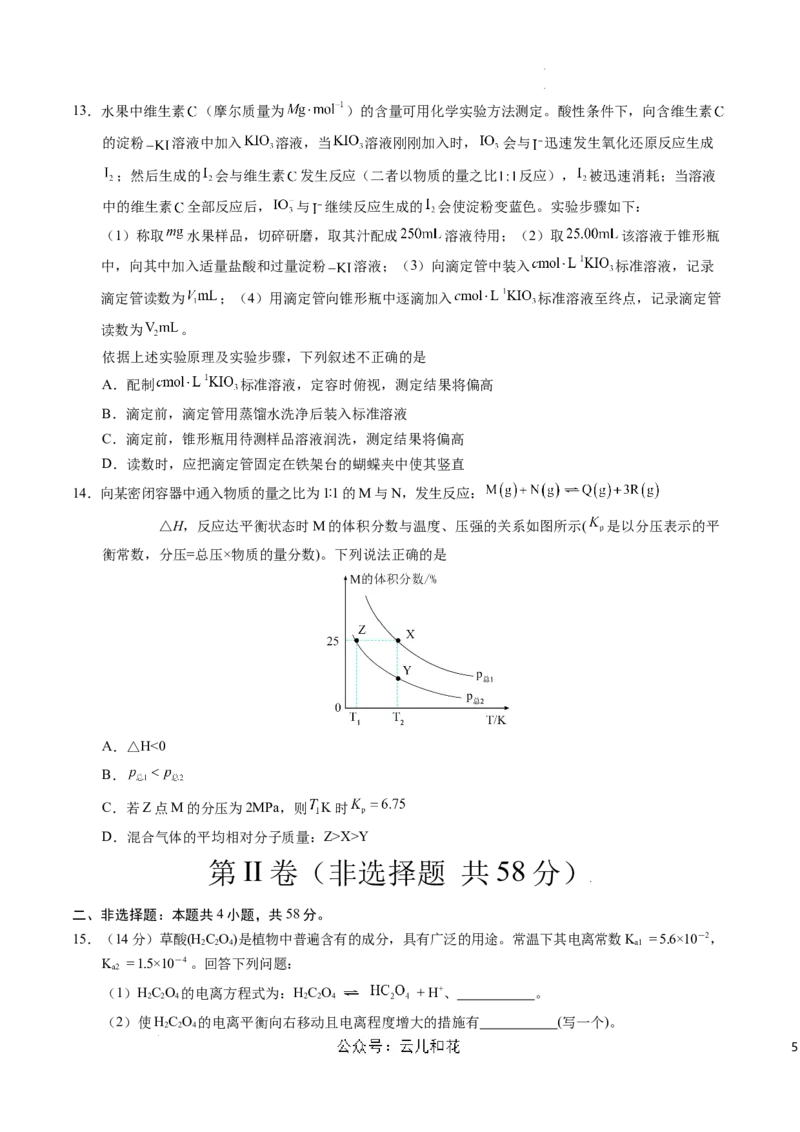
11.在容积不变的密闭容器中存在如下反应:2A(g)+B(g) 3C(g);ΔH<0,某研究小组研究了
其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是溶液进行下列实验,结合实
验,下列说法正确的是
A.图Ⅰ表示的是 t 时刻增大反应物的浓度对反应速率的影响
1
B.图Ⅱ表示的一定是 t 时刻加入催化剂后对反应速率的影响
1
C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
D.图Ⅲ表示的是不同催化剂对平衡的影响,且甲的催化效率比乙高
12.乳酸是一种重要的化工原料,可用于制备聚乳酸(PLA)生物可降解性塑料。已知常温下,乳酸的电离
常数 。下列有关说法正确的是
A.乳酸稀溶液加水稀释的过程中,溶液中 减小
B.在乳酸稀溶液中滴加少量盐酸,乳酸的电离平衡逆向移动, 变小
C.恒温下,在乳酸稀溶液中滴加少量 溶液,乳酸的电离常数
D.常温下,体积为 的醋酸溶液和乳酸溶液分别加水稀释至1000mL,若稀释后溶液的
pH:醋酸<乳酸,则电离常数:醋酸<乳酸
4
学学科科网网((北北京京))股股份份有有限限公公司司13.水果中维生素 (摩尔质量为 )的含量可用化学实验方法测定。酸性条件下,向含维生素
的淀粉 溶液中加入 溶液,当 溶液刚刚加入时, 会与 迅速发生氧化还原反应生成
;然后生成的 会与维生素 发生反应(二者以物质的量之比 反应), 被迅速消耗;当溶液
中的维生素 全部反应后, 与 继续反应生成的 会使淀粉变蓝色。实验步骤如下:
(1)称取 水果样品,切碎研磨,取其汁配成 溶液待用;(2)取 该溶液于锥形瓶
中,向其中加入适量盐酸和过量淀粉 溶液;(3)向滴定管中装入 标准溶液,记录
滴定管读数为 ;(4)用滴定管向锥形瓶中逐滴加入 标准溶液至终点,记录滴定管
读数为 。
依据上述实验原理及实验步骤,下列叙述不正确的是
A.配制 标准溶液,定容时俯视,测定结果将偏高
B.滴定前,滴定管用蒸馏水洗净后装入标准溶液
C.滴定前,锥形瓶用待测样品溶液润洗,测定结果将偏高
D.读数时,应把滴定管固定在铁架台的蝴蝶夹中使其竖直
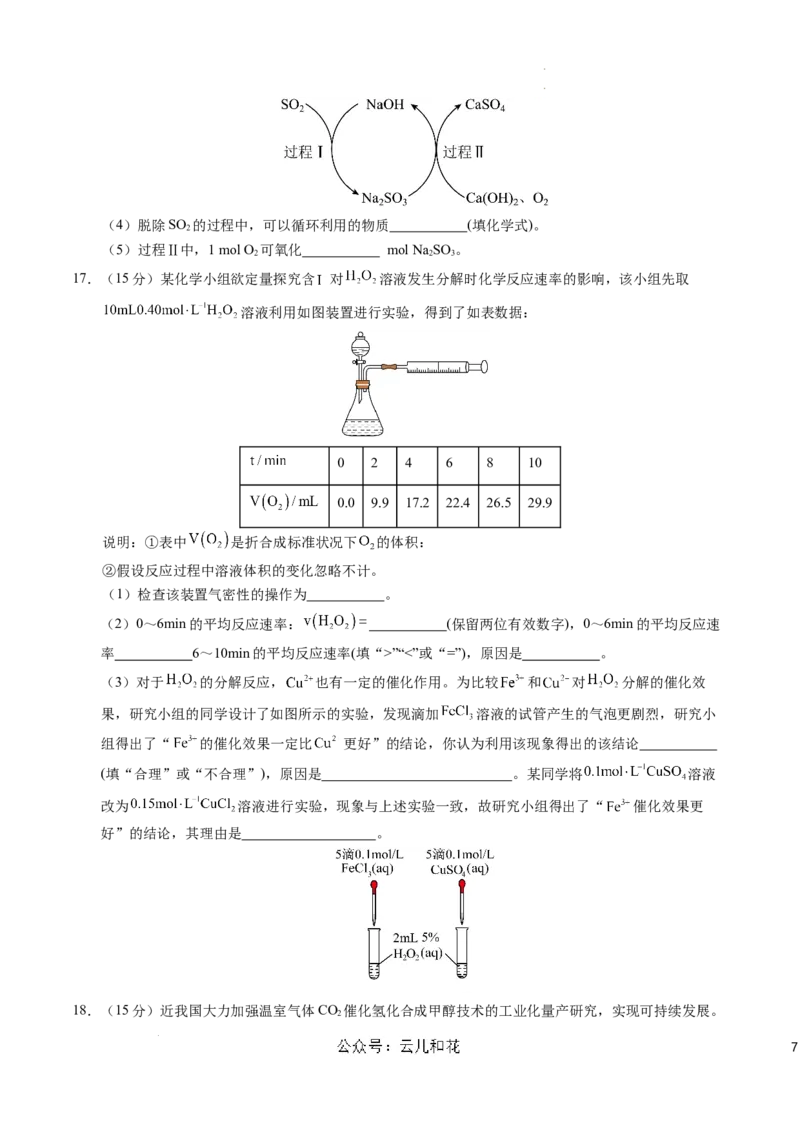
14.向某密闭容器中通入物质的量之比为1∶1的M与N,发生反应:
△H,反应达平衡状态时M的体积分数与温度、压强的关系如图所示( 是以分压表示的平
衡常数,分压=总压×物质的量分数)。下列说法正确的是
A.△H<0
B.
C.若Z点M的分压为2MPa,则 K时
D.混合气体的平均相对分子质量:Z>X>Y
第 II 卷(非选择题 共 58 分)
二、非选择题:本题共4小题,共58分。
15.(14分)草酸(H C O)是植物中普遍含有的成分,具有广泛的用途。常温下其电离常数K = 5.6×10-2,
2 2 4 a1
K = 1.5×10-4 。回答下列问题:
a2
(1)HC O 的电离方程式为:HC O + H+、 。
2 2 4 2 2 4
(2)使HC O 的电离平衡向右移动且电离程度增大的措施有 (写一个)。
2 2 4
5
学学科科网网((北北京京))股股份份有有限限公公司司(3)设计实验证明HC O 为弱酸的方案及其现象均正确的是___________(单选,填字母)。
2 2 4
A.室温下,取0.005 mol/L的HC O 溶液,测其pH = 2
2 2 4
B.室温下,相同c(H+)的HC O 溶液和盐酸分别与同样颗粒大小的锌反应时,产生H 的起始速率相等
2 2 4 2
C.室温下,取pH= a (a<3)的HC O 溶液稀释至原体积的100倍后,测其pH< a+2
2 2 4
D.标准状况下,取0.10 mol/L的HC O 溶液100 mL与足量锌粉反应,收集到H 的体积为224 mL
2 2 4 2
(4)医学上常用酸性KMnO 溶液与HC O 溶液反应来测血液中血钙的含量。测定方法是取2mL血
4 2 2 4
液用蒸馏水稀释后,向其中加入足量的(NH )C O 溶液,反应生成CaC O 沉淀,将沉淀用稀硫酸溶解
4 2 2 4 2 4
得到HC O 后,再用KMnO 溶液滴定,滴定过程中发生的反应为:2 + 5H C O + 6H+ = 2Mn2+
2 2 4 4 2 2 4
+10CO ↑ + 8H O。
2 2
①溶解沉淀时不能用稀HCl代替稀HSO ,原因是 。
2 4
②终点现象为:当最后半滴KMnO 标准液滴入时, 。
4
③若上述滴定中消耗了1.0×10-4 mol/L KMnO 溶液20 mL,则200 mL该血液中含钙 g。
4
④下列操作会引起测定结果偏高的是 (双选,填字母)。
A.滴定管在盛装KMnO 溶液前未润洗
4
B.滴定过程中,部分液体溅出锥形瓶外
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,用待测液润洗
16.(14分)工业生产过程中产生的二氧化硫会造成环境问题,可用多种方法脱除。回答下列问题:
Ⅰ.由次氯酸钠碱性废水(含有杂质Ca2+)处理硫酸工业尾气的流程如下:
(1)控制合适的条件有利于提高SO 的吸收率(脱硫率)。
2
①脱硫时需保持溶液呈碱性,此过程的主要反应之一为SO +2OH-= +H O;另一个为二氧化硫与次
2 2
氯酸钠发生的氧化还原反应,请写出该反应的离子方程式: 。
②提高脱硫率的可行措施有 (填序号)。
a.加快通入尾气的速率
b.吸收塔中喷淋的碱液与气体逆向接触
c.提高碱液pH
③温度控制在40~60 ℃之间,脱硫率较高,原因是 。
(2)滤渣的主要成分为 (填化学式)。
Ⅱ.为实现燃煤脱硫,向煤中加入浆状Mg(OH) ,使燃烧产生的SO 转化为稳定的MgSO 。
2 2 4
(3)写出该反应的化学方程式: 。
Ⅲ. 双碱法脱除烟气中SO 的过程如图所示。
2
6
学学科科网网((北北京京))股股份份有有限限公公司司(4)脱除SO 的过程中,可以循环利用的物质 (填化学式)。
2
(5)过程Ⅱ中,1 mol O 可氧化 mol Na SO 。
2 2 3
17.(15分)某化学小组欲定量探究含 对 溶液发生分解时化学反应速率的影响,该小组先取
溶液利用如图装置进行实验,得到了如表数据:
0 2 4 6 8 10
0.0 9.9 17.2 22.4 26.5 29.9
说明:①表中 是折合成标准状况下 的体积:
②假设反应过程中溶液体积的变化忽略不计。
(1)检查该装置气密性的操作为 。
(2)0~6min的平均反应速率: (保留两位有效数字),0~6min的平均反应速
率 6~10min的平均反应速率(填“>”“<”或“=”),原因是 。
(3)对于 的分解反应, 也有一定的催化作用。为比较 和 对 分解的催化效
果,研究小组的同学设计了如图所示的实验,发现滴加 溶液的试管产生的气泡更剧烈,研究小
组得出了“ 的催化效果一定比 更好”的结论,你认为利用该现象得出的该结论
(填“合理”或“不合理”),原因是 。某同学将 溶液
改为 溶液进行实验,现象与上述实验一致,故研究小组得出了“ 催化效果更
好”的结论,其理由是 。
18.(15分)近我国大力加强温室气体CO 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
2
7
学学科科网网((北北京京))股股份份有有限限公公司司回答下列问题:
(1)已知:CO₂(g)+H₂(g)=H O (g)+ CO (g) ΔH =+41.1 kJ·mol-1;
2 1
CO(g)+2H₂(g)=CH OH(g) ΔH = -90.0 kJ·mol-1。
3 2
根据CO₂催化氢化合成甲醇的热化学方程式,求算出对应的焓变:
kJ·mol-1。
(2)为提高CHOH (g)的产率,理论上应采用的条件是 (填字母)。
3
a.高温高压 b.低温高压 c.高温低压 d.低温低压
(3)250℃时,在恒容密闭容器中由CO(g)催化氢化合成CHOH (g),如图为不同投料比
2 3
[n(H )/ n(CO )]时某反应物X的平衡转化率的变化曲线。
2 2
反应物x是 (填“CO”或“H”)。
2 2
(4)250℃时,在体积为20L的恒容密闭容器中加入6mol H、2 mol CO 和催化剂,10min 时反应达
2 2
到平衡,测得 (CHCOOH)=0.75 mol·L-1。
3
①前 10 min 内平均反应速率。(H )= mol·L-1·min-1。
2
②化学平衡常数K= 。
③催化剂和反应条件与反应物的转化率和产物的选择性高度相关,控制相同投料比和相同反应时间,
得到四组数据如表所示:
实验编
温度/K 催化剂 CO 的转化率/% 甲醇的选择性/%
2
号
A 543 Cu/ZnO纳米棒 12.3 42.3
B 543 Cu/ZnO纳米片 11.9 72.7
C 553 Cu/ZnO纳米棒 15.3 39.1
D 553 Cu/ZnO纳米片 12.0 70.6
根据上表所给数据,用CO 生产甲薛的最优条件为 (填实验编号)。
2
8
学学科科网网((北北京京))股股份份有有限限公公司司