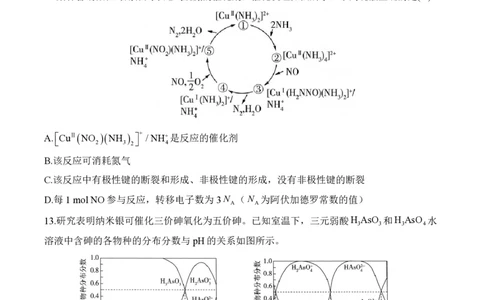
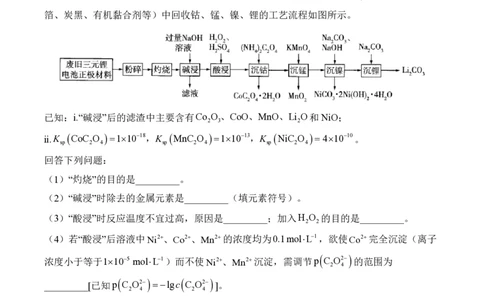
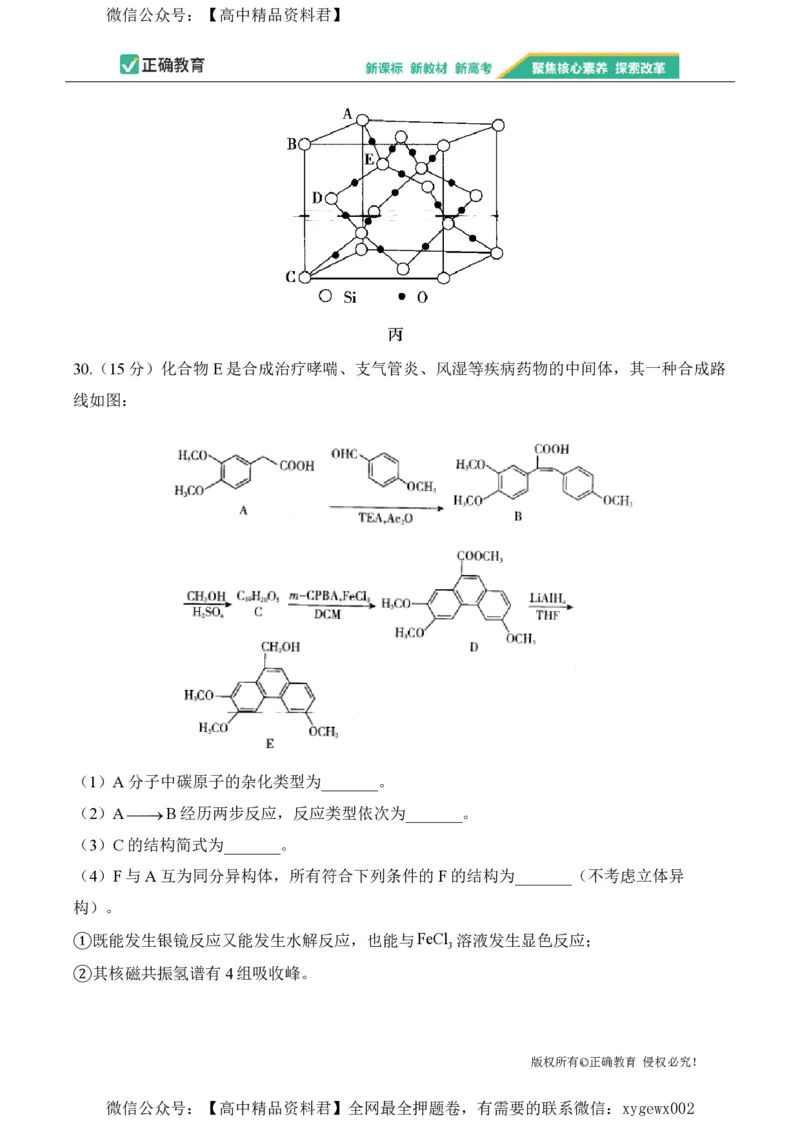
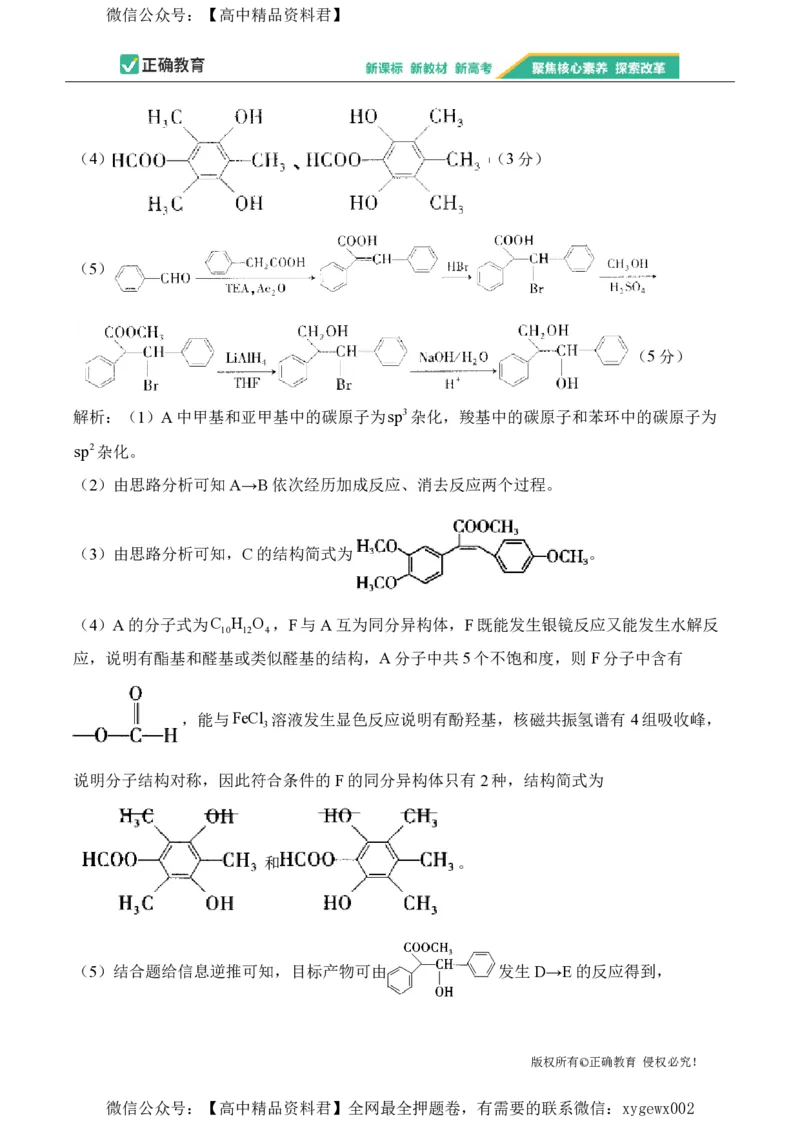
文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【新课标卷】
可能用到的相对原子质量:H-1、N-14
一、选择题:本题共 7小题,每小题 6分,共 42分。在每小题给出的四个选项中,只有一项
符合题目要求。
7.中华文化博大精深,为世界的发展做出了重要的贡献。下列说法正确的是( )
A.指南针的磁石的主要成分是三氧化二铁
B.蔡侯纸的主要成分属于合成高分子材料
C.瓷器是以黏土为主要原料烧制而成
D.制作豆腐时,需添加石膏使蛋白质变性
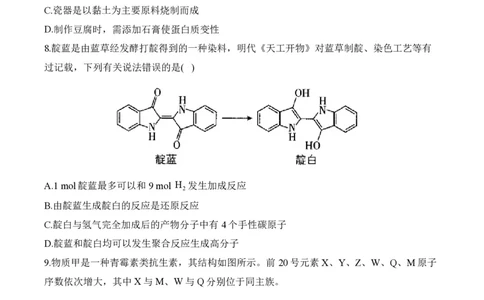
8.靛蓝是由蓝草经发酵打靛得到的一种染料,明代《天工开物》对蓝草制靛、染色工艺等有
过记载,下列有关说法错误的是( )
A.1 mol靛蓝最多可以和9 mol H 发生加成反应
2
B.由靛蓝生成靛白的反应是还原反应
C.靛白与氢气完全加成后的产物分子中有4个手性碳原子
D.靛蓝和靛白均可以发生聚合反应生成高分子
9.物质甲是一种青霉素类抗生素,其结构如图所示。前20号元素X、Y、Z、W、Q、M原子
序数依次增大,其中X与M、W与Q分别位于同主族。
下列说法正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
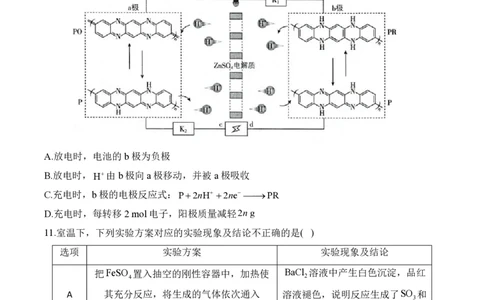
A.最简单气态氢化物的稳定性:WQ
C.基态原子的未成对电子数:Y=Q D.电负性:W
N,则最简单气态氢化物的稳定性:H O NH ,A 2 3 错误;K与S2核外电子排布相同,S2核电荷数小,半径大,B错误;基态C原子的价层电 子排布式为2s22p2,基态S原子的价层电子排布式为3s23p4,二者未成对电子数都是2,C正 确;同主族元素从上到下电负性逐渐减小,电负性:O>S,D错误。 10.答案:D 解析:根据以上分析,放电时,a极为正极,b极为负极,A正确;放电时,阳离子由负极 (b极)移向正极(a极),即H由b极向a极移动,并被a极吸收,B正确;充电时,b极 为阴极,发生还原反应:P2nH 2ne PR,C正确;充电时,根据阳极(a极)反 应,每转移2 mol电子,阳极失去2 mol H,质量减轻 2 g,D错误。 11.答案:B 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 △ 解析:FeSO 受热发生分解,化学方程式为2FeSO Fe O SO SO ,SO 可与水反应 4 4 2 3 2 3 3 产生SO2进而与BaCl 反应生成BaSO 白色沉淀,混合气体通入BaCl 溶液中产生白色沉淀, 4 2 4 2 说明反应生成了SO ,通入品红溶液,品红溶液褪色,说明反应生成了SO ,A正确;加入 3 2 过量Ba(OH) 溶液,NH AlSO 溶液中NH、Al3、SO2均参加反应,离子方程式中离子 2 4 4 2 4 4 的化学计量数之比应符合该化学式中的离子配比,即n NH :n Al3 :n SO2 =1:1:2,对应 4 4 △ 的离子方程式应为NH Al3 2SO2 2Ba2 5OH NH AlO 2BaSO 3H O,B 4 4 3 2 4 2 错误;装有NO 和N O 气体的烧瓶中存在反应2NO (g)N O (g),将烧瓶浸泡在热水 2 2 4 2 2 4 中,观察到烧瓶内气体红棕色加深,说明NO 浓度增大,上述平衡逆向移动,故能说明反应 2 2NO (g)N O (g)是放热反应,C正确;CuSO 溶液中滴加氨水,先生成Cu(OH) 沉 2 2 4 4 2 淀,然后Cu(OH) 溶于过量氨水生成CuNH 2 ,加入乙醇降低溶剂的极性,析出深蓝色 2 3 4 的晶体CuNH SO H O,D正确。 3 4 4 2 12.答案:D 解析:CuⅡNO NH /NH先生成,后被消耗,是反应的中间产物,A错误;由图可 2 3 2 4 知,该反应生成氮气,且氮气没有被消耗,B错误;③→④的反应涉及极性键和非极性键的 形成以及极性键的断裂,④→⑤的反应涉及非极性键的断裂,C错误;由催化机理图可知总 催化剂 反应为4NH 4NOO 4N 6H O,每1 mol NO参与反应,转移电子数为3N ,D 3 2 2 2 A 正确。 13.答案:B c AsO3 c H 解析:H AsO 的三级电离常数K H AsO 4 ,根据图2可知,当 3 4 a3 3 4 c HAsO2 4 c HAsO2 c AsO3 时,pH为11.5,所以K H AsO 1011.5,其数量级为1012,A正 4 4 a3 3 4 确;根据图1可知,H AsO 的一级电离常数K H AsO 109.2,则0.1molL1 H AsO 溶液 3 3 a1 3 3 3 3 一级电离产生的c2 H 109.20.1mol2L2,则c H 105.1 molL1,H AsO 还有二级电 3 3 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 离及三级电离,故溶液中c H 105.1 molL1,pH<5.1,B错误;0.2molH AsO 与0.3 mol 3 4 NaOH完全反应生成0.1mol NaH AsO 和0.1mol NaHAsO ,由图2可推出 2 4 4 K H AsO 102.2,K H AsO 107.0,故HAsO2的水解常数K HAsO2 107.0,则 a1 3 4 a2 3 4 4 h 4 有c H AsO c HAsO2 ,此时溶液显中性,有c H c OH ,C正确;pH=10时,三 2 4 4 价砷主要存在形式为H AsO,五价砷主要存在形式为HAsO2,Ag为催化剂,故其转化的离 2 3 4 Ag 子方程式为2H AsO O 2OH 2HAsO2 2H O,D正确。 2 3 2 4 2 27.(14分)答案:(1)除去正极材料中的炭黑及有机黏合剂,将金属元素转化为氧化物 (1分) (2)Al(1分) (3)防止H O 分解(2分);将Co O 还原为Co2(2分) 2 2 2 3 (4)12p C O2 13(2分) 2 4 (5)3Mn2 2MnO 2H O 5MnO 4H(2分);2:3(2分) 4 2 2 (6)Na CO 浓度过高会使Li沉淀,影响Ni2和Li的分离(2分) 2 3 解析:(1)“灼烧”时,正极材料中的炭黑及有机黏合剂会燃烧转化为气体除去, LiCo Mn Ni O 转化为相应的氧化物。 x y z 2 (2)向灼烧渣中加入过量氢氧化钠溶液碱浸,Al元素会转化为NaAl(OH) 除去。 4 (3)由“酸浸”时加入的物质有H O 可知,温度不宜过高的原因是防止H O 分解;根据“碱 2 2 2 2 浸”后的滤渣中含有Co O ,Co O 中Co为+3价,“酸浸”后沉钴时Co为+2价可知,加入 2 3 2 3 H O 的目的是将Co O 还原为Co2。 2 2 2 3 (4)已知K CoC O c Co2 c C O2 11018,钴离子完全沉淀时,溶液中 sp 2 4 2 4 c C O2 11018 molL1 1013 molL1,则p C O2 13;已知 2 4 1105 2 4 K MnC O c Mn2 c C O2 11013,锰离子浓度为0.1molL1,要不使锰离子沉 sp 2 4 2 4 淀,需使溶液中c C O2 11013 molL1 1012 molL1,即p C O2 12,所以使溶液中 2 4 0.1 2 4 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 钴离子完全沉淀,而锰离子、镍离子不沉淀的p C O2 的范围为12p C O2 13。 2 4 2 4 (5)“沉锰”时,加入高锰酸钾的目的是将溶液中的锰离子转化为二氧化锰,反应的离子方程 式为3Mn2 2MnO 2H O 5MnO 4H;其中MnO为氧化剂,Mn2为还原剂,则 4 2 2 4 氧化剂与还原剂的物质的量之比为2:3。 (6)碳酸钠溶液浓度过高会使溶液中的锂离子转化为碳酸锂沉淀,从而影响镍离子和锂离子 的分离,所以沉镍时选择加入氢氧化钠溶液和较低浓度的碳酸钠溶液。 △ 28.(15分)答案:(1)a(或c)(2分);NH H O NH H O(或 3 2 3 2 NH H OCaO Ca(OH) NH )(2分) 3 2 2 3 (2)防倒吸(1分) (3)肼有还原性,会与氯气以及次氯酸钠发生氧化还原反应,降低肼的产量(合理即可) (2分) (4)2NH ClO N H H OCl(2分) 3 2 4 2 (5)滴入最后半滴碘液,溶液由无色变为蓝色,且半分钟内不褪色(2分) (6)bcd(2分) 32V V (7) 2 1 (2分) 245m 解析:(1)实验室制备氨气总共有三种方法,化学方程式分别为 △ △ 2NH ClCa(OH) CaCl 2NH 2H O、NH H O NH H O、 4 2 2 3 2 3 2 3 2 NH∣H OCaO NH Ca(OH) [提示:不能用类似启普发生器的装置]。 3 2 3 2 (2)氨气极易溶于水,多孔球泡气孔较小,内部体积大,可起到防倒吸的作用。 (4)由题干可知次氯酸钠与氨气反应制备水合肼的离子方程式为 2NH ClO N H H OCl。 3 2 4 2 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 (5)由信息可知肼与碘单质反应生成碘离子,当滴加最后半滴碘液时,溶液由无色变为蓝 色,且半分钟内不褪色,此时表明反应完全[点拨:判断颜色变化时,要判断当滴加最后半滴 碘液时,溶液中多出来的是碘液还是与碘液反应的物质]。 (6)a项,第二次读数时,若左侧液面低,会导致测量体积偏小,最终导致肼的含量测量值 偏低;b项,若反应过程中没有导管,装置内压强偏大,气体体积偏大,会使测量结果偏 高;c项,滴定后俯视,导致测量体积偏大,测量结果偏高;d项,反应结束时,装置未恢复 至室温,导致气体体积偏大,测量结果会偏高。 (7)该过程涉及反应N H 2I N 4HI,此时测量氮气体积为V V mL,则生成 2 4 2 2 2 1 V V 103 氮气的物质的量为 2 1 mol,则粗产品中肼的纯度为 24.5 32V V 103 32V V 2 1 100% 2 1 %。 24.5m 245m 29.(14分)答案:(1)4FeS(s)7O (g) 2Fe O (s)4SO (g) H 2454.94kJ/mol(2 2 2 3 2 分) (2)BD(1分) 7 2 (3) P 0.2 P 0.1 P 0.352(2分);该反应的正反应是气体分子数增大的反 0 0.65 0 0.65 0 0.65 应,随着氩气通入量的增大,平衡体系中各气体的分压减小,平衡向正反应方向移动(1 分);0.7(1分) (4)正四面体形(1分);相同(1分);FePO Li e LiFePO (1分) 4 4 1 3 3 8a (5)( , , )(2分); 107(2分) 4 4 4 3 解析:(1)FeS煅烧生成Fe O 和SO 的化学方程式为4FeS7O 2Fe O 4SO ;根据 2 3 2 2 2 3 2 盖斯定律,③×3+④×4-①×4-②×2可得该反应的热化学方程式为 4FeS(s)7O (g) 2Fe O (s)4SO (g) H 2454.94kJ/mol。 2 2 3 2 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 (2)NH Fe SO (OH) 为固体,加入固体,平衡不移动,A不符合题意;使 4 3 4 2 6 SO、NH 、H O液化并及时分离,可使平衡正向移动,平衡转化率增大,B符合题意;催化 3 3 2 剂不能使平衡移动,不改变平衡转化率,C不符合题意;该反应的正反应是气体分子数增大 的反应,保持压强不变充人氦气,随着氩气通入量的增大,平衡向正反应方向移动,平衡转 化率增大,D符合题意。 3 7 (3)根据NH Fe SO (OH) (s) Fe O (s)2SO (g)NH (g) H O(g)可知,达 4 n 4 2 6 2 2 3 3 3 2 2 到平衡后,当NH 的物质的量为0.1 mol,则SO 的物质的量为0.2 mol,H O的物质的量为 3 3 2 0.35 mol,气体的总物质的量为0.65 mol,此时压强平衡常数 7 2 0.2 0.1 0.352;该反应的正反应是气体分子数增大的反应,随着氩 K P P P p 0 0.65 0 0.65 0 0.65 气通入量的增大,平衡体系中各气体的分压减小,平衡向正反应方向移动,NH 的量增大。 3 由图甲可知,n(Ar)0.1mol时,nNH 0.2mol,由方程式中的系数可知 3 nH O0.7mol。 2 (4)PO3的价层电子对个数为4且不含孤电子对,根据价层电子对互斥理论可知PO3的 4 4 VSEPR模型为正四面体结构;FePO 16 中铁元素的化合价为+2,LiFePO 中铁元素的化 4 6 4 合价为+2,二者化合价相同。 (5)由晶胞结构图丙可知,若A原子的原子坐标为(0,1,1),C原子的原子坐标为(0, 1 3 3 0,0),则白球E原子的原子坐标为( , , );Si—O键长为a nma107 cm,设晶 4 4 4 1 胞边长为l,硅氧原子在体对角线上,硅氧键的键长为体对角线的 ,根据几何关系可知 8 8a l 107 cm。 3 30.(15分)答案:(1)sp3、sp2(2分) (2)加成反应、消去反应(2分) (3) (3分) 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 (4) (3分) (5) (5分) 解析:(1)A中甲基和亚甲基中的碳原子为sp3杂化,羧基中的碳原子和苯环中的碳原子为 sp2杂化。 (2)由思路分析可知A→B依次经历加成反应、消去反应两个过程。 (3)由思路分析可知,C的结构简式为 。 (4)A的分子式为C H O ,F与A互为同分异构体,F既能发生银镜反应又能发生水解反 10 12 4 应,说明有酯基和醛基或类似醛基的结构,A分子中共 5个不饱和度,则F分子中含有 ,能与FeCl 溶液发生显色反应说明有酚羟基,核磁共振氢谱有4组吸收峰, 3 说明分子结构对称,因此符合条件的F的同分异构体只有 2种,结构简式为 和 。 (5)结合题给信息逆推可知,目标产物可由 发生D→E的反应得到, 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 可由 与CH OH反应得到, 可由 3 与 发生A→B中的反应、生成的碳碳双键与HBr加 成、—Br再水解得到,为避免酯化时发生副反应以及酯基在碱性条件下水解,—Br应最后水 解,具体路线见答案。 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】 版权所有©正确教育 侵权必究! 微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002