文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【江苏版】
可能用到的相对原子质量:H-1、N-14、S-32、Cl-35.5、Co-59、Cd-112
一、单项选择题:本题共 13小题,每小题 3分,共 39分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.中秋节是我国民间传统节日之一,自古便有祭月、赏月、吃月饼、燃灯、饮桂花酒等民
俗,流传至今,经久不息。下列说法不正确的是( )
A.若人体内缺少乙醛脱氢酶,饮桂花酒会产生醉酒症状
B.月饼中的油脂易被氧化,保存时常放入装有铁粉的透气袋
C.“万里婵娟,几许雾屏云幔”中“云”和“雾”均为气态
D.“燃灯”“酿桂花酒”过程中均涉及化学变化
2.汽车剧烈碰撞时,安全气囊中发生反应:10NaN 2KNO K O5Na O16N 。下列
3 3 2 2 2
有关说法正确的是( )
A.N 的电子式为 B.N的空间结构为V形
2 3
C.反应的还原产物为N D.反应为复分解反应
2
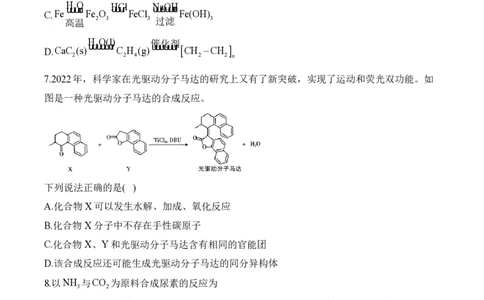
3.实验室制取并收集少量NH ,同时进行性质实验,下列实验装置和操作能达到实验目的的
3
是( )
A.用装置甲制取并干燥NH
3
B.用装置乙证明NH 的氧化性
3
C.用装置丙收集NH 并验满
3
D.用装置丁收集并吸收多余的NH
3
4.某抗癌药物Q的结构简式如图所示,图中W、X、Y、Z是原子序数依次增大的短周期主族
元素,W、Y原子的最外层电子数目相同。下列叙述正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.最简单氢化物的沸点:X>W
B.原子半径:Y>X>W
C.最高价氧化物对应水化物的酸性:W>Z
D.单质活泼性:W>Y
5.阅读下列材料,完成下列题:
硫有许多重要化合物。SO 具有还原性,可被强氧化剂氧化成SO ;SO 可使品红溶液、酸
2 3 2
性高锰酸钾溶液褪色。Na S在染料工业中用于生产硫化染料。硫代硫酸钠(Na S O )可用
2 2 2 3
作含氮尾气的中和剂、媒染剂、麦秆和毛的漂白剂以及纸浆漂白时的脱氯剂等。
(1)下列说法正确的是( )
A.基态硫原子的价电子轨道表示式为
B.SO 与SO 分子中的中心硫原子杂化轨道类型不同
2 3
C.Na S O 中三种元素电负性大小关系为O>S>Na
2 2 3
D.O和S同族,因此水和硫化氢的微粒间作用力类型相同
(2)下列表达式正确的是( )
A.Na S O 与盐酸反应的离子方程式为S O2 2H SO SH O
2 2 3 2 3 2 2
B.Na S水解的离子方程式为S2 2H O‡ˆ ˆˆ†ˆ 2OH H S
2 2 2
C.用惰性电极电解H SO 溶液时,阳极的电极反应式为2H O2e 2OH H
2 4 2 2
D.铜与浓硫酸反应制备SO 的化学方程式为Cu2H SO (浓) CuSO SO 2H O
2 2 4 4 2 2
(3)下列物质的性质与用途对应关系正确的是( )
A.二氧化硫具有漂白性,能使酸性高锰酸钾溶液褪色
B.硫化钠具有还原性,可用作废水中Hg2的沉淀剂
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
C.浓硫酸具有吸水性,可用作干燥剂
D.Na S O 具有碱性,可用于鞣革时处理重铬酸盐
2 2 3
6.在给定条件下,下列选项所示的物质间转化能实现的是( )
O H SO
uur2 uu2uuuur4
A.Na Na O Na SO
2 2 4
点燃
电解 Cl (g)
uuuur uuu2uuur
B.Al O (熔融) Al(s) AlCl (s)
2 3 冰晶石 △ 3
H
uu2u
O
ur
HuuCurl NuuauOuuHur
C.Fe Fe O FeCl Fe(OH)
高温 2 3 3 过滤 3
H O(l) 催化剂
D.CaC (s) uu2uuuur C H (g) uuuuuurCH CH
2 2 4 2 2 n
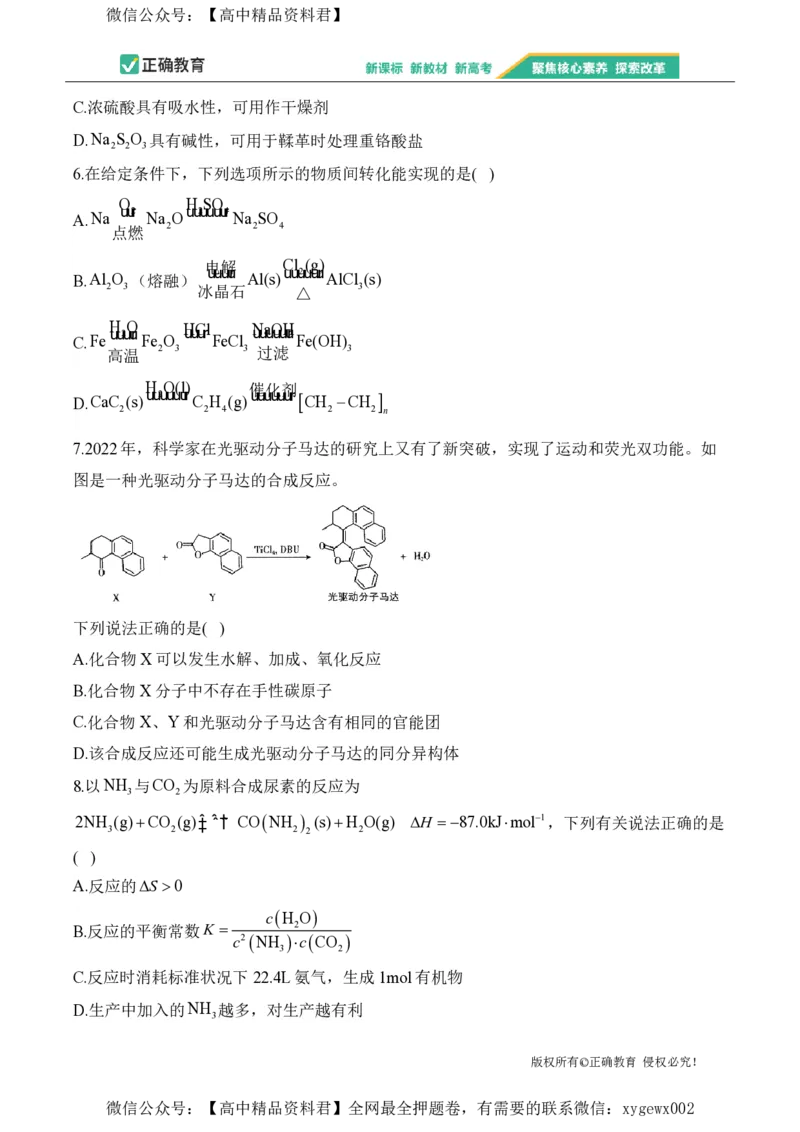
7.2022年,科学家在光驱动分子马达的研究上又有了新突破,实现了运动和荧光双功能。如
图是一种光驱动分子马达的合成反应。
下列说法正确的是( )
A.化合物X可以发生水解、加成、氧化反应
B.化合物 X分子中不存在手性碳原子
C.化合物 X、Y和光驱动分子马达含有相同的官能团
D.该合成反应还可能生成光驱动分子马达的同分异构体
8.以NH 与CO 为原料合成尿素的反应为
3 2
2NH (g)CO (g)‡ˆ ˆˆ†ˆ CONH (s)H O(g) H 87.0kJmol1,下列有关说法正确的是
3 2 2 2 2
( )
A.反应的S 0
cH O
B.反应的平衡常数K 2
c2NH cCO
3 2
C.反应时消耗标准状况下22.4L氨气,生成1mol有机物
D.生产中加入的NH 越多,对生产越有利
3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
9.室温下,下列实验方案(和现象)能达到实验目的的是( )
选项 实验方案(和现象) 实验目的
取少量溶液于试管中,滴加BaCl 溶液, 检验溶液中是否存在
2
A
有白色沉淀生成,加稀硝酸沉淀不溶解 SO2
4
向FeCl 和KSCN的混合溶液中滴入少量 验证Ag和Fe3氧化性
2
B
酸化的AgNO 溶液 强弱
3
分别取少量 NaCl溶液和NaNO 溶液于两 鉴别NaCl溶液与
2
C
支试管中,再滴加酸性KMnO 溶液 NaNO 溶液
4 2
向FeCl 溶液中滴入几滴30%的H O 溶 验证Fe3能催化H O 分
3 2 2 2 2
D 液,有气体产生,一段时间后FeCl 溶液颜 解,且该分解反应为放
3
色加深 热反应
A.A B.B C.C D.D
10.常温下,丙酸CH CH COOH溶液中含碳粒子的分布系数(δ)与溶液pH的关系如图
3 2
甲,向20 mL 0.1 molL1丙酸溶液中滴加0.1 molL1 NaOH溶液,溶液pH与滴入NaOH溶液
cCH CH COOH
体积的关系如图乙。已知:CH CH COOH 3 2 。
3 2 cCH CH COOHc CH CH COO
3 2 3 2
下列说法错误的是( )
A.由图甲知,丙酸的电离平衡常数K 1104.88
a
B.由图乙知,①对应的溶液中存在:
2c H cCH CH COOH2c OH c CH CH COO
3 2 3 2
C.由图乙知,②对应的溶液中存在:c CH CH COO 102.12cCH CH COOH
3 2 3 2
D.由图乙知,③对应的溶液中存在:CH CH COOHc Na cCH CH COOH
3 2 3 2
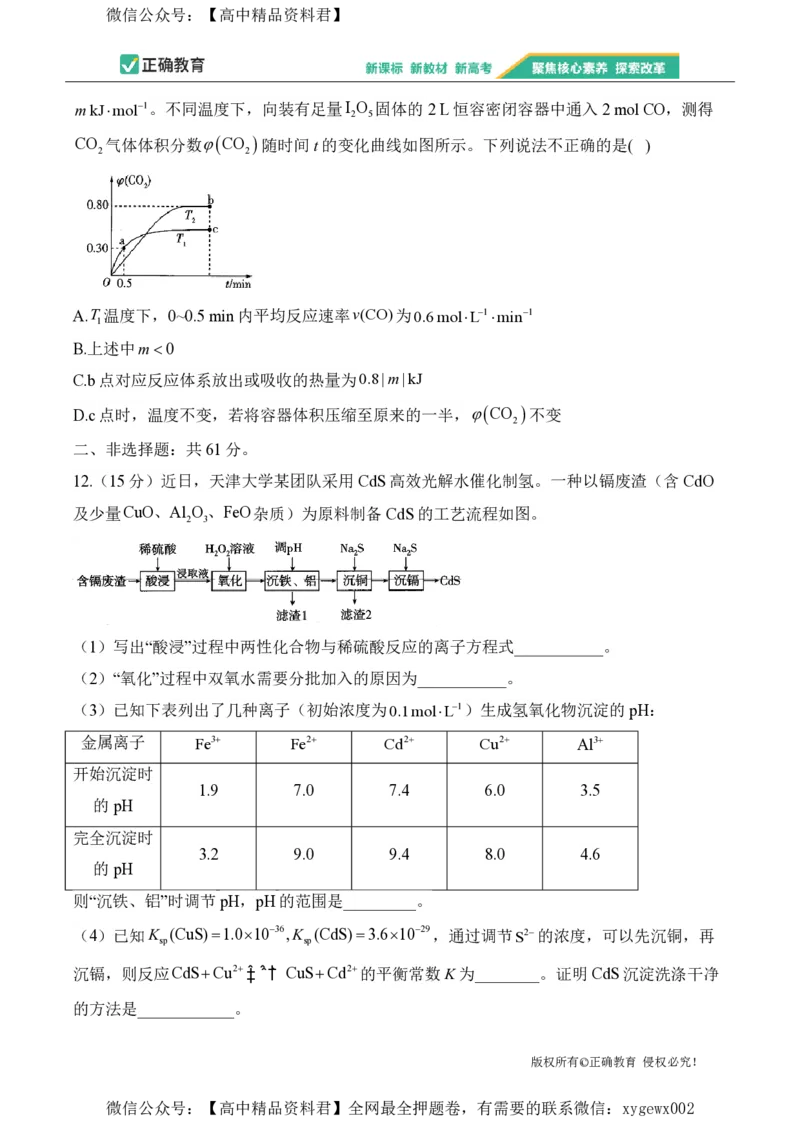
11.利用I O 可消除CO污染,其反应为I O (s)5CO(g)‡ˆ ˆˆ†ˆ 5CO (g)I (s) ΔH
2 5 2 5 2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
m kJmol1。不同温度下,向装有足量I O 固体的2 L恒容密闭容器中通入2 mol CO,测得
2 5
CO 气体体积分数CO 随时间t的变化曲线如图所示。下列说法不正确的是( )
2 2
A.T 温度下,0~0.5 min内平均反应速率v(CO)为0.6 molL1min1
1
B.上述中m0
C.b点对应反应体系放出或吸收的热量为0.8|m|kJ
D.c点时,温度不变,若将容器体积压缩至原来的一半,CO 不变
2
二、非选择题:共61分。
12.(15分)近日,天津大学某团队采用CdS高效光解水催化制氢。一种以镉废渣(含CdO
及少量CuO、Al O、FeO杂质)为原料制备CdS的工艺流程如图。
2 3
(1)写出“酸浸”过程中两性化合物与稀硫酸反应的离子方程式___________。
(2)“氧化”过程中双氧水需要分批加入的原因为___________。
(3)已知下表列出了几种离子(初始浓度为0.1 molL1)生成氢氧化物沉淀的pH:
金属离子 Fe3 Fe2 Cd2 Cu2 Al3
开始沉淀时
1.9 7.0 7.4 6.0 3.5
的pH
完全沉淀时
3.2 9.0 9.4 8.0 4.6
的pH
则“沉铁、铝”时调节pH,pH的范围是_________。
(4)已知K (CuS)1.01036,K (CdS)3.61029,通过调节S2的浓度,可以先沉铜,再
sp sp
沉镉,则反应CdSCu2‡ˆ ˆˆ†ˆ CuSCd2的平衡常数K为________。证明CdS沉淀洗涤干净
的方法是____________。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(5)“沉铁、铝”时多次洗涤形成的铁、铝沉淀的原因是____________。
(6)已知CdS晶体的晶胞结构如图所示,若CdS晶体的密度为 gcm3,则图中a、b两原
子的核间距离为_________cm。
13.(13分)吡唑类化合物是重要医药中间体,如图是吡唑类物质L的一种合成路线:
已知:①
一定条件
uuuuuuuuur
②R CHOR NH R CH NR
1 2 2 1 2
(1)I中含有的官能团名称为__________。
(2)A→B的反应类型为__________。
(3)K的分子式为C H O ,K的结构简式为__________。
10 8 2
(4)写出符合下列条件的I的一种同分异构体的结构简式:__________。
①含苯环;
②只含一种含氧官能团;
③有 3种不同化学环境的氢原子;
④不考虑结构的稳定性
(5)以 和乙酸为原料,利用题中信息及所学知识,选用必要的无机试剂,合
反应试剂
uuuuuuuuur
成 ,写出合成路线。(合成路线的表示方式为:甲 乙……目标产物)
反应条件
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
14.(17分)三氯化六氨合钴(III){CoNH Cl ,M 267.5 gmol1}在工业上用途广泛。
3 6 3
实验室以活性炭作为催化剂,H O 作氧化剂氧化CoCl 制备三氯化六氨合钴,反应过程放
2 2 2
热。
已知:①钴单质在300 ℃以上易被氧气氧化,CoCl 易潮解;
2
②Co2不易被氧化,Co3具有强氧化性;CoNH 2 具有较强的还原性,CoNH 3
3 6 3 6
性质稳定。
I.CoCl 的制备(装置如图甲,夹持及加热装置略)。
2
(1)使用仪器a滴加浓盐酸的优点是__________。上述装置有一处缺陷,改进的方法是
_________。
(2)实验时,要先滴加浓盐酸,装置中开始生成氯气,待_________(填现象)时,再加热
钴粉。
Ⅱ.三氯化六氨合钴(III)的制备(如图乙,部分装置省略)。
①先向三颈烧瓶中加入活性炭、CoCl 和NH Cl溶液;
2 4
②向三颈烧瓶中___________;
③60 ℃水浴加热并充分搅拌,经过一系列操作可得三氯化六氨合钴(III){CoNH Cl }
3 6 3
粗产品。
(3)补充填写步骤②:_____________。
图乙装置A中制备三氯化六氨合钴(III)的总反应化学方程式为_____________。
III.纯度测定。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
称取2.8 g粗产品与氢氧化钠在空气中混合煅烧得氧化钴,酸溶后配成250 mL溶液。
a.取25.00 mL待测液于锥形瓶中,向锥形瓶中加入稍过量的KI溶液(Co3被还原后的产物
为Co2),充分反应。
b.用淀粉溶液作指示剂,用0.050 molL1 Na S O 标准溶液滴定
2 2 3
(2Na S O I Na S O 2NaI)。
2 2 3 2 2 4 6
c.平行滴定三次,消耗标准溶液的平均体积为 20.00 mL。
(4)该产品的纯度为__________(保留四位有效数字,写出计算过程)。
15.(16分)绿水青山就是金山银山。我们要加快形成绿色发展方式,构建经济与环境协同共
进的地球家园。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染
具有重要意义。回答下列问题:
(1)利用高效催化剂处理汽车尾气中的NO和CO,发生反应
2CO(g)2NO(g)2CO (g)N (g) H dkJmol1(d 0)。
2 2
已知:部分化学键的键能数据如表(CO以CO键构成)。
化学键 CO N N C O
E/ kJmol1 a b c
①NO中化学键的键能为_____kJmol1(用含a、b、c、d的代数式表示)。
②写出既可以加快化学反应速率又有利于提高 NO平衡转化率的措施_____(一条即可)。
③向 1L恒容密闭容器中充入 1molCO和1mol NO发生上述反应,在一定温度下达到平衡,
保持温度不变,t min时再而容器丙加入1molCO和1mol NO,再次达到平衡,N 的体积分
1 2
数_____(填“增大”“减小”或“不变”),整个过程容器中的压强(p)与反应时间(t)的关系曲线
如图1所示,已知m:n40:69,则用平衡分压代替平衡浓度表示的压强平衡常数K
p
_____。(分压=总压×物质的量分数,列出含 n 的代数式即可)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(2)工业上可将SO 和NO 混合转化,发生反应
2 2
SO (g)NO (g)SO (g)NO(g) H 0。在容积固定的绝热密闭容器中,能判断该反
2 2 3
应已达到化学平衡状态的是_____(填字母)。
A.SO (g)和NO(g)的浓度之比保持不变
3
B.混合气体的颜色保持不变
C.容器中压强不再变化
D.混合气体的密度保持不变
(3)科研团队在以H 为还原剂清除NO的研究方面取得了显著成果,其相关反应如下:
2
主反应:2NO(g)2H (g)N (g)2H O(g) H
2 2 2 1
副反应:2NO(g)H (g)N O(g)H O(g) H
2 2 2 2
n(NO)
在催化剂作用下,将原料气NO、H 按 1充入某刚性密闭容器中,在不同温度下,反
2 nH
2
应相同时间时测得混合气体中N 、N O的体积分数随温度的变化关系如图2所示。
2 2
①由图 2可知,混合气体中N 的体积分数明显高于N O的原因可能是______(填1种)。
2 2
②温度高于205℃时,N 的体积分数随温度的升高而减小的原因可能是______(列出1
2
点)。
(4)新型ZnCO 水介质电池放电时,温室气体CO 被转化为储氢物质甲酸(HCOOH),
2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
这为解决环境和能源问题提供了一条新途径。电池工作原理如图3所示,电极为金属锌和选
择性催化材料。放电时,正极的电极反应式为______。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:C
解析:乙醛脱氢酶参与人体内酒精的代谢,若人体缺少乙醛脱氢酶,喝酒后易产生醉酒症
状,A正确;铁粉具有还原性,易与氧气反应,起到吸氧作用,从而防止月饼中的油脂被氧
化,B正确;云由小水滴和小冰品组成,雾是飘浮在空气中的细小水珠,C错误;“燃灯”涉
及燃料的燃烧,“酿桂花酒”涉及糖类转化为乙醇的反应,均发生化学变化,D正确。
2.答案:C
解析:N 的电子式为 ,A错误;N与CO 互为等电子体,具有相似的结构特点,
2 3 2
故N的空间结构为直线形,B错误;由题给反应中N元素的化合价变化可知,N 既是还原
3 2
产物,也是氧化产物,C正确;该反应中N元素化合价发生变化,是氧化还原反应,不属于
复分解反应,D错误。
3.答案:D
解析:生石灰即氧化钙,与水反应放热可以促进浓氨水中氨气的挥发,且生成强碱氢氧化
钙,也利于氨气挥发,该装置可以制取氨气,但氨气为碱性气体,不能用浓硫酸干燥,A错
误;加热条件下氨气和氧化铜(黑色)反应,生成铜(红色)、氮气和水,证明氨气可以还
原氧化铜,证明了氨气的还原性,B错误;氨气密度比空气小,应该用向下排空气法收集氨
气,导管应该伸到试管底部,C错误;氨气密度比空气小,采用排空气法收集时,短管进氨
气,长管出空气(长管要伸到瓶底),收集方法正确,氨气难溶于四氯化碳,且四氯化碳的
密度比水大,所以导管伸入下层四氯化碳中可以避免导管口直接与水接触,可以防倒吸,该
装置可以吸收多余氨气,D正确。
4.答案:A
解析:常温下H O是液体,NH 是气体,H O的沸点较高,A项正确;原子半径:P>N>O,
2 3 2
B项错误;HClO 是最强的无机含氧酸,C项错误;N 化学性质稳定,而磷的化学性质活
4 2
泼,D项错误。
5.答案:(1)C
(2)A
(3)C
解析:(1)根据能量最低原理,同一电子层中电子应先排满s能级,再排p能级,故基态硫
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
原子的价电子轨道表示式应为 ,A错误;SO 与SO 分子中的中心S原子
2 3
的杂化轨道类型相同,均为sp2,B错误;同一周期,主族元素的电负性从左到右依次增大,
同一主族,元素的电负性从上到下呈现减小的趋势,故Na S O 中三种元素电负性大小关系
2 2 3
为O>S>Na,C正确;虽然O和S同族,但由于O的原子半径小、非金属性强,水分子之间
存在氢键,而硫化氢分子之间不存在氢键,D错误。
(2)Na S O 与盐酸反应的离子方程式为S O2 2H SO SH O,A正确;S2分
2 2 3 2 3 2 2
步水解,以第一步水解为主,故水解的离子方程式为S2 H O‡ˆ ˆˆ†ˆ OH HS,B错误;用
2
惰性电极电解H SO 溶液时,阳极上发生氧化反应,故阳极的电极反应式为
2 4
2H O4e O 4H,C错误;铜和浓硫酸反应必须加热,不加热不能反应,正确的化
2 2
△
学方程式应为Cu2H SO (浓) CuSO SO 2H O,D错误。
2 4 4 2 2
(3)二氧化硫能使酸性高锰酸钾溶液褪色是因为其具有还原性,A错误;硫化钠与Hg2反
应生成HgS沉淀,与Na S具有还原性无关,B错误;浓硫酸可用作干燥剂是因为其具有吸水
2
性,C正确;Na S O 具有还原性,可用作鞣革时处理重铬酸盐的还原剂,D错误。
2 2 3
6.答案:B
点燃 高温
解析:2NaO Na O ,A错误;3Fe4H O(g) Fe O 4H ,C错误;
2 2 2 2 3 4 2
CaC 2H O Ca(OH) C H ,D错误。
2 2 2 2 2
7.答案:D
解析:化合物X分子中含有羰基和苯环,可以发生加成反应,一定条件下可以发生氧化反
应,但不能发生水解反应,A错误;化合物X分子中连接甲基的碳原子为手性碳原子,B错
误;化合物X分子中含有的官能团为羰基,化合物 Y分子中含有的官能团为酯基,光驱动分
子马达含有的官能团为酯基和碳碳双键,C错误;根据题给反应和反应物结构的变化可以推
出,光驱动分子马达中碳碳双键形成时,可能形成顺反异构体,D正确。
8.答案:B
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
解析:题给反应的正反应是气体总分子数减小的反应,因此S 0,A项错误;反应中
cH O
CONH 为固体,H O为气体,故反应的平衡常数K 2 ,B项正确;反应
2 2 2 c2NH cCO
3 2
体系中只有尿素是有机物,反应消耗标准状况下22.4L(即1 mol)氨气时,生成0.5mol尿
素,C项错误;加入NH 可以提高尿素的产量,但NH 的平衡转化率也会降低,生产中加入
3 3
氨气的量过多会增加生产成本,对生产不一定有利,D项错误。
9.答案:D
解析:
选项 分析 结果
溶液中滴加BaCl 溶液产生不溶于稀硝酸的白色沉淀,该沉淀
2
A 可以是AgCl、BaSO 、BaSO ,故无法确定溶液中是否存在 错误
4 3
SO2
4
酸性条件下AgNO 中的NO也能将Fe2氧化为Fe3,故无法比
3 3
B 错误
较Ag和Fe3的氧化性强弱
C 酸性条件下Cl和NO均能还原高锰酸钾溶液使其褪色 错误
2
向FeCl 溶液中加入H O 溶液有气体产生,说明Fe2能催化
3 2 2
D H O 的分解,一段时间后FeCl 溶液颜色加深,说明Fe3的水 正确
2 2 3
解被促进,证明该分解反应为放热反应
10.答案:C
解析:由图甲知,当含碳粒子的分布系数0.5时,
pH4.88,c CH CH COO cCH CH COOH,则丙酸的电离常数
3 2 3 2
c
CH CH
COO
c
H
K 3 2 c H 1104.88,A正确;由图乙知,①对应的溶液中溶质
a cCH CH COOH
3 2
为等物质的量浓度的CH CH COOH和CH CH COONa,由质子守恒可得
3 2 3 2
2c H cCH CH COOH2c OH c CH CH COO ,B正确;②对应的溶液中溶质为
3 2 3 2
CH CH COOH和CH CH COONa,此时pH=7即c H 1107 molL1,结合丙酸电离常数
3 2 3 2
K 1104.88可求得c CH CH COO 102.12cCH CH COOH,C错误;③对应的溶液中
a 3 2 3 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
溶质为CH CH COONa,由物料守恒得
3 2
cCH CH COOH
c Na c CH CH COO cCH CH COOH 3 2 ,所以
3 2 3 2 CH CH COOH
3 2
CH CH COOHc Na cCH CH COOH,D正确。
3 2 3 2
11.答案:C
解析:由图象分析可知,T 温度下,0.5 min时CO 的体积分数为0.30,设转化的CO的物质
1 2
的量为xmol,列三段式:
x
则 0.30,解得x0.6,所以0~0.5 min内的平均反应速率
2xx
0.6mol
2L ,A项正确;根据图中曲线,“先拐先平数值大”,可知
v(CO) 0.6 molL1min1
0.5min
T T ,即b点温度低于c点,降低温度,平衡正向移动,说明该反应为放热反应,m0,
1 2
B项正确;该反应前后气体分子数不变,b点时,CO 的体积分数为0.80,则CO 的物质的量
2 2
为0.82 mol1.6 mol,根据题给热化学方程式知该反应生成5 mol CO 时放出的热量为
2
|m|kJ,则生成1.6 mol CO 时放出的热量为0.32|m|kJ,C项错误;该反应前后气体分子数
2
不变,温度不变时,将容器体积压缩至原来的一半,平衡不移动,CO 不变,D项正
2
确。
12.答案:(1)Al O 6H 2Al3 3H O(2分)
2 3 2
(2)避免反应过快、放出热量较多:减少双氧水分解,以免造成氧化剂损失(2分)
(3)4.6pH6.0(2分)
(4)3.6107(2分);取少量最后一次的洗涤液于试管中,向其中滴入盐酸酸化的BaCl 溶
2
液,若不出现白色沉淀,则证明CdS沉淀洗涤干净(3分)
(5)铝、铁形成沉淀时易形成胶体,其能吸附较多的Cd2(2分)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
2 576
(6)
3
(2分)
2 N
A
解析:(1)Al O 为两性氧化物,“酸浸”过程中,其与稀硫酸反应的离子方程式为
2 3
Al O 6H 2Al3 3H O。
2 3 2
(2)生成的铁离子对双氧水分解起催化作用,分批加入双氧水,避免反应过快、放出热量较
多,减少双氧水分解,以免造成氧化剂损失。
(3)“沉铁、铝”时,铁离子和铝离子完全沉淀,Cd2、Cu2不能生成沉淀,故pH的范围为
4.6pH6.0。
c
Cd2
c
Cd2
c
S2
K (CdS) 3.61029
(4)K sp 3.6107。取少量最后一次的洗涤
c Cu2 c Cu2 c S2 K (CuS) 1.01036
sp
液于试管中,向其中滴入盐酸酸化的BaCl 溶液,若不出现白色沉淀,则证明CdS沉淀洗涤
2
干净。
(5)铝、铁形成沉淀时易形成胶体,其能吸附较多的Cd2,故需要多次洗涤。
1 1
(6)由晶胞图可知S原子位于晶胞的顶点和面心,S原子个数为6 8 4,Cd原子位
2 8
于晶胞内部,Cd原子个数为4,设晶胞的边长为acm,则晶体密度
4144 576
gcm3 gcm3,解得a
3
,则图中a、b两原子的横间距离为
N a3 N
A A
2 2 576
a cm cm。
3
2 2 N
A
13.答案:(1)碳碳双键、酯基(2分)
(2)取代反应(2分)
(3) (2分)
(4) (其他合理答案也可)(3分)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(5) (4分)
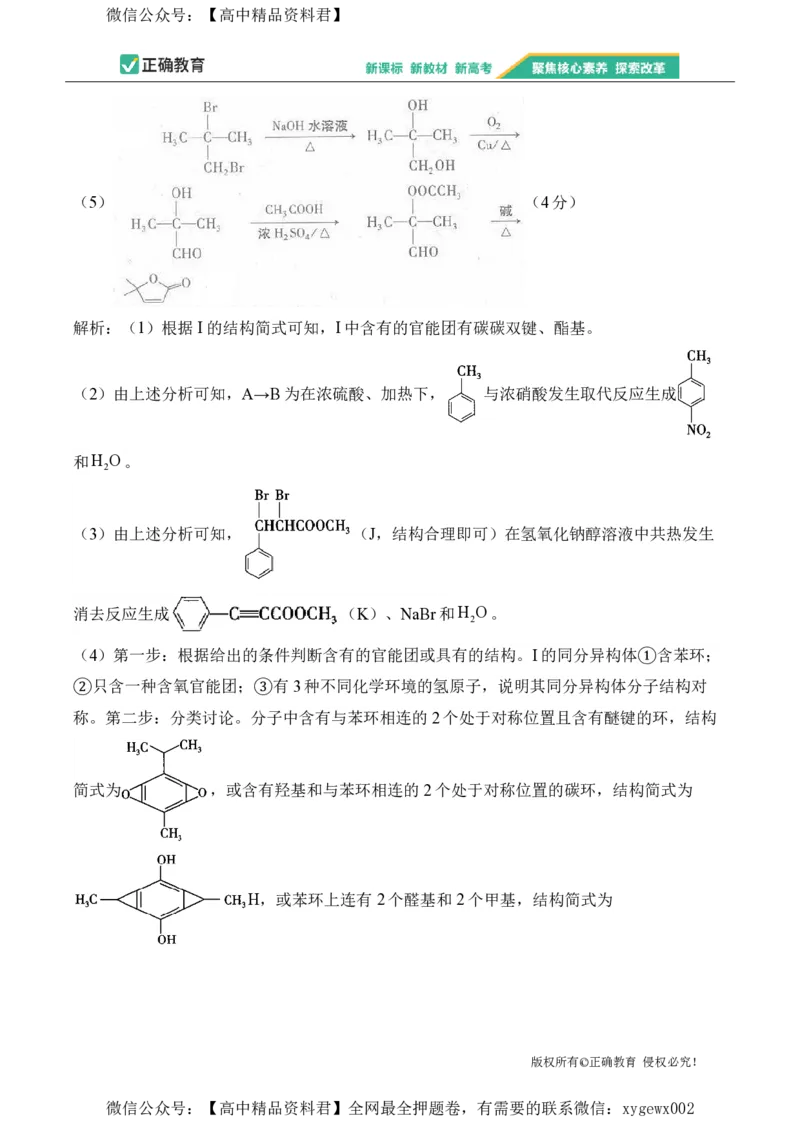
解析:(1)根据I的结构简式可知,I中含有的官能团有碳碳双键、酯基。
(2)由上述分析可知,A→B为在浓硫酸、加热下, 与浓硝酸发生取代反应生成
和H O。
2
(3)由上述分析可知, (J,结构合理即可)在氢氧化钠醇溶液中共热发生
消去反应生成 (K)、NaBr和H O。
2
(4)第一步:根据给出的条件判断含有的官能团或具有的结构。I的同分异构体①含苯环;
②只含一种含氧官能团;③有3种不同化学环境的氢原子,说明其同分异构体分子结构对
称。第二步:分类讨论。分子中含有与苯环相连的2个处于对称位置且含有醚键的环,结构
简式为 ,或含有羟基和与苯环相连的2个处于对称位置的碳环,结构简式为
H,或苯环上连有2个醛基和 2个甲基,结构简式为
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
,等等。
(5)由题中信息及所学知识可知, 在氢氧化钠溶液中发生水解反应生成
,在铜的催化作用下, 与氧气发生催化氧化反应生成
,在浓硫酸作用下, 与乙酸共热发生酯化反应生成
,在碱性溶液中加热 发生类似已知信息①的反应生成
。
14.答案:(1)平衡气压,使浓盐酸顺利流下(2分);在装置B后增加盛装浓硫酸的洗气瓶
(其他合理答案均可)(2分)
(2)装置内充满黄绿色气体(2分)
(3)先滴加稍过量的浓氨水,充分反应后,再滴加H O 溶液并不断搅拌(2分);
2 2
催化剂
10NH 2CoCl 2NH ClH O 2CoNH Cl 2H O(3分)
3 2 4 2 2 △ 3 6 3 2
(4)95.54%(2分);由得失电子守恒可得关系式:
2CoNH Cl 2Co3 I 2Na S O ,25.00 mL待测液消耗0.050molL1Na S O 标准溶
3 6 3 2 2 2 3 2 2 3
液的平均体积为20.00 mL,则2.8 g粗产品的纯度为
250mL
0.050 molL1 20.00103 L 267.5 gmol1
25.00mL 100%95.54%。(4分)
2.8g
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
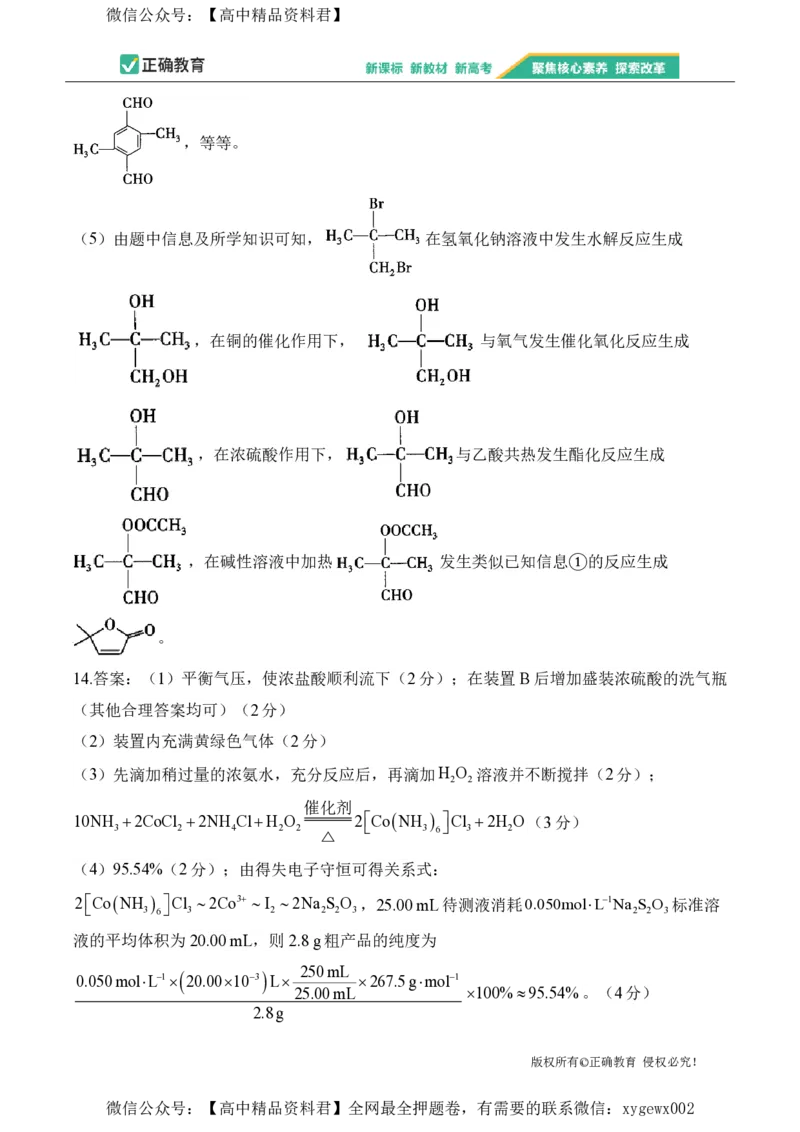
解析:(1)盛放浓盐酸的仪器为恒压滴液漏斗,可以起到平衡气压,使浓盐酸顺利流下的作
用。CoCl 易潮解,经过装置B的氯气会带有水蒸气,应在装置B后增加一个干燥装置,可
2
选用盛装浓硫酸的洗气瓶等。
(2)钴单质在300 ℃以上易被氧气氧化,故反应前应排尽装置内的空气。装置内充满黄绿色
气体时,说明氧气已被氯气排尽,此时可以加热钴粉。
(3)由题中信息结合题图乙可知,制备三氯化六氨合钴的反应是在活性炭作催化剂和60 ℃
水浴条件下,H O 与CoCl 、NH Cl、浓氨水反应生成CoNH Cl 和水,反应的化学方
2 2 2 4 3 6 3
催化剂
程式为10NH 2CoCl 2NH ClH O 2CoNH Cl 2H O。由已知②可得,
3 2 4 2 2 △ 3 6 3 2
Co2不易被氧化,CoNH 2 易被氧化,故应先加入浓氨水,使Co2转化为
3 6
CoNH 2 ,再加入氧化剂H O ;且该反应为放热反应,反应过程中会放出大量的热,
3 6 2 2
先滴加稍过量的浓氨水,充分反应后,再滴加H O 并不断搅拌,可防止H O 加入后,温度
2 2 2 2
迅速升高,氨气大量挥发,氯化铵和过氧化氢受热分解。
4cb2ad
15.答案:(1)① (2分);②增大压强或增大 CO的投料(2分);③增大
2
2
0.55 1.1
n n
3.45 3.45
(2分); (2分)
2 2
0.9 0.9
n n
3.45 3.45
(2)BC(2分)
(3)①催化剂对主反应的选择性大于对副反应的选择性或主反应的反应速率大于副反应的
反应速率(2分);②温度升高,催化剂逐渐失活或平衡后,温度升高,主反应逆向进行(2
分)
(4)CO 2e 2H HCOOH(2分)
2
解析:(1)①设NO中化学键的键能为xkJmol1,根据题给热化学方程式和表中数据可
4cb2ad
知,2a2x22cbd,解得x 。②升高温度、增大压强、增大反应物
2
的浓度或加入高效的催化剂可加快化学反应速率,该反应的正反应为气体分子数减小的放热
反应,若要提高NO的平衡转化率,可以增大压强、降低温度或者增大CO与NO的投料
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
比,综上可知增大压强或增大CO的投料既可以加快化学反应速率又可以提高 NO的平衡转
化率。③保持温度不变,t min时再向容器内加入1mol CO和1mol NO,相当于在1L恒容密
1
闭容器中充入2molCO和2molNO,压强增大,平衡正向移动,再次达到平衡时N 的体积分
2
数增大,再次达到平衡时总压为nkPa,设平衡时N 物质的量为 y mol,则可列三段式如
2
下:
2NO(g)2CO(g)N (g)2CO (g)
2 2
起始量/mol 2 2 0 0
变化量/mol 2y 2y y 2y
平衡量/mol 22y 22y y 2y
2 40
平衡时容器中气体总物质的量为(4 y)mol。由m:m : n40:69可得 ,解得
4 y 69
y=0.55,则平衡时,NO、CO、N 、CO 的物质的量分别为0.9mol、0.9mol、0.55 mol、
2 2
2
0.55 1.1
n n
3.45 3.45
1.1mol,n(总)3.45mol,则K 。
p 2 2
0.9 0.9
n n
3.45 3.45
(2)起始时SO (g)和NO(g)的浓度都为0,随着反应的进行,SO (g)和NO(g)的
3 3
浓度之比始终保持不变,所以SO (g)和NO(g)的浓度之比不变时,反应不一定达到平衡
3
状态,A项错误;混合气体的颜色保持不变,则表明NO 的浓度不变,反应达到平衡状态,
2
B项正确;反应前后气体的分子数相等,但在绝热情况下,温度变,压强就变,所以当压强
不变时,反应到达平衡状态,C项正确;恒容密闭容器中混合气体的质量不变、体积不变,
则密度始终不变,所以混合气体的密度不变时,反应不一定达到平衡状态,D项错误。
(4)由图可知,该电池放电时Zn作负极,失去电子,被氧化成Zn(OH)2,CO 在正极得到
4 2
电子,被还原成HCOOH,故放电时,正极的电极反应式为CO 2e 2H HCOOH。
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002