文档内容
★启用前注意保密
2025 届大湾区普通高中毕业年级联合模拟考试(一)
化 学
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分 100 分。考试时间75分钟。
注意事项:1.答卷前,考生务必将自己的学校、班级、姓名、考场号、座位号和准考证
号填写在答题卡上,将条形码横贴在答题卡“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用2B铅笔在答题卡上将对应题目选项
的答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案。答案
不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题
目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新
答案;不准使用铅笔和涂改液。不按以上要求作答无效。
4.考生必须保证答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32
第 I 卷(选择题,共 44 分)
一、选择题 (本小题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每
小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
1. 参观博物馆是我们学习传统文化的重要方式。下列文物主要由合金材料制成的是
文物
选项 A.青铜铸钱币 B.云龙纹瓷盘 C.青龙瓦当 D.石质日晷
2. 我国科技发展取得巨大成就。下列有关说法正确的是
A.“蛟龙号”发动机使用的氮化硅陶瓷属于分子晶体
B.珠海航展中歼-35所用的航空煤油可以通过石油蒸馏得到
C.深中通道建设所用的钢缆中含有的铁元素位于周期表p区
D.神舟十九号携带了二氧化碳处理器,CO 的电子式为
2
3. 元素交织,激情燃烧—化学智慧点亮运动赛场。以下说法不正确的是
A.赛场使用太阳能电池板发电,单质硅可用于太阳能电池板
B.奖牌采用合金材质制成,主要是利用合金硬度大、耐腐蚀的性能
C.残疾运动员佩戴的假肢可由碳纤维制成,碳纤维属于有机化合物
D.冠军服使用再生尼龙、涤纶等环保面料,该面料属于有机高分子材料
大湾区联考高三化学 第 1 页 共 8 页
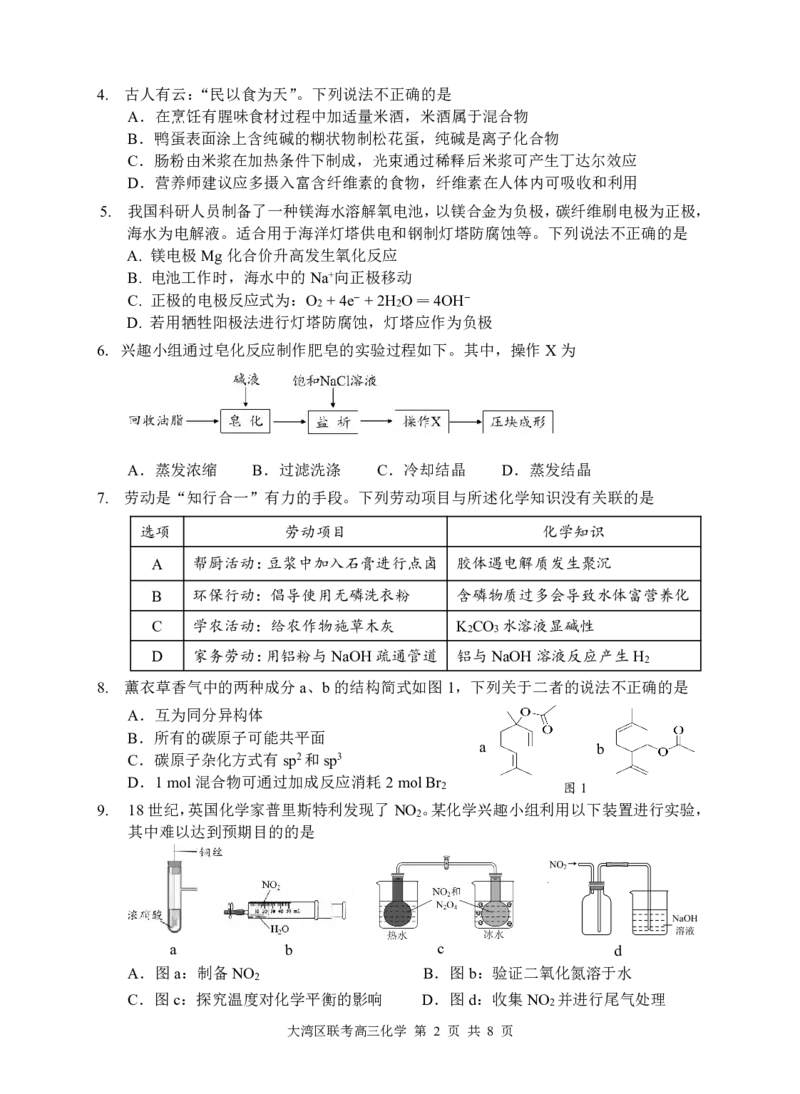
{#{QQABIYSEogCgQAIAARhCUwGgCAMQkgAAAQgGxBAEMAIAyRFABCA=}#}4. 古人有云:“民以食为天”。下列说法不正确的是
A.在烹饪有腥味食材过程中加适量米酒,米酒属于混合物
B.鸭蛋表面涂上含纯碱的糊状物制松花蛋,纯碱是离子化合物
C.肠粉由米浆在加热条件下制成,光束通过稀释后米浆可产生丁达尔效应
D.营养师建议应多摄入富含纤维素的食物,纤维素在人体内可吸收和利用
5. 我国科研人员制备了一种镁海水溶解氧电池,以镁合金为负极,碳纤维刷电极为正极,
海水为电解液。适合用于海洋灯塔供电和钢制灯塔防腐蚀等。下列说法不正确的是
A. 镁电极Mg化合价升高发生氧化反应
B. 电池工作时,海水中的Na+向正极移动
C. 正极的电极反应式为:O +4e-+2H O=4OH-
2 2
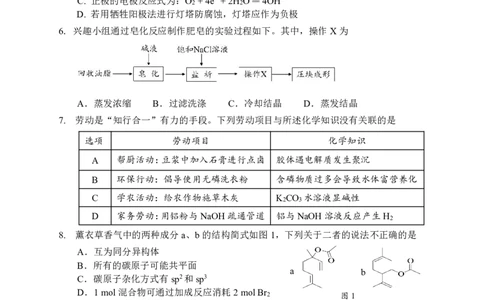
D. 若用牺牲阳极法进行灯塔防腐蚀,灯塔应作为负极
6. 兴趣小组通过皂化反应制作肥皂的实验过程如下。其中,操作X为
A.蒸发浓缩 B.过滤洗涤 C.冷却结晶 D.蒸发结晶
7. 劳动是“知行合一”有力的手段。下列劳动项目与所述化学知识没有关联的是
选项 劳动项目 化学知识
A 帮厨活动:豆浆中加入石膏进行点卤 胶体遇电解质发生聚沉
B 环保行动:倡导使用无磷洗衣粉 含磷物质过多会导致水体富营养化
C 学农活动:给农作物施草木灰 K CO 水溶液显碱性
2 3
D 家务劳动:用铝粉与NaOH疏通管道 铝与NaOH溶液反应产生H
2
8. 薰衣草香气中的两种成分a、b的结构简式如图1,下列关于二者的说法不正确的是
A.互为同分异构体
B.所有的碳原子可能共平面
a b
C.碳原子杂化方式有sp2和sp3
D.1mol混合物可通过加成反应消耗2molBr
2 图1
9. 18世纪,英国化学家普里斯特利发现了NO 。某化学兴趣小组利用以下装置进行实验,
2
其中难以达到预期目的的是
a b c d
A.图a:制备NO B.图b:验证二氧化氮溶于水
2
C.图c:探究温度对化学平衡的影响 D.图d:收集NO 并进行尾气处理
2
大湾区联考高三化学 第 2 页 共 8 页
{#{QQABIYSEogCgQAIAARhCUwGgCAMQkgAAAQgGxBAEMAIAyRFABCA=}#}10. 利用NaClO氧化除去氨的总反应方程式:2NH +3NaClO= N +3H O+3NaCl。设
3 2 2
N 为阿伏加德罗常数的值,下列说法正确的是
A
A.14gN 含有的孤电子对数为2N
2 A
B.1mol·L-1NaClO溶液中ClO-数目一定少于N
A
C.若反应断裂3molN-H键,则转移电子数为3N
A
D.标准状况下,2.24LH O中含有原子数为0.3N
2 A
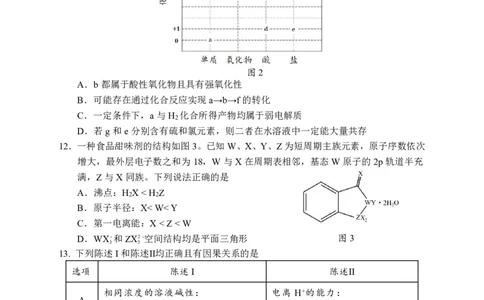
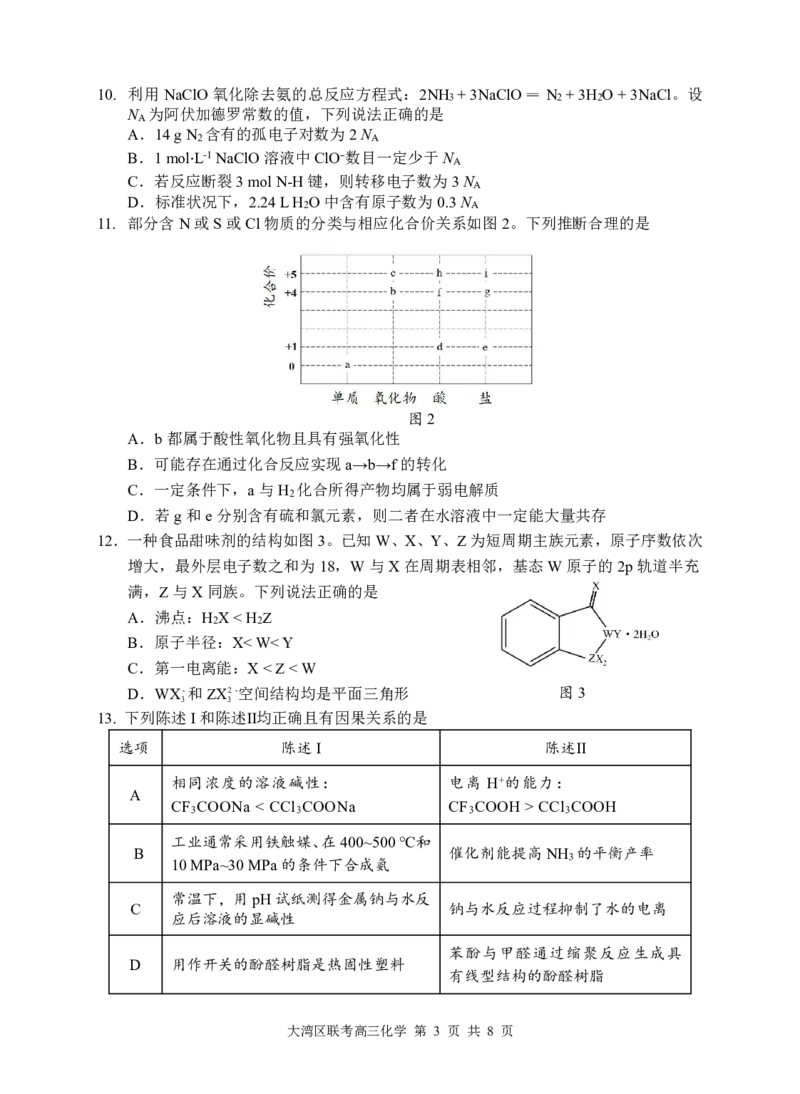
11. 部分含N或S或Cl物质的分类与相应化合价关系如图2。下列推断合理的是
图2
A.b都属于酸性氧化物且具有强氧化性
B.可能存在通过化合反应实现a→b→f的转化
C.一定条件下,a与H 化合所得产物均属于弱电解质
2
D.若g和e分别含有硫和氯元素,则二者在水溶液中一定能大量共存
12.一种食品甜味剂的结构如图3。已知W、X、Y、Z为短周期主族元素,原子序数依次
增大,最外层电子数之和为18,W与X在周期表相邻,基态W原子的2p轨道半充
满,Z与X同族。下列说法正确的是
A.沸点:H X CCl COOH
3 3 3 3
工业通常采用铁触媒、在400~500℃和
B 催化剂能提高NH 的平衡产率
3
10MPa~30MPa的条件下合成氨
常温下,用pH试纸测得金属钠与水反
C 钠与水反应过程抑制了水的电离
应后溶液的显碱性
苯酚与甲醛通过缩聚反应生成具
D 用作开关的酚醛树脂是热固性塑料
有线型结构的酚醛树脂
大湾区联考高三化学 第 3 页 共 8 页
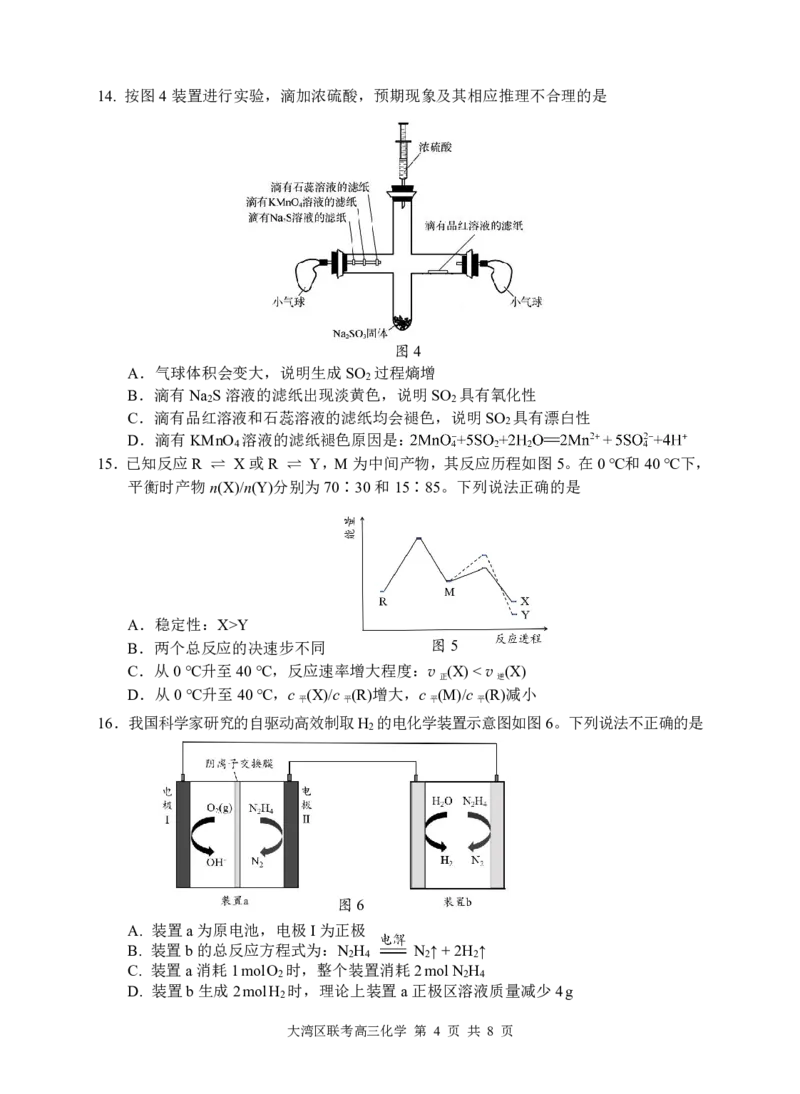
{#{QQABIYSEogCgQAIAARhCUwGgCAMQkgAAAQgGxBAEMAIAyRFABCA=}#}14. 按图4装置进行实验,滴加浓硫酸,预期现象及其相应推理不合理的是
图4
A.气球体积会变大,说明生成SO 过程熵增
2
B.滴有Na S溶液的滤纸出现淡黄色,说明SO 具有氧化性
2 2
C.滴有品红溶液和石蕊溶液的滤纸均会褪色,说明SO 具有漂白性
2
D.滴有KMnO 溶液的滤纸褪色原因是:
4
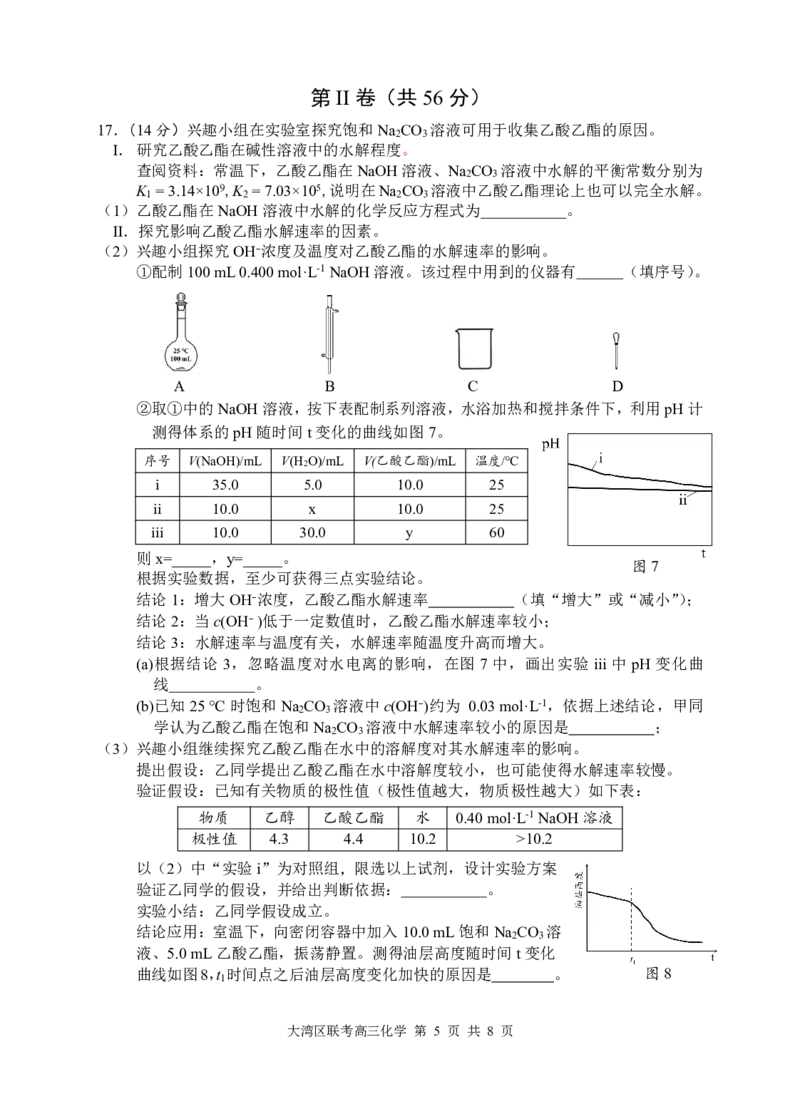
15.已知反应R ⇌ X或R ⇌ Y,M为中间产物,其反应历程如图5。在0℃和40℃下,
平衡时产物n(X)/n(Y)分别为70∶30和15∶85。下列说法正确的是
A.稳定性:X>Y
B.两个总反应的决速步不同 图5
C.从0℃升至40℃,反应速率增大程度:v (X)10.2
以(2)中“实验i”为对照组,限选以上试剂,设计实验方案
验证乙同学的假设,并给出判断依据: 。
实验小结:乙同学假设成立。
结论应用:室温下,向密闭容器中加入10.0mL饱和Na CO 溶
2 3
液、5.0mL乙酸乙酯,振荡静置。测得油层高度随时间t变化
曲线如图8,t 时间点之后油层高度变化加快的原因是 。 图8
1
大湾区联考高三化学 第 5 页 共 8 页
{#{QQABIYSEogCgQAIAARhCUwGgCAMQkgAAAQgGxBAEMAIAyRFABCA=}#}18. (14分)利用焙烧—半湿法从铜阳极泥(含有Cu、PbSO 、Ag Se、Cu Se、Au等)中
4 2 2
提取金、银等金属的过程如下:
已知:①“焙烧”后烧渣主要成分是CuSO 、PbSO 、Ag SO 、Au
4 4 2 4
②PbSO 在足量盐酸中发生反应:PbSO +Cl- PbCl++SO2-
4 4 4
③[Ag(S O ) ]3- Ag++2S O2-
2 3 2 2 3 ⇌
回答下列问题:
⇌
(1)基态铜原子的价层电子排布式为 。
(2)“烟气”的主要成分是 SeO 和 SO ,用水吸收生成单质Se和 (填化学式)。
2 2
(3)“水浸”步骤需加入NaCl固体但不能过量的原因是 。
(4)“分银”步骤中发生反应:AgCl(s)+2S O2-(aq) [Ag(S O ) ]3-(aq)+Cl-(aq) 该反应
2 3 2 3 2
的平衡常数K=5.04×103,若反应达平衡后溶液中c(Cl-)=0.1mol·L-1,则
⇌
c2(S O2-) c([Ag(S O ) ]3-) (填“>”“<”或“=”)。
2 3 2 3 2
(5)通过电解“分银液”,在阴极得到银单质,阴极电极反应式为 ,电解后
阴极区溶液中 (填化学式)可以循环使用。
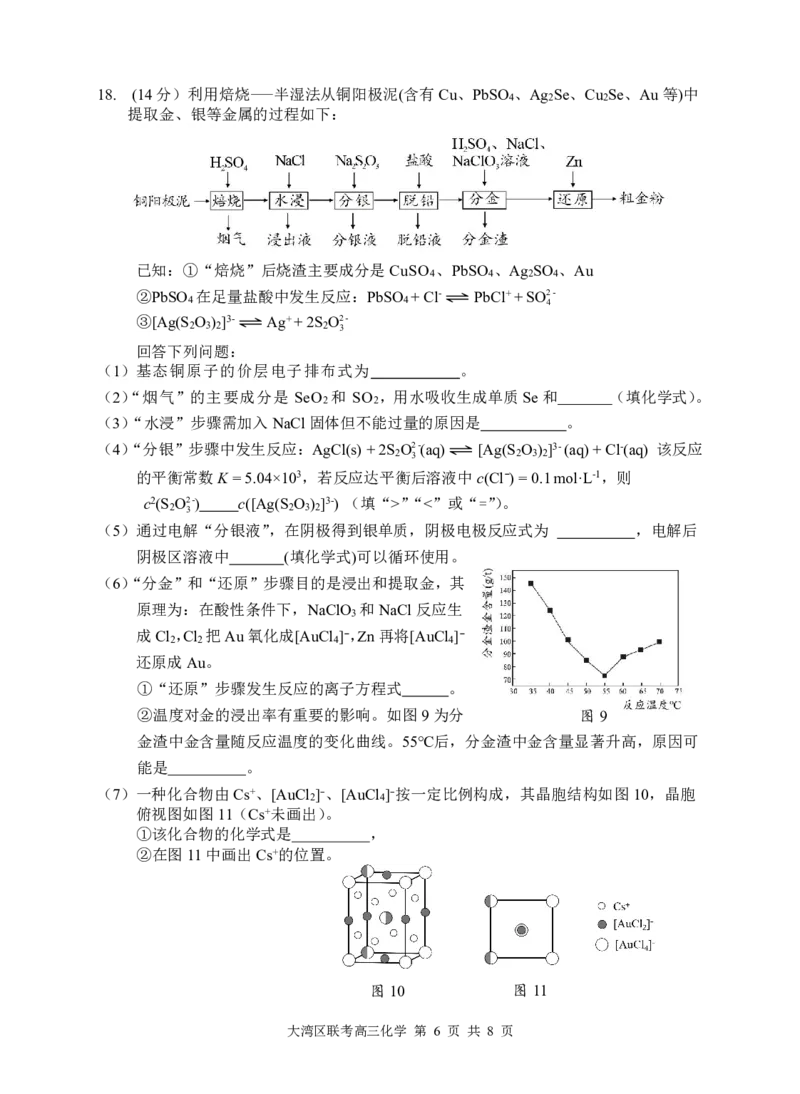
(6)“分金”和“还原”步骤目的是浸出和提取金,其
原理为:在酸性条件下,NaClO 和NaCl反应生
3
成Cl ,Cl 把Au氧化成[AuCl ]-,Zn再将[AuCl ]-
2 2 4 4
还原成Au。
①“还原”步骤发生反应的离子方程式 。
②温度对金的浸出率有重要的影响。如图9为分 图9
金渣中金含量随反应温度的变化曲线。55℃后,分金渣中金含量显著升高,原因可
能是 。
(7)一种化合物由Cs+、[AuCl ]-、[AuCl ]-按一定比例构成,其晶胞结构如图10,晶胞
2 4
俯视图如图11(Cs+未画出)。
①该化合物的化学式是 ,
②在图11中画出Cs+的位置。
图10 图11
大湾区联考高三化学 第 6 页 共 8 页
{#{QQABIYSEogCgQAIAARhCUwGgCAMQkgAAAQgGxBAEMAIAyRFABCA=}#}19. (14分)CO 的捕集、利用与封存技术是实现碳达峰、碳中和的热点研究方向。乙醇
2
胺(化学式为HOCH CH NH ,以下简写为RNH )在工业上可用作CO 吸收剂。
2 2 2 2 2
Ⅰ. CO 的吸收:用RNH 吸收CO 发生反应a:2RNH +CO ⇌ RNHCOO- + X 。
2 2 2 2 2
(1)乙醇胺分子中电负性最强的元素是_______(填元素符号)。
(2)X的化学式是____________。
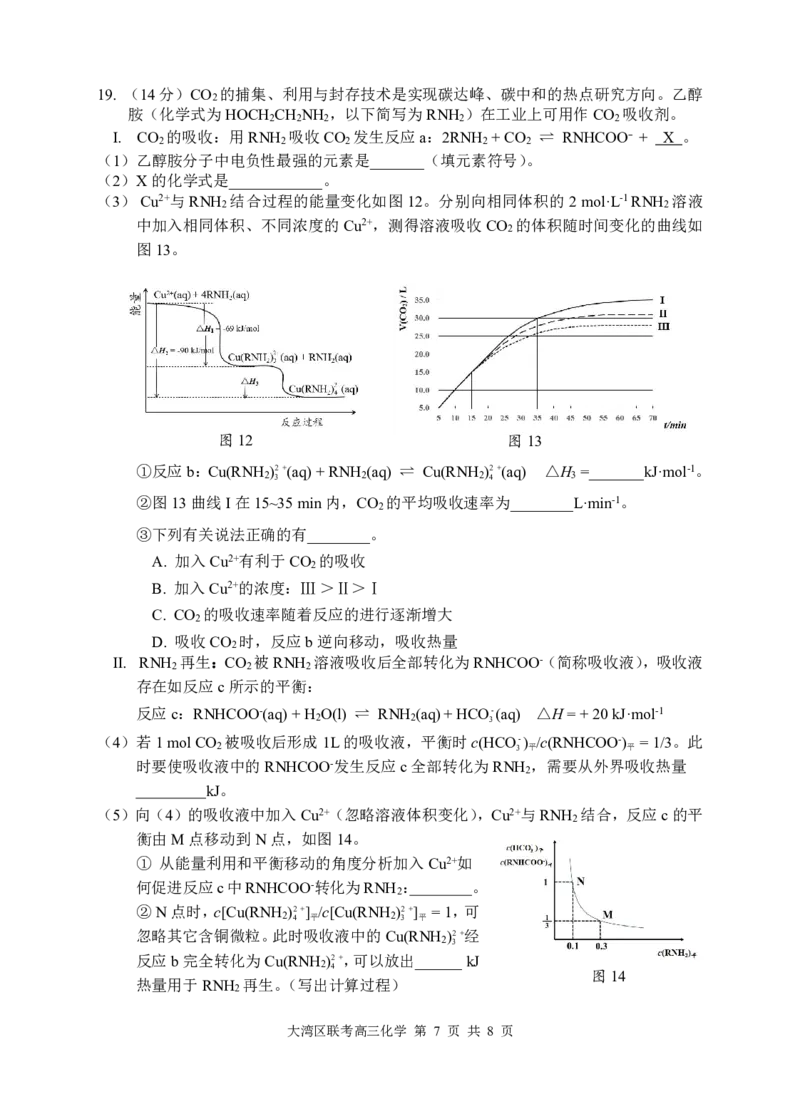
(3)Cu2+与RNH 结合过程的能量变化如图12。分别向相同体积的2mol·L-1RNH 溶液
2 2
中加入相同体积、不同浓度的Cu2+,测得溶液吸收CO 的体积随时间变化的曲线如
2
图13。
图12 图13
①反应b:Cu(RNH )2+(aq)+RNH (aq) ⇌ Cu(RNH )2+(aq) △H =_______kJ·mol-1。
2 3 2 2 4 3
②图13曲线Ⅰ在15~35min内,CO 的平均吸收速率为________L·min-1。
2
③下列有关说法正确的有________。
A. 加入Cu2+有利于CO 的吸收
2
B. 加入Cu2+的浓度:Ⅲ>Ⅱ>Ⅰ
C. CO 的吸收速率随着反应的进行逐渐增大
2
D. 吸收CO 时,反应b逆向移动,吸收热量
2
Ⅱ. RNH 再生:CO 被RNH 溶液吸收后全部转化为RNHCOO-(简称吸收液),吸收液
2 2 2
存在如反应c所示的平衡:
反应c:RNHCOO-(aq)+H O(l) ⇌ RNH (aq)+HCO-(aq) △H=+20kJ·mol-1
2 2 3
(4)若1molCO 被吸收后形成1L的吸收液,平衡时c(HCO-) /c(RNHCOO-) =1/3。此
2 3 平 平
时要使吸收液中的RNHCOO-发生反应c全部转化为RNH ,需要从外界吸收热量
2
kJ。
(5)向(4)的吸收液中加入Cu2+(忽略溶液体积变化),Cu2+与RNH 结合,反应c的平
2
衡由M点移动到N点,如图14。
① 从能量利用和平衡移动的角度分析加入Cu2+如
何促进反应c中RNHCOO-转化为RNH : 。
2
②N点时,c[Cu(RNH )2+] /c[Cu(RNH )2+] =1,可
2 4 平 2 3 平
忽略其它含铜微粒。此时吸收液中的Cu(RNH )2+经
2 3
反应b完全转化为Cu(RNH )2+,可以放出______kJ
2 4
图14
热量用于RNH 再生。(写出计算过程)
2
大湾区联考高三化学 第 7 页 共 8 页
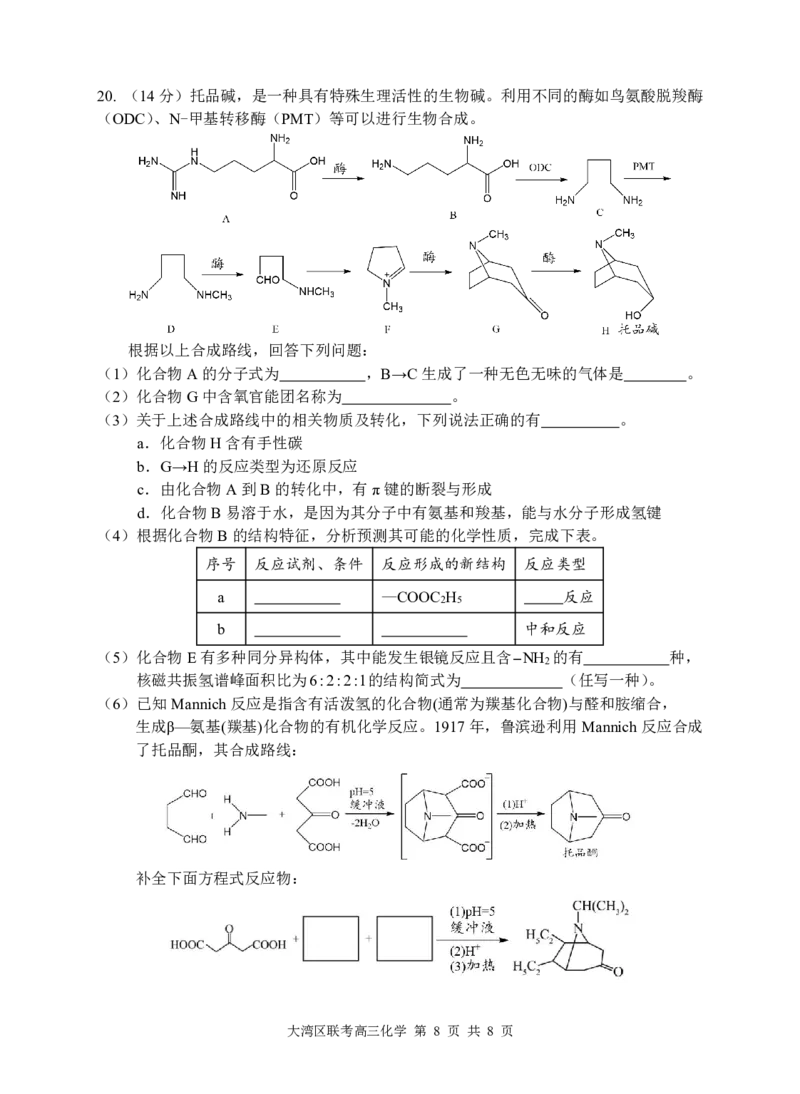
{#{QQABIYSEogCgQAIAARhCUwGgCAMQkgAAAQgGxBAEMAIAyRFABCA=}#}20. (14分)托品碱,是一种具有特殊生理活性的生物碱。利用不同的酶如鸟氨酸脱羧酶
(ODC)、N-甲基转移酶(PMT)等可以进行生物合成。
根据以上合成路线,回答下列问题:
(1)化合物A的分子式为 ,B→C生成了一种无色无味的气体是 。
(2)化合物G中含氧官能团名称为 。
(3)关于上述合成路线中的相关物质及转化,下列说法正确的有 。
a.化合物H含有手性碳
b.G→H的反应类型为还原反应
c.由化合物A到B的转化中,有π键的断裂与形成
d.化合物B易溶于水,是因为其分子中有氨基和羧基,能与水分子形成氢键
(4)根据化合物B的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a —COOC H 反应
2 5
b 中和反应
(5)化合物E有多种同分异构体,其中能发生银镜反应且含-NH 的有 种,
2
核磁共振氢谱峰面积比为6:2:2:1的结构简式为 (任写一种)。
(6)已知Mannich反应是指含有活泼氢的化合物(通常为羰基化合物)与醛和胺缩合,
生成β—氨基(羰基)化合物的有机化学反应。1917年,鲁滨逊利用Mannich反应合成
了托品酮,其合成路线:
补全下面方程式反应物:
大湾区联考高三化学 第 8 页 共 8 页
{#{QQABIYSEogCgQAIAARhCUwGgCAMQkgAAAQgGxBAEMAIAyRFABCA=}#}