文档内容
2025—2026 学年度上期高 2026 届入学考试
化学试卷
考试时间:75分钟 满分:100分
相对原子质量:H-1 Li-7 C-12 N-14 O-16 F- 19 S-32 Ni-59 Co-59 Cl-35.5
一、 选择题(本题包含15个小题,每题只有一个选项符合题意,每小题3分,共45分)
1. 材料是人类赖以生存和发展的物质基础,下列说法正确的是
A.岩彩壁画颜料所用贝壳粉,主要成分属于硅酸盐
B.油画颜料调和剂所用核桃油,属于有机高分子
C.竹胎漆画颜料赭石的主要成分氧化铁,耐酸、碱
D.尼龙66由己二酸和己二胺缩聚合成,强度高、韧性好
2.下列化学用语或图示表达正确的是
A. H S分子的球棍模型: B. AlCl 的价层电子对互斥模型:
2 3
··
C. KI的电子式:K·I· D. CH CH(CH CH ) 的名称:3-甲基戊烷
· · 3 2 3 2
··
3. 共价化合物Al Cl 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
2 6
Al Cl +2NH =2Al(NH )Cl ,下列说法正确的是
2 6 3 3 3
A. 17g
1
N H
3
的体积是22.4L
B.0.1 mol/L的氨水溶液中 N H +4 分子数小于0.1 N
A
C.1mol Al(NH )Cl 中含有的孤电子对数目为9
3 3
N
A
D. Al Br 比Al Cl 更难与NH 发生反应
2 6 2 6 3
4. W、X、Y、Z为四种短周期非金属元素,W原子中电子排布已充满的能级数与最高能级
中的电子数相等,X与W同族,Y与X相邻且Y原子比X原子多一个未成对电子,Z位
于W的对角线位置。下列说法错误的是
A.第二电离能:X<Y B.原子半径:Z<W
C.单质沸点:Y<Z D.电负性:W<X
5. 下列有关电极方程式或离子方程式错误的是
A.丙烯腈电解制己二腈,阴极电极反应式为:2CH =CHCN+2H++2e− =NC(CH ) CN
2 2 4
B. 向甲醛溶液中加入足量的银氨溶液并加热:
HCHO+4Ag(NH ) + +4OH− ⎯ ⎯→CO2−+2NH++ 4Ag+6NH +2H O
3 2 3 4 3 2
C.K CrO 酸性溶液测酒:3CH CH OH+2CrO2−+16H+ ⎯⎯→3CH COOH+4Cr3++11H O
2 2 7 3 2 2 7 3 2
D.往酸性MnSO 溶液中加入难溶于水的NaBiO 固体,溶液出现紫红色:
4 3
5BiO−+2Mn2++14H+ =5Bi3++2MnO−+7H O
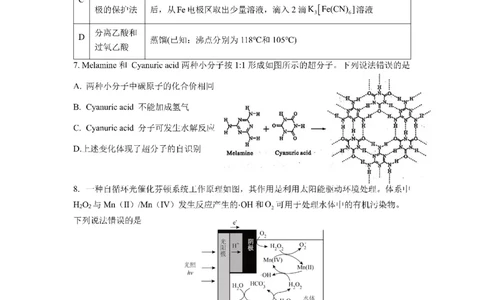
3 4 29. 在葡萄糖水溶液中,各种结构的平衡转化关系及百分含量如图。下列说法错误的是
A.ΔH +ΔH =ΔH +ΔH B.b转化为c是加成反应
1 2 3 4
C. a与b互为同分异构体 D.a分子有5个手性碳
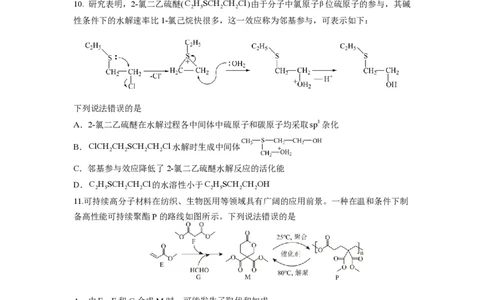
10. 研究表明,2-氯二乙硫醚(
3
C
2
H
5
S C H
2
C H
2
C l )由于分子中氯原子β位硫原子的参与,其碱
性条件下的水解速率比1-氯己烷快很多,这一效应称为邻基参与,可表示如下:
下列说法错误的是
A.2-氯二乙硫醚在水解过程各中间体中硫原子和碳原子均采取 s p 3 杂化
B.ClCH CH SCH CH Cl水解时生成中间体
2 2 2 2
C.邻基参与效应降低了2-氯二乙硫醚水解反应的活化能
D.C H SCH CH Cl的水溶性小于C H SCH CH OH
2 5 2 2 2 5 2 2
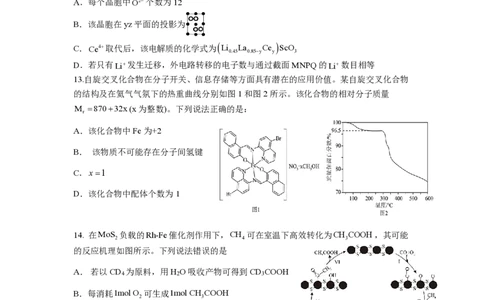
11.可持续高分子材料在纺织、生物医用等领域具有广阔的应用前景。一种在温和条件下制
备高性能可持续聚酯P的路线如图所示。下列说法错误的是
A.由 E 、 F 和G合成M时,可能发生了取代和加成
B.P在碱性条件下能够发生水解反应而降解
C.由E、F和G合成M时,有HCOOH生成
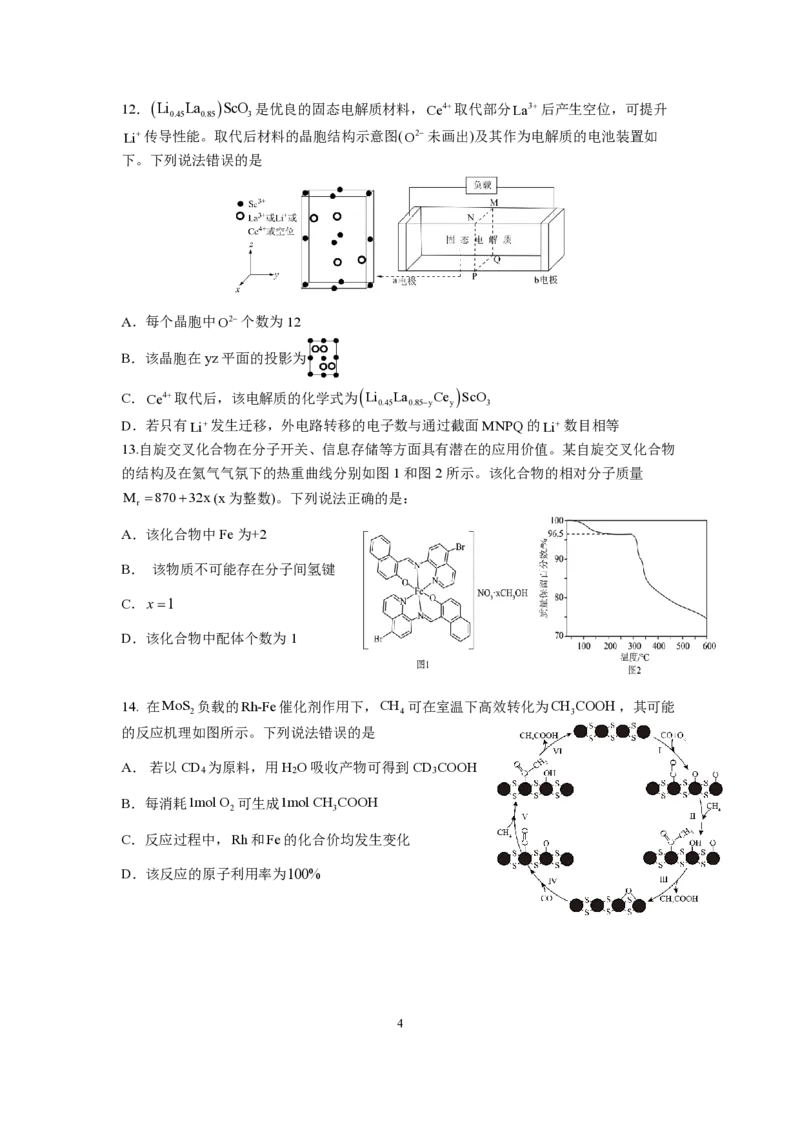
D.P解聚生成M的过程中,存在C−O键的断裂与形成12.(Li La )ScO 是优良的固态电解质材料,
0.45 0.85 3
4
C e 4 + 取代部分 L a 3 + 后产生空位,可提升
Li+传导性能。取代后材料的晶胞结构示意图( O 2 − 未画出)及其作为电解质的电池装置如
下。下列说法错误的是
A.每个晶胞中 O 2 − 个数为12
B.该晶胞在yz平面的投影为
( )
C.Ce4+取代后,该电解质的化学式为 Li La Ce ScO
0.45 0.85−y y 3
D.若只有 L i + 发生迁移,外电路转移的电子数与通过截面MNPQ的 L i + 数目相等
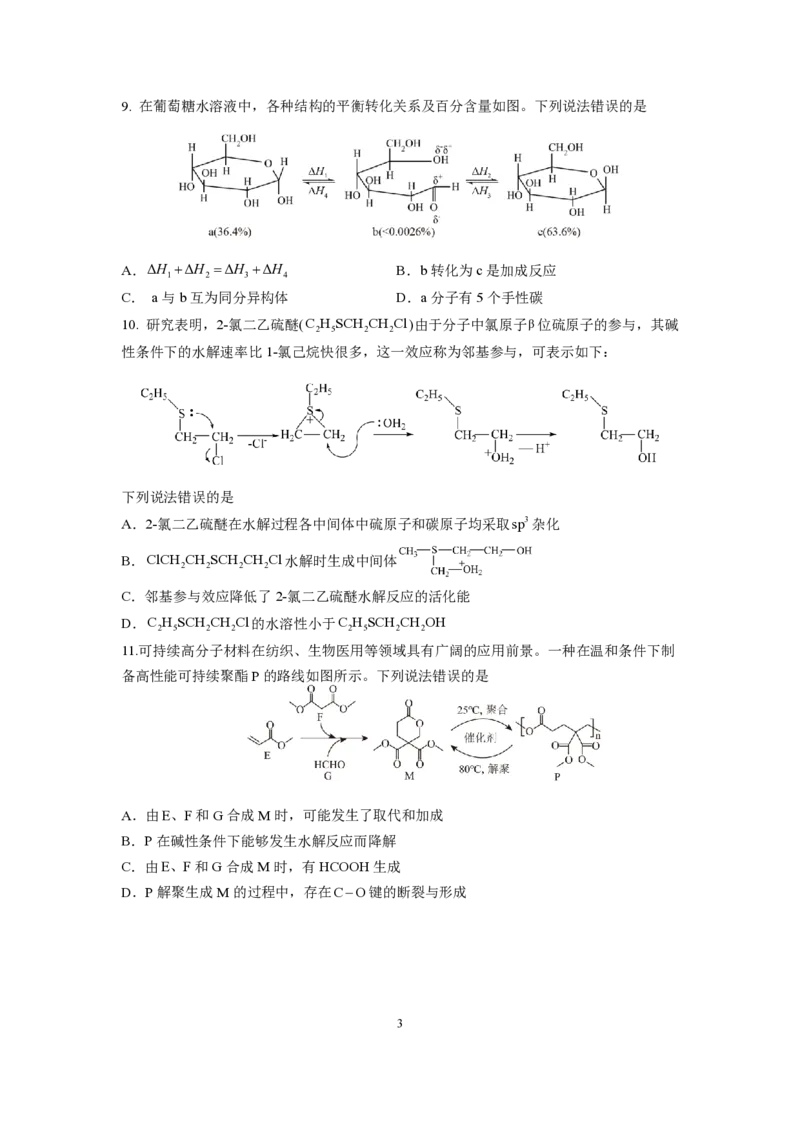
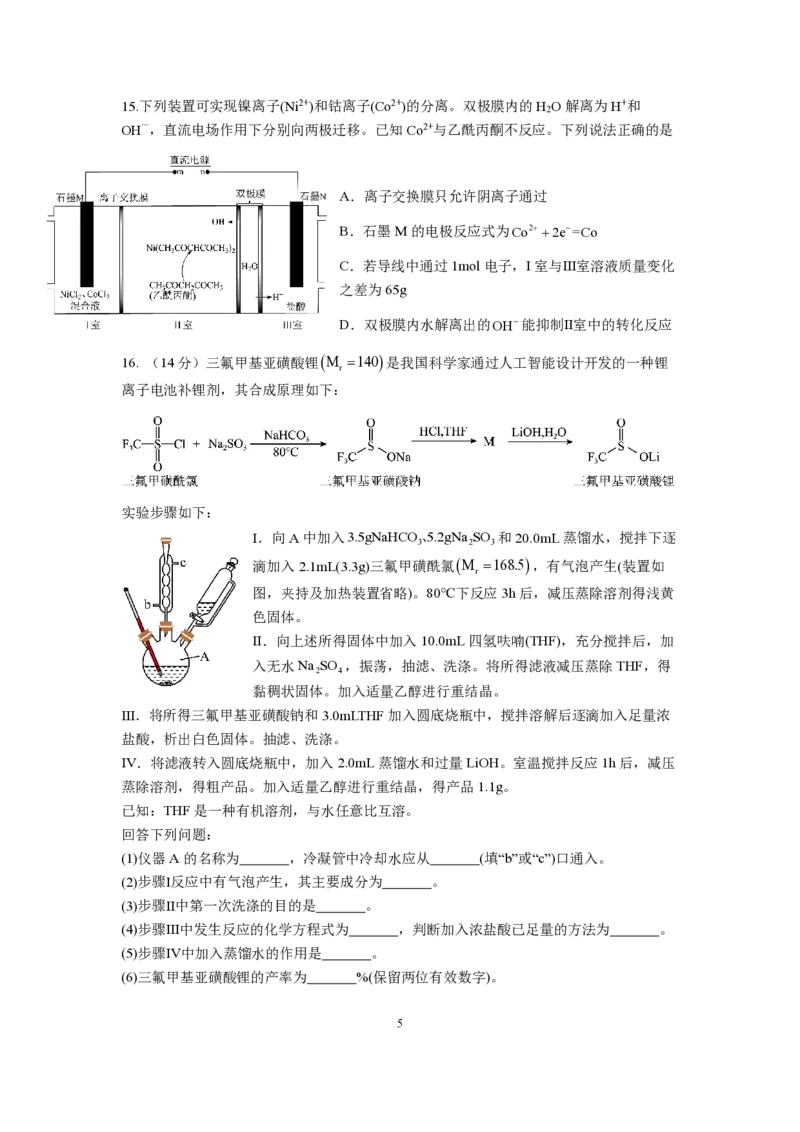
13.自旋交叉化合物在分子开关、信息存储等方面具有潜在的应用价值。某自旋交叉化合物
的结构及在氦气气氛下的热重曲线分别如图1和图2所示。该化合物的相对分子质量
M =870+32x(x为整数)。下列说法正确的是:
r
A.该化合物中Fe为+2
B. 该物质不可能存在分子间氢键
C.x=1
D.该化合物中配体个数为1
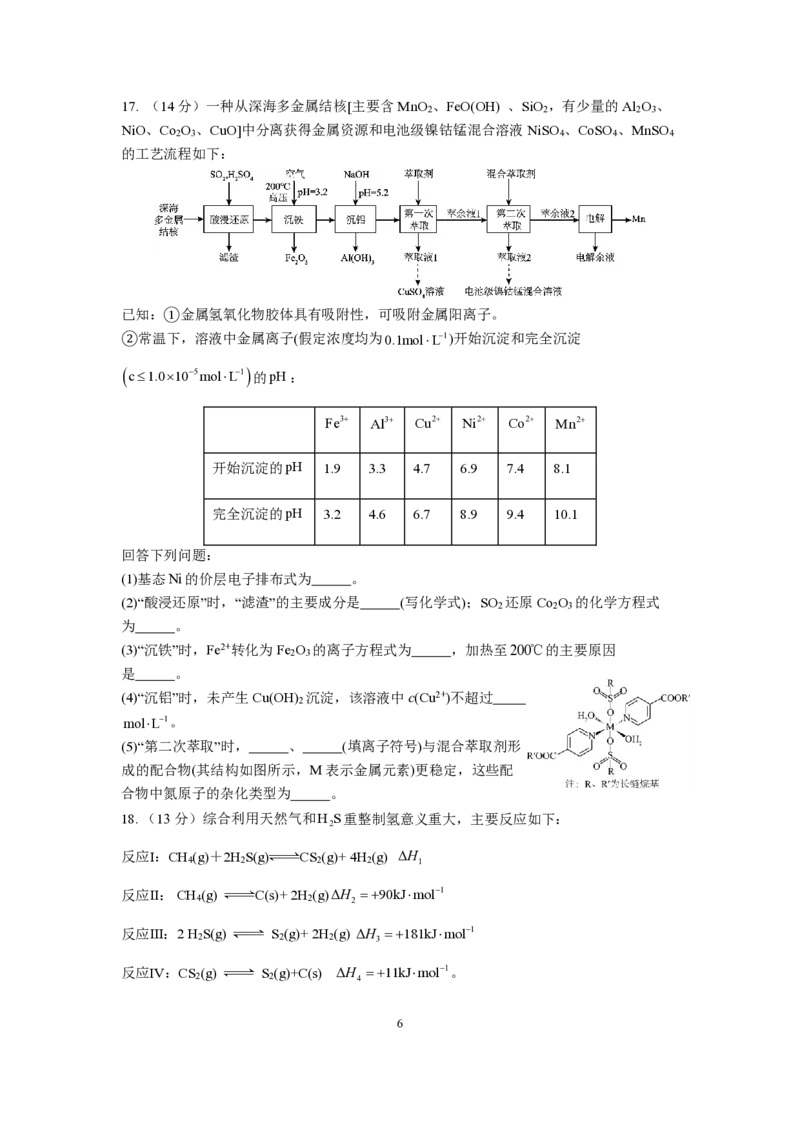
14. 在MoS 负载的
2
R h - F e 催化剂作用下,CH 可在室温下高效转化为CH COOH,其可能
4 3
的反应机理如图所示。下列说法错误的是
A. 若以CD 为原料,用H O吸收产物可得到CD COOH
4 2 3
B.每消耗 1 m o l O
2
可生成1mol CH COOH
3
C.反应过程中,Rh和Fe的化合价均发生变化
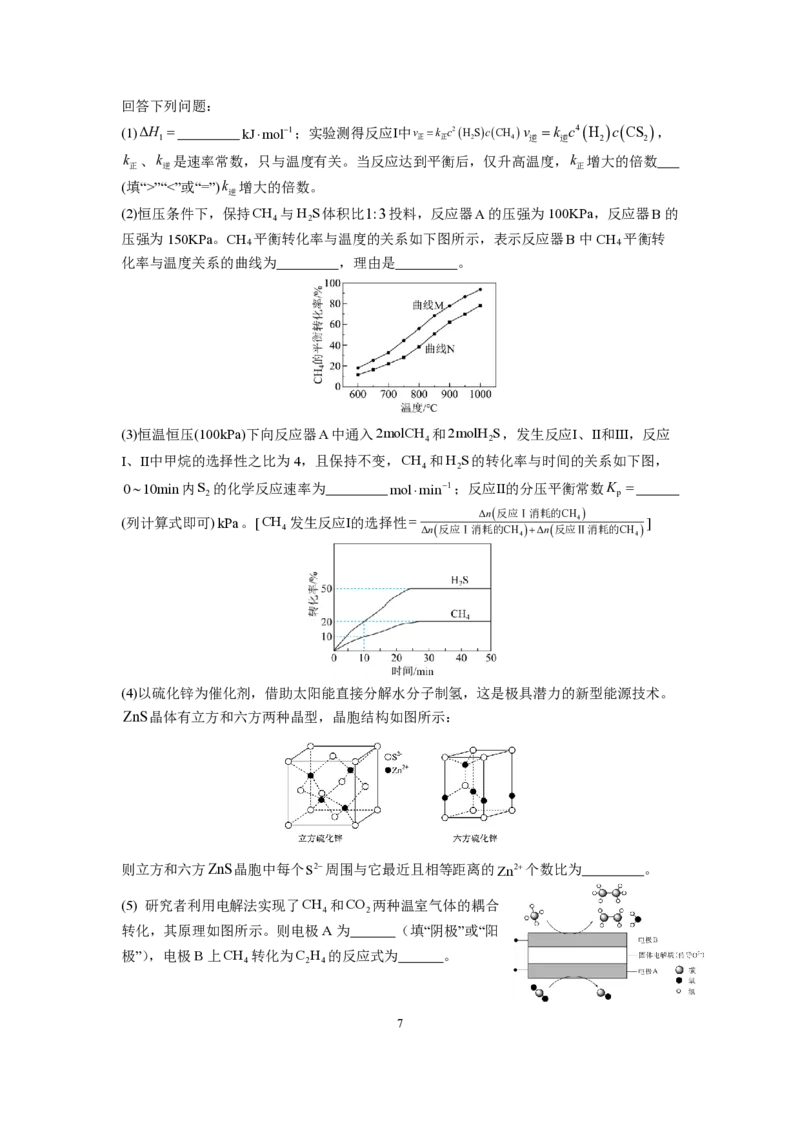
D.该反应的原子利用率为100%15.下列装置可实现镍离子(Ni2+)和钴离子(Co2+)的分离。双极膜内的H O解离为H+和
2
OH—,直流电场作用下分别向两极迁移。已知Co2+与乙酰丙酮不反应。下列说法正确的是
A.离子交换膜只允许阴离子通过
B.石墨M的电极反应式为
5
C o 2 + + 2 e − = C o
C.若导线中通过1mol电子,I室与Ⅲ室溶液质量变化
之差为65g
D.双极膜内水解离出的 O H − 能抑制Ⅱ室中的转化反应
16. (14分)三氟甲基亚磺酸锂 ( M
r
= 1 4 0 ) 是我国科学家通过人工智能设计开发的一种锂
离子电池补锂剂,其合成原理如下:
实验步骤如下:
Ⅰ.向A中加入3.5gNaHCO、5.2gNa SO 和20.0mL蒸馏水,搅拌下逐
3 2 3
滴加入2.1mL(3.3g)三氟甲磺酰氯(M =168.5),有气泡产生(装置如
r
图,夹持及加热装置省略)。80℃下反应3h后,减压蒸除溶剂得浅黄
色固体。
Ⅱ.向上述所得固体中加入10.0mL四氢呋喃(THF),充分搅拌后,加
入无水 N a
2
S O
4
,振荡,抽滤、洗涤。将所得滤液减压蒸除THF,得
黏稠状固体。加入适量乙醇进行重结晶。
Ⅲ.将所得三氟甲基亚磺酸钠和3.0mLTHF加入圆底烧瓶中,搅拌溶解后逐滴加入足量浓
盐酸,析出白色固体。抽滤、洗涤。
Ⅳ.将滤液转入圆底烧瓶中,加入2.0mL蒸馏水和过量LiOH。室温搅拌反应1h后,减压
蒸除溶剂,得粗产品。加入适量乙醇进行重结晶,得产品1.1g。
已知:THF是一种有机溶剂,与水任意比互溶。
回答下列问题:
(1)仪器A的名称为 ,冷凝管中冷却水应从 (填“b”或“c”)口通入。
(2)步骤Ⅰ反应中有气泡产生,其主要成分为 。
(3)步骤Ⅱ中第一次洗涤的目的是 。
(4)步骤Ⅲ中发生反应的化学方程式为 ,判断加入浓盐酸已足量的方法为 。
(5)步骤Ⅳ中加入蒸馏水的作用是 。
(6)三氟甲基亚磺酸锂的产率为 %(保留两位有效数字)。17. (14分)一种从深海多金属结核[主要含MnO 、FeO(OH) 、SiO ,有少量的Al O 、
2 2 2 3
NiO、Co O 、CuO]中分离获得金属资源和电池级镍钴锰混合溶液NiSO 、CoSO 、MnSO
2 3 4 4 4
的工艺流程如下:
已知:①金属氢氧化物胶体具有吸附性,可吸附金属阳离子。
②常温下,溶液中金属离子(假定浓度均为
6
0 .1 m o l L − 1 )开始沉淀和完全沉淀
( c1.010−5molL−1)
的 p H :
F e 3 + A l 3 + C u 2 + N i 2 + C o 2 + Mn2+
开始沉淀的 p H 1.9 3.3 4.7 6.9 7.4 8.1
完全沉淀的 p H 3.2 4.6 6.7 8.9 9.4 10.1
回答下列问题:
(1)基态 N i 的价层电子排布式为 。
(2)“酸浸还原”时,“滤渣”的主要成分是 (写化学式);SO 还原Co O 的化学方程式
2 2 3
为 。
(3)“沉铁”时,Fe2+转化为Fe O 的离子方程式为 ,加热至
2 3
2 0 0 ℃ 的主要原因
是 。
(4)“沉铝”时,未产生Cu(OH) 沉淀,该溶液中c(Cu2+)不超过
2
molL−1。
(5)“第二次萃取”时, 、 (填离子符号)与混合萃取剂形
成的配合物(其结构如图所示,M表示金属元素)更稳定,这些配
合物中氮原子的杂化类型为 。
18. (13 分)综合利用天然气和H S重整制氢意义重大,主要反应如下:
2
反应Ⅰ:CH (g)+2H S(g) CS (g)+ 4H (g)
4 2 2 2
Δ H
1
反应Ⅱ: CH (g) C(s)+ 2H (g)ΔH =+90kJmol−1
4 2 2
反应Ⅲ:2 H S(g) S (g)+ 2H (g) ΔH =+181kJmol−1
2 2 2 3
反应Ⅳ:CS (g) S (g)+C(s) ΔH =+11kJmol−1。
2 2 4回答下列问题:
(1)ΔH =
1
7
k J m o l − 1 ;实验测得反应Ⅰ中v =k c2(HS)c(CH )
正 正 2 4
v
逆
= k
逆
c 4 H
2
c C S
2
( ) ( ),
k 、
正
k
逆
是速率常数,只与温度有关。当反应达到平衡后,仅升高温度, k
正
增大的倍数
(填“>”“<”或“=”) k
逆
增大的倍数。
(2)恒压条件下,保持CH 与H S体积比
4 2
1 : 3 投料,反应器 A 的压强为100KPa,反应器 B 的
压强为150KPa。CH 平衡转化率与温度的关系如下图所示,表示反应器
4
B 中CH 平衡转
4
化率与温度关系的曲线为 ,理由是 。
(3)恒温恒压(100kPa)下向反应器A中通入 2 m o lC H
4
和 2 m o lH
2
S ,发生反应Ⅰ、Ⅱ和Ⅲ,反应
Ⅰ、Ⅱ中甲烷的选择性之比为4,且保持不变, C H
4
和 H
2
S 的转化率与时间的关系如下图,
0 1 0 m in 内 S
2
的化学反应速率为 m o l m in − 1 ;反应Ⅱ的分压平衡常数 K
p
=
(列计算式即可) k P a 。[ C H
4
Δn(反应Ⅰ消耗的CH )
发生反应Ⅰ的选择性= 4 ]
Δn(反应Ⅰ消耗的CH )+Δn(反应Ⅱ消耗的CH )
4 4
(4)以硫化锌为催化剂,借助太阳能直接分解水分子制氢,这是极具潜力的新型能源技术。
Z n S 晶体有立方和六方两种晶型,晶胞结构如图所示:
则立方和六方ZnS晶胞中每个 S 2 − 周围与它最近且相等距离的 Z n 2 + 个数比为 。
(5) 研究者利用电解法实现了CH 和
4
C O
2
两种温室气体的耦合
转化,其原理如图所示。则电极A为 (填“阴极”或“阳
极”),电极B上CH 转化为C H 的反应式为 。
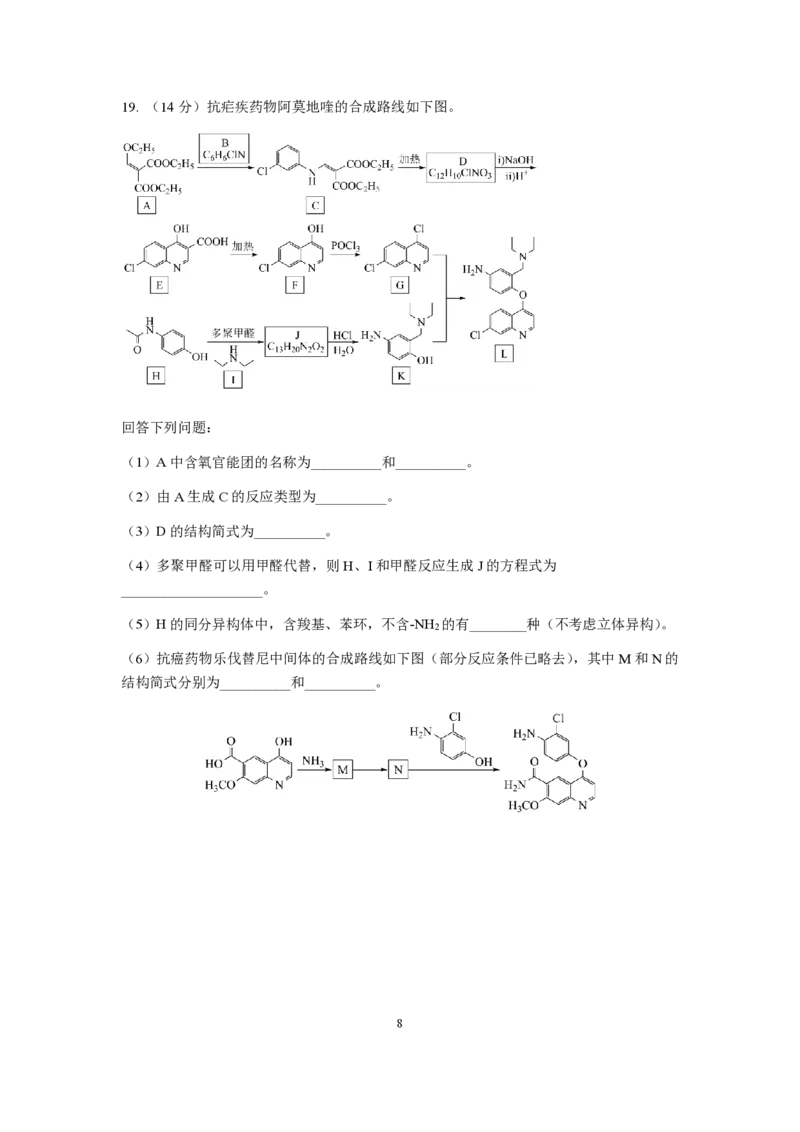
4 2 419. (14 分)抗疟疾药物阿莫地喹的合成路线如下图。
回答下列问题:
(1)A中含氧官能团的名称为__________和__________。
(2)由A生成C的反应类型为__________。
(3)D的结构简式为__________。
(4)多聚甲醛可以用甲醛代替,则H、I和甲醛反应生成J的方程式为
____________________。
(5)H的同分异构体中,含羧基、苯环,不含-NH 的有________种(不考虑立体异构)。
2
(6)抗癌药物乐伐替尼中间体的合成路线如下图(部分反应条件已略去),其中M和N的
结构简式分别为__________和__________。
8