文档内容
绝密★启用前
邯郸市 届高三年级第二次调研监测
2025
化学试卷
班级 姓名
注意事项:
1 .答卷前,考生先将自己的姓名、班级、考场/座位号填写在答题卡上。
2 .回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本
试卷上无效。
3 .考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 0 16
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
L “挖掘文物价值,讲好中国故事”。下刻疽关文物的叙述错误的是
清•绛丝朝袍 唐•红陶生肖俑 北齐•汉白玉佛像 西汉•铜朱雀衔环杯
A.舞丝的主要材质为蛋白质
B.陶俑以黏土为主要原料,经高温烧结而成
C.汉白玉佛像耐酸雨腐蚀
D.为减缓铜朱雀衔环杯腐蚀,可将其置于铁质托盘上
2.实验安全至关重要。下列表述错误的是
A.误食可溶性领盐,可服用碳酸钠溶液解毒
B.用小刀切割金属钠时,要放在玻璃片上操作
C.进行苯的硝化实验时,需戴手套和护目镜
D.眼睛溅进酸液,立即用大量水冲洗
3.高分子材料在人类生产生活中有着重要用途。下列说法错误的是
A,塑料和橡胶都是高分子,其中某些能导电
B.利用高分子分离膜进行海水淡化,比蒸储法耗能少
高三化学 第1页(共8页)C.以CH3—C=c-CH3为单体可制得高分子(ECHzCHndHCHz士)
D.酚醛树脂可由苯酚和甲箧在酸或碱的催化作用下通过缩聚反应合成
4. Co[C1(NH3)s]C12 为一种紫色的配合物,制备原理为 2coeI2+2NH4cI + 8NH3 + H2O2
===2Co[C1(NH3)5]C12+2H2O1,设Na为阿伏加德罗常数的值,下列叙述错误的是
A 1 mol Co[CKNH3)5了 + 中。键数目为 16NA
B.标准状况下,2. 24 L 15NH3中质子数为Na
C. 34 g H2O2完全分解为02,转移电子数为Na
D.向1 L 1 mol・L_1的NH4cl溶液中加氨水至中性,此时溶液中NHj数目为Na
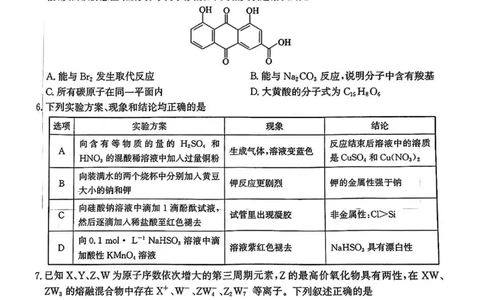
5.大黄酸(结构如下)通过干扰巨噬细胞的积累和极化来调节氧化还原介导的NLRP3炎性体激
活,从而预防急性结肠炎。关于大黄酸,下列相关表述错误的是
A.能与Bq发生取代反应 B.能与Na2CO3反应,说明分子中含有较基
〔ex所有碳原子在同一平面内 D.大黄酸的分子式为C15H8Os
6;下列实验方案、现象和结论均正确的是
选项 实验方案 现象 结论
向含有等物质的量的H2SO4和 反应结束后溶液中的溶质
A 生成气体,溶液变蓝色
hno3的混酸稀溶液中加入过量铜粉 是 CuSO4 和 Cu(NO3)2
向装满水的两个烧杯中分别加入黄豆
B 钾反应更剧烈 钾的金属性强于钠
大小的钠和钾
向硅酸钠溶液中滴加1滴酚献试液,-
cT 试管里出现凝胶 非金属性:CASi
然后逐滴加入稀盐酸至红色褪去
向 0.1 moi • L-1 NaHSO3 溶液中滴
D 溶液紫红色褪去 NaHSO3具有漂白性
加酸性KMnO.溶液
7.已知X、Y、Z、W为原子序数依次增大的第三周期元素,Z的最高价氧化物具有两性,在XW、
ZW3的熔融混合物中存在X+、W—、ZW;、Z2W7等离子。下列叙述正确的是
A简单离子半径:Y>Z>W B.第一电离能:Z>Y>X
C.化合物熔点:XZW4 >XZaW7 d. zw;与cior的空间结构相同
8.对下列有关实例的解释错误的是
选项 实例 解释
A 硅原子间难以形成穴键 硅的原子半径较大,未杂化的P轨道较难重叠
B 二氯乙酸的酸性大于一氯乙酸 二氯乙酸分子间作用力更大
C 标准状况下,HF为液态、HC1为气态 HF分子间存在氢键
D 与在⑸中的溶解度大于在乙醇中的溶解度 S8和8都是非极性分子
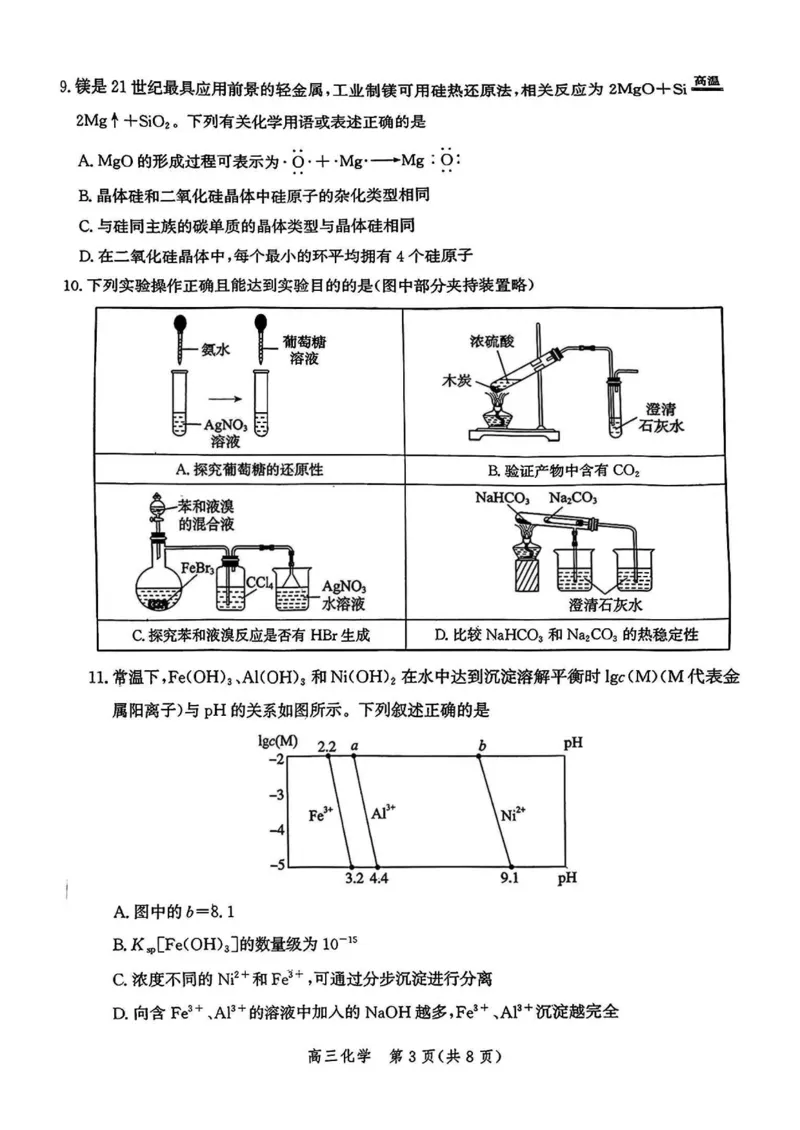
高三化学 第2页(共8页)9 .镁是21世纪最具应用前景的轻金属,工业制镁可用硅热还原法,相关反应为2MgO+Si^
2Mgf+SiO2o下列有关化学用语或表述正确的是
A MgO的形成过程可表示为• 6 • + -Mg•―-Mg : O :
• • • •
B.晶体硅和二氧化硅晶体中硅原子的杂化类型相同
C.与硅同主族的碳单质的晶体类型与晶体硅相同
D.在二氧化硅晶体中,每个最小的环平均拥有4个硅原子
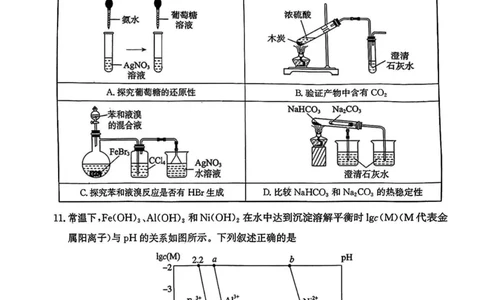
10 .下列实验操作正确且能达到实验目的的是(图中部分夹持装置略)
前萄糖
溶翻液
B.验证产物中含有CO2
澄清石灰水
C.探究苯和液浪反应是否有HBr生成 D.比较NaHCO3和Na2c。3的热稳定性
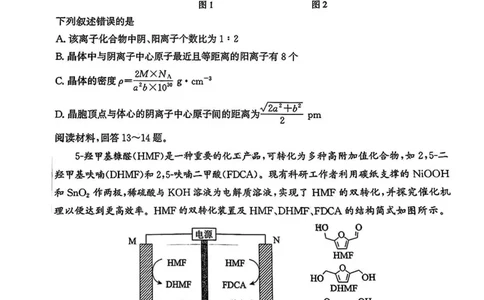
11,常温下,Fe(OH)3、AKOH)s和NKOH为在水中达到沉淀溶解平衡时lgc(M)(M代表金
属阳离子)与pH的关系如图所示。下列叙述正确的是
A.图中的6=8.1
B.K¥CFeCOH%]的数量级为 10~15
C.浓度不同的Ni2+和F3+,可通过分步沉淀进行分离
D.向含Fe3+、AE+的溶液中加入的NaOH越多,Fe&+、AF+沉淀越完全
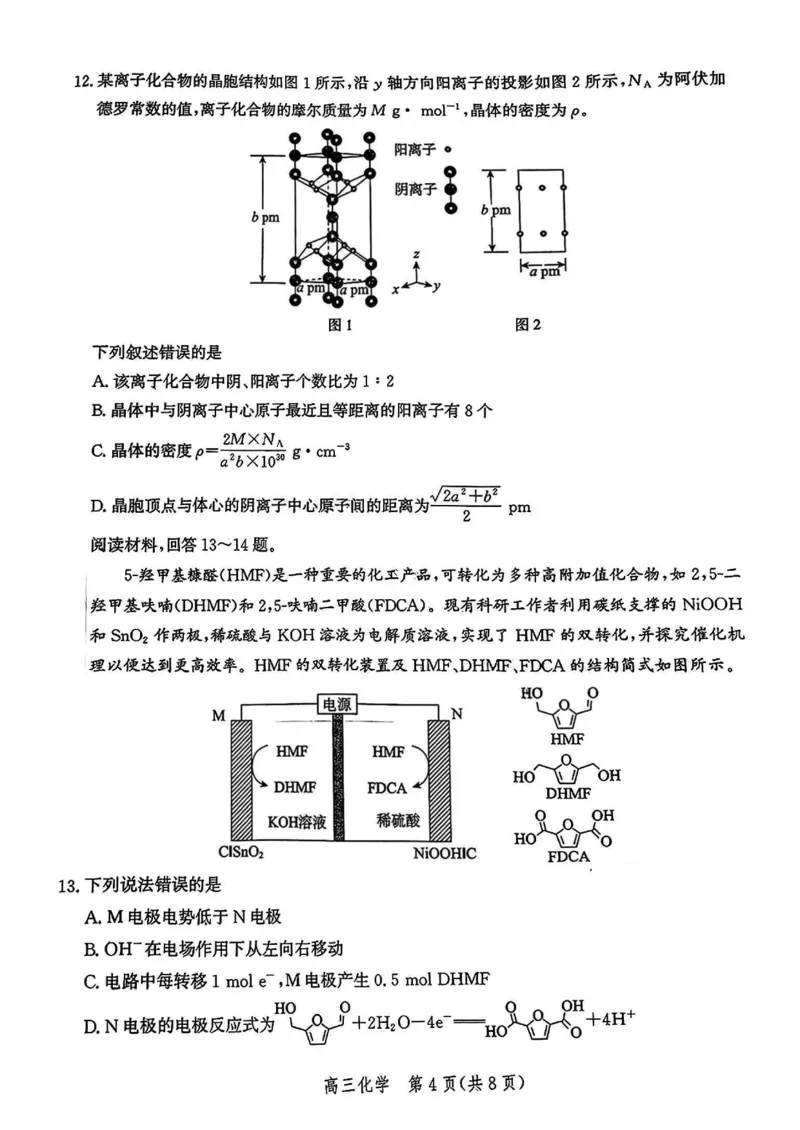
高三化学 第3页(共8页)12.某离子化合物的晶胞结构如图1所示,沿y轴方向阳离子的投影如图2所示,Na为阿伏加
德罗常数的值,离子化合物的摩尔质量为M g - ,晶体的密度为p。
图1 图2
下列叙述错误的是
A,该离子化合物中阴、阳离子个数比为1 : 2
B.晶体中与阴离子中心原子最近且等距离的阳离子有8个
。
- 口 /&一$ 2MXNa
C,晶体的密度P=/6xio3 g ,加
D.晶胞顶点与体心的阴离子中心原子间的距离为返孚出
阅读材料,回答13〜14题。
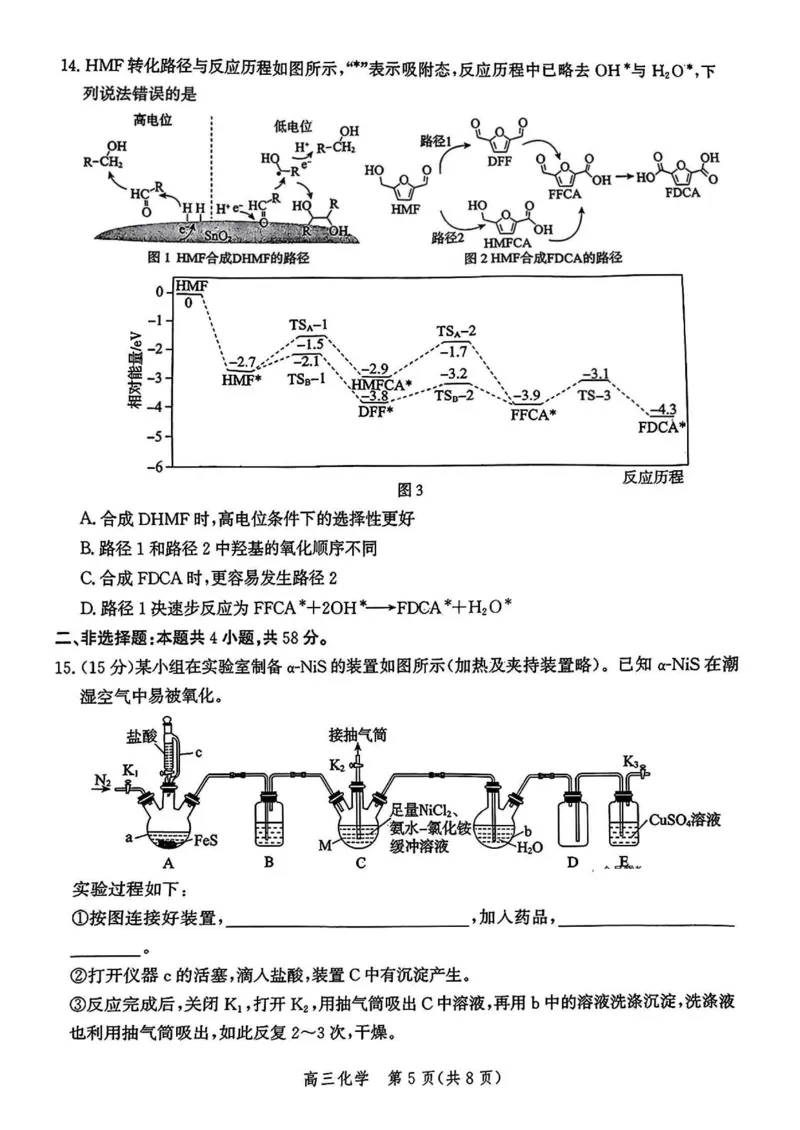
5-羟甲基糠醛(HMF)是一种重要的化父产品,可转化为多种高附加值化合物,如2,5-二
羟甲基吠喃(DHMF)和2,5-吹喃二甲酸庄1心4。现有科研工作者利用碳纸支撑的NiOOH
和S11O2作两极,稀硫酸与KOH溶液为电解质溶液,实现了 HMF的双转化,并探究催化机
理以便达到更高效率。HMF的双转化装置及HMF、DHMF、FDCA的结构简式如图所示。
HMF
DHMF
O c OH
ho;Sj^o
FDCA
13.下列说法错误的是
A. M电极电势低于N电极
B. 0H一在电场作用下从左向右移动
C.电路中每转移1 mol e-,M电极产生0. 5 mol DHMF
HO 0 O c OH
D. N电极的电极反应式为+2h0—46一一ho八&《0 +©1
高三化学第4页(共8页)14.
HMF转化路径与反应历程如图所示表示吸附态,反应历程中已略去oh*与%0*,下
HMF
0
DFF* FFCA*
FDCA*
— 反应历程
图3
A合成DHMF时,高电位条件下的选择性更好
B.路径1和路径2中羟基的氧化顺序不同
C.合成FDCA时,更容易发生路径2
D.路径 1 决速步反应为 FFCA *+20H *—>FDCA *+H2 O *
二、非选择题:本题共4小题,共58分。
15. (15分)某小组在实验室制备a-NiS的装置如图所示(加热及夹持装置略)o已知a-NiS在潮
湿空气中易被氧化。
实验过程如下:
①按图连接好装置,,加入药品,
②打开仪器c的活塞,滴人盐酸,装置C中有沉淀产生。
③反应完成后,关闭K,打开用抽气筒吸出C中溶液,再用b中的溶液洗涤沉淀,洗涤液
也利用抽气筒吸出,如此反复2〜3次,干燥。
高三化学 第5页(共8页)请回答下列问题:
(1)补全①中横线上的实验操作:,加入药品,
(2)仪器a的名称为;装置B中盛放的试剂最好是。
(3)写出装置C中产生沉淀的离子方程式:°
(4)步骤③用b中的溶液洗涤沉淀的优点为.
(5)装置E的作用为 、»
(6)NiS在空气中易被氧化为Ni(OH)S,该反应的化学方程式为。
(7)去掉D装置,实验中可能带来的后果是(填一条即可)。
16. (14分)近日,内蒙古赤峰市发现一处大型铝(Mo)矿床,初步探明铝资源矿石量约1亿吨。金
属铢(Re)和铝广泛用于电气化工和航空航天等领域。以铝精矿(主要成分MO&,还有少髭
的ReS)为原料提取铝和铢的流程如下:
试剂X 凡
t
辔建I反萃取
生石灰、硫酸、 还可卜悯斛>[砺原
空气 软镒矿
t
有机相 空气
1
铝精矿咂逅画*•一酶
KN。,溶液LiOH溶液
J I
水相
浸渣 川酸化沉铝M碱溶Flumoo,溶液
滤液
已知:“焙烧”工序中MoS2、ReS2分别转化为CWoO,、Ca(ReO“ )2。
(D已知在元素周期表中,络和铝为同族相邻元素。基态铝原子价层电子轨道表示式为
(2)已知Mo&中铝元素的化合价为+4,写出“焙烧”工序中M0S2与生石灰、足量空气反应
的化学方程式:<,
(3)“浸出”工序中,要不断搅拌并适当加热,其目的是 0
(4)“萃取”机理为R3N+H++ReO; -R3N ♦ HReO,。“反萃取”过程中加入的试剂X用
氨水、NH4 cl混合溶液比单一的氨水或氯化钱溶液要好,其原因为。
(5)若实验室完成“萃取”和“热解”操作,所需装置分别为、(填标号工
“热解”工序中,NHReO,发生反应生成Re?。?的化学方程式为
高三化学第6页(共8页)17. (15分)乙烯酮(0=C=CH2)是一种重要的有机中间体,主要用于化工基本原料及试剂的合
成。制备乙烯酮的原理有如下两种:
I .CH3COCH3(g)^=iO=C=CH2(g)+CH4(g) △H1=+84 kJ ♦ mol-1
il. CH3COOH(g):?=:=^O=C=CH2(g)+H2O(g) △H2 = 4-132.1 kJ • mol-1
请回答下列问题:
(1)标准摩尔生成熔(A/H*)是指一定条件下,由稳定的单质生成1 mol该物质的给变。稳定
单质的△/H*=00根据下表数据计算a =。
物质 CH3COCH3(g) CH,(g) CH3COOH(g) H2O(g)
△zH^/(kJ • mor1) a -74.8 -432. 2 -241.8
(2)氯乙酰氯(Cl、A)是合成各类除草剂的主要原材料,可由乙烯酮(CH?=C=O)与
Cl2反应生成,该反应说明乙烯酮分子中较易断裂的是 绿“c=c”或
“C=O”)键,试解释其原因:。
(3)向压强为九kPa的恒压容器中通入1 mol CH3coe玲⑷和2 mol ECKg),仅发生反应
i和ii,平衡时丙酮的分解率随反应温度工的变化如图所示:
①下列叙述可以判断反应i和II达到平衡状态的是(填标号)。
a.容器内气体密度不再变化
b. 0=C=CH2(g)和CH(g)的浓度比保持不变
c. O =C =CH2 (g)消耗速率与CH4生成速率相等
②To时,若0=C=CH2(g)与CH3coOH(g)的平衡体积分数之比为1 : 2,则
CECOOHlg)的体积分数为(用分数表示);To下,反应i的压强平衡常数
K.W kPa(用含&的代数式表示)。
③保持温度和压强不变,若起始时多通入3 mol Ar(g),丙酮的平衡分解率(填
“增大”“减小”或“不变”,下同),反应i的压强平衡常数/。
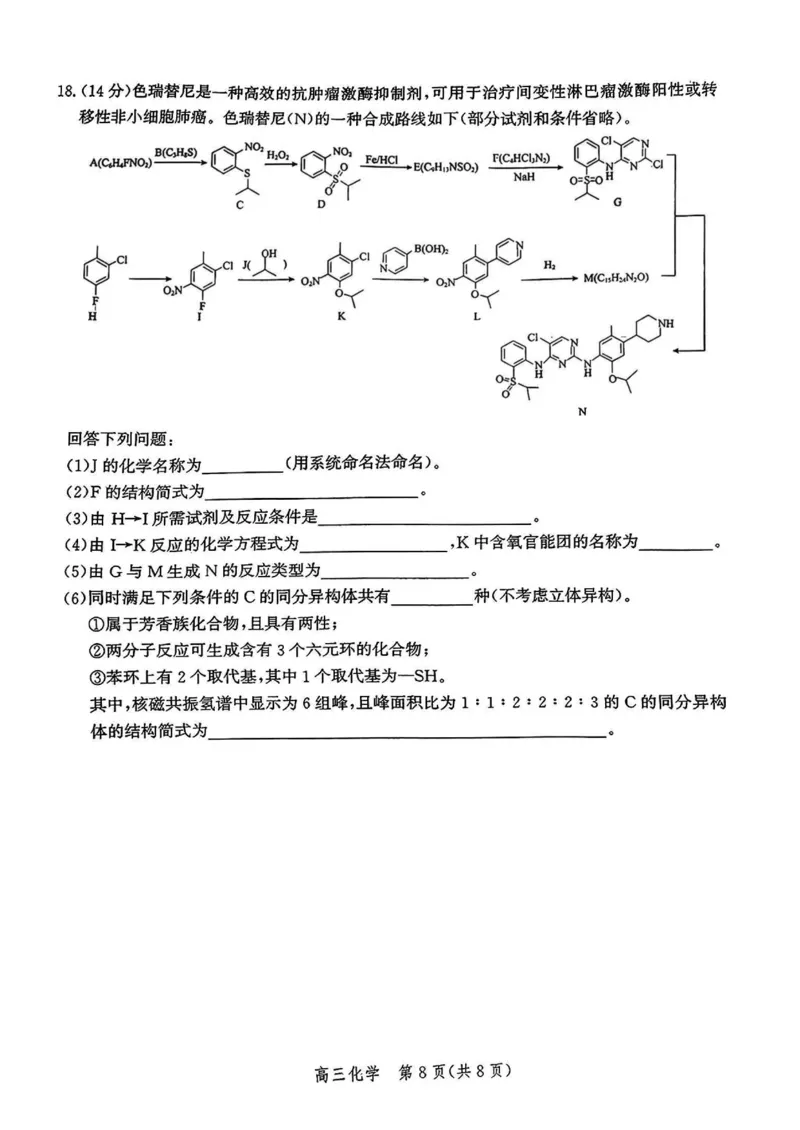
高三化学 第7页(共8页)18. (14分)色瑞替尼是一种高效的抗肿瘤激酶抑制剂,可用于治疗间变性淋巴瘤激酶阳性或转
移性非小细胞肺癌。色瑞替尼(N)的一种合成路线如下(部分试剂和条件省略)。
N
回答下列问题:
(1)J的化学名称为(用系统命名法命名)。
(2)F的结构简式为。
(3)由H—I所需试剂及反应条件是。
(4)由If K反应的化学方程式为,K中含氧官能团的名称为。
(5)由G与M生成N的反应类型为。
(6)同时满足下列条件的C的同分异构体共有 种(不考虑立体异构)。
①属于芳香族化合物,且具有两性;
②两分子反应可生成含有3个六元环的化合物;
③苯环上有2个取代基,其中1个取代基为一SH。
其中,核磁共振氢谱中显示为6组峰,且峰面积比为1 : 1 : 2 : 2 : 2 : 3的C的同分异构
体的结构简式为。
高三化学第8页(共8页)